Tratamiento médico para enfermedad inflamatoria intestinal
Medical therapy for inflammatory bowel disease
Fabián Juliao Baños (1)
(1) Médico Internista Universidad Nacional de Colombia. Gastroenterólogo Clínico Pontificia Universidad Javeriana. Jefe Unidad de Gastroenterología Hospital Pablo Tobón Uribe Medellín - Colombia
Fecha recibido: 30-08-07 / Fecha aceptado: 23-10-07
RESUMEN
El tratamiento médico óptimo de los pacientes con enfermedad inflamatoria intestinal requiere que el médico tratante obtenga una buena historia clínica, evalúe al paciente, realice los procedimientos diagnósticos necesarios, y luego prescriba un tratamiento adecuado, basado en la evidencia de estudios clínicos controlados. Las metas del tratamiento farmacológico en pacientes con enfermedad inflamatoria intestinal son mejorar la calidad de vida, reducir el riesgo de complicaciones y evitar intervenciones quirúrgicas. Las recomendaciones de la nueva clasificación de Montreal con respecto a enfermedad de Crohn y colitis ulcerativa deben ser implementadas en nuestra práctica clínica. Finalmente, la introducción de la terapia biológica (Infliximab, adalimumab) ha mejorado las opciones de tratamiento en el manejo de la enfermedad inflamatoria intestinal.
Palabras clave
Enfermedad inflamatoria intestinal, colitis ulcerativa, enfermedad de Crohn, clasificación de Montreal, terapia biológica.
]]> SUMMARYThe optimal medical treatment of patients with inflammatory bowel disease requires that the treating physician obtain a good history, evaluate the patient, perform necessary diagnostic procedures, and then prescribe an appropriate treatment based in the evidence from controlled clinical trials. The goals of pharmacology treatment in patients with inflammatory bowel disease are to improve quality of life, reduce the risk of complications and avoid surgical interventions. The recommendations of the new Montreal classification with respect to Crohn`s Disease and Ulcerative Colitis might be used in our clinical practice. Finally, the introduction of biological therapy (Infliximab, adalimumab), has greatly improved the treatment options in the management of inflammatory bowel disease.
Key Words
Inflammatory Bowel Disease, Crohn`s Disease, Ulcerative Colitis, Montreal classification, biological therapy.
Introducción
En los últimos años se han presentado múltiples avances en el tratamiento de la enfermedad inflamatoria intestinal (EII), la cual incluye colitis ulcerativa (CU) y enfermedad de Crohn (EC), sin embargo, persiste dificultad muchas veces en diferenciar estas dos entidades debido a que no hay formas patognomónicas, a pesar del descubrimiento de nuevos marcadores serológicos y genéticos. Para poder realizar el diagnóstico diferencial debe tenerse en cuenta la historia clínica, el examen físico y los hallazgos endoscópicos, radiológicos e histológicos; a pesar de lo anterior, cerca de 10% de casos permanece como colitis indeterminada. De otra parte, no hay acuerdo mundial en la utilización de los múltiples índices de actividad descritos para estas entidades, con el fin de establecer la eficacia terapéutica de los diferentes medicamentos utilizados.
Clasificación de Montreal
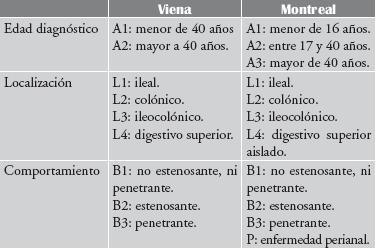
Otra dificultad en el enfoque de esta enfermedad ha sido la falta de consenso en establecer una clasificación adecuada, que le permita al gastroenterólogo iniciar un tratamiento adecuado y definir un pronóstico al paciente. Recientemente se publicó la clasificación de Montreal (1), la cual fue presentada en el Congreso Mundial de Gastroenterología celebrado en dicha ciudad en septiembre del 2005, la cual revisa las clasificaciones previas de Roma en 1991 y de Viena en 1998. Para la enfermedad de Crohn, la clasificación de Viena tenía en cuenta la edad de inicio (menor o mayor a 40 años), la localización y el comportamiento de la enfermedad (inflamatoria, estenosante, y penetrante). La clasificación de Montreal conserva dichas categorías, pero admite que pueden cambiar con el tiempo, además en cuanto a la edad, separa la población pediátrica creando un nuevo grupo con inicio de enfermedad antes de los 16 años. En la localización de la enfermedad, considera que no deben ser excluyentes y pueden combinarse, y separa las fístulas perianales de las fístulas intestinales internas. Un comparativo de las clasificaciones de la enfermedad de Crohn entre Montreal y Viena se muestra en la tabla 1.
Tabla 1. Clasificación de enfermedad de Crohn: Viena y Montreal.
]]> A diferencia de las clasificaciones previas de Roma y Viena, la de Montreal incorpora la clasificación de colitis ulcerativa, teniendo en cuenta la extensión y la severidad de la enfermedad. La extensión se clasificó en tres grupos teniendo en cuenta el comportamiento biológico y la respuesta del paciente al tratamiento médico (tabla 2), a pesar que se ha encontrado que la enfermedad puede cambiar con el tiempo con tasas variables de progresión (41-54%) y de regresión (71%) en 10 años de seguimiento endoscópico. En cuanto a la severidad, la divide en cuatro grupos (tabla 3), considera que el término colitis fulminante es confuso por lo cual proponen eliminarlo, lo mismo que la idea de introducir la edad y la presencia de colangitis esclerosante como subgrupos separados. Una propuesta del grupo de Copenhagen de clasificar la colitis ulcerativa según el curso de los síntomas en remisión prolongada, síntomas intermitentes o actividad permanente, no fue aceptada y creen que requiere futura validación (2). El término colitis indeterminada lo reservan para pacientes que son llevados a colectomía y en la cual el patólogo es incapaz de definir si se trata de enfermedad de Crohn o colitis ulcerativa.Tabla 2. Clasificación de Montreal: extensión de colitis ulcerativa.
Tabla 3. Clasificación de Montreal: severidad de colitis ulcerativa.
Tratamiento de la enfermedad de Crohn
Antes de iniciar o modificar el tratamiento para enfermedad de Crohn, el médico debe evaluar bien al paciente, con una historia clínica completa que incluya la edad de inicio, la duración, la extensión y el curso de la enfermedad, los medicamentos previos y actuales, la respuesta a cada intervención, las cirugías previas y el estado actual de los síntomas. Adicionalmente, debe tener tránsito intestinal y colonoscopia reciente, para definir extensión, severidad y descartar complicaciones como fístulas, estenosis, y excluir causas medicamentosas e infecciosas de colitis (3).
Las guías del Colegio Americano de Gastroenterología (ACG) (4) describen unos criterios para definir la actividad clínica de la enfermedad de Crohn y recomiendan utilizarlo para establecer severidad en dichos pacientes (tabla 4). Esta clasificación es importante para definir si se hospitaliza al paciente y si requiere manejo con esteroides intravenosos. A diferencia de lo anterior, existe un índice de actividad de enfermedad de Crohn (CDAI), que se utiliza para medir eficacia de terapia médica, sobre todo en estudios de investigación (tabla 5).
Tabla 4. Actividad clínica de enfermedad de Crohn.
]]> Tabla 5. Índice de actividad de enfermedad de Crohn (CDAI).Nota: Remisión: CDAI < 150, actividad leve: CDAI 150-219, actividad moderada: CDAI: 220-450, actividad severa: CDAI > 450.
La meta en el manejo de estos pacientes es inducir y mantener remisión clínica, y en lo posible lograr una remisión endoscópica de la enfermedad. Los medicamentos que se utilizan para el manejo de la enfermedad de Crohn, se señalan a continuación.
Ácido 5 aminosalicílico (5-ASA)
A pesar de existir varias preparaciones que incluyen 5-ASA a nivel mundial, en Colombia sólo disponemos de presentaciones orales de sulfasalazina y mesalazina, de esta última contamos adicionalmente con supositorios y enemas.
La sulfasalazina contiene 5-ASA unido por anillo azo con sulfapiridina, que le sirve de transporte, este último es liberado en el colon por bacterias, y luego se absorbe y es el responsable de la mayoría de efectos colaterales como epigastralgia, cefalea, hepatitis, anemia, leucopenia, rash cutáneo, entre otras. Estudios en pacientes con enfermedad de Crohn demostraron que dosis de sulfasalazina de 3-6 g/día son efectivas en paciente con actividad leve a moderada, sobre todo cuando el compromiso es colónico o ileocolónico. Dosis de sulfasalazina de 1,5-3 g/día, no han demostrado ser útiles en el mantenimiento de remisión en pacientes con enfermedad de Crohn.
Contrario a los estudios con sulfasalazina, la utilidad de la mesalazina en el mantenimiento de remisión clínica en estos pacientes ha sido muy controversial. Un metanálisis con 15 estudios aleatorizados y controlados, con 2.097 pacientes, encontró una diferencia significativa en reducir el riesgo de recaídas sintomáticas en pacientes sometidos a cirugía (-13,1%, NNT: 10), pero no en pacientes tratados médicamente (-4,7%, NNT: 20), comparados con placebo (5). Posteriormente, un estudio europeo prospectivo, multicéntrico, aleatorizado, doble ciego y controlado con placebo, diseñado para prevenir recaídas postoperatorias en 318 pacientes con enfermedad de Crohn, no encontró diferencia significativa entre el grupo asignado a mesalazina 4 g/día y placebo después de 18 meses de seguimiento (24,5% vs. 31,4%, p: 0,10) (6). Une reciente revisión sistemática de Cochrane, del uso de 5-ASA en el mantenimiento de remisión clínica inducida médicamente en pacientes con enfermedad de Crohn, no demostró diferencias significativas en seis estudios que cumplían los criterios de inclusión, cuando se comparaban con placebo (7).
Corticosteroides
Desde hace varios años los corticosteroides han demostrado su efectividad en controlar la actividad inflamatoria en pacientes con enfermedad de Crohn, siendo superiores a la sulfasalazina y mesalazina, con un inicio de acción más rápido. Tradicionalmente, en Estados Unidos se ha utilizado prednisona oral en dosis de 40-60 mg/día, extrapolando la dosis utilizadas en colitis ulcerativa, aunque algunos estudios europeos prefieren utilizarla en dosis de 1 mg/kg/día. Otra presentación oral de esteroides es la budesonida de liberación ileal, sin efecto de primer paso por el hígado, con una afinidad por el receptor glucocorticoide 50 veces superior a la prednisona, lo cual la hace más potente y menos tóxica, en dosis de 6-9 mg/día, es ideal en Crohn con compromiso de ileon distal y colon derecho. Un metanálisis en pacientes con enfermedad de Crohn activa encontró que prednisona a dosis de 40 mg/día es superior a budesonida 9 mg/día, aunque esta última presenta menos efectos colaterales y demostró ser superior a 5-ASA (8).
]]> Tabla 6. Actividad clínica de enfermedad de Crohn.Tabla 7. Índice de actividad de enfermedad de Crohn (CDAI).
Nota: Remisión: CDAI < 150, actividad leve: CDAI 150-219, actividad moderada: CDAI: 220-450, actividad severa: CDAI > 450.
En paciente con enfermedad de Crohn activa severa, se prefiere la utilización de esteroides intravenosos, como hidrocortisona 300-400 mg/día o metilprednisolona en dosis de 40-60 mg/día, la cual tiene mínimo efecto mineralocorticoide.
En el mantenimiento de remisión en pacientes con enfermedad de Crohn, ni prednisona en dosis de 0,5 mg/kg (10-30 mg/día), ni budesonida en dosis de 6 mg/día han logrado demostrar disminución en el número de recaídas (9). Además de los efectos adversos que se presenta con el uso de esteroides a largo plazo.
Un estudio realizado por Faubión, en la población de Olmsted en Minnesota, sobre la historia natural de la enfermedad de Crohn en 173 pacientes, encontró que 73 de ellos (43%) fueron tratados con esteroides, de éstos 43 (58%) lograban remisión clínica completa y 19 (26%) remisión parcial. Al año de seguimiento, 24 (32%) tuvieron respuesta prolongada y no requirieron cirugía, ni recibían esteroides, 21 (28%) eran dependientes de esteroides y 28 de ellos (38%) requirieron cirugía (10).
Inmunosupresores
Azatioprina y 6-mercaptopurina
La azatioprina y su metabolito, la 6-mercaptopurina son análogos de tiopurina. Las dosis que han demostrado ser efectivas en sujetos con Crohn son 2-3 mg/kg/día y 1,5 mg/kg/día, respectivamente. Estos medicamentos son efectivos en inducir y mantener remisión en pacientes con enfermedad de Crohn, como también en facilitar la suspensión de esteroides, por lo cual son considerados "ahorradores" de esteroides. Una vez los pacientes inician manejo con estos medicamentos debe continuarse en forma indefinida a no ser que se presenten efectos colaterales serios; el beneficio clínico se hace evidente después de 2 a 3 meses de tratamiento.
]]> La azatioprina es metabolizada a 6-mercaptopurina que es el metabolito activo, la cual a su vez es metabolizada a 6-tioinosina 5-monofosfato (TIMP) por la enzima hipoxantina fosforibosil transferasa (HPRT), posteriormente la 6-TIMP es metabolizada al nucleótido 6-tioguanina (6-TGN), el cual se intercambia por guanina en el DNA, lo cual conduce a apoptosis de linfocitos T, tanto citotóxicos como los "asesinos" naturales (natural killer). Otros dos metabolitos de la 6-mercaptopurina son la 6-metilmercaptopurina por la enzima tiopurina-metiltransferasa (TPMT) y el ácido 6-tiourico por la enzima xantina oxidasa (XO). Las tres enzimas compiten por el metabolismo de la 6-mercaptopurina y se ha demostrado que el 84% del medicamento es metabolizado por la xantina oxidasa y el 16% restante se lo dividen las otras dos enzimas. Se han descrito 12 mutaciones en los genes que codifican la enzima TPMT, localizados en el cromosoma 6, lo que ocasiona un déficit en la actividad de esta enzima favoreciendo la acumulación de metabolitos activos como la 6-TGN, lo cual pude ser tóxico para el paciente. Se ha encontrado que 0,3% de individuos tiene mutación tipo homocigoto y 11% mutación tipo heterocigoto, lo cual se correlaciona inversamente con la respuesta al medicamento. Actualmente, no es costo-efectiva la medición rutinaria de niveles de metabolitos como 6-TGN en individuos recibiendo azatioprina, con el objeto de predecir toxicidad (11).Una revisión sistemática de Cochrane de 8 estudios aleatorizados, controlados y comparados con placebo, para inducción de remisión en pacientes con enfermedad de Crohn activa, encontró un Odds Ratio (OR) de 2,36, lo que corresponde a un número necesario a tratar (NNT) de 5; cuando el tratamiento es superior a 17 semanas el OR se incrementa a 2,51. Adicionalmente, se demostró un OR de 3,86 (NNT: 3) en su efecto de "ahorrar" esteroides. El número de pacientes tratados para producir un efecto adverso con estos medicamentos es de 14 (NNH), los más frecuentes son alergias, leucopenia, hepatitis, pancreatitis, fiebre, rash y náuseas, entre otros, lo cual hace necesario un control cada 2 a 3 meses de cuadro hemático y perfil hepático en estos pacientes para vigilar toxicidad (12).
Una revisión sistemática en 5 estudios aleatorizados, doble ciego y controlados con placebo, demostró que la azatioprina tiene un efecto positivo en el mantenimiento de remisión en pacientes con enfermedad de Crohn con un OR: 2.1 y un NNT: 7, y un efecto ahorrador de esteroides con OR: 5,22 para un NNT: 3, con un número necesario a dañar (NNH) de 19 (13). Se ha documentado un cierto riesgo de linfoma no Hodking en pacientes recibiendo azatioprina. Un reciente metanálisis con 6 estudios demostró un riesgo de cuatro veces de padecer linfoma comparado con la población general (RR: 4,18) (14).
Metotrexate
El metotrexate es un antagonista de ácido fólico que conduce a la inhibición de la síntesis de purina, con inhibición de la formación de ácidos nucleicos y de la fase S del ciclo celular. Dentro de la célula es convertido al metabolito activo metotrexate poliglutamato por la enzima folato poliglutamasa sintetasa.
Se utiliza por vía oral a dosis de 12,5-22,5 mg semanales, y por vía subcutánea o intramuscular en dosis de 15-25 mg semanales. Tiene como efectos secundarios hepatotoxicidad y mielosupresión, por lo cual requiere vigilancia con cuadro hemático y perfil hepático cada 1-3 meses, con biopsia hepática después de una dosis acumulada de 1 g.
Hay pocos estudios que demuestren la efectividad de metotrexate en pacientes con enfermedad de Crohn, sin embargo, dos estudio multicéntricos, aleatorizado, controlado con placebo y doble ciego, publicados por Feagan (15, 16), el primero de ellos demostró que metotrexate en dosis de 25 mg intramuscular semanal es eficaz en inducir remisión de enfermedad de Crohn cuando se comparó con placebo (39,4% vs. 19,1%, p: 0,025), con una reducción significativa en el uso de esteroides, en 16 semanas de seguimiento. De otro lado, los mismos autores encontraron que dosis de 15 mg IM semanales son útiles en mantener remisión de la enfermedad, comparado con placebo (65% vs. 39%, p: 0,04), con menos requerimiento de utilización de prednisona en caso de recaída (28 vs. 58%, p: 0,01), con seguimiento a 40 semanas y no se presentaron efectos adverso serios.
Ciclosporina
La ciclosporina es un inhibidor de calcineurina, lo que conduce a inhibición selectiva de la interleuquina (IL)-2. Varios estudios utilizando ciclosporina a dosis de 5 mg/kg/día, no han demostrado efectividad en inducción de remisión, ni en mantenimiento de la misma en pacientes con enfermedad de Crohn, a diferencia de la utilidad demostrada con el uso de este medicamento en pacientes con colitis ulcerativa severa como veremos más adelante.
Terapia biológica
]]> InfliximabEl infliximab es un anticuerpo monoclonal quimérico (75% humano y 25% murino) tipo IgG1, contra el factor de necrosis tumoral alfa (TNF-a). La justificación para el uso de infliximab por más de 10 años en el manejo de enfermedad de Crohn, está basado en la hipótesis que la respuesta celular en esta enfermedad es del tipo Th 1, e incluye mediadores inflamatorios entre los que se encuentra el factor de necrosis tumoral alfa (TNF-a), el interferón y la interleuquina 12 (IL-12) entre otros, bloqueando la formación de granulomas y disminuyendo las concentraciones séricas del TNF-a, lo cual se ha correlacionado con reducción en la actividad de la enfermedad.
Estudios clínicos han demostrado que este medicamento es efectivo, tanto para inducción como en mantenimiento de remisión, en pacientes que no responden a terapia convencional. El esquema de tratamiento y dosis sugerida es infusión de 5 mg/kg en 0, 2 y 6 semanas, para luego continuar con 5 mg/kg cada 8 semanas, en forma indefinida. El primer estudio controlado con placebo, aleatorizado y multicéntrico con infliximab, se realizó en 108 pacientes con enfermedad de Crohn moderada a severa, refractaria a manejo convencional, comparando la eficacia de una sola dosis de 5 mg/kg con placebo, logrando una respuesta clínica de 81% vs. 17% (p<0,001) y una remisión clínica en 33% vs. 4% (p: 0,005), en 4 semanas. Dosis de infliximab de 10 y 20 mg/kg, no lograron una respuesta clínica superior y se encontró una disminución de la respuesta clínica inicial a las 12 semanas de seguimiento (17).
En vista de lo anterior, se diseñó el estudio ACCENT I, con 573 pacientes, los que respondieron a una dosis inicial de 5 mg/kg, se aleatorizaron en tres grupos: 5 mg/kg, 10 mg/kg y placebo, los cuales se administraban en 2 y 6 semanas, y luego cada 8 semanas por 46 semanas; 335 pacientes (58%) respondieron a la dosis inicial de 5 mg/kg y a las 30 semanas de seguimiento, la respuesta clínica fue de 39% (p: 0,003), 45% (p: 0,0002) y 21%, respectivamente. No se encontró diferencia significativa entre la dosis de 5 mg/kg y 10 mg/kg (18).
El efecto adverso más frecuente asociado al uso de infliximab es la formación de anticuerpos antiquiméricos humanos (HACAS) ente 17-21% de los pacientes, los cuales son responsables de reacciones alérgicas presentadas con las subsecuentes infusiones, su formación se reduce con el uso concomitante de inmunosupresores como azatioprina. Otros efectos colaterales incluyen: aparición de anticuerpos antinucleares (34%), lupus inducido por droga, posible linfoma no-Hodking, aparición de infecciones oportunistas y reactivación de tuberculosis latente, lo cual hace necesario solicitar prueba de tuberculina y radiografía de tórax previo a la iniciación de la medicación (19).
Adalimumab
El adalimumab es un anticuerpo monoclonal humanizado tipo IgG1, que contiene sólo secuencias de péptidos humanos, lo cual lo diferencia del infliximab, y se une con alta afinidad al factor de necrosis tumoral alfa TNF-a, neutralizando su actividad tanto en la forma soluble, como el que se encuentra acoplado al receptor celular. A pesar de ser el infliximab un excelente medicamento para el manejo de pacientes con enfermedad de Crohn, algunos pacientes presentan una disminución en la respuesta con el tiempo, o no toleran la infusión, lo cual se ha asociado a la formación de anticuerpos (17-21%). Por lo anterior, se ha propuesto la utilización de adalimumab en estos pacientes, debido a que se elimina el riesgo de desarrollar anticuerpos.
Un reporte inicial de una serie de casos con 13 pacientes con enfermedad de Crohn activa y respuesta atenuada al infliximab, a quienes se les aplicó 80 mg subcutáneos (sc), seguidos por 40 mg sc cada 2 semanas por un período de 6 meses, demostró que 7 pacientes (54%) tuvieron una respuesta completa y en 4 (31%) la respuesta fue parcial. En 8 de los 11 pacientes que respondieron se pudo disminuir o retirar los esteroides. El medicamento fue bien tolerado (20).
Un estudio más reciente (CHARM), multicéntrico, aleatorizado, doble ciego y controlado con placebo, en 778 pacientes con enfermedad de Crohn moderada a severa, con el objeto de inducir y mantener remisión, a los cuales se les aplicaban 80 mg sc de adalimumab, seguidos por 40 mg sc a las 2 semanas, momento en el cual se aleatorizaban los pacientes a recibir 40 mg sc cada semana, o cada 15 días o placebo. La respuesta clínica obtenida fue de 41%, 36% y 12% (p< 0,001), respectivamente, con un seguimiento a 56 semanas. No hubo diferencia significativa entre la dosis semanal o cada 15 días y la medicación fue bien tolerada (21).
Enfoque para el manejo de enfermedad de Crohn
]]> Inducción y mantenimiento de remisión en enfermedad de Crohn leve y moderadaTradicionalmente el tratamiento de primera línea para enfermedad de Crohn leve y moderada, tanto para inducción como en mantenimiento de remisión, ha sido con 5-ASA y antibióticos, en caso de no respuesta, se adicionan esteroides. Dosis orales de mesalazina 4 g/día y antibióticos, se han utilizado en estos pacientes pero los resultados de estudios clínicos no demuestran eficacia clínica.
Basado en la evidencia clínica descrita anteriormente, la sulfasalazina en dosis de 3-6 g/día, con adición de ácido fólico 1-5 mg por riesgo de anemia ha demostrado ser efectiva en pacientes con enfermedad de Crohn con actividad leve a moderada y con compromiso colónico, lo mismo que la budesonida a dosis de 9 mg/día, en individuos con compromiso ileal o de colon derecho. Lo anterior se recomienda por 8-16 semanas de tratamiento. En caso de fracaso del tratamiento anterior, se inicia prednisona a dosis de 40-60 mg/día (Estados Unidos) o 1 mg/kg/día (Europa), en este caso debe suspenderse la budesonida y adicionarse calcio y vitamina D para prevenir osteoporosis. La dosis de prednisona se mantiene igual por 2-4 semanas hasta obtener remisión clínica, luego se disminuye 5 mg por semana hasta dosis de 20 mg/día y luego 2,5 mg por semana hasta suspenderla. En caso de que el paciente logre remisión completa de los síntomas, se puede mantener sin tratamiento. Si presentan recaída durante la disminución de prednisona, requiriendo dosis ente 10-30 mg/día, se consideran esteroide-dependientes y deben recibir manejo con inmunosupresores como azatioprina o metotrexate. Lo mismo se hace en caso de que presenten recaída temprana durante los primeros 6-12 meses. Si el paciente presenta recaída tardía (> 12 meses) debe iniciarse nuevamente otro ciclo de sulfasalazina o budesonida, y en caso de respuesta a esta última, debe continuarse en dosis de 6 mg/día, la cual ha demostrado no producir osteoporosis, y es una alternativa al manejo con inmunosupresores.
Enfermedad de Crohn refractaria
Los pacientes con enfermedad de Crohn que no responden a dosis oral de prednisona 40-60 mg/día, se considera que tienen actividad moderada y se denominan refractarios, además, necesitan manejo intrahospitalario con esteroides intravenosos, con lo cual se obtienen niveles séricos superiores. Adicionalmente, estos pacientes requieren manejo con azatioprina en dosis de 2-3 mg/kg, o metotrexate 25 mg/semana intramuscular o subcutáneo, por 16 semanas, y luego se diminuye a 15 mg/semanal como mantenimiento. La azatioprina actúa en forma lenta y demora entre 2-3 meses en lograr su eficacia clínica completa, mientras que el metotrexate requiere 6-8 semanas. No hay evidencia clínica que demuestre beneficio adicional de 5-ASA, sulfasalazina o antibióticos con los inmunosupresores, por lo tanto deben suspenderse.
En caso de ser refractario a esteroides, azatioprina y/o metotrexate, los pacientes son candidatos para terapia biológica con infliximab a dosis de 5 mg/kg en semanas 0, 2 y 6 y luego cada 8 semanas, y debe continuarse manejo inmunosupresor con azatioprina o metotrexate, para prevenir la aparición de anticuerpos contra el infliximab. Estos pacientes requieren vigilancia estricta de aparición de infecciones oportunistas, tales como hongos o tuberculosis. En casos en que se disminuya respuesta a infliximab o se presente intolerancia al mismo queda la opción de utilizar adalimumab, en dosis de 80 mg por vía subcutánea, seguido por 40 mg sc cada 2 semanas.
Enfermedad de Crohn severa
En este grupo se incluyen pacientes con actividad severa, megacolon tóxico, obstrucción intestinal o con abscesos intraabdominales. Estos pacientes se caracterizan por presentar dolor abdominal, diarrea severa, taquicardia, deshidratación, fiebre y anemia. El tratamiento incluye hospitalización, reposo intestinal, hidratación, antibióticos de amplio espectro (ciprofloxacina y metronidazol) y esteroides intravenosos. En caso de falla al tratamiento anterior se podría utilizar infliximab aunque la evidencia en este tópico es limitada. Los pacientes con obstrucción intestinal deben recibir manejo quirúrgico, lo mismo en aquellos que no respondan a manejo médico después de 7-10 días de tratamiento con esteroides intravenosos o después de 5 días de adición de dosis única de infliximab 5 mg/kg. En la figura 1 se muestra un diagrama de flujo con el manejo médico de pacientes con enfermedad de Crohn leve/moderada y refractaria.
Figura 1. Enfoque manejo enfermedad de Crohn.
]]> Tratamiento de enfermedad de Crohn con fístula perianalLa frecuencia de enfermedad perianal en pacientes con enfermedad de Crohn varía entre 17-43% según los diferentes estudios, siendo más frecuentes cuando existe compromiso colónico, sobretodo rectal. 5% de paciente con enfermedad de Crohn pueden manifestarse con compromiso perianal como única manifestación clínica (22). Existen dos teorías para explicar la aparición de fístulas, la primera es que provienen de úlceras profundas en ano o recto, que se vuelven tractos fistulosos, y la segunda es que se originan en abscesos de las glándulas anales. Desde 1976, existe una clasificación anatómica descrita por Parks (23), teniendo en cuanta la localización de la fístula con respecto a los esfínteres anales interno y externo, dividiéndola en 5 tipos: A. Superficial, B. Interesfintérica, C. Transesfintérica. D. Supraesfintérica y E. Extraesfintérica (figura 2). Sin embargo, recientemente se estableció una nueva clasificación clínica, por la Asociación Americana de Gastroenterología (AGA), en simples y complejas (figura 3) (24). Las simples son superficiales o bajas, con orificio externo único, no dolorosas, ni fluctuantes y tienen mayor tasa de cicatrización. Las complejas son altas, con orificios múltiples, con dolor y/o induración (abscesos), en ocasiones recto-vaginales y asociadas a estenosis, se relacionan con mayor actividad de la enfermedad y son más difíciles de manejar.
Figura 2. Clasificación anatómica de Parks de fístulas perianales.
Figura 3. Fístulas simples y complejas.
En el manejo de la enfermedad de Crohn perianal se han utilizado antibióticos, azatioprina y 6-mercaptopurina, ciclosporina, tacrolimus e infliximab. No hay estudios controlados que demuestren que los antibióticos sean efectivos en el manejo de fístulas perianales. Los estudios existentes no son controlados y tienen escaso número de pacientes. Un estudio con 21 pacientes con metronidazol a dosis de 20 mg/kg/día por 3-4 meses, demostró cicatrización de la fístula en 56% de los sujetos, en 6-8 semanas de seguimiento, sin embargo el 50% de los pacientes presentó parestesias como efecto adverso al metronidazol. El otro antibiótico utilizado es la ciprofloxacina, a dosis de 1.000-1500 mg/día por 3 meses, con respuesta variable de 70-55% de los casos. La combinación de estos dos antibióticos en un estudio de Solomon en 14 pacientes, demostró una respuesta clínica adecuada en 9 de ellos (23).
La evidencia clínica de la utilización de azatioprina en fístula perianal proviene de un meta-análisis con 5 estudios controlados, donde se encontró que 22 de 41 pacientes (54%) cicatrizaron su fístula, comparados con 6 de 29 pacientes (21%) tratados con placebo, OR: 4,44 (25).
A diferencia de la ciclosporina que ha demostrado poco utilidad en el manejo de fístulas perianales, un estudio con otro inhibidor de calcioneurina, tacrolimus, en 48 pacientes, controlado con placebo, en dosis oral de 0,2 mg/kg/día, demostró una respuesta clínica (disminución en 50% de la actividad de la fístula) en 43% de los pacientes tratados comparado con 8% con placebo, lo cual fue significativo (p: 0,004), a 10 semanas de seguimiento. Sin embargo no se encontró diferencia significativa en la tasa de remisión o cierre de la fístula 10% vs. 8%, comparado con placebo (p: 0,86). Los autores proponen al tacrolimus como una terapia "puente" para manejo posterior con azatioprina (26).
Con el advenimiento de la terapia biológica, el manejo médico de la enfermedad de Crohn perianal ha mostrado mejores resultados. Un estudio inicial con infliximab, multicéntrico, aleatorizado, doble ciego y controlado con placebo, en 94 pacientes con fístula perianal, comparando dosis de 5 mg/kg y 10 mg/kg con placebo, con infusiones en 0, 2 y 6 semanas, encontraron una respuesta clínica (disminución en 50% en actividad de fístulas) en 68% vs. 56% vs. 26% respectivamente, lo cual fue significativo (p: 0,02). En cuanto al cierre total de la fístula la diferencia también fue significativa 55% vs. 38% vs. 13% (p: 0.001). No se encontró diferencia en la formación de abscesos en los tres grupos 6% vs. 16% vs. 3% (27). Posteriormente se realizó un segundo estudio denominado ACCENT II, con infliximab como terapia de mantenimiento, el cual fue multicéntrico, doble ciego, aleatorizado y controlado con placebo, inicialmente con 306 pacientes, a los cuales se les administró Infliximab 5 mg/kg en 0, 2 y 6 semanas, encontrando una respuesta clínica inicial (disminución en 50% en actividad de fístulas), en 195 pacientes (69%) a 3 meses de seguimiento, tiempo en el cual se aleatorizaron los individuos para recibir dosis de infliximab 5 mg/kg cada 8 semanas comparado con placebo. A las 54 semanas de seguimiento la respuesta fue de 36 vs. 19%, lo cual fue significativo (p: 0,009) (28). Un seguimiento de este mismo estudio recientemente publicado, demostró que la tasa de abscesos de "novo" en los pacientes con infliximab es similar a la encontrada en el grupo placebo, 15% vs. 19% (p: 0,526) (29).
]]> En conclusión podemos decir que el uso de terapia biológica con infliximab es muy útil en el manejo de la enfermedad de Crohn perianal, y en conjunto con el manejo quirúrgico, son pilares fundamentales en la mejoría clínica de estos pacientes. En la figura 4 se describe un diagrama de flujo con una propuesta de manejo para la enfermedad de Crohn perianal.Figura 4 . Manejo de fístula perianal.
Tratamiento de colitis ulcerativa
La extensión y la severidad son los factores más importantes para definir el manejo y evaluar respuesta a tratamiento en colitis ulcerativa, como lo definió la clasificación de Montreal (tablas 2 y 3). Otros factores a tener en cuenta son el tiempo de evolución de la colitis, la respuesta a tratamientos previos, infecciones gastrointestinales concomitantes, la presencia de menstruación en las mujeres, factores ambientales como el estrés, antecedentes familiares de enfermedad inflamatoria intestinal, el tabaquismo, el uso de antiinflamatorios no esteroideos (AINE´s) y complicaciones como anemia, trombosis y manifestaciones extraintestinales con compromiso articular, ocular o de piel, entre otras (30).
La meta en el manejo de estos pacientes, tanto en enfermedad de Crohn como en colitis ulcerativa es inducir y mantener remisión clínica, y en lo posible lograr una remisión endoscópica de la enfermedad (figura 5). Los medicamentos que se utilizan para el manejo de colitis ulcerativa, se muestran a continuación.
Figura 5. Metas en tratamiento EII.
Ácido 5 aminosalicílico (5-ASA)
A diferencia de la poca evidencia existente en el manejo de enfermedad de Crohn con 5-ASA, su papel en el manejo de colitis ulcerativa con actividad leve y moderada es fundamental. Existen diversos compuestos y presentaciones de 5-ASA, no todos, disponibles en Colombia, los cuales se describen en la tabla 8. Una revisión sistemática demostró que las diferentes preparaciones de 5-ASA orales en dosis equivalentes, incluyendo la sulfasalazina, tienen una exposición sistémica comparable entre ellos (farmacocinética), medida por la excreción urinaria y fecal de los diferentes medicamentos (31). Los agentes tópicos son eficaces dependiendo de la extensión del compromiso colónico.
]]> Tabla 8. Preparaciones de 5 aminosalicilatos.Una reciente revisión sistemática en Cochrane sobre el mantenimiento de remisión en colitis ulcerativa con 5-ASA, incluye 16 estudios con 2479 pacientes, en 11 estudios se comparo con sulfasalazina y en 5 con placebo, y encontraron un OR de 0.47 para falla en mantener remisión clínica o endoscópica en pacientes con 5-ASA comparados con placebo, con un NNT de 6, pero cuando se compara con sulfasalazina el OR es de 1,29, en estudios de 6 meses de duración, sugiriendo que esta última tiene mayor efectividad. Sin embargo, cuando se tienen en cuenta estudios con 12 meses de seguimiento, esta diferencia estadística se pierde. En cuanto a efectos adversos, presentan un perfil muy similar, no hubo diferencias cuando se compararon con placebo, y se encontró que la sulfasalazina tiene un OR de 1,16 con un NNH de 171 y 5-ASA presenta OR de 1,31 con NNH de 78. Algunos estudios fueron heterogéneos, y muchos de ellos utilizaron olsalazina, la cual no es muy bien tolerada y se ha encontrado que hasta 10% de los pacientes con esta medicación presentan diarrea, esto obviamente altera los resultados antes descritos. No obstante, hay que tener en cuenta que los medicamentos 5-ASA son más costosos que la sulfasalazina (32).
En cuanto a la inducción de remisión con 5-ASA en pacientes con colitis ulcerativa activa, se publicó otra revisión sistemática por los mismos autores, incluyendo 21 estudios con 2124 pacientes, 9 de ellos controlados con placebo y 12 comparados con sulfasalazina. Los medicamentos 5 ASA fueron superiores a placebo con un OR de 0,40 para falla a inducir remisión, esta respuesta fue dosis dependiente. Cuando 5 ASA se comparó con sulfasalazina también fue superior, con un OR de 0,83 para falla a inducir remisión clínica y de 0.66 para falla a inducir remisión endoscópica. En cuanto a efectos adversos, no se encontró diferencia con placebo, y los medicamentos 5 ASA fueron mejor tolerados que sulfasalazina. Los autores consideran que la utilización en algunos estudios de dosis altas de 5-ASA, comparado con controles con dosis estándar de sulfasalazina (2-4 g/día), pueden explicar los anteriores resultados (33).
Las anteriores revisiones sistemáticas confirman que los medicamentos 5-ASA son efectivos tanto en inducción como en mantenimiento de remisión, en pacientes con colitis ulcerativa. Para decidir cual 5 ASA utilizar debe tenerse en cuenta que 1 gramo de sulfasalazina equivale a 400 mg de mesalazina, que dosis de sulfasalazina superiores a 4 g/diarios son poco toleradas en el 50% de los pacientes por presentar efectos adversos, el costo de la medicación, la posibilidad de infertilidad en pacientes masculinos y si el individuo ha presentado efectos adversos a la sulfasalazina previamente. También es factor importante determinar la adherencia que los pacientes tengan al medicamento. Se realizó un estudio piloto con dosis única diaria de mesalazina comparado con dosis múltiples, encontrando una mayor adherencia 100% vs. 70% (p: 0,04) a 3 meses de seguimiento. En la ingesta promedio de la medicación formulada también se encontró diferencia significativa 90 vs. 75% (p: 0,02). No hubo diferencias significativas en cuanto a recaída clínica en los dos grupos (34).
Para determinar la dosis con la cual obtener la mejor respuesta con mesalazina, se realizó un estudio en 386 pacientes con colitis ulcerativa leve y moderada activa (ASCEND II), comparando dosis de 4,8 g/día con 2,4 g/día, por 6 semanas, encontrando que el tratamiento fue exitoso en 72% vs. 59% (p: 0,036), lo cual fue significativo. No hubo diferencia significativa en cuanto a eventos adversos (35). Lo anterior confirma la respuesta dosis dependiente, de mesalazina en pacientes con colitis ulcerativa activa.
De otra parte, se diseñó un estudio con mesalazina oral combinada con enemas de mesalazina, y se comparó con un grupo con solo mesalazina, en pacientes con colitis ulcerativa extensa con actividad leve y moderada. Este estudio incluyó 127 pacientes, que recibieron 4 g/día de mesalazina por 8 semanas, y durante las primeras 4 semanas un grupo recibió 1 gramo de mesalazina por enema rectal en la noche y el otro grupo placebo. Los resultados después de 8 semanas de seguimiento fueron: remisión clínica en 64% vs. 43% (p: 0,03), y mejoría clínica en 86% vs. 68% (p: 0,026), respectivamente, lo cual fue significativo. No hubo diferencias en cuanto a efectos colaterales (36).
Ha sido difícil establecer la dosis óptima de mesalazina en el mantenimiento de pacientes con colitis ulcerativa en remisión clínica. Recientemente, un estudio italiano comparó dosis de mesalazina 2,4 g/día vs. 1,2 g/día, en 157 pacientes con remisión clínica. Al año de seguimiento, no hubo diferencia significativa entre los dos grupos de tratamiento en cuanto al número de pacientes que permanecían en remisión clínica (30 vs. 24%), sin embargo los pacientes que recibían dosis de 2,4 g/día, duraron más tiempo en remisión, 175 vs. 129 días (p: 0,001), lo cual fue significativo, los dos esquemas fueron bien tolerados (37).
Recientemente se ha establecido una relación entre el uso de 5 ASA y la disminución del riesgo de cáncer colorrectal en pacientes con enfermedad inflamatoria intestinal, lo mismo se propone con la adición de ácido fólico en dosis de 5 mg en estos pacientes. El mecanismo de quimio prevención atribuido a 5-ASA no es muy conocido, pero se cree que disminuye el recambio epitelial, promueve la apoptosis e inactiva radicales libres, disminuyendo el estrés oxidativo sobre el DNA. Una reciente revisión sistemática de 9 estudios, que evaluaban este aspecto, con 334 casos de cáncer de colon y 140 casos con displasia, encontró un papel protector de medicamentos 5-ASA con un OR: 0.51 para cáncer de colon, pero no demostró ser protector para displasia, con un OR de 1:18, esta última se reportó sólo en 2 de los 9 estudios. Los autores proponen que la dosis mínima de 5-ASA que tiene efecto en quimio prevención es de 1,2 g/día (38).
Corticosteroides
]]> Los corticosteroides son los medicamentos de elección en el manejo de pacientes con colitis ulcerativa con actividad moderada o severa. Desde 1955, Truelove y Witts comprobaron la eficacia de los esteroides en el manejo de estos pacientes, utilizando dosis diaria de cortisona 100 mg. Posteriormente, diversos estudios con prednisona en dosis de 40 mg/día, han demostrado una tasa de remisión clínica en alrededor de 70-90% de los casos, una vez logrado esto, se inicia manejo con medicamentos 5 ASA y se reduce la dosis de prednisona 5 mg/semana hasta que se alcance 20 mg/día, y luego se realiza una disminución gradual de 2,5 mg/semana hasta suspenderla. En caso de no lograr retirar los esteroides por recaída de la enfermedad, los pacientes se consideran dependientes de esteroides y posiblemente van a requerir medicamentos "ahorradores" de esteroides como la azatioprina. Diversos estudios han encontrado una eficacia limitada de los esteroides en el mantenimiento de remisión en pacientes con colitis ulcerativa, además de sus efectos colaterales con el uso crónico, como insuficiencia adrenal y osteoporosis.Los pacientes con colitis ulcerativa activa que no respondan a esteroides orales, o que tengan actividad severa requieren hospitalización y deben ser manejados con esteroides intravenosos a dosis de 300-400 mg/día de hidrocortisona o 40 mg/día de metilprednisolona, logrando tasas de remisión hasta en un 80% de los casos. En caso de no respuesta, deben ser manejados con infliximab o ciclosporina, o por último ser llevados a colectomía. En cuanto a terapia con esteroides tópicos, se ha utilizado budesonida en dosis de 2 mg/día por enemas, sin embargo, no han demostrado ser superior a terapia tópica con 5 ASA (30, 39).
Inmunosupresores
Azatioprina y 6-mercaptopurina
Los análogos de purinas como la azatioprina y la 6-mercaptopurina han sido utilizados por más de 30 años para el mantenimiento de remisión en pacientes con colitis ulcerativa refractaria a manejo con 5 ASA y esteroides, o como "ahorradores" de esteroides en pacientes dependientes de estos. La azatioprina se utiliza en dosis de 2,5 mg/kg, con un inicio de acción lento, tardándose hasta 2-3 meses para lograr un efecto pleno. Algunos autores recomiendan iniciar con dosis de 50 a 100 mg, e ir aumentando 25 mg cada 2 semanas con controles frecuentes de recuento de leucocitos, hasta lograr la dosis adecuada o cuando se presente una disminución de leucocitos hasta 4.000, con el objetivo de prevenir toxicidad. Lo ideal es medir niveles de 6-tioguanina o la actividad de la enzima tiopurina metiltransferasa (TPMT), como se expresó anteriormente, pero es difícil en nuestro medio y no es costo-efectivo.
A pesar de las recomendaciones anteriores y la experiencia que se tiene al respecto es poca la evidencia clínica que soporta el uso de azatioprina en pacientes con colitis ulcerativa, la mayoría son estudios con pocos pacientes, de poca calidad, a diferencia de los estudios que si se tienen con el uso de azatioprina en enfermedad de Crohn. Sin embargo, un estudio italiano prospectivo reciente, en 72 pacientes con colitis ulcerativa activa dependiente de esteroides, los cuales fueron aleatorizados a recibir azatioprina 2 mg/kg/día o mesalazina 3.2 g/día por 6 meses, demostró que 58% de los pacientes con azatioprina lograron remisión clínica y endoscópica, y suspendieron esteroides, comparados con sólo 21% de los que recibieron mesalazina, (OR: 5,26) (40).
Otro punto en discusión es si los pacientes que reciben azatioprina requieren manejo concomitante con 5 ASA. Un estudio griego con 70 pacientes para mantenimiento de remisión de colitis ulcerativa dependiente de esteroides, los cuales se aleatorizaron para recibir solo azatioprina 2,2 mg/kg o combinada con olsalazina 1,5 g/día, y se realizó un seguimiento a 2 años, encontrando que no hubo diferencias en el porcentaje de recaídas ente los dos grupos (18% vs. 19%), se presentaron más efecto adversos con la combinación que con azatioprina sola (41). Los autores proponen no adicionar 5 ASA en pacientes recibiendo azatioprina para mantenimiento de colitis ulcerativa.
Ciclosporina
La ciclosporina es un inhibidor de la enzima citosólica calcineurina, lo cual conduce a una inhibición selectiva de la interleuquina (IL)-2 producida por los linfocitos T. Este medicamento es utilizado como terapia de "rescate" para pacientes con colitis ulcerativa severa que son refractarios al uso de esteroides intravenoso por 7-10 días. La meta es inducir remisión y servir de "puente" a manejo posterior con azatioprina. La dosis tradicional ha sido de 4 mg/kg/día por vía intravenosa, hasta lograr niveles séricos terapéuticos entre 200-400 ng/ml a los 2 días de iniciarse la infusión. Pacientes con síndrome convulsivo no deben recibir la medicación, lo mismo que hipertensos no controlados. Debe tenerse en cuenta los niveles de electrolitos séricos en particular del magnesio, y valores de creatinina y colesterol sérico, niveles por debajo de 120 mg/dL, pueden favorecer la aparición de convulsiones con la infusión del medicamento. Después de 7 días de la infusión y en caso de obtenerse respuesta clínica, los pacientes se deben pasar a ciclosporina oral, y adicionar profilaxis con trimetoprim-sulfametoxasol 160/800 mg para prevenir neumonía por pneumocistis carinii (11).
Un estudio europeo en 74 pacientes con colitis ulcerativa severa y utilizando ciclosporina como terapia de "rescate", comparó las dosis de 4 vs. 2 mg/kg/día, encontrando una respuesta clínica similar de 84,2% vs. 85,7%, con una tasa de colectomía de 13,1% vs. 8,6%, respectivamente. No hubo diferencia significativa entre los dos grupos, pero si se detectaron más efectos adversos como hipertensión arterial (23,7 vs. 8,6%), con la dosis más alta (42).
]]> En una reciente revisión sistemática en Cochrane para determinar la utilidad de ciclosporina A para inducción de remisión en colitis ulcerativa severa, sólo encontraron dos estudios aleatorizados y controlados, que cumplían los criterios de inclusión, uno de ellos controlado con placebo y el otro con metilprednisolona, con escaso número de pacientes. A pesar de la adecuada respuesta a corto plazo de la ciclosporina, sus efectos a largo plazo medidos por el número de pacientes que requieren colectomía no se diferencian de los controles, además de su potencial nefrotoxicidad a largo plazo, por lo cual ponen en duda su utilización en este tipo de pacientes (43).Terapia biológica
Infliximab
A diferencia de la hipótesis de respuesta celular Th 1 en enfermedad de Crohn, lo cual justifica el uso de inhibidores del TNF-a). La respuesta celular en colitis ulcerativa es del tipo Th 2, en la que participan citoquinas como las IL-10, IL-5 e IL- 4, y en mucho menos proporción participa el TNF-a). Sin embargo, se ha encontrado que pacientes con ataques agudos de colitis ulcerativa presenta niveles séricos y fecales elevados de TNF-a), con aumento en las células productoras de esta citoquina, similar a lo que ocurre en la enfermedad de Crohn. De otra parte, se ha establecido que la verdadera acción del Infliximab radica en inducir apoptosis de células inflamatorias que expresan TNF, más que la inactivación directa (44).
Con las hipótesis anteriores, se diseñaron varios estudios con agentes anti-TNF-a, en pacientes con colitis ulcerativa. En un estudio europeo multicéntrico, aleatorizado y doble ciego, en 45 pacientes con colitis ulcerativa severa, que no respondieron a esteroides intravenosos por 7 días, se utilizó infliximab como "terapia de rescate" a dosis única de 5 mg/kg comparado con placebo, encontrando que a 3 meses de seguimiento, 7 pacientes (29%) en el grupo de infliximab y 14 (67%) en el grupo placebo habían requerido colectomía, diferencia que fue significativa (p: 0,017). Los autores concluyen que a pesar del poco número de pacientes en el estudio, el infliximab es un medicamento seguro y efectivo, que puede utilizarse como una alternativa al uso de ciclosporina, con probablemente menos efectos colaterales (45).
Adicionalmente, se publicaron dos estudios aleatorizados, doble ciego y controlados con placebo, denominados ACT 1 y ACT 2 (Active Ulcerative Colitis Trials), en pacientes con colitis moderada o severa, a pesar de manejo convencional con 5 ASA, azatioprina y esteroides. El ACT 1 se realizó en Europa, multicéntrico, con 364 pacientes, se aleatorizaron en tres grupos para recibir infliximab 5 mg/kg, 10 mg/kg o placebo, los cuales se aplicaron en 0, 2 y 6 semanas, y luego cada 8 semanas por 54 semanas de seguimiento. En la semana 8, la respuesta clínica a las dosis mencionadas fue de 69% vs. 61% vs. 37%, respectivamente, diferencia que fue significativa (p <0,001). A la semana 54, la respuesta clínica fue de 45% vs. 44% vs. 20%, (p < 0,001) y la tasa de cicatrización de la mucosa fue de 45% vs. 46% vs. 18% (p < 0,001), las cuales también fueron significativas. No hubo diferencias entre las dosis de 5 y 10 mg/kg. La proporción de eventos adversos como infecciones en los diferentes grupos fue muy similar. El ACT 2 se realizó en Estados Unidos, multicéntrico y con el mismo número de pacientes, el seguimiento se realizó por 30 semanas, y la respuesta clínica con dosis de 5 mg/kg, 10 mg/kg y placebo fue de 47% vs. 60% vs. 26% a 30 semanas de seguimiento, lo cual fue significativo (p < 0,001) (46).
Enfoque de manejo en colitis ulcerativa
En general, los medicamentos mencionados han demostrado ser efectivos en el manejo de colitis ulcerativa y una adecuada selección de los mismos nos va a garantizar un tratamiento adecuado de los pacientes. Otros medicamentos como nicotina, antibióticos, metotrexate, heparina y probióticos, entre otros, no han mostrado resultados contundentes, y potenciales blancos de terapia biológica como inhibidores de IL-2 y anti-CD3, se encuentran en estudios experimentales. Se ha propuesto la pirámide de tratamiento para colitis ulcerativa teniendo en cuenta la severidad de la enfermedad, la cual se presenta en la figura 6.
Figura 6. Pirámide terapéutica en colitis ulcerativa.
]]> Proctitis ulcerativaLos medicamentos 5 ASA tópicos han demostrado ser los más efectivos en el manejo inicial de pacientes con proctitis ulcerativa para inducir remisión, bien se utilizando enemas (1 g/día) o supositorios (500-1000 mg/día), aplicados preferiblemente por la noche. La administración de 5 ASA por vía oral ha sido menos efectiva que por vía tópica en proctitis ulcerativa, sin embargo, en caso de no respuesta, se prefiere la combinación, aunque algunos pacientes no se sienten cómodos con la aplicación rectal de enemas o supositorios. Una alternativa al manejo con 5 ASA, es la aplicación de esteroides tópicos como la budesonida, y en caso de no respuesta solicitar una colonoscopia total para descartar infecciones o extensión proximal, y adicionar esteroides por vía oral, dependiendo de la actividad. Para mantenimiento de remisión, se prefiere utilizar 5 ASA tópico cada 48-72 horas y en caso de recaída, volver al esquema con el cual se logró la remisión inicial. Un diagrama de flujo con el manejo de proctitis ulcerativa se presenta en la figura 7.
Figura 7. Proctitis ulcerativa activa.
Colitis ulcerativa izquierda y extensa
Los pacientes con colitis ulcerativa más allá del recto con actividad leve y moderada deben tratarse con medicamentos 5 ASA oral (mesalazina 4,0 g o su equivalente) o combinado inicialmente (1 mes), con aplicación diaria de enemas de 4g de mesalazina. La combinación ha demostrado ser más efectiva que cada una por separado, como mencionamos previamente. Soy un poco escéptico en la utilidad de enemas de mesalazina como monoterapia en el manejo de colitis izquierda. En individuos con actividad severa, se prefieren utilizar esteroides orales (prednisona 40-60 mg/día o 1 mg/kg/día), con adición de calcio y vitamina D siempre por el riesgo de osteoporosis, y en caso de no respuesta es prudente realizar colonoscopia para descartar extensión proximal, lo cual es raro, o infecciones asociadas por patógenos entéricos como clostridium, amebas, bacterias, lo que ameritaría manejo adicional con antibióticos como metronidazol o ciprofloxacina. Los pacientes que se vuelven dependientes a esteroides orales deben ser manejados con azatioprina y si no responden, adicionar infliximab según los esquemas señalados. Para mantenimiento se prefiere 5 ASA oral, con dosis mínima de 1,2 g/día por su efecto quimioprotector de cáncer colorrectal. No hay consenso en la utilidad de la combinación de azatioprina con medicamentos 5 ASA, para mantenimiento de remisión en pacientes con colitis ulcerativa izquierda o extensa. Un diagrama de flujo con el manejo de colitis ulcerativa izquierda o extensa se presenta en la figura 8.
Figura 8. Colitis ulcerativa izquierda o extensa activa.
Colitis ulcerativa severa
En caso de actividad severa de la enfermedad o no respuesta a esteroides orales, se prefiere manejo intrahospitalario con esteroides intravenosos (hidrocortisona 300-400 mg/día o metilprednisolona 60 mg/día) por 7-10 días, en caso de no respuesta existen dos opciones, utilizar infliximab 5 mg/kg en dosis única o ciclosporina 2 mg/kg/día por 7-10 días, vigilando efectos adversos como se describió previamente. En caso de respuesta adecuada debe continuarse con infliximab y azatioprina según el esquema ya mencionado, o ciclosporina oral asociado a azatioprina. Cuando persiste actividad de la enfermedad a pesar del tratamiento médico de "rescate", el paciente es candidato a colectomía total. En la figura 9 se resume el manejo de colitis ulcerativa severa.
]]>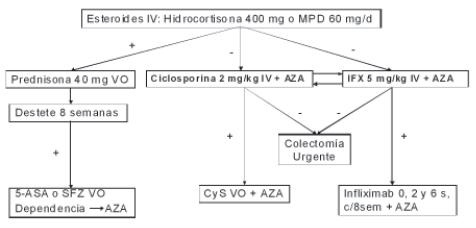
Figura 9. Colitis ulcerativa severa.
Conclusión
La enfermedad inflamatoria intestinal es una entidad no curable, que requiere manejo médico y/o quirúrgico para mantener el control de síntomas, mejorar calidad de vida, minimizar complicaciones y toxicidad de medicamentos, tanto a corto como a largo plazo.
Referencias
1. Satsangi J, Silverberg MS, Vermeire S, Colombel JF. The Montreal classification of inflammatory bowel disease: controversies, consensus, and implications. Gut 2006; 55: 749-753. [ Links ]
2. Langolz E, Munkholm P, Davidsen M, et al. Course of ulcerative colitis: analyses of changes in disease activity over years. Gastroenterology 1994; 107: 3-11. [ Links ]
3. Sandborn WJ, Sartor RB. Medical Therapy for Crohn´s disease. Kirsner´s Inflammatory Bowel Disease 2004; 34: 531-554. [ Links ]
4. Hanauer SB, Sandborn WJ. Management of Crohn´s disease in adults. Am J Gastroenterol 2001; 96: 635-643. [ Links ]
5. Cammá C, Giunta M, Rosselli M, Cottone M. Mesalamine in the maintenance treatment of Crohns Disease: A meta-analysis adjusted for confounding variables. Gastroenterology 1997; 113: 1465-1473. [ Links ]
6. Lochs H, Mayer M, et al. Prophylaxis of postoperative relapse in Crohn´s Disease with mesalamine: European Cooperative Crohn´s Disease study IV. Gastroenterology 2000; 118: 264-273. [ Links ]
7. Akobeng AK, Gardener E. Oral 5-aminosalicylic acid for maintenance of medically-induced remission in Crohn´s Disease (Review). Cochrane database of systematic reviews 2005; (1), CD 003715. [ Links ]
8. Kane SV, Schoenfeld P, Sandborn WJ, Tremaine W, Feagan BG. Systematic review: the effectiveness of budesonide therapy for Crohn´s disease. Aliment Pharmacol Ther 2002; 16(8): 1509-1517. [ Links ]
9. Simms L, Steinhart AH. Budesonide for maintenance of remission in Crohn´s disease (Review). Cochrane database of systematic reviews 2001; (1), CD 002913. [ Links ]
10. Faubion W, Loftus EV, Sandborn WJ, et al. The natural history of corticosteroids therapy for inflammatory bowel disease: a population-based study. Gastroenterology 2001; 121: 255-60. [ Links ]
11. Aberra FN, Lichtenstein GR. Review article: monitoring of immunomodulators in inflammatory bowel disease. Aliment Pharmacol Ther 2005; 21: 307-319. [ Links ]
12. Sandborn W, Sutherland L, Pearson D, et al. Azathioprine or 6-mercaptopurine for induction of remission in Crohn´s disease (Review). Cochrane database of systematic reviews 1998; (3), CD 000545. [ Links ]
13. Pearson DC, May GR, Sutherland LR. Azathioprine for maintenance of remission in Crohn´s disease (Review). Cochrane database of systematic reviews 1998; (4), CD 000067. [ Links ]
14. A Kandiel, A G Fraser, B I Korelitz, C Brensinger, and J D Lewis. Increased risk of lymphoma among inflammatory bowel disease patients treated with azathioprine and 6-mercaptopurine. Gut 2005; 54: 1121-1125. [ Links ]
15. Feagan BG, Fedorak RN, Hanauer SB, et al. Methotrexate for the treatment of Crohn´s disease. N Engl J Med 1995; 332: 292-7. [ Links ]
16. Feagan BG, Fedorak RN, Hanauer SB, et al. A comparison of methotrexate with placebo for the maintenance of remission in Crohn´s disease. N Engl J Med 2000; 342: 1627-32. [ Links ]
17. Targan SR, Hanauer SB, Present DH, Rutgeerts PJ, et al. A short-term study of chimeric monoclonal antibody cA2 to tumor necrosis factor a for Crohn´s disease. N Engl J Med 1997; 337: 1029-35. [ Links ]
18. Hanauer SB, Feagan BG, Rutgeerts P, et al. Maintenance infliximab for Crohn´s disease: the ACCENT I randomised trial. Lancet 2002; 359: 1541-49. [ Links ]
19. Keane J, Gershon S, Wise RP, et al. Tuberculosis associated with infliximab, a tumor necrosis factor alpha-neutralizing agent. N Engl J Med 2001; 345: 1098-1104. [ Links ]
20. Papadakis KA, Shaye OA, Targan SR, Abreu MT, et al. Safety and efficacy of adalimumab (D2E7) in Crohn´s disease patients with an attenuated response to infliximab. Am J Gastroenterol 2005; 100: 75-79. [ Links ]
21. Colombel JF, Sandborn WJ, Rutgeerts P, et al. Adalimumab for maintenance of clinical response and remission in patients with Crohn´s disease: The CHARM trial. Gastroenterology 2007; 132: 52-65. [ Links ]
22. Schawrtz DA, Pemberton JH, Sandborn WJ. Diagnosis and treatment of perianal fistulas in Crohn disease. Ann Intern Med 2001; 135: 906-18. [ Links ]
23. Parks AG, Gordon PH, Hardcastle JD. A classification of fistula in ano. Br J Surg 1976; 63: 1-12. [ Links ]
24. Sandborn WJ, Fazio VW, Feagan BG, Hanauer SB. AGA medical position statement: Perianal Crohn Disease. Gastroenterol 2003; 125: 1508-30. [ Links ]
25. Pearson DC, May GR, Fick GH, Sutherland LR. Azathioprine and 6-mercaptopurine in Crohn disease. A meta-analysis. Ann Intern Med 1995; 123: 132-142. [ Links ]
26. Sandborn WJ, Present DH, Sandler MC, et al. Tacrolimus for the treatment of fistulas in patients with Crohn´s disease. Gastroenterology 2003; 125: 380-388. [ Links ]
27. Present DH, Rutgeerts P, Targan S, Hanauer S, et al. Infliximab for the treatment of fistulas in patients with Crohn´s disease. N Engl J Med 1999; 340: 1398-405. [ Links ]
28. Sands BE, Anderson FH, Rutgeerts P, et al. Infliximab maintenance therapy for fistulizing Crohn´s Disease. N Engl J Med 2004; 350: 876-85. [ Links ]
29. Sands BE, Blank MA, Van Deventer J. Maintenance infliximab does not result in increased abscess development in fistulizing Crohn´s disease: results from the ACCENT II study. Aliment Pharm Ther 2006; 23(8): 1127-36. [ Links ]
30. Hanauer SB. Medical Therapy for Ulcerative colitis. Kirsner´s Inflammatory Bowel Disease 2004; 33: 503-530. [ Links ]
31. Sandborn WB, Hanauer SB. Systematic review: the pharmacokinetics profiles of oral mesalazine formulations and mesalazine prodrugs used in the management of ulcerative colitis. Alim Pharmac Ther 2003; 17: 29-42. [ Links ]
32. Sutherland L, Mc Donald JK. Oral 5-amonisalicylic acid for maintenance of remission in ulcerative colitis (Review). Cochrane Database of Systematic Reviews 2006, (2): CD000544. [ Links ]
33. Sutherland L, Mc Donald JK. Oral 5-amonisalicylic acid for induction of remission in ulcerative colitis (Review). Cochrane Database of Systematic Reviews 2006; (2): CD000543. [ Links ]
34. Kane S, Huo D, Magnanti K. A Pilot Feasibility Study of Once Daily Versus Conventional Dosing Mesalamine for Maintenance of Ulcerative Colitis. Clin Gastroen Hepatol 2003; 1: 170-3. [ Links ]
35. Hanauer SB, Sandborn WJ, Ajayi F, et al. Delayed-release oral mesalamine at 4.8 g/day (800 mg tableta) for the treatment of moderately active ulcerative colitis: The ASCEND trial. Am J Gastroenterol 2005; 100: 2478-2485. [ Links ]
36. Marteau P, Probert CS, Lindaren S, et al. Combined oral and enema treatment with pentasa (mesalazine) is superior to oral therapy alone in patients with extensive mild/moderate active ulcerative colitis: a randomised, double blind, placebo controlled study. Gut 2005; 54: 960-965. [ Links ]
37. Paoluzi OA, Iacopini F, Pica P, et al. Comparison of two different daily dosages (2.4 vs. 1.2 g) of oral mesalazine in maintenance of remission in ulcerative colitis patients: 1-year follow-up study. [ Links ]
38. Velayos FS, Terdiman JP, Walsh JM. Effect of 5-Aminosalicylate use on colorectal cancer and dysplasia risk: A systematic review and metaanalysis of observational studies. Am J Gastroenterol 2005; 100: 1345-1353. [ Links ]
39. Podolsky DK. Inflammatory bowel disease. N Engl J Med 2002; 347(6): 417-429. [ Links ]
40. Ardizzone S, Maconi G, Russo A, Bianchi G, et al. Randomized controlled trial of azathioprine and 5-aminosalicylic acid for treatment of steroid dependent ulcerative colitis. Gut 2006; 55: 47-53. [ Links ]
41. Mantzaris G. Petraki K, et al. A prospective randomized observer -blind- 2 years trial of azathioprine monotherapy vs azathioprine and olsalazine for the maintenance of remission of steroid-dependent ulcerative colitis. Am J Gastroenterol 2004; 99(6): 1123-8. [ Links ]
42. Van Assche G, DHaens G, Rutgeerts P. Randomized, double-blind comparison of 4 mg/kg versus 2 mg/kg intravenous cyclosporine in severe ulcerative colitis. Gastroenterology 2003; 125: 1025-31. [ Links ]
43. Shibolet O, Regushevskaya E, Brezis M, Soares-Weiser K. Cyclosporine A for induction of remission in severe ulcerative colitis. Cochrane Database of Systematic Reviews 2005 (1): CD 004277. [ Links ]
44. D´Haens G. Infliximab for ulcerative colitis: Finally some answers. Gastroenterology 2005; 128: 2161-2166. [ Links ]
45. Jarnerot G, Hertervig E, Curman B, et al. Infliximab as rescue therapy in severe to moderately severe ulcerative colitis: A randomized, placebo-controlled study. Gastroenterology 2005; 128: 1805-1811. [ Links ]
46. Rutgeerts P, Sandborn WJ, Feagan BG, et al. Infliximab for induction and maintenance therapy for ulcerative colitis. N Engl J Med 2005: 353: 2462-76. [ Links ] ]]>