MARÍA EUGENIA MORENO FERNÁNDEZ1, MARÍA TERESA RUGELES LÓPEZ2, CARLOS JULIO MONTOYA GUARÍN3
Grupo de Inmunovirología-Biogénesis, Universidad de Antioquia Correspondencia: María Teresa Rugeles López, Bact, MSc, DSci. Calle 62 # 52 - 59, Torre 2, Lab. 532 Sede de Investigación Universitaria - Universidad de Antioquia Medellín, Colombia Teléfono: 210 65 51 Fax: 210 64 81. Dirección electrónica: mtrugel@catios.udea.edu.co
Recibido: agosto 03 de 2006.
Aceptado: septiembre 25 de 2006.
Las células NK exhiben actividad espontánea contra células tumorales o células infectadas, particularmente por virus. Ellas se caracterizan por la expresión de las moléculas CD16 y CD56, y se subdividen en dos poblaciones, CD16Low/CD56Hi y CD16Hi/CD56Low, que difieren en las citoquinas que producen y en la capacidad citotóxica. La activación de las células NK está regulada por la expresión de receptores inhibidores y activadores que interactúan con diferentes ligandos de las células blanco. La actividad efectora de estas células incluye la lisis de las células blanco por diferentes mecanismos y la producción de citoquinas; las células NK participan por medio de estos factores solubles en diversos procesos fisiológicos, como la hematopoyesis y la regulación de otras células del sistema inmune. Durante la infección por el VIH-1, las células NK ayudan al control de la replicación viral tanto por mecanismos citotóxicos como por la producción de citoquinas, particularmente alfa-quimoquinas. Sin embargo, el VIH-1 ha desarrollado mecanismos para evadir la respuesta antiviral mediada por las células NK. Adicionalmente, esta infección induce anormalidades cuantitativas y funcionales en estas células que pueden presentarse muy temprano en la evolución de la enfermedad y que hacen parte de la inmunosupresión severa característica del SIDA.
PALABRAS CLAVE
CÉLULAS NK
RECEPTORES KIR
RECEPTORES NCR
VIH-1
SUMMARY
NK Cells: characteristics and role during the infection by rype-1 human immunodeficiency virus (HIV-1)
NK cells exhibit spontaneous activity against tumor and infected cells, particularly with virus. They are characterized by the expression of the CD16 and CD56 molecules. Two NK cell subpopulations have been described: CD16Low/CD56Hi and CD16Hi/CD56Low that differ in the cytokines produced and their cytotoxic ability. NK cell activation is regulated by the expression of inhibition and activation receptors, which interact with different ligands on the target cells. The effector activity of these cells includes lysis of target cells by different mechanisms and the production of cytokines; through these soluble factors NK cells participate in diverse physiological processes such as hematopoyesis and regulation of different immune cells. During HIV-1 infection, NK cells participate in the control of viral replication by both, cytotoxic mechanisms and production of cytokines, particularly -chemokines.
]]> However, the HIV-1 has developed mechanisms to evade the antiviral response exerted by NK cells. In addition, HIV-1 infection induces quantitative and functional abnormalities in NK cells that could be developed very early during the evolution of this viral infection contributing to the severe immunosuppression characteristic of AIDS.KEY WORDS
HIV-1
KIR RECEPTORS
NCR RECEPTORS
NK CELLS
INTRODUCCIÓN
Las células asesinas naturales, también conocidas como células NK (del inglés Natural Killer), son una sub-población de linfocitos no T (CD3 negativos) y no B (CD19 negativos) caracterizada por su tamaño grande y los numerosos gránulos citoplasmáticos. Las células NK constituyen entre un 5 y 14% de los mononucleares de sangre periférica, y fenotípicamente han sido caracterizadas por la expresión en su membrana las moléculas CD16 y CD56.1 Funcionalmente estas células se caracterizan porque pueden destruir células tumorales en forma espontánea, es decir, sin haber sido sensibilizadas previamente; además, constituyen una de las primeras líneas de defensa contra los microorganismos patógenos invasores, principalmente los virus.2-4
Las células NK producen citoquinas como IFN-gamma, TNF-alfa, IL-1 beta, IL-4, IL-13, GM-CSF, TGF-beta1, RANTES (CCL5), MIP-1alfa (CCL3) y MIP-1beta(CCL4).<>5 Estos factores solubles juegan un papel importante en la regulación de la hematopoyesis, la supresión no citolítica de la replicación viral y la regulación de las respuestas inmunes innata y adaptativa.2, 6-8
La activación de las células NK está regulada por la expresión de receptores inhibidores y activadores en su membrana citoplasmática. Los receptores inhibidores (iNKR, del inglés Inhibitory Natural Killer Cell Receptors) son específicos para las moléculas del complejo mayor de histocompatibilidad clase I (CMH-I). Los receptores activadores proporcionan la señal de encendido que induce la activación de las células NK durante su interacción con la célula blanco. Adicionalmente, estas células expresan otras moléculas que funcionan como correceptores y que regulan la actividad citolítica y la producción de citoquinas, como las moléculas NKR-P1A (CD161), CD96 y 2B4 (CD244).9-11
]]> Varios modelos clínicos de infección viral resaltan la importancia de las células NK en la salud humana. En particular se ha establecido que las células NK presentan mecanismos efectores que pueden ayudar a controlar la infección por el virus de la inmunodeficiencia humana tipo 1 (VIH-1),3,12 sin embargo, en los individuos infectados por el VIH-1 se han observado alteraciones cuantitativas y funcionales en las células NK,7 las cuales hacen parte del complejo proceso inmunopatogénico característicamente generado por el VIH-1. En esta revisión se describen los aspectos generales más importantes relacionados con la ontogenia y función de las células NK, y el papel que juegan estas células durante la infección por el VIH-1.GENERALIDADES
Origen y morfología de las células NK
Las células NK maduras se producen en la médula ósea a partir de un progenitor linfoide común derivado previamente de la célula madre hematopoyética pluripotencial. En la ontogenia de las células NK se reconocen varios pasos: del progenitor linfoide se diferencia inicialmente un progenitor bipotencial T/NK, que luego se convierte en un progenitor NK, el cual finalmente madura para dar origen a las células NK.5 Morfológicamente las células NK son los linfocitos más grandes (diámetro de 10 a 15 μm) y contienen numerosos gránulos citoplasmáticos, razón por la cual también se denominan linfocitos grandes granulares. Esos gránulos, igual que los de los linfocitos T citotóxicos, contienen perforina, granzimas, proteoglucanos (condroitín sulfato-A) y citoquinas como el factor de necrosis tumoral beta (TNF-beta).13 La mayoría de las células NK se encuentra en los órganos linfoides, especialmente en el bazo; no obstante, también se observa una importante cantidad en el hígado, en la decidua en las mujeres embarazadas y en sangre periférica.14
Fenotipo y marcadores de superficie
Las células NK se han identificado fenotípicamente por la expresión en su superficie de la moléculas CD16 (el receptor de baja afinidad para la fracción Fc de la inmunoglobulina G, o Fcgamma-RIIIA) y CD56 (de la familia de moléculas de adhesión de las células nerviosas, NCAM). Además, otras moléculas de superficie presentes en las células NK son las proteínas de adhesión celular CD2 y LFA-1.13,15
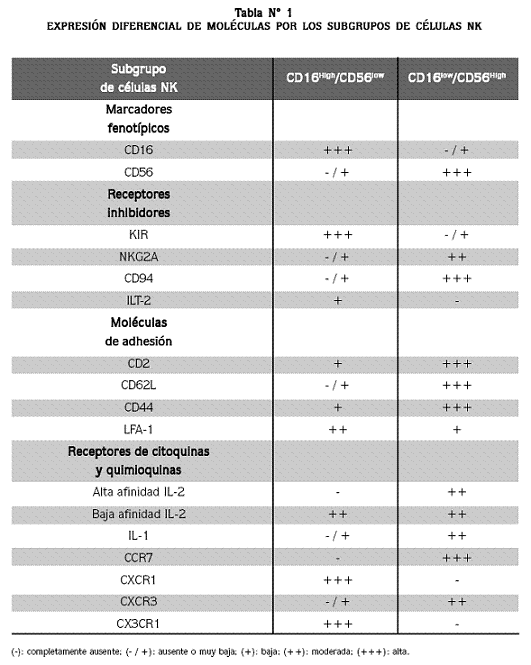
Con base en la expresión de los marcadores de superficie CD16 y CD56 se han descrito dos subpoblaciones de células NK (Tabla N°1), que difieren en las citoquinas y quimioquinas que producen y en su actividad citotóxica.16 La primera subpoblación corresponde a las células CD16Low /CD56Hi, que constituye un 10% de las células NK de sangre periférica y la mayoría de las que se encuentran en los órganos linfoides; esta subpoblación produce grandes cantidades de quimoquinas y citoquinas como el IFN-gamma, expresa el receptor de alta afinidad para la IL-12, no expresan perforina y su actividad citolítica y antitumoral es reducida. La segunda subpoblación corresponde a las células NK CD16Hi/ CD56Low, que representa el 90% de las células NK de sangre periférica, que se caracterizan por producir poco IFN-gamma; estas células NK expresan perforina, son principalmente citotóxicas y participan activamente en el proceso de citotoxicidad celular mediada por anticuerpos (ADCC, del inglés Antibody-Dependent Cellular Cytotoxicity). 8,17
MECANISMOS DE RECONOCIMIENTO
Para la activación funcional de las células NK, ellas inicialmente interactúan con las células blanco (tumorales o infectadas) por medio de los receptores inhibidores y/o activadores (Figura Nº1), y de las moléculas de adhesión.18 La interacción física entre las dos células se establece en una zona particular de la membrana celular, formando lo que se denomina como sinapsis inmunológica. Cuando en esta interacción predominan las señales derivadas de los receptores inhibidores, se resuelve la sinapsis inmunológica y la célula blanco no es destruida. Si por el contrario, prevalecen las señales activadoras, se inicia el proceso de activación de la célula NK que lleva finalmente a la destrucción de la célula blanco.19
]]>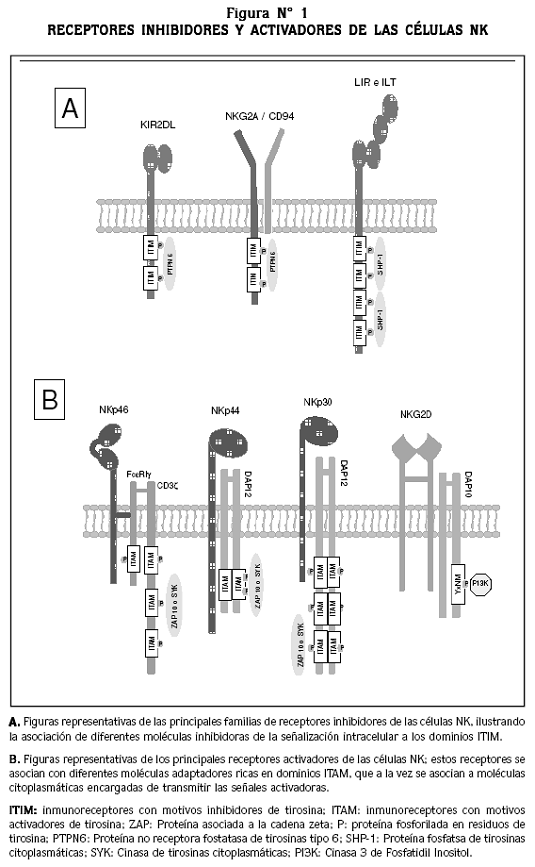
Receptores inhibidores de las células NK (iNKR)
Estos receptores se clasifican en dos grupos: el primer grupo de iNKR incluye los receptores inhibidores de la superfamilia de las inmunoglobulinas (KIR, del inglés Killer Inhibitory Receptors) y la familia de receptores con transcriptos tipo inmunoglobulina (ILT, del inglés Immunoglobulin-Like Transcripts), los cuales reconocen moléculas clásicas del CMH-I. El segundo grupo de iNKR incluye el receptor CD94/ NKG2A (una lectina tipo C), que reconoce moléculas no clásicas del CMH-I.20, 21
RECEPTORES KIR E ILT: los receptores KIR son codificados por una familia de genes ubicados en el cromosoma 19, y son glicoproteínas integrales de membrana que se expresan como monómeros. Se conocen dos isoformas de receptores KIR, inhibidores y activadores, según la longitud de los residuos citoplasmáticos: los KIR inhibidores tienen una cadena intracelular larga (L, del inglés Long) que contiene dominios mediadores de señales inhibidoras tipo ITIM; los KIR activadores tienen una cadena citoplasmática corta (S, del inglés Short) que no transmite señales directamente, sin embargo, esta cadena se asocia con proteínas adaptadoras que tienen dominios generadores de señales activadoras tipo ITAM.9, 22 Además, con base en el número de dominios extracelulares tipo inmunoglobulina, los KIR reciben un número que complementa su clasificación. En consecuencia, se conocen varios grupos de KIR: KIR2DL, KIR2DS, KIR3DL y KIR3DS.
Cuando los KIR inhibidores KIR2DL y KIR3DL son activados, los dominios ITIM (inmunoreceptores con motivos inhibitorios de tirosina) reclutan y activan las fosfatasas de tirosina citoplasmáticas SHP-1 y SHP-2, que defosforilan e inactivan moléculas de señalización de las vías de activación de las células NK, fenómeno que conduce a la inhibición de la actividad citotóxica.19
Los genes que codifican los receptores tipo ILT se encuentran localizados en el cromosoma 19, cerca a los genes para los receptores KIR.23 Estos receptores se expresan en una variedad de células de linaje mieloide y linfoide incluyendo monocitos, macrófagos, células dendríticas, linfocitos B, linfocitos T y células NK.24De esta familia de receptores, en las células NK se encuentran expresados ILT2 e ILT5, que presentan dominios inhibidores tipo ITIM en su porción intracitoplasmática. Los ILT poseen cuatro dominios extracelulares tipo inmunoglobulina, y sus dominios intracelulares se encuentran asociados a las fosfatasas inhibidoras SHP-1.25
Se ha demostrado que algunos de estos receptores inhibidores son específicos para ciertas moléculas del CMH-I, así: KIR2DL1 reconoce las moléculas HLA-Cw 2, 5 y 6; KIR2DL2 reconoce HLA-Cw 1, 3, 7 y 8; KIR2DL4 reconoce HLA-G; ILT2 reconoce HLA-G y el ILT 4 reconoce HLA-F.25
RECEPTORES DE LA FAMILIA 2/CD94: estas moléculas son glicoproteínas de membrana de la familia de las lectinas tipo C; en la membrana celular forman un heterodímero conformado por las proteínas NKG2 y CD94. Tanto NKG2 como CD94 son proteínas codificadas por genes localizados en el cromosoma 12, en una región denominada genes del complejo NK. Las proteínas NKG2 son codificadas por cinco genes distintos: A/B, C, D/F, E y H,20, 26, 27 pero sólo existe un gen para CD94. Mientras que las proteínas NKG2 tienen dominios intracelulares involucrados en la señalización, CD94 carece de residuos citoplasmáticos, lo que hace que no pueda transmitir señales; se considera que la función de CD94 es actuar como una chaperona que facilita el transporte de NKG2 hasta la membrana celular.28
De los receptores NKG2/CD94 se conocen isoformas inhibidoras y activadoras.28 Las isoformas inhibidoras NKG2A/CD94 y NKG2B/CD94, al igual que los KIR, contienen residuos citoplasmáticos largos con dos dominios ITIM responsables de inhibir las señales que conducen a la actividad citotóxica de las células NK. Estos receptores inhibidores son específicos para la molécula HLAE, proteína no clásica del CMH-I.19, 28
Receptores activadores de las células NK
]]> Los receptores activadores de las células NK también se pueden clasificar en dos grupos: los que reconocen moléculas del CMH-I y los que reconocen otros tipos de moléculas.26RECEPTORES ACTIVADORES QUE RECONOCEN MOLÉCULAS DEL CMH-I: estos receptores se dividen en dos subgrupos. En el primero se encuentran los ya mencionados receptores KIR2DS y KIR3DS, que poseen una región intracitoplasmática corta (S); en su región transmembrana presentan residuos de arginina o lisina que les permiten asociarse con proteínas adaptadoras ricas en dominios ITAM, tales como DAP10 y DAP12. Estos ITAM reclutan y activan las cinasas de tirosina Zap70 y SKY, encargadas de continuar con las señales activadoras que hacen que las células NK eliminen las células blanco y secreten citoquinas inmunomoduladoras.22 El receptor KIR2DS reconoce moléculas del HLA-C, mientras que los ligandos para KIR3DS no han sido identificados.9,15,25,26
El segundo grupo incluye los receptores NKG2C y NKG2E que pertenecen a la familia NKG2/CD94; en humanos estos receptores reconocen la molécula HLA-E.26,29 El dominio extracelular de NKG2C y NKG2E posee un alto grado de homología con la secuencia de aminoácidos de los receptores inhibidores de esta misma familia (NKG2A y NKG2B), lo que indica que ambos tipos de receptores pueden reconocer un mismo tipo de molécula, el HLA-E.10
RECEPTORES QUE RECONOCEN OTROS TIPOS DE MOLÉCULAS: existen dos tipos de receptores activadores que reconocen moléculas diferentes a las del CMH-I: el receptor NKG2D y los receptores naturales de citotoxicidad (NCR, del inglés Natural Cytotoxicity Receptors). La molécula NKG2D pertenece a la familia de los receptores NKG2/CD94,15 pero su secuencia de aminoácidos difiere dramáticamente con respecto a la de los otros miembros de esa familia (solo un 25% de homología); además, no se asocia a CD94 y se expresa como un homodímero en la membrana de las células NK.10,25,26 Los ligandos para NKG2D pertenecen a un grupo de moléculas inducidas por estrés celular, como MIC-A y MIC-B, que son expresadas en células tumorales, y la ULPB o proteína de unión UL16, que se expresa en diferentes células. La función de NKG2D depende de su asociación con la subunidad de señalización DAP10/KAP10, que contiene dominios ITAM que reclutan la molécula Cinasa 3 de Fosfatidil Inositol (PIK3) para transmitir las señales que llevan a la activación de las células NK.4,25,26
El grupo de los receptores NCR incluye las moléculas NKp46, NKp30, NKp44 y NKp80, pertenecientes a la superfamilia de las inmunoglobulinas.15 NKp46 y NKp30 se expresan constitutivamente en las células NK, y aparentemente son exclusivas de estas células.
NKp44 no se expresa en células NK inactivas, pero se regula positivamente por la activación con IL-2 y/o IL-12; este receptor también ha sido detectado en los linfocitos Tgd.15, 30 NKp80 fue recientemente identificado en la superficie de las células NK y en una minoría de los linfocitos T CD3+CD56+.
El gen que codifica para NKp46 se encuentra en el cromosoma 19, en una región que contiene genes para varios tipos de receptores de los leucocitos.31,32 Esta molécula presenta dos dominios extracelulares de Ig tipo C2; la región transmembrana contiene un residuo de arginina involucrado en la interacción con las moléculas FceRgI y CD3z, proteínas adaptadoras que contienen dominios ITAM encargados de la transmisión de las señales activadoras.10,15 Se demostró que NKp46 reconoce directamente proteínas virales como la hemaglutinina del virus de influenza y la hemaglutinina y neuraminidasa de los virus Sendai y parainfluenza.26,29
NKp30 es una glicoproteína caracterizada por un dominio extracelular tipo región variable de las inmunoglobulinas, y una región transmembrana que contiene un residuo de arginina.33 El gen que codifica para NKp30 se encuentra en el cromosoma 6, en la región del MHC-II entre los genes para LTB y AIF1.10,15,25,34 La porción citoplasmática de este receptor carece de dominios ITAM, por lo cual para la transmisión de las señales activadoras NKp30 se asociación con la cadena CD3z. Aunque todavía no se conocen sus ligandos, se sabe que NKp30 es el receptor que induce más eficientemente la muerte de células tumorales.
NKp44, al igual que NKp30, es una glicoproteína con un único dominio extracelular tipo región variable de las inmunoglobulinas; el gen que codifica para NKp44 se encuentra en el cromosoma 6.35 Este receptor tampoco contiene ITAMs, pero su porción transmembrana contiene un residuo de lisina que se asocia con el complejo ARAP/DAP12 que presentan un solo ITAM; KARAP/DAP12 es necesario para la expresión en la superficie de NKp44 y para la transmisión de las señales activadoras.10, 15 Debido a que la expresión de NKp44 está restringida a las células NK luego de la activación con IL-12, actualmente se considera que este receptor es el primer marcador específico de la activación de las células NK.36 Además de la activación por citoquinas, se considera que la expresión de NKp44 puede ser inducida por el estrés celular presente en las células tumorales y en las células infectadas por virus.10 Los ligandos específicos para NKp44 no han sido caracterizados.
El gen que codifica para receptor NKp80 se encuentra ubicado en el cromosoma 12, en la región denominada como genes del complejo NK.37 NKp80 se expresa como un dímero y no se encuentra asociado a proteínas con dominios ITAM; su región transmembrana contiene un dominio de lectina tipo C y un aminoácido no polar, mientras que la región citoplasmática contiene dos motivos basados en tirosinas. Se ha postulado que NKp80 funciona más como un correceptor que como un receptor clásico, y que al parecer tiene una acción sinérgica con otros NCR.38
]]> FUNCIONES EFECTORAS DE LAS CÉLULAS NKLos mecanismos efectores de las células NK pueden ser de dos tipos, líticos y no líticos. Los mecanismos líticos incluyen tanto la destrucción directa de las células blanco como el fenómeno de ADCC. La citotoxidad directa puede ser mediada por perforinas y granzimas, o por una apoptosis independiente de estas dos proteínas.39,40 La función efectora no lítica corresponde a la producción de diferentes quimoquinas y citoquinas inmunomoduladoras, por medio de las cuales estas células regulan la hematopoyesis y diferentes células y eventos de la respuesta inmune.41, 42
Citotoxicidad mediadapor perforinas y granzimas
Las células NK destruyen las células blanco por un mecanismo similar al utilizado por los linfocitos T CD8+, el cual involucra la liberación del contenido de los gránulos ricos en perforinas y granzimas. Las perforinas son moléculas que se integran a la membrana celular y forman poros que pueden conducir a una lisis osmótica.43 Las granzimas son proteínas que entran a la célula blanco y activan el programa de apoptosis por varias vías.44 La incorporación de las granzimas dentro de la célula blanco no requiere necesariamente de la acción previa de las perforinas, y puede ser mediada eficiente y rápidamente por endocitosis. Adicionalmente, la granzima B se puede unir al receptor de manosa 6-fosfato formando un complejo que la internaliza.45 Estudios recientes sugieren que tanto las perforinas como las granzimas también pueden formar parte de un complejo macromolecular asociado al proteoglicano serglicina, el cual media la entrada de estas proteínas a la célula blanco.46
Se han descrito 11 tipos de granzimas, de las cuales 5 se han encontrado en los humanos (los tipos A, B, H, K y M).39 La granzima A induce la muerte celular por una vía independiente de las caspasas, pues genera cortes en el DNA de cadena sencilla, causando fragmentación oligonucleosomal del DNA.40,47 La granzima B juega un papel crítico en la activación de la apoptosis por medio de diferentes mecanismos, tales como: a) induciendo la liberación de la deoxirribonucleasa activada por caspasas (CAD), enzima que directamente ocasiona fragmentación del DNA; b) ocasionando la ruptura enzimática de la procaspasa, paso necesario para activar la caspasa 3 e iniciar la apoptosis por esta vía; y c) activando la proteína proapoptótica BID, para que se transloque a la mitocondria y libere el citocromo C, molécula que también activa la vía de las caspasas.48,49 Grandes niveles de granzima M son expresados en las células NK; ésta es una proteasa que, en presencia de perforinas, tiene la capacidad de mediar la muerte celular en una forma independiente de caspasas que no incluye fragmentación del DNA ni alteraciones en la mitocondria.50 La granzima M produce cortes después de residuos alifáticos tales como metionina, norleucina y leucina. La granzima H es una proteasa que hace cortes después de residuos aromáticos y causa una muerte celular caracterizada por la rápida externalización de fosfatidilserina, condensación nuclear y colapso celular.
Inducción de apoptosis porreceptores de muerte celular
La apoptosis por los receptores de muerte celular involucra la activación de enzimas que digieren el DNA. Esta forma de apoptosis se inicia cuando una célula blanco expresa un receptor de muerte celular como Fas, mientras que la célula efectora (célula NK en este caso) expresa el ligando denominado FasL; la interacción de estas moléculas hace que la porción intracelular de Fas se una a un factor adaptador intermediario denominado FADD (del inglés Fas-Associated Death Domain), interacción molecular que lleva a la activación de la vía de las caspasas.48,49 Inicialmente, este proceso activa las caspasas 8 y 10, las que a su vez activan directamente otras caspasas efectoras como la caspasa 3; esta última proteína actúa sobre una amplia variedad de sustratos, incluyendo proteínas de la envoltura nuclear y nucleasas, para iniciar la fragmentación del DNA y el daño nuclear característicos de la apoptosis.48 Por otro lado, la caspasa 8 activa al factor propapoptótico BID, el cual interactúa con la proteína BAX que se encuentra insertada en la membrana mitocondrial, para permitir la liberación del citocromo C; este citocromo activa la caspasa 9, que también recluta las caspasas efectoras 3 y 6.49 La muerte celular se produce como consecuencia de las alteraciones en el núcleo, en la membrana plasmática y en las mitocondrias. En el núcleo se degrada el DNA, y se condensa la cromatina para formar aglomerados que se desplazan hacia la membrana nuclear. 15
Citotoxicidad celular dependiente de anticuerpos (ADCC)
La molécula CD16 ó FcRgammaIII es expresada densamente en la mayoría de las células NK, y se une con baja afinidad a la fracción Fc de la inmunoglobulina (Ig)G que se encuentre unida a epítopes localizados en la superficie de una célula, pero no a las moléculas de IgG libre. La interacción CD16/IgG unida a las células genera en las células NK las señales intracelulares de activación dependientes de las proteínas cinasas de tirosina ZAP-70, y de SYK; estas cinasas fosforilan tirosinas de la fosfolipasa C gama (PLC-gamma), enzima que una vez se activa corta fosfoinositoles localizados en la cara interna de la membrana celular. De esta reacción se generan el diacylglicerol (DAG) y el inositol trifosfato (IP3). El IP3 interactúa con sus receptores que se encuentran en la membrana del retículo endoplásmico para activar la liberación de calcio al citoplasma, incrementando el calcio intracelular hasta los niveles requeridos para inducir la secreción hacia la célula blanco de los gránulos ricos en moléculas mediadoras de citotoxicidad.51
Producción de citoquinas
]]> Las células NK representan una fuente importante de citoquinas que participan en la regulación de la hematopoyesis y de la respuesta inmune; los factores solubles más importantes que son secretados por las células NK son: IFN-gamma, TNF-alfa, G-CSF, IL-4, IL-5, IL-8, IL-10, quimoquinas como MIP-1a, MIP-1beta, RANTES, MDC y linfotactina, y las a defensinas. Algunos de estos factores son necesarios en la respuesta inicial de control de los microorganismos patógenos, así como para la promoción de la respuesta inmune adaptativa específica y de larga vida contra ellos.42,52LAS CÉLULAS NK EN LA INFECCIÓN POR EL VIH-1
Papel de las células NK en el control de la infección por el VIH-1
Diferentes estudios han aportado evidencias sobre el potencial que tienen las células NK para ayudar a controlar la infección por el VIH-1, tanto por mecanismos citolíticos como no líticos.8,53 Entre estos últimos se destaca la capacidad de las bquimoquinas MIP-1alfa, MIP-1beta y RANTES, secretadas por las células NK activadas, para bloquear la infección por los virus que utilizan como correceptor la molécula CCR5, denominados cepas R5 trópicas; en este bloqueo las beta-quimoquinas mencionadas inhiben competitivamente la unión de la glicoproteína de envoltura gp120 del VIH-1 al correceptor CCR5 (receptor natural para esas beta-quimoquinas).2,54-56
La respuesta citotóxica mediada por los linfocitos T CD8+ y las células NK es, aparentemente, muy fuerte durante las primeras etapas de la infección por el VIH-1. Las proteínas Nef, Tat y Vpu del VIH-1 tienen la capacidad de regular negativamente la expresión de moléculas del CMH-I, en particular del HLA-A y HLA-B; esta regulación se puede presentar por: a) internalización de estas moléculas; b) inhibición de la transcripción de los genes del CMH-I; y c) retención de las cadenas nacientes en el retículo endoplásmico. Esta regulación negativa disminuye la capacidad que tienen los linfocitos T citotóxicos CD8+ para reconocer y destruir las células infectadas por el VIH-1.57,58 Sin embargo, la baja expresión de estas moléculas debería hacer que las células infectadas fueran susceptibles a la destrucción mediada por las células NK, pues se pierden los ligandos para muchos de los iNKR. No obstante, la susceptibilidad de las células infectadas por el VIH-1 a la lisis dependiente de las células NK parece no ser muy notable, pues se ha demostrado que proteínas del VIH-1 inducen un aumento en la expresión de las moléculas HLA-C y HLA-E, las que pueden ser reconocidas por los Inc. y disminuyen la capacidad de las células NK para producir una respuesta citotóxica efectiva.59,60
Las células NK, en conjunto con los anticuerpos tipo IgG específicos contra proteínas del VIH-1, pueden destruir células infectadas por este virus por medio de la ADCC. Estos anticuerpos reconocen proteínas virales expresadas en la superficie de las células infectadas, y luego se unen por la fracción FC a la molécula CD16 expresada en la célula NK; esta interacción genera las señales de activación requeridas para que las células NK secreten el contenido de sus gránulos y destruyan la célula blanco.61 Las proteínas virales de envoltura (gp120 y gp41), expresadas en las células infectadas con replicación activa, son los principales antígenos reconocidos por los anticuerpos IgG para desencadenar la ADCC.62,63 La ADCC es clínicamente importante durante la infección por el VIH-1, pues se ha observado que una fuerte actividad de ADCC se asocia con una mayor duración del estado clínico asintomático y una mejor evolución clínica.64
Otro mecanismo por el cual las células NK pueden destruir células infectadas por el VIH-1 es la inducción de ligandos para los NCR mediada por proteínas del virus. Vieillar et al demostraron que la proteína de envoltura gp41 y su precursor gp160 tienen la capacidad de inducir la expresión de un ligando para NKp44 en los linfocitos T CD4+ infectados, aumentando la susceptibilidad de esas células a la lisis mediada por células NK activadas.12
Recientemente se demostró una actividad significativamente aumentada de las células NK en individuos expuestos al VIH-1 que no se infectaron (expuestos seronegativos, ESN); en particular, las células NK de estos individuos presentaban un aumento en la secreción de IFN-gamma, y de otras citoquinas como TNF- alfa y beta-quimioquinas.53,65 El IFN-gamma, tiene actividad anti-VIH-1 directa, mediada principalmente por un antagonismo de la transactivación viral inducida por la proteína viral Tat.66 Además, el IFN-gamma es importante para la activación de la respuesta inmune adaptativa y se ha propuesto como uno de los mecanismos responsables de la resistencia natural a la infección por el VIH-1.67
Efecto de la infección por el VIH-1 sobre el fenotipo y función de las células NK
La infección por el VIH-1 y las proteínas de este virus inducen diversas anormalidades cuantitativas, fenotípicas y funcionales en las células NK,3,8,68,69 entre las cuales se encuentran la modulación de la expresión de moléculas superficie, la producción de citoquinas y quimoquinas, y la actividad citolítica, alteraciones que en conjunto llevan a un funcionamiento deficiente de las células NK.8
]]> En los individuos infectados con el VIH-1 no se ha logrado observar consistentemente una deficiencia cuantitativa de las células NK.8,69 En nuestra evaluación periódica de las células de la inmunidad innata en individuos crónicamente infectados por el VIH-1, hemos logrado definir que en ellos existe una deficiencia en el porcentaje y número absoluto de las células NK de sangre periférica, alteración que es significativa en los pacientes que no reciben terapia antirretroviral, o en los que tienen este tratamiento pero no controlan la replicación del VIH-1 (Figura Nº 2; Montoya et al, resultados preliminares aún no publicados). Esto sugiere que una replicación viral activa puede conducir a una disminución en la frecuencia de las células NK de sangre periférica, por mecanismos aún no establecidos pero que pueden involucrar: a) la migración de las células NK a los órganos linfoides, sitios de mayor replicación viral; b) inducción de apoptosis por proteínas del virus o por hiperactivación inmunológica; c) infección y lisis directa de las células NK. Nuestros estudios también han permitido definir que las células NK de sangre periférica de los individuos infectados con el VIH-1 tienen una mayor expresión del marcador de activación CD69, cuando se compara con las células NK de sujetos sanos no infectados; este hallazgo soporta la hiperactivación inmunológica como un posible mecanismo de alteración cuantitativa y funcional de las células NK en esta infección.Además, la infección por el VIH-1 de un subgrupo de células NK que expresan CD4 y CCR5 fue reportada recientemente.7
Una anormalidad en la frecuencia de las subpoblaciones de células NK en sangre periférica se ha demostrado en los infectados por el VIH-1 que tienen cargas virales elevadas.17 Característicamente, ellos presentan una disminución significativa en la frecuencia de las células NK CD16low/CD56Hi (subpoblación inmunorreguladora) y una expansión de la subpoblación de células CD16Hi/CD56Low (subpoblación citotóxica); sin embargo, estas células NK anormalmente expandidas exhiben deficiente actividad citotóxica, baja producción de citoquinas, aumento en la expresión de receptores inhibidores (KIR2DL2 e ILT2) y baja expresión de los NCR activadores (NKp30, NKp44 y NKp46).3 La disminución en la expresión de los NCR se ha asociado con un aumento en la producción de TGF-beta, citoquina que regula negativamente la expresión de estos receptores.70 Esta alteración fenotípica y funcional se ha asociado con la mayor frecuencia de infecciones oportunistas y cáncer en estos individuos. No obstante, aunque no se ha establecido claramente como se modula la expresión de estos receptores durante la evolución de la infección por el VIH-1, se ha observado que los pacientes VIH-1+ que reciben terapia antirretroviral por más de dos años restablecen la frecuencia normal de las dos subpoblaciones de células NK, aunque la recuperación funcional de ellas no es completa.8
En los infectados por el VIH-1 se ha demostrado que las células NK secretan menor cantidad de las beta-quimoquinas que son ligandos naturales del correceptor CCR5, fenómeno que impide el bloqueo a la entrada del virus que normalmente pueden ejercer estas citoquinas.3 Esta anormalidad en la producción de quimioquinas y citoquinas como el IFN-gamma se correlaciona con la carga viral plasmática.68
Se han descubierto otros mecanismos más complejos de alteración de la función de las células NK, los que son mediados por las proteínas del VIH-1. Como ejemplo, la proteína viral Tat inhibe el flujo de calcio intracelular, y de esta forma impide la lisis de las células infectadas mediada por las células NK; un incremento en el calcio intracelular es necesario para la desencadenar la degranulación y secreción de las enzimas líticas por las células NK.71
CONCLUSIÓN
Las células NK hacen parte importante de los mecanismos efectores de la inmunidad innata, contribuyendo activamente al control de las células tumorales y de las infectadas con microorganismos intracelulares. Numerosos estudios indican que la actividad citolítica de las células NK se asocia con el control de la viremia en pacientes infectados con el VIH-1. Adicionalmente, mecanismos efectores de estas células, como la producción de IFN-gamma, se han postulado entre los factores que previenen el establecimiento de la infección en individuos expuestos seronegativos. De hecho, el papel crucial que pueden jugar estas células en el control de la infección por el VIH-1, en conjunto con otras células de la inmunidad innata, se destaca si se tiene en cuenta que la respuesta inmune específica está significativamente suprimida en los pacientes infectados por la eliminación masiva de linfocitos T CD4+. Sin embargo, varios estudios demostraron alteraciones cuantitativas y funcionales en las células NK en individuos infectados con el VIH-1; desafortunadamente los mecanismos responsables de estas alteraciones no están claramente establecidos, y deben ser objeto de estudios futuros que permitan establecer estrategias terapéuticas que potencien la respuesta inmune, incluyendo la actividad de las células NK. Considerando la importancia que tienen estas células durante la fase temprana de la respuesta anti-VIH-1, no es sorprendente que los virus hayan desarrollado mecanismos de evasión de la respuesta antiviral de las células NK, los cuales también deben ser claramente definidos para poder modularlos.
REFERENCIAS
1. Bueno JC, Cadavid AP. Células citotóxicas y mecanismos de citotoxicidad. In: Rugeles MT, Patiño PJ, editors. Inmunología. Una ciencia activa. Medellín: Biogénesis Fondo Editorial; 2004. p. 219-238. [ Links ]
2. Kottilil S, Chun TW, Moir S, Liu S, Mclaughlin M, Hallahan CW, et al. Innate immunity in human immunodeficiency virus infection: effect of viremia on natural killer cell function. J Infect Dis 2003;187: 1038-1045. [ Links ]
3. Ahmad A, Ahmad R. HIV's evasion of host's NK cell response and novel ways of its countering and boosting anti-HIV immunity. Curr HIV Res 2003; 1: 295-307. [ Links ]
4. Moretta L, Biassoni R, Bottino C, Mingari MC, Moretta A. Natural killer cells: a mystery no more. Scand J Immunol 2002; 55: 229-232. [ Links ]
5. Yplpua,a WM, Kin S, French AR. The dynamic life of natural killer cells. Annu Rev Immunol 2004; 22: 405-429. [ Links ]
6. Montoya CJ, Rugeles MT, Landay Y AL. The innate immune system: prospective for a new HIV immunotherapy. Anuario de Enfermedades Infecciosas 2004; 2: 9-29. [ Links ]
7. Mavilio D, Benjamin J, Daucher M, Lombardo G, Kottilit S, Planta MA, et al. Natural killer cells in HIV-1 infection: dichotomous effects of viremia on inhibitory and activating receptors and their functional correlates. Proc Natl Acad Sci U S A 2003;100: 15011-15016. [ Links ]
8. Fauci AS, Mavilio D, Kottilill S. NK cells in HIV infection: paradigm for protection or targets for ambush. Nat Rev Immunol 2005; 5: 835-843. [ Links ]
9. Moretta L, Biassoni R, Bottino C, Cantoni C, Pende D, Mingari MC, et al. Human NK cells and their receptors. Microbes Infect 2002; 4: 1539-1544. [ Links ]
10. Biassoni R, Cantoni C, Falco M, Pende D, Millo R, Moretta L, et al. Human natural killer cell activating receptors. Mol Immunol 2000; 37: 1015-1024. [ Links ]
11. Galiani MD, Aguado E, Tarazona R, Romero P, Molina I, Santamaria M, et al. Expression of killer inhibitory receptors on cytotoxic cells from HIV-1-infected individuals. Clin Exp Immunol 1999; 115: 472-476. [ Links ]
12. Vieillard V, Strominger JL, Debre P. NK cytotoxicity against CD4+ T cells during HIV-1 infection: a gp41 peptide induces the expression of an NKp44 ligand. Proc Natl Acad Sci U S A 2005;102: 10981-10986. [ Links ]
13. Moretta A, Bottino C, Mingari MC, Biassoni R, Moretta L. What is a natural killer cell? Nat Immunol 2002; 3: 6-8. [ Links ]
14. Abbas AK, Lichtman AH. Innate Immunity. In: Abbas AK, Lichtman AH, editors. Cellular and Molecular Immunology. Fifth Edition ed. Philadelphia: Elsevier Science; 2003. p. 289-292. [ Links ]
15. Moretta A, Bottino C, Vitale M, Pende D, Cantoni C, Mingari MC, et al. Activating receptors and coreceptors involved in human natural killer cell-mediated cytolysis. Annu Rev Immunol 2001;19: 197-223. [ Links ]
16. Cooper MA, Fehniger TA, Caligiuri MA. The biology of natural killer-cell subsets. Trends Immunol 2001; 22: 633-640. [ Links ]
17. Mavilio D, Lombardo G, Benjamin J, Kim D, Follman D, Marcenaro E, et al. Characterization of CD56-/CD16+ natural killer (NK) cells: a highly dysfunctional NK subset expanded in HIV-infected viremic individuals. Proc Natl Acad Sci U S A 2005; 102: 2886-2891. [ Links ]
18. Timonen T, Helander TS. Natural killer cell-target cell interactions. Curr Opin Cell Biol 1997; 9: 667-673. [ Links ]
19. Backstrom E, Kristensson K, Ljunggren HG. Activation of natural killer cells: underlying molecular mechanisms revealed. Scand J Immunol 2004; 60:14-22. [ Links ]
20. Lanier LL. NK cell receptors. Annu Rev Immunol 1998; 16: 359-393. [ Links ]
21. Moretta L, Bottino C, Pende D, Mingari MC, Biassoni R, Moretta A. Human natural killer cells: their origin, receptors and function. Eur J Immunol 2002; 32: 1205-1211. [ Links ]
22. Djeu JY, Jiang K, Wei S. A view to a kill: signals triggering cytotoxicity. Clin Cancer Res 2002; 8: 636-640. [ Links ]
23. Borges L, Hsu ML, Fanger N, Kubin M, Cosman D. A family of human lymphoid and myeloid Ig-like receptors, some of which bind to MHC class I molecules. J Immunol 1997;159: 5192-5196. [ Links ]
24. Colonna M, Nakajima H, Navarro F, Lopez-Botet M. A novel family of Ig-like receptors for HLA class I molecules that modulate function of lymphoid and myeloid cells. J Leukoc Biol 1999; 66: 375-381. [ Links ]
25. Biassoni R, Cantoni C, Pende D, Sivori S, Parolini S, Vitale M, et al. Human natural killer cell receptors and co-receptors. Immunol Rev 2001; 181: 203-214. [ Links ]
26. Diefenbach A, Raulet DH. Strategies for target cell recognition by natural killer cells. Immunol Rev 2001;181: 170-184. [ Links ]
27. Long EO. Regulation of immune responses through inhibitory receptors. Annu Rev Immunol 1999;17: 875-904. [ Links ]
28. Wada H, Matsumoto N, Maenaka K, Suzuki K, Yamamoto K. The inhibitory NK cell receptor CD94/NKG2A and the activating receptor CD94/NKG2C bind the top of HLA-E through mostly shared but partly distinct sets of HLA-E residues. Eur J Immunol 2004; 34: 81-90. [ Links ]
29. Arase H, Lanier LL. Virus-driven evolution of natural killer cell receptors. Microbes Infect 2002; 4: 1505-1512. [ Links ]
30. Vitale M, Bottino C, Sivori S, Sanseverino L, Castriconi R, Marcenaro E, et al. NKp44, a novel triggering surface molecule specifically expressed by activated natural killer cells, is involved in non-major histocompatibility complex-restricted tumor cell lysis. J Exp Med 1998;187: 2065-2072. [ Links ]
31. Pessino A, Sivori S, Bottino C, Malaspina A, Morelli L, Moretta L, et al. Molecular cloning of NKp46: a novel member of the immunoglobulin superfamily involved in triggering of natural cytotoxicity. J Exp Med 1998; 188: 953-960. [ Links ]
32. Barten R, Torkar M, Haude A, Trowsdale J, Wilson MJ. Divergent and convergent evolution of NK-cell receptors. Trends Immunol 2001; 22: 52-57. [ Links ]
33. Pende D, Parolini S, Pessino A, Sivori S, Augugliaro R, Morelli L, et al. Identification and molecular characterization of NKp30, a novel triggering receptor involved in natural cytotoxicity mediated by human natural killer cells. J Exp Med 1999; 190: 1505-1516. [ Links ]
34. Neville MJ, Campbell RD. A new member of the Ig superfamily and a V-ATPase G subunit are among the predicted products of novel genes close to the TNF locus in the human MHC. J Immunol 1999; 162: 4745-4754. [ Links ]
35. Cantoni C, Bottino C, Vitale M, Pessino A, Augugliaro R, Malaspina A, et al. NKp44, a triggering receptor involved in tumor cell lysis by activated human natural killer cells, is a novel member of the immunoglobulin superfamily. J Exp Med 1999; 189: 787-796. [ Links ]
36. Ferrini S, Miescher S, Zocchi MR, Von Fliedner V, Moretta A. Phenotypic and functional characterization of recombinant interleukin 2 (rIL 2)-induced activated killer cells: analysis at the population and clonal levels. J Immunol 1987; 138: 1297-1302. [ Links ]
37. Renedo M, Arce I, Rodriguez A, Carretero M, Lanier LL, Lopez-Botet M, et al. The human natural killer gene complex is located on chromosome 12p12-p13. Immunogenetics 1997; 46: 307-311. [ Links ]
38. Vitale M, Falco M, Castriconi R, Parolini S, Zambello R, Semenzato G, et al. Identification of NKp80, a novel triggering molecule expressed by human NK cells. Eur J Immunol 2001; 31: 233-242. [ Links ]
39. Smyth MJ, Cretney E, Kelly JM, Westwood JA, Street SE, Yagita H, et al. Activation of NK cell cytotoxicity. Mol Immunol 2005; 42: 501-510. [ Links ]
40. Lieberman J, Fan Z. Nuclear war: the granzyme Abomb. Curr Opin Immunol 2003; 15: 553-559. [ Links ]
41. Loza MJ, Perussia B. The IL-12 signature: NK cell terminal CD56+high stage and effector functions. J Immunol 2004; 172: 88-96. [ Links ]
42. Robertson MJ. Role of chemokines in the biology of natural killer cells. J Leukoc Biol 2002; 71:173-183. [ Links ]
43. Podack ER. Functional significance of two cytolytic pathways of cytotoxic T lymphocytes. J Leukoc Biol 1995; 57: 548-552. [ Links ]
44. Simon MM, Hausmann M, Tran T, Ebnet K, Tschopp J, Thahla R, et al. In vitro- and ex vivo-derived cytolytic leukocytes from granzyme A x B double knockout mice are defective in granule-mediated apoptosis but not lysis of target cells. J Exp Med 1997;186:1781-1786. [ Links ]
45. Trapani JA, Browne KA, Smyth MJ, Jans DA. Localization of granzyme B in the nucleus. A putative role in the mechanism of cytotoxic lymphocyte-mediated apoptosis. J Biol Chem 1996; 271: 4127-4133. [ Links ]
46. Metkar SS, Wang B, Aguilar-Santelises M, Raja SM, Uhlin-Hansen L, Podack E, et al. Cytotoxic cell granule-mediated apoptosis: perforin delivers granzyme B-serglycin complexes into target cells without plasma membrane pore formation. Immunity 2002; 16: 417-428. [ Links ]
47. Beresford PJ, Xia Z, GreenberG AH, Lieberman J. Granzyme A loading induces rapid cytolysis and a novel form of DNA damage independently of caspase activation. Immunity 1999;10: 585-594. [ Links ]
48. Abbas AK, Lichtman AH. Immunologic Tolerance. In: Abbas AK, Lichtman AH, editors. Cellular and Molecular Immunology. Fifth Edition ed. Philadelphia: Elsevier Science; 2003. p. 227-230. [ Links ]
49. King KL, Cidlowski JA. Cell cycle regulation and apoptosis. Annu Rev Physiol 1998; 60: 601-617. [ Links ]
50. Kelly JM, Waterhouse NJ, CretneY E, Browne KA, Ellis S, Trapani JA, et al. Granzyme M mediates a novel form of perforin-dependent cell death. J Biol Chem 2004; 279: 22236-22242. [ Links ]
51. Jacobs R, Heiken H, Schmidt RE. Mutual interference of HIV and natural killer cell-mediated immune response. Mol Immunol 2005; 42: 239-249. [ Links ]
52. Fehniger TA, Carson WE, Caligiuri MA. Costimulation of human natural killer cells is required for interferon gamma production. Transplant Proc 1999; 31: 1476-1478. [ Links ]
53. Montoya CJ, Velilla PA, Chougnet C, LandaY AL, Rugeles MT. Increased IFN-gamma production by NK and CD3+/CD56+ cells in sexually HIV-1-exposed but uninfected individuals. Clin Immunol 2006; 120: 138-146. [ Links ]
54. Oliva A, Kinter AL, Vaccarezza M, Rubbert A, Catanzaro A, Moir S, et al. Natural killer cells from human immunodeficiency virus (HIV)-infected individuals are an important source of CC-chemokines and suppress HIV-1 entry and replication in vitro. J Clin Invest 1998;102: 223-231. [ Links ]
55. Fehniger TA, Herbein G, Yu H, Parra MI, Bernstein ZP, O'brien WA, et al. Natural killer cells from HIV-1+ patients produce C-C chemokines and inhibit HIV-1 infection. J Immunol 1998;161: 6433-6438. [ Links ]
56. Choe H, Farzan M, Sun Y, Sullivan N, Rollins B, Ponath PD, et al. The beta-chemokine receptors CCR3 and CCR5 facilitate infection by primary HIV-1 isolates. Cell 1996; 85: 1135-1148. [ Links ]
57. Piguet V, Trono D. Living in oblivion: HIV immune evasion. Semin Immunol 2001;13: 51-57. [ Links ]
58. Cohen GB, Gandhi RT, Davis DM, Mandelboim O, Chen BK, Strominger JL, et al. The selective downregulation of class I major histocompatibility complex proteins by HIV-1 protects HIV-infected cells from NK cells. Immunity 1999;10: 661-671. [ Links ]
59. Uhrberg M, Valiante NM, Shum BP, Shilling HG, Lienert-Weidenbach K, Corliss B, et al. Human diversity in killer cell inhibitory receptor genes. Immunity 1997; 7: 753-763. [ Links ]
60. Malnati MS, Lusso P, Ciccone E, Moretta A, Moretta L, Long EO. Recognition of virus-infected cells by natural killer cell clones is controlled by polymorphic target cell elements. J Exp Med 1993; 178: 961-969. [ Links ]
61. Ruggeri L, Capanni M, Tosti A, Urbani E, Posati S, Aversa F, et al. Innate immunity against hematological malignancies. Cytotherapy 2002; 4: 343-346. [ Links ]
62.Tyler DS, Lyerly HK, Weinhold KJ. Anti-HIV-1 ADCC. AIDS. Res Hum Retroviruses 1989; 5: 557-563. [ Links ]
63. Tanneau F, Mcchesney M, Lopez O, Sansonetti P, Montagnier L, Riviere Y. Primary cytotoxicity against the envelope glycoprotein of human immunodeficiency virus-1: evidence for antibodydependent cellular cytotoxicity in vivo. J Infect Dis 1990; 162: 837-843. [ Links ]
64. Ahmad A, Morisset R, Thomas R, Menezes J. Evidence for a defect of antibody-dependent cellular cytotoxic (ADCC) effector function and anti-HIV gp120/41-specific ADCC-mediating antibody titres in HIV-infected individuals. J Acquir Immune Defic Syndr 1994;7: 428-437. [ Links ]
65. Scott-Algara D, Truong LX, Versmisse P, David A, Luong TT, Nguyen NV, et al. Cutting edge: increased NK cell activity in HIV-1-exposed but uninfected Vietnamese intravascular drug users. J Immunol 2003;171: 5663-5667. [ Links ]
66. Emilie D, Maillot MC, Nicolas JF, Fior R, Galanaud P. Antagonistic effect of interferon-gamma on tatinduced transactivation of HIV long terminal repeat. J Biol Chem 1992; 267: 20565-20570. [ Links ]
67. Clerici M, Clivio A, Shearer GM. Resistance to HIV infection: the genes are only part of the solution. Trends Microbiol 1997; 5: 2-4. [ Links ]
68. Kottilil S. Natural killer cells in HIV-1 infection: role of NK cell-mediated non-cytolytic mechanisms in pathogenesis of HIV-1 infection. Indian J Exp Biol 2003; 41: 1219-1225. [ Links ]
69. Douglas SD, Durako SJ, Tustin NB, Houser J, Muenz L, Starr SE, et al. Natural killer cell enumeration and function in HIV-infected and high-risk uninfected adolescents. AIDS. Res Hum Retroviruses 2001; 17: 543-552. [ Links ]
70. Lotz M, Seth P. TGF beta and HIV infection. Ann N Y Acad Sci 1993; 685: 501-511. [ Links ]
71. Zocchi MR, Rubartelli A, Morgavi P, Poggi A. HIV-1 Tat inhibits human natural killer cell function by blocking L-type calcium channels. J Immunol 1998; 161: 2938-2943. [ Links ] ]]>