Approach to transfusion support in patients with positive compatibility tests and in those with autoimmune hemolytic anemia
JULIÁN MIGUEL ARISTIZÁBAL ARISTIZÁBAL1, JOSÉ DOMINGO TORRES2
Recibido: noviembre 16 de 2006
Aceptado: julio 03 de 2007
RESUMEN
Es frecuente la presencia de pruebas de compatibilidad positivas en pacientes que requieren soporte transfusional. Los pacientes con anemia hemolítica autoinmune presentan autoanticuerpos calientes o fríos que reaccionan contra antígenos de los eritrocitos y producen reacciones hemolíticas, que pueden ir desde leves hasta graves. Los pacientes multitransfundidos o con insuficiencia renal crónica o con anemia de células falciformes, presentan aloanticuerpos que dificultan el tratamiento con derivados de la sangre. La frecuencia de los mismos es hasta de 32% en algunas series. Dado el perfeccionamiento de las técnicas de laboratorio, en la actualidad son posibles la detección y determinación de la especificidad de los autoanticuerpos y aloanticuerpos; el enfoque integral del paciente y el conocimiento de dichas técnicas son los mejores fundamentos para un soporte transfusional seguro.
]]> PALABRAS CLAVEALOANTICUERPOS
ANEMIA HEMOLÍTICA AUTOINMUNE
AUTOANTICUERPOS
TRANSFUSIÓN
SUMMARY
Positive compatibility tests in patients who need blood transfusions are common. Patients with autoimmune hemolytic anemia may have warm or cool autoantibodies that react with red blood cell antigens and produce hemolytic transfusion reactions. Multitransfused patients, and those with either chronic renal disease or sickle cell disease, have alloantibodies that make blood transfusion difficult. In some series the frequency of such antibodies is as high as 32%. Detection and determination of specificity of autoantibodies and alloantibodies are now possible because of technical developments in laboratory. An integral approach to patients and the knowledge of these procedures are the best bases to offer secure blood transfusions.
KEY WORDS
ALLOANTIBODIES
AUTOANTIBODIES ]]>
INTRODUCCIÓN
En el contexto clínico actual el soporte transfusional se ha convertido en una práctica cotidiana. Con cierta frecuencia, los clínicos se enfrentan a pacientes con pruebas de compatibilidad positivas, así como a otros con anemia hemolítica autoinmune (AHAI), quienes constituyen retos terapéuticos que deben ser resueltos apropiadamente y con celeridad, tomando la decisión más acertada que disminuya los riesgo para el paciente. Nuestro objetivo es brindar una visión integral que permita tomar la mejor decisión y así obtener los mayores beneficios con los mínimos riesgos para el paciente.
Los componentes sanguíneos para dar soporte transfusional a pacientes en condiciones críticas están cada vez más disponibles para el clínico. Muchas situaciones e indicaciones médicas y quirúrgicas ameritan las transfusiones. En hospitales de alto nivel de complejidad, el banco de sangre es un servicio fundamental, con una dinámica propia y una responsabilidad muy importante para garantizar a los pacientes la provisión de componentes sanguíneos con todas las condiciones de seguridad que amerita el proceso de transfundir. El alto número de transfusiones que se realizan en la actualidad lleva a la presentación de problemas de compatibilidad entre las muestras del donante y el receptor. Los clínicos se enfrentan a un reto fundamental: garantizar el suministro de la sangre que el paciente requiere evitando al máximo la aparición de complicaciones relacionadas con la transfusión. En este contexto adquiere trascendencia el conocimiento del manejo del paciente con pruebas de compatibilidad positivas.
GENERALIDADES
Los pacientes multitransfundidos con anemias dependientes de transfusión, como los que tienen enfermedad de células falciformes, insuficiencia renal crónica o mielodisplasia, constituyen uno de los grupos que mayores dificultades generan. La presencia de aloanticuerpos, producto de las transfusiones previas, facilita el desarrollo de reacciones transfusionales hemolíticas que pueden dificultar el tratamiento.1
Los pacientes con AHAI presentan con frecuencia un grado de anemia tan grave como para requerir soporte transfusional.2,3 Un problema común para el clínico es encontrar sangre compatible, dado que los autoanticuerpos en el suero del paciente reaccionan con los eritrocitos normales e inclusive pueden enmascarar la presencia de aloanticuerpos que podrían producir una reacción hemolítica transfusional (RHT) grave.4 En esta situación son fundamentales el conocimiento y la comprensión de las pruebas especiales de compatibilidad para brindar al paciente la mejor alternativa posible con el mínimo riesgo de reacciones adversas.
Se deben considerar las siguientes situaciones que orientan hacia el origen probable o la causa de la incompatibilidad:
• Uso de sustancias como metildopa o procainamida que podría hacer sospechar la presencia de autoanticuerpos inducidos por medicamentos.5
]]> • Historia de enfermedad linfoproliferativa o del colágeno que sugiera anemia hemolítica autoinmune.6• Historia transfusional previa o antecedente gestacional que indicarían la presencia de aloanticuerpos.
DEFINICIONES
Aloanticuerpos
Están presentes en pacientes con transfusiones o embarazos previos. La frecuencia de aloanticuerpos contra ciertos antígenos eritrocitarios fue reportada así en un estudio norteamericano:
• Anti E 20,8%; anti Le a 18,6%; anti K 14,7%; anti D 12,9%; anti Le b 9,4%; anti M 7,2%; anti C 6,8%; anti P 6,7%; anti Fya 6,3%7
En otras series los más frecuentes fueron anti E, anti K, anti c, anti Jk, anti Fya.1,8 En pacientes que han recibido múltiples transfusiones la frecuencia de aloanticuerpos puede ser hasta de 34%, e inclusive un 3% de los pacientes tenían 3 diferentes aloanticuerpos.6
Autoanticuerpos
La anemia hemolítica autoinmune puede ocurrir como resultado de la presencia de autoanticuerpos en el suero del paciente, generalmente en el contexto de una enfermedad autoinmune o hematológica, por exposición a medicamentos o en forma primaria. El diagnóstico se basa en la demostración de anemia hemolítica (disminución de la hemoglobina, elevación del recuento de reticulocitos y del nivel de deshidrogenasa láctica e hiperbilirrubinemia indirecta) con prueba de globulina o Coombs directo positivo.
Los autoanticuerpos responsables de la AHAI pueden reaccionar a la temperatura corporal (anticuerpos calientes) y por lo general son del tipo IgG; en cambio, los autoanticuerpos reactivos al frío, por debajo de 37 ºC, usualmente son IgM; en la hemoglobinuria paroxística al frío los anticuerpos son del tipo IgG.
]]> Estos anticuerpos reaccionan con antígenos eritrocitarios propios y se detectan mediante la prueba de Coombs directa. Si se hace el fraccionamiento del Coombs, los autoanticuerpos calientes son positivos con anti-IgG y los fríos son positivos con anti-C3.9IMPLICACIONES DE LA PRESENCIA DE ANTICUERPOS CONTRA DETERMINADOS GRUPOS SANGUÍNEOS
• ABO: los antígenos A y B son los más inmunogénicos. En forma natural y espontánea se generan anticuerpos antieritrocitarios anti A o anti B que son del tipo IgM. La transfusión de glóbulos rojos con incompatibilidad de grupo ABO genera reacciones hemolíticas graves que pueden ser fatales pues la IgM produce hemólisis intravascular y genera coagulación intravascular diseminada e insuficiencia renal aguda.10 En raras ocasiones la incompatibilidad de grupo puede producir enfermedad hemolítica del recién nacido (EHRN) cuando se forman anticuerpos del tipo IgG que atraviesan la barrera placentaria.11,12
• Rh: la mayoría de estos anticuerpos son del tipo IgG y se adquieren después de un contacto transfusional previo o por embarazo. Pueden causar reacciones hemolíticas significativas, así como EHRN. El anti D, que es del tipo IgG, lleva a la forma más grave de EHRN. Anti c y anti e son también causas frecuentes de EHRN así como de reacciones hemolíticas tardías.12 Anti C puede producir hemólisis y hemoglobinuria.13
• Lewis, P1, anti I, anti P1 se consideran de poca significación clínica. Anti Lewis con poca frecuencia causa reacciones hemolíticas. Anti I generalmente no ocasiona problemas en las transfusiones. Estos son anticuerpos de reacción en frío.1,10
• MNSs: el anticuerpo anti M en general no causa reacciones transfusionales a menos que sea reactivo a la temperatura corporal. El anti N se considera de poca significancia clínica. El anti En (a) produce reacciones hemolítcas graves pero es muy raro. Tanto anti S como anti s pueden provocar reacciones hemolíticas transfusionales, la mayoría de ellas entre leves y moderadas. Son del tipo IgG por lo que pueden atravesar la placenta y causar EHRN. El anti U puede producir reacciones hemolíticas graves y EHRN.1,10
• Kell: el anti K puede generar reacciones hemolíticas graves y EHRN; junto con anti D, anti c y anti E son las principales causas de EHRN clínicamente significativa. El anti k es uno de los anticuerpos más comunes contra antígenos de alta frecuencia y puede producir reacciones hemolíticas transfusionales entre leves y moderadas.10
• Duffy: el anti Fya puede desencadenar reacciones hemolíticas transfusionales y EHRN. El anti Fyb es infrecuente, y cuando produce hemólisis ésta es leve.
• Kidd: tanto anti Jka como anti Jkb son responsables de RHT graves, dado que son anticuerpos IgG que pueden unir el complemento y causar hemólisis; además, desaparecen rápidamente de la circulación y pueden no ser detectados la próxima vez que el paciente requiera una transfusión.10,14
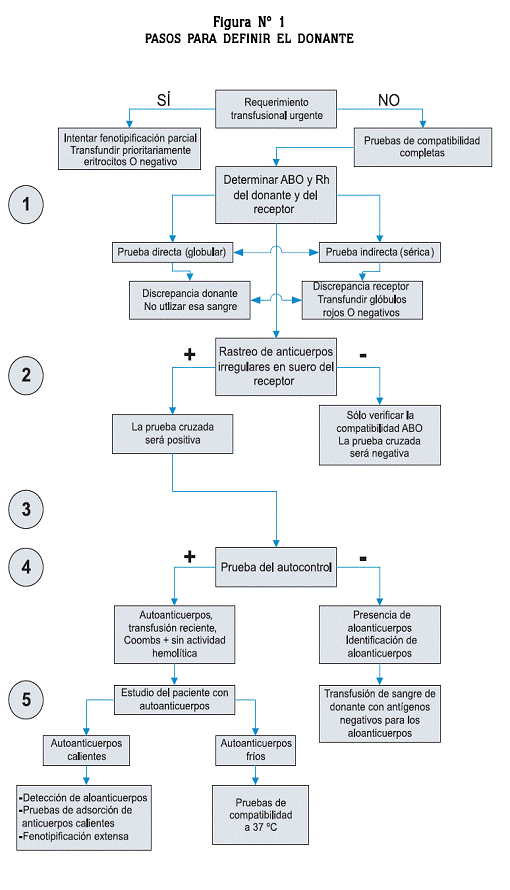
PASOS PARA DEFINIR EL DONANTE
]]> Se recomiendan los siguientes pasos para analizar y establecer el donante (figura No. 1):1. Determinación del ABO y Rh del receptor.2,10,15
2. Determinación del ABO y Rh del donante. La determinación del grupo ABO se debe efectuar tanto con la prueba directa o globular como con la indirecta o sérica y siempre debe existir concordancia entre una y otra. Si hay discrepancia en el caso del donante no se debe utilizar esa sangre y si la discrepancia de grupo es en el receptor se deben utilizar glóbulos rojos O negativos.
3. Rastreo de anticuerpos irregulares (RAI) con potencial de reacción hemolítica en el suero del receptor.15
4. Pruebas cruzadas o de compatibilidad del suero del paciente con los eritrocitos del donante que permitan detectar la incompatibilidad tanto de grupo ABO como de los otros anticuerpos antieritrocitarios clínicamente significativos.
5. Prueba del autocontrol: se enfrenta el suero del receptor con sus propios eritrocitos.
Si el RAI en el suero del receptor es negativo, solo se requiere verificar la compatibilidad ABO; si se hace la prueba cruzada, ésta no muestra aglutinación, es decir, es negativa y en consecuencia los glóbulos rojos de ese donante se pueden transfundir. En la situación problema, la presencia de aloanticuerpos o autoanticuerpos producirá RAI positivo.
Por lo general, si el RAI es positivo la prueba cruzada será incompatible. El siguiente paso es el análisis de la prueba del autocontrol.
a. Autocontrol negativo, es decir, no hay aglutinación de los eritrocitos del receptor con su propio suero: significa que el receptor posee un aloanticuerpo contra un antígeno eritrocitario ausente en su fenotipo. Esta aloinmunización se produjo por embarazos o transfusiones previas. Es una situación frecuente en los individuos multitransfundidos como los pacientes con insuficiencia renal crónica, enfermedad de células falciformes, mielodisplasias y, en general, anemias dependientes de transfusión.
]]> Para su adecuada transfusión se debe efectuar la identificación del aloanticuerpo correspondiente mediante el enfrentamiento del suero del receptor con un panel de glóbulos rojos. Una vez identificado el aloanticuerpo, se debe seleccionar un donante que carezca del antígeno contra el cual va dirigido ese aloanticuerpo; por ejemplo, si es un anti Kell, el donante seleccionado debe ser Kell negativo.b. Autocontrol positivo: por lo general traduce autoinmunidad y en algunas ocasiones transfusión reciente. También podría corresponder a un subgrupo pequeño de la población general (1-2%) cuyos integrantes presentan Coombs directo positivo y, por lo tanto, autocontrol positivo pero sin actividad hemolítica. En este caso el estudio del paciente se lleva a cabo como se refiere en los párrafos siguientes.
Pruebas de compatibilidad en AHAI por anticuerpos calientes
Estas pruebas se hacen para detectar e identificar anticuerpos con potencial para causar reacciones hemolíticas transfusionales.3,15 Los eritrocitos compatibles no reaccionan con los anticuerpos eritrocitarios en el suero del paciente. Sin embargo, en la AHAI los autoanticuerpos reaccionarán con todas las unidades de glóbulos rojos (GR) haciendo imposible proveer sangre compatible. Además, los autoanticuerpos pueden enmascarar la presencia de aloanticuerpos en las pruebas de compatibilidad.16,17 Estos aloanticuerpos se desarrollan como resultado de transfusiones previas o embarazos y pueden producir reacciones hemolíticas transfusionales. Están dirigidos contra varios antígenos de diferentes sistemas de grupos sanguíneos: Rh, Kell, Duffy, Kidd. Se detectan aloanticuerpos hasta en el 32% de los pacientes con AHAI. Estos anticuerpos pueden ser la causa del aumento de la hemólisis posterior a la transfusión que es atribuida, de manera errónea, a un incremento en la gravedad de la AHAI.2
Detección de aloanticuerpos
Se detectan e identifican probando el suero del paciente contra un panel estándar de eritrocitos con fenotipos conocidos. El problema en la AHAI es que los autoanticuerpos en el suero generalmente reaccionan con los eritrocitos probados, por lo que se deben hacer procedimientos especiales.18
a. Prueba de adsorción de anticuerpos calientes.
Esta prueba remueve los autoanticuerpos del suero del paciente permitiendo la detección e identificación de los aloanticuerpos en el suero adsorbido. En este examen, algunos de los autoanticuerpos son eluidos de los eritrocitos del paciente con un reactivo enzimático (ZZAP) que contiene una mezcla de dithiothreitol 0,1 M y papaína activada con cisteína al 0,1% y posteriormente estas células se usan para adsorber los autoanticuerpos del suero del paciente a 37 ºC . En el suero adsorbido se puede entonces evaluar la presencia de aloanticuerpos, dado que estos no serían adsorbidos por los propios eritrocitos del paciente. Este es el método más efectivo para detectar la presencia de aloanticuerpos en pacientes con AHAI por anticuerpos calientes y se denomina prueba de autoadsorción. No es efectiva en pacientes transfundidos en los últimos tres meses, porque un pequeño porcentaje de las células transfundidas pueden adsorber el aloanticuerpo invalidando la prueba. En esta situación debe efectuarse la prueba de adsorción alogénica en la que se utilizan eritrocitos de varios fenotipos conocidos para adsorber los autoanticuerpos del suero del paciente y así probar más tarde la existencia de aloanticuerpos remanentes.19
b. Fenotipificación extensa.17
Consiste en la detección e identificación del mayor número posible de antígenos en los eritrocitos del paciente y del donante. Con estas pruebas es posible detectar cuáles aloanticuerpos pudo desarrollar un paciente como resultado de transfusiones o embarazos previos. Para que exista la suficiente seguridad se deben tipificar numerosos antígenos (C, D, E, c, E, K, Jkª, Jkb , Fyª, etc). Una vez conocido el fenotipo del receptor, se deben seleccionar glóbulos rojos de un donante con el fenotipo más similar con el fin de evitar una reacción hemolítica.20
]]> Pruebas de compatibilidad en AHAI por anticuerpos fríosEs relativamente menos dispendioso el estudio de compatibilidad en estos casos. En el síndrome de aglutininas frías los autoanticuerpos no reaccionan a 37 ºC, mientras que los aloanticuerpos sí lo hacen. Entonces, la prueba de compatibilidad se debe hacer a esta temperatura, o realizar pruebas de adsorción que eliminen las reacciones que ocurren a 37 ºC.2,3,16
En la hemoglobinuria paroxística al frío los autoanticuerpos tampoco reaccionan a 37 ºC. Los autoanticuerpos son muy específicos para el antígeno P eritrocitario. Estos pacientes pueden presentar reacciones hemolíticas transfusionales graves por lo que deben ser transfundidos con sangre compatible.2,20
INDICACIONES PARA TRANSFUSIÓN EN PACIENTES CON ANEMIA
En esencia las indicaciones para transfundir al paciente con AHAI son similares a las que tienen los pacientes con anemia de otro origen.2,3,21 Algunas veces la incertidumbre con respecto a la seguridad y efectividad de la transfusión de glóbulos rojos incompatibles por la presencia de autoanticuerpos contra los eritrocitos, hace que el clínico no ordene la transfusión en pacientes que en realidad la requieren. La experiencia clínica ha mostrado que cuando la incompatibilidad es solo de autoanticuerpos, la supervivencia de los eritrocitos transfundidos es similar a la de los eritrocitos del receptor, por lo que se obtiene beneficio clínico de la transfusión.21 Está claro que la presencia de aloanticuerpos puede generar RHT, por lo que se deben hacer las pruebas de compatibilidad necesarias. Sin embargo, la decisión de transfundir al paciente no depende de los resultados de las pruebas de compatibilidad sino de las necesidades de transfusión del individuo dadas por su estado clínico.
CONSIDERACIONES PARA TENER EN CUENTA
• La estabilidad clínica del paciente y la respuesta a la terapia sugieren que la transfusión puede no ser necesaria.
• La reticulocitopenia indica alta posibilidad de requerimientos transfusionales.
• No se debe utilizar el concepto de la "unidad menos incompatible",22 sino hacer las pruebas necesarias para garantizar la detección e identificación de aloanticuerpos y disminuir el riesgo de reacción hemolítica transfusional.
• El estado clínico del paciente es el que define la necesidad de transfusión: los signos de compromiso neurológico o hemodinámico, entre otros, sugieren la necesidad urgente de transfusión.
]]> • Se deben utilizar eritrocitos leucorreducidos para disminuir las reacciones febriles no hemolíticas que pueden generar confusión al simular una RHT.• Cuando se decide transfundir se debe utilizar el mínimo de unidades necesario para aliviar los síntomas.
Transfusiones urgentes
En situaciones críticas, con pacientes que tengan requerimientos transfusionales urgentes, las pruebas completas de compatibilidad pueden tardar demasiado tiempo como para permitir decisiones oportunas. En estos casos se deben tener en cuenta las siguientes indicaciones:2
• Pocos pacientes hospitalizados tienen aloanticuerpos; si la transfusión es demasiado urgente debe ser llevada a cabo antes de completar todos los pasos sugeridos.
• Se podría realizar al menos la fenotipificación parcial con eritrocitos O negativo.
• En caso de disponer del tiempo suficiente se debe hacer el estudio completo de compatibilidad.
REFERENCIAS BIBLIOGRÁFICAS
1. Schonewille H, van de Watering LM, Loomans DS, Brand A. Red blood cell alloantibodies after transfusion: factors influencing incidence and specificity. Transfusion 2006; 46: 250-256. [ Links ]
2. Petz LD. A physician's guide to transfusion in autoimmune haemolytic anaemia. Br J Haematol 2004; 124: 712-716. [ Links ]
3. Garratty G, Petz LD. Transfusing patients with autoimmune haemolytic anaemia. Lancet 1993; 341: 1220. [ Links ]
4. Sachs UJ, Roder L, Santoso S, Bein G. Does a negative direct antiglobulin test exclude warm autoimmune haemolytic anaemia? A prospective study of 504 cases. Br J Haematol 2006; 132: 655-656. [ Links ]
5. Kleinman S, Nelson R, Smith L, Goldfinger D. Positive direct antiglobulin tests and immune hemolytic anemia in patients receiving procainamide. N Engl J Med 1984; 311: 809-812. [ Links ]
6. Schonewille H, Haak HL, van Zijl AM. Alloimmunization after blood transfusion in patients with hematologic and oncologic diseases. Transfusion 1999; 39: 763-771. [ Links ]
7. Winters JL, Pineda AA, Gorden LD, Bryant SC, Melton LJ, 3rd, Vamvakas EC, et al. RBC alloantibody specificity and antigen potency in Olmsted County, Minnesota. Transfusion 2001; 41: 1413-1420. [ Links ]
8. Pineda AA, Vamvakas EC, Gorden LD, Winters JL, Moore SB. Trends in the incidence of delayed hemolytic and delayed serologic transfusion reactions. Transfusion 1999; 39: 1097-1103. [ Links ]
9. Semple JW, Freedman J. Autoimmune pathogenesis and autoimmune hemolytic anemia. Semin Hematol 2005; 42: 122-130. [ Links ]
10. Petz LD, Calhoun L. Erythrocite antigens and antibodies. In: Beutler ELM, ed. Williams's Hematology, 6th ed, New York: Mc Graw-Hill; 2001; 1843-1858 [ Links ]
11. Schonewille H, Haak HL, van Zijl AM. RBC antibody persistence. Transfusion 2000; 40: 1127-1131. [ Links ]
12. Avent ND, Reid ME. The Rh blood group system: a review. Blood 2000; 95: 375-387. [ Links ]
13. Westhoff CM. The Rh blood group system in review: a new face for the next decade. Transfusion 2004; 44: 1663-1673. [ Links ]
14. Schonewille H, van de Watering LM, Brand A. Additional red blood cell alloantibodies after blood transfusions in a nonhematologic alloimmunized patient cohort: is it time to take precautionary measures? Transfusion 2006; 46: 630-635. [ Links ]
15. Buetens OW, Ness PM. Red blood cell transfusion in autoimmune hemolytic anemia. Curr Opin Hematol 2003; 10: 429-433. [ Links ]
16. Branch DR, Petz LD. Detecting alloantibodies in patients with autoantibodies. Transfusion 1999; 39: 6-10. [ Links ]
17. Shirey RS, Boyd JS, Parwani AV, Tanz WS, Ness PM, King KE. Prophylactic antigen-matched donor blood for patients with warm autoantibodies: an algorithm for transfusion management. Transfusion 2002; 42: 1435-1441. [ Links ]
18. Reardon JE, Marques MB. Laboratory evaluation and transfusion support of patients with autoimmune hemolytic anemia. Am J Clin Pathol 2006; 125 Suppl: S71-77. [ Links ]
19. Wright MS, Smith LA. Laboratory investigation of autoimmune hemolytic anemias. Clin Lab Sci 1999; 12: 119-122; quiz 123-115. [ Links ]
20. Garratty G, Petz LD. Approaches to selecting blood for transfusion to patients with autoimmune hemolytic anemia. Transfusion 2002; 42: 1390-1392. [ Links ]
21. Salama A, Berghofer H, Mueller-Eckhardt C. Red blood cell transfusion in warm-type autoimmune haemolytic anaemia. Lancet 1992; 340: 1515-1517. [ Links ]
22. Petz LD. "Least incompatible" units for transfusion in autoimmune hemolytic anemia: should we eliminate this meaningless term? A commentary for clinicians and transfusion medicine professionals. Transfusion 2003; 43: 1503-1507. [ Links ] ]]>