EFFECT OF SOME ORGANIC SOLVENTS IN SATURATION ON THE THERMODYNAMIC FUNCTIONS OF DISSOLUTION FOR NAPROXEN IN AQUEOUS MEDIA AT PHYSIOLOGICAL pH
Carolina P. MORA G.1, Helber J. BARBOSA B.1 y Fleming MARTÍNEZ R.1*
1 Sección de Farmacotecnia, Departamento de Farmacia, Universidad Nacional de Colombia. A.A. 14490. Bogotá, Colombia
* Autor a quien se debe dirigir la correspondencia: fmartinezr@unal.edu.co
Recibido: Enero 12 de 2007 Aceptado: Marzo 27 de 2007
RESUMEN
El naproxén (NAP) es un anti-inflamatorio no esteroidal de amplio uso en la actualidad; sin embargo, sus propiedades fisicoquímicas aún no han sido totalmente estudiadas. Como una contribución a la caracterización fisicoquímica del NAP en solución acuosa, en la presente investigación se evalúa el efecto de algunos solventes orgánicos en saturación acuosa sobre las funciones termodinámicas de solución del NAP a pH fisiológico. A partir de valores de solubilidad a diferentes temperaturas, mediante las ecuaciones de Gibbs y de van't Hoff, se determinan las funciones termodinámicas energía libre de Gibbs, entalpía y entropía, para los procesos de solución y de solvatación del NAP en tres medios acuosos a pH 7,4 y saturados, cada uno de ellos con octanol, W(ROH), miristato de isopropilo, W(MIP) o cloroformo, W(CLF). Los resultados se comparan con los obtenidos para el mismo fármaco en buffer puro, W, presentados previamente en la literatura. La solubilidad del NAP a 25,0 °C se incrementa en el siguiente orden: W(ROH) < W < W(MIP) ≤ W(CLF). En todos los sistemas, las entalpías y entropías de solución de este fármaco son positivas y negativas, respectivamente; mientras que las funciones termodinámicas de solvatación presentan valores negativos en todos los casos. Los resultados se discuten en términos de interacciones soluto-solvente.
Palabras clave: Naproxén, solubilidad, solvatación, termodinámica.
ABSTRACT
Naproxen (NAP) is a widely used non-steroidal anti-inflammatory drug, whose physicochemical properties have not been thoroughly studied. As a contribution to the physicochemical characterization of NAP in aqueous solution, we evaluated the effect of some organic solvents in aqueous saturation on the thermodynamic functions of a NAP solution at physiological pH. Based on solubility values at different temperatures, using the equations of Gibbs and Van´t Hoff, the thermodynamic functions Gibb´s free energy, enthalpy and enthropy were determined for the solution and salvation processes of NAP in three aqueous saturated media at pH 7,4, each one of them with octanol W(ROH), isopropyl myristate W(IPM), or chloroform W(CLF). Results were compared with those obtained for NAP in pure buffer, W, previously reported. Solubility of NAP at 25º C increased in the following order: W(ROH) < W < W(IPM) ≤ W(CLF). In every system, enthalpies and enthropies of the solution of this drug were, respectively, positive and negative; on the other hand, solvation thermodynamic functions were negative in all cases. Results are discussed in terms of solute-solvent interactions.
Keywords: Naproxen, solubility, solvation, thermodynamics.
INTRODUCCIÓN
]]> El naproxén (NAP) es un fármaco anti-inflamatorio no esteroidal (AINE), que también posee efecto analgésico y antipirético sin producir adicción (1). Es utilizado ampliamente en Colombia y administrado principalmente por vía peroral en forma de tabletas, cápsulas y suspensiones; también está disponible como gel para uso tópico y como solución inyectable destinada a la administración intramuscular (2).La determinación de la solubilidad acuosa es de gran importancia en la caracterización fisicoquímica de los compuestos de interés farmacéutico, así como en el diseño de nuevos fármacos y de nuevas formas farmacéuticas de dosificación. De otro lado, la dependencia de la solubilidad con la temperatura permite realizar el correspondiente tratamiento termodinámico, el cual, a su vez, permite proponer mecanismos para el proceso de disolución (3).
Por estas razones, el principal objetivo del presente estudio fue evaluar el efecto de algunos solventes orgánicos en saturación acuosa sobre las funciones termodinámicas de solución del NAP a pH fisiológico. Los solventes orgánicos estudiados fueron el octanol (ROH), el miristato de isopropilo (MIP) y el cloroformo (CLF), los cuales encuentran gran utilidad en el planteamiento de correlaciones cuantitativas entre la estructura molecular y la actividad biológica (modelos QSAR) (4).
El ROH ha sido ampliamente utilizado como medio orgánico estándar en experimentos de reparto para el desarrollo de modelos QSAR de diferentes clases de compuestos, ya que el coeficiente de reparto octanol-agua (log P) es un parámetro muy importante para modelar membranas biológicas y, por lo tanto, para predecir el transporte y la distribución de fármacos en el organismo (4). El ROH, al ser un alcohol, actúa como donor y aceptor de protones en el establecimiento de enlaces de hidrógeno, gracias a su grupo hidroxilo. El MIP está relacionado con la absorción transdérmica de principios activos, puesto que su naturaleza anfifílica, esto es, polar y no-polar, simula la naturaleza compleja de la piel (de tipo matriz semipolar). El MIP actúa como aceptor de protones en el establecimiento de enlaces de hidrógeno, gracias a su grupo carboxilo, ya que es un éster. Finalmente, el CLF es un solvente orgánico que actúa principalmente como donor de protones en el establecimiento de enlaces de hidrógeno (5).
El análisis termodinámico se realizó mediante el método de van't Hoff, incluyendo las respectivas contribuciones por fusión y mezcla, y por sublimación y solvatación, al proceso de solución. Esta investigación amplía los estudios desarrollados con este fármaco por Perlovich et al. (6, 7) y por Mora y Martínez (8), entre otros, en algunos medios acuosos.
MATERIALES Y MÉTODOS
Materiales
Naproxen USP (9); octanol extra puro, Merck; miristato de isopropilo P.S., Merck; cloroformo R.A., Mallinckrodt; agua destilada (W), conductividad < 2 µS, Laboratorio de Farmacotecnia de la Universidad Nacional de Colombia; cloruro de potasio R.A. Merck, fosfatos mono y di sódico R.A. Merck; unidades de filtración Swinnex®-13 Millipore Corp.
Determinaciones de solubilidad
En frascos de vidrio ámbar se adicionó un exceso de NAP a 20 cm3 de cada medio acuoso -solución regulada a pH 7,4 y ajustada a fuerza iónica, µ 0,15 mol L-1, los cuales son los valores fisiológicos de la sangre (10, 11)- saturado de ROH, MIP o CLF, según el caso. Las mezclas sólido-líquido se agitaron en un agitador mecánico Wrist Action, Burrel, model 75 durante una hora. Posteriormente, las dispersiones acuosas fueron ubicadas en un baño termostatizado Magni Whirl Blue M. Electric Company estabilizado a 40,0 ± 0,05 ºC, durante al menos cinco días hasta alcanzar el equilibrio.
]]> Después de este tiempo, las soluciones sobrenadantes fueron filtradas a temperatura constante para asegurar la ausencia de partículas no disueltas antes del muestreo para análisis. Las concentraciones de NAP en las soluciones saturadas se determinaron midiendo las respectivas absorbancias después de realizar las diluciones apropiadas e interpolando estos valores en la curva de calibración UV, utilizando un espectrofotómetro UV/Vis Unicam UV2-100 v 4.00 de acuerdo a una metodología validada (12). Posteriormente, la temperatura del baño termostatizado se disminuyó en 5,0 °C y, por lo tanto, se estabilizó en 35,0 °C durante al menos dos días para permitir la precipitación del exceso de fármaco disuelto.Una vez alcanzado el equilibrio, se procedió al análisis de la concentración del NAP, como se describió previamente. Estos procedimientos se desarrollaron disminuyendo la temperatura de 5,0 °C en 5,0 °C cada vez, hasta alcanzar los 20,0 °C. Todos los experimentos se realizaron al menos por triplicado. Para realizar la conversión de unidades de concentración entre molaridad y fracción molar, se determinó la densidad de las soluciones utilizando un densímetro digital DMA 45 Anton Paar.
RESULTADOS Y DISCUSIÓN
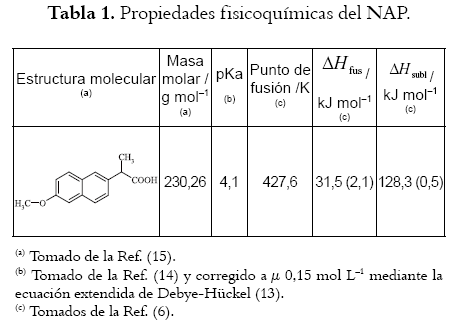
En la tabla 1 se presentan la estructura molecular y algunas propiedades fisicoquímicas del NAP. El pKa se corrigió a µ 0,15 mol L-1 mediante la ecuación extendida de Debye-Hückel (13), considerando el valor presentado por Betageri et al. (14). La temperatura de fusión, la entalpía de fusión y la entalpía de sublimación fueron reportadas por Perlovich et al. (6).
Este fármaco en solución acuosa actúa principalmente como un ácido de Lewis para establecer enlaces de hidrógeno con los grupos aceptores de protones en los solventes (oxígeno en los grupos -OH y >C=O); aunque también puede actuar como base de Lewis, mediante sus grupos hidroxilo, carbonilo y metoxilo (8).
Solubilidad experimental del NAP
En la tabla 2 se presenta la solubilidad experimental del NAP en los diferentes medios acuosos en función de la temperatura, expresada en molaridad y en fracción molar. Los valores de solubilidad expresados en fracción molar obtenidos en buffer puro están en total desacuerdo con los presentados por Perlovich et al. (7) a 20, 25 y 30 °C, los cuales son: 1,34 × 10-5, 1,39 × 10-5, y 1,44 × 10-5, respectivamente. Estas enormes diferencias pueden en principio ser atribuidas a las composiciones de las soluciones buffer empleadas en cada investigación, en particular el efecto de la fuerza iónica 0,15 mol L-1 y el uso de KCl, el cual, como es bien conocido, puede afectar la estructura del agua (7).
Comparando la solubilidad del NAP en los medios acuosos saturados de los solventes orgánicos y el buffer puro, la tabla 2 muestra que esta propiedad disminuye de la forma: W(CLF) > W(MIP) > W > W(ROH). Sin embargo, con el fin de verificar si existen diferencias entre los buffers saturados y el buffer puro se realizaron tres análisis de varianza (ANOVA), así: a. W vs. W(ROH), b. W vs. W(MIP) y c. W vs. W(CLF). Los análisis estadísticos se presentan en el Anexo adjunto, y a partir de ellos se evidencia que efectivamente la solubilidad del NAP en buffer a pH 7,4 es influenciada por la saturación con los solventes orgánicos.
]]> De esta manera, los valores más bajos obtenidos en W(ROH) podrían explicarse por la hidratación hidrofóbica que ocurre en torno a la cadena alquílica de las moléculas del octanol, conduciendo a que se disminuyan las interacciones del agua con el fármaco. Además debe considerarse que, según ha sido reportado, el agua saturada de octanol posee una estructura ligeramente más asociada que el agua pura (4, 16).En el caso del W(CLF) se observa un incremento en la solubilidad respecto al buffer puro, debido a que el cloroformo posee una mayor solubilidad en agua (0,822 % m/m, X = 0,00126 (17)) comparado con el octanol (0,000059 (18)), lo cual estaría generando una disminución en la polaridad del medio, la cual aumentaría la solubilidad del NAP por efecto dieléctrico; aunque debe considerarse que este fármaco se encuentra preferentemente en forma disociada a este valor de pH y, por lo tanto, de esta forma sería más afín por medios de alta polaridad. De ahí que, posiblemente, el aumento de la solubilidad en este medio sea más bien una consecuencia de variaciones en la estructura del agua.
De otro lado, el análisis estadístico indica que también existen diferencias entre lo obtenido en el buffer puro y en el buffer saturado de MIP, y si bien en la literatura se ha considerado a este solvente orgánico como insoluble en agua, es casi evidente que, en este caso, el MIP presenta interacciones con el agua lo suficientemente importantes como para modificar el medio, y por lo tanto, afectar la solubilidad del NAP. Sin embargo, para poder explicar este comportamiento más adecuadamente, sería necesario disponer de datos de la solubilidad de este solvente en el agua en función de la temperatura, como es el caso del octanol (16, 18). Estos datos permitirían realizar el respectivo análisis termodinámico de disolución del MIP en el agua, el cual, a su vez, permitiría evaluar los posibles efectos del solvente orgánico sobre la estructura del agua (16). Esto también es válido para el CLF. El comportamiento del NAP es contrario al que presentan otros fármacos, tales como la benzocaína (19), el acetaminofén (5) y el ibuprofén (20), para los cuales no se encontró diferencia significativa en la solubilidad en W y en W(MIP).
En este punto debe resaltarse que la solubilidad del NAP en W(MIP) y en W(CLF) es muy similar a todas las temperaturas, aún cuando las solubilidades de los dos solventes orgánicos en el agua sean muy diferentes.
Funciones termodinámicas de solución
De acuerdo con el análisis clásico de van't Hoff, el cambio entálpico estándar de solución (ΔH0soln ) se obtiene a partir de la pendiente de una gráfica de ln X2 en función de 1/T. Sin embargo, en algunos tratamientos más recientes se han introducido algunas adaptaciones a la ecuación tradicional de van't Hoff con el objeto de disminuir la propagación de errores y, por lo tanto, separar los efectos puramente químicos de aquellos debidos únicamente a los tratamientos matemáticos y estadísticos utilizados en el tratamiento de los datos de equilibrio y en el desarrollo de gráficos de compensación entálpicaentrópica. Por esta razón, se utiliza la temperatura armónica media (Thm) en estos análisis. La Thm se calcula como: 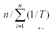 , en la cual n es el número de temperaturas estudiadas. En esta investigación, la Thm obtenida es justamente 303 K. De acuerdo con lo anterior, la expresión modificada de van't Hoff es la siguiente (21, 22):
, en la cual n es el número de temperaturas estudiadas. En esta investigación, la Thm obtenida es justamente 303 K. De acuerdo con lo anterior, la expresión modificada de van't Hoff es la siguiente (21, 22):
La figura 1 corresponde a la gráfica modificada de van't Hoff de la solubilidad del NAP en los diferentes medios acuosos. Se encontraron modelos lineales con muy buenos coeficientes de determinación en los tres sistemas estudiados. Por esta razón, se considera que la ecuación 1 es útil para estimar los valores de ΔH0soln.
El cambio de energía libre estándar para el proceso de solución (ΔH0soln) ha sido calculado tradicionalmente como: -RT ln X2 (23). Sin embargo, al considerar la aproximación propuesta por Krug et al. (21, 22), esta propiedad se calcula más correctamente por medio de:
]]>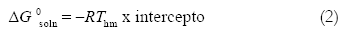
en la cual, el intercepto utilizado es el obtenido en las gráficas de ln X2 en función de 1/T - 1/Thm (Ec. 1). El cambio entrópico estándar para el proceso de solución (ΔS0soln) se obtiene de los respectivos valores de ΔH0soln y ΔG0soln utilizando la expresión:
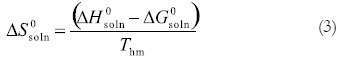
Las funciones termodinámicas relativas al proceso de solución del NAP en los diferentes medios acuosos se presentan en la tabla 3. Para el cálculo de estas funciones se utilizaron algunos métodos de propagación de errores (24). La energía libre de Gibbs de solución es positiva en todos los casos, según lo cual el proceso de solución aparentemente no sería espontáneo, lo que resulta contradictorio, ya que el proceso de disolución del NAP hasta la saturación se sucede experimentalmente. Este resultado puede ser explicado en términos de la escala de concentración utilizada (fracción molar), en la cual el estado de referencia es una solución ideal de concentración unitaria de NAP, esto es, sería el soluto sólido puro. Los valores de ΔG0soln son bastante diferentes respecto a los reportados por Perlovich et al. (7), esto es, 27,7 kJ mol-1, lo que, a su vez, está de acuerdo con las grandes diferencias encontradas en la solubilidad (Tabla 2).
La entalpía de solución es positiva en todos los casos indicando que el proceso es endotérmico, mientras que la entropía de solución es negativa. De lo anterior se tiene que el proceso de disolución no tiene conducción entálpica ni entrópica. De forma análoga a lo sucedido con los valores de solubilidad y ΔG0soln, los valores de ΔH0soln son muy diferentes a los reportados por Perlovich et al. (7) (5.2 kJ mol-1). Por lo tanto, debido a las grandes diferencias presentadas entre los datos de ΔG0soln y ΔH0soln obtenidos en el trabajo de Perlovich et al. (7) y en esta investigación, también se presentan grandes diferencias en los valores de ΔS0soln ( -75,5 J mol-1 K-1 según la Ref. 7). Como se indicó previamente, todas estas diferencias pueden ser atribuidas a variaciones en la composición de los medios acuosos, lo cual podría afectar la estructura del agua y por lo tanto, su capacidad disolvente.
Para evaluar las contribuciones relativas de la entalpía (%ζH) y la entropía (%ζTS) al proceso de solución, se utilizaron las ecuaciones 4 y 5, respectivamente.
De los datos de la tabla 3 se tiene que el principal contribuyente a la energía libre de solución en el sistema W(ROH) es la entropía, mientras que en los otros tres sistemas, las contribuciones son muy similares, si bien predomina la entalpía en los sistemas W(MIP) y W(CLF) y la entropía en el buffer puro.
Nuevamente resulta interesante observar que las funciones termodinámicas de solución del NAP son muy similares en W(MIP) y en W(CLF) aunque los dos solventes orgánicos presentan estructuras moleculares muy diferentes entre sí.
]]> Funciones termodinámicas aparentes de mezclaDe acuerdo con la ley de Hess, el proceso de solución en el caso de solutos del tipo no electrolito, puede esquematizarse mediante las siguientes etapas hipotéticas: Soluto(Sólido) → Soluto(Líquido) → Soluto(Solución), donde los procesos parciales son la fusión y la mezcla a 303 K (3). Este tratamiento permite calcular las contribuciones termodinámicas individuales mediante las ecuaciones 6 y 7:
donde, ΔH303fus y ΔS303fus representan las funciones termodinámicas relativas al proceso de fusión del NAP a la temperatura armónica (en este caso 303 K). ΔH303fusse calculó mediante la expresión ΔHMPfus ; ΔCp (Tfus ; T) , utilizando el valor de ΔSMPfus (73.7 J mol-1 K-1) en lugar de ∆Cp, con lo que se obtuvo el valor de 22.32 kJ mol-1. Este valor es coincidente con la entalpía de solución ideal presentada por Mora y Martínez para este fármaco (8). En cambio, la entropía de fusión a 303 K no es coincidente con la entropía ideal de solución a esta misma temperatura (48.3 J mol-1 K-1). Por lo tanto, para los propósitos prácticos de esta investigación, se utilizó el valor de ΔS0idsolnen lugar del valor de ΔH303fus.
Sin embargo, como se indicó previamente, a pH 7,4 el NAP se encuentra disociado prácticamente en su totalidad, por lo que es necesario indicar que el proceso de mezcla estaría incluyendo un término adicional relativo a la desprotonación del fármaco, y que sería de naturaleza endotérmica, puesto que se requiere suministrar energía para romper la unión -OH del carboxilo, si bien posteriormente los dos iones formados se hidratan (carboxilato e hidrogenión, respectivamente) y, como consecuencia de este último proceso, se libera energía (etapa exotérmica).
En la tabla 4 se presentan todas las funciones termodinámicas para el proceso aparente de mezcla del NAP en los diferentes medios acuosos estudiados.
De los resultados anteriores, se observa que las contribuciones parciales de la solubilidad ideal (relacionada con la fusión del fármaco) a la entalpía y entropía de solución son positivas, mientras que las dos contribuciones debidas al proceso de mezcla son negativas. De acuerdo con lo anterior, el proceso de solución de este fármaco en estos medios acuosos sería conducido por la entalpía de mezcla y por la entropía de fusión.
Los valores de ΔH0mix resultan de la contribución de diferentes tipos de interacciones. La entalpía de formación de la cavidad en el solvente (requerida para alojar al soluto) es endotérmica, puesto que se requiere energía para superar las fuerzas cohesivas presentes en el solvente. Este proceso contribuye a disminuir la solubilidad. De otro lado, la entalpía de interacción soluto-solvente es exotérmica y se origina principalmente en interacciones de van der Waals, ácido-base de Lewis o del tipo ion-dipolo. Este proceso contribuye a aumentar la solubilidad. La estructuración de las moléculas de agua alrededor de los grupos no polares de los solutos no electrolitos (hidratación hidrofóbica) y la hidratación de los iones contribuyen a disminuir el calor neto de mezcla en solución acuosa hasta valores pequeños, e incluso negativos, como se observa en la tabla 4.
De otro lado, el proceso de estructuración del agua contribuye a disminuir la entropía de mezcla, lo cual efectivamente es observado para el NAP en todos los medios acuosos estudiados. Como se indicó previamente, a pH 7,4 el NAP se encuentra principalmente en forma disociada, el cual interactúa con el agua principalmente por interacciones ion-dipolo, lo cual a su vez implica la inmovilización de las moléculas de agua alrededor del grupo carboxílico ionizado del fármaco. La contribución de estos efectos entrópicos se observa también en la Tabla 4, puesto que los valores por entropía (%ζTS > 66 %) predominan sobre los debidos a entalpía (%ζH < 34 %). Los anteriores valores fueron calculados usando ecuaciones análogas a las ecuaciones 4 y 5.
]]> Funciones termodinámicas de solvataciónEn adición al esquema expuesto anteriormente, de acuerdo con la ley de Hess, el proceso de solución también puede esquematizarse mediante las siguientes etapas hipotéticas: Soluto(Sólido) → Soluto(Vapor) → Soluto(Solución), donde los procesos parciales son la sublimación y la solvatación (3). Este tratamiento permite calcular las contribuciones termodinámicas individuales mediante las ecuaciones 8 a 10:
donde, el valor ΔH0subl = 115.8 kJ mol-1 fue tomado de Perlovich et al. (6) y, por lo tanto, los valores de la función ΔH0solv fueron calculados a partir de los valores de ΔH0soln presentados en la tabla 3. De acuerdo a Mora y Martínez (8) los valores de energía libre y entropía de sublimación del NAP son 57.32 kJ mol-1 y 234.3 J mol-1 K-1 a 303 K, respectivamente. En la Tabla 5 se presentan las correspondientes funciones termodinámicas de solvatación del NAP en los diferentes medios acuosos. Adicionalmente, se utilizaron dos ecuaciones análogas a las ecuaciones 4 y 5 para comparar las contribuciones relativas de la entalpía (%ζH) y la entropía (%ζTS) al proceso de solvatación.
De forma análoga a lo encontrado en el estudio del acetaminofén (3) y el ibuprofén (20), el proceso de solvatación del NAP en los diferentes medios acuosos es conducido por la entalpía (valores negativos en todos los casos). De los valores de %ζH y %ζTS presentados en la Tabla 5 se tiene que el principal contribuyente en el proceso de solvatación del NAP en los cuatro medios acuosos es la entalpía (%ζH son cercanos al 59 %).
De otro lado, en adición al análisis de la principal función termodinámica conductora del proceso de solvatación, también es importante evaluar el balance entre las interacciones específicas y no específicas involucradas en la solvatación; por esta razón se evaluaron algunos parámetros adicionales que describen la relación existente entre las interacciones soluto-solvente específicas y no específicas, en términos de entalpías (%εH) y entropías (%εS). Esto se realizó de acuerdo con las siguientes definiciones introducidas por Perlovich et al. (6):
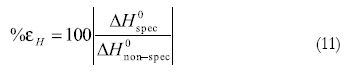
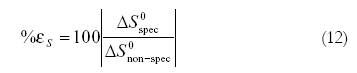
El ciclohexano (CH) ha sido escogido como solvente “inerte” puesto que interactúa con las moléculas del fármaco únicamente mediante interacciones no específicas (fuerza de dispersión), mientras que los medios acuosos interactúan con el NAP mediante interacciones específicas, tales como los enlaces de hidrógeno y aquellas de tipo ion-dipolo. Las cantidades termodinámicas de solución del NAP en CH a 303 K son ΔG0soln(CH) = 23,7 kJ mol-1, ΔH0soln(CH) = 57,5 kJ mol-1, y ΔS0soln(CH) = 111,5 J mol-1 K-1 (8).
]]> Los valores de %εH y %εS para la solvatación del NAP también se presentan en la Tabla 5. Estos valores indican que durante la disolución del NAP en estos medios acuosos, las interacciones específicas soluto-solvente (principalmente del tipo iondipolo) afectan enormemente el término entrópico de la energía libre respecto a las interacciones no específicas, puesto que los valores son mayores del 130 %. Respecto al término entálpico, se tiene que las interacciones no específicas soluto-solvente predominan, ya que los respectivos valores son menores del 70 %.Funciones termodinámicas de transferencia desde el buffer puro hasta los diferentes medios acuosos saturados
Finalmente, un tratamiento adicional realizado con la información de la Tabla 3 consistió en el cálculo de las cantidades termodinámicas de transferencia del NAP desde el buffer puro hasta cada uno de los medios acuosos saturados. Esto se hizo restando el valor de cada función termodinámica de solución en el buffer puro, respecto al valor presentado en el buffer saturado de solvente orgánico.
En la tabla 6 se presentan las respectivas funciones termodinámicas de transferencia (ΔΨ0W→W(org)). Como puede observarse, la transferencia del NAP desde el buffer puro hasta el W(MIP) y hasta el 45 W(CLF) es espontánea (ΔG0W→W(org) < 0) y conducida por la entropía (ΔS0W→W(org) > 0), mientras que la transferencia hasta el W(ROH) no espontánea (ΔG0W→W(org) > 0), aunque en este último caso la entalpía es negativa, y por lo tanto favorable, la entropía es también negativa, lo cual desfavorece el proceso de transferencia hasta el buffer saturado de octanol.
Como era de esperar por los valores de solubilidad y las funciones termodinámicas de solución, los comportamientos de la transferencia del NAP desde el buffer puro hasta el W(MIP) y el W(CLF) presentan valores muy similares. Sin embargo, para poder concluir que los mecanismos involucrados en los diferentes procesos estudiados son análogos en estos dos medios acuosos, se requeriría de otro tipo de experimentación, el cual involucraría técnicas espectroscópicas, entre otras.
CONCLUSIONES
De todo lo anteriormente expuesto puede concluirse que la saturación del buffer a pH fisiológico con los solventes orgánicos estudiados presenta un claro efecto sobre la solubilidad y la termodinámica del proceso de solución del NAP, lo cual podría resultar muy importante en el entendimiento de los procesos dinámicos que se suceden con este fármaco dentro del organismo, ya que éstos son dependientes de las diferentes interacciones intermoleculares que se presentan con los diferentes componentes celulares, y que son, así mismo, afectados por la composición química del medio acuoso en los órganos y tejidos, así como en el medio intracelular.
ANEXO: ANÁLISIS ANOVA
Con el objeto de establecer si existen diferencias significativas entre los valores de solubilidad del NAP, en fracción molar (X2), determinados en buffer pH 7,4, µ 0.15 mol L-1 (W) y los obtenidos en este mismo medio saturado de solventes orgánicos (W(ROH), W(MIP) y W(CLF)), se realizó el tratamiento estadístico de los resultados mediante un ANOVA, en el cual se incluyeron los datos de solubilidad reportados en la tabla 2 a cada temperatura de estudio. En las tablas A1 a A3 se reportan los resultados y las conclusiones del ANOVA realizado en cada caso, de acuerdo con el planteamiento de las siguientes hipótesis:
]]> 1. Hipótesis nula: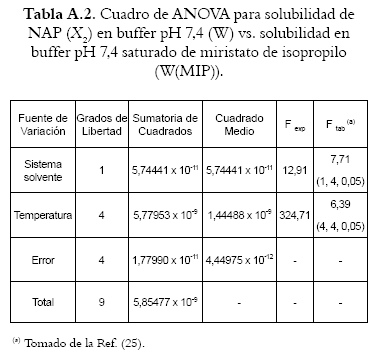
Conclusiones W vs. W(ROH)
Sistema solvente: Como F exp > F tab (9,68 > 7,71), se rechaza Ho, por lo tanto, existe diferencia significativa entre los valores de solubilidad de NAP, en fracción molar, obtenidos en buffer pH 7,4 y buffer pH 7,4 saturado de octanol. Temperatura: Como F exp > F tab (88,05 > 6,39), existe diferencia significativa en la solubilidad de NAP, cuando ésta se determina a diferentes temperaturas, en los dos sistemas solventes empleados.
Conclusiones W vs. W(MIP)
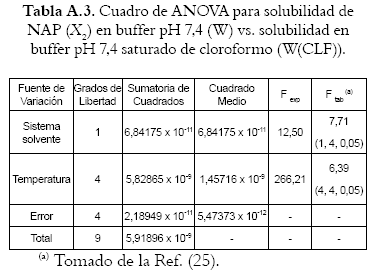
Sistema solvente: Como F exp > F tab (12,91 > 7,71), se rechaza Ho, por lo tanto, existe diferencia significativa entre los valores de solubilidad de NAP, en fracción molar, obtenidos en buffer pH 7,4 y buffer pH 7,4 saturado de miristato de isopropilo. Temperatura: Como F exp > F tab (324,71 > 6,39), existe diferencia significativa en la solubilidad de NAP, cuando ésta se determina a diferentes temperaturas, en los dos sistemas solventes empleados.
Conclusiones W vs. W(CLF)
Sistema solvente: Como F exp > F tab (12,50 > 7,71), se rechaza Ho, por lo tanto, existe diferencia significativa entre los valores de solubilidad de NAP, en fracción molar, obtenidos en buffer pH 7,4 y buffer pH 7,4 saturado de cloroformo. Temperatura: Como F exp > F tab (266,21 > 6,39), existe diferencia significativa en la solubilidad de NAP, cuando ésta se determina a diferentes temperaturas, en los dos sistemas solventes empleados.
]]> AGRADECIMIENTOSFormalmente agradecemos a la DIB-DINAIN de la Universidad Nacional de Colombia (UNC) por el apoyo financiero, y al Departamento de Farmacia de la misma universidad, por facilitar los equipos y laboratorios utilizados en esta investigación.
REFERENCIAS BIBLIOGRÁFICAS
1. Roberts II LJ, Morrow JD. Analgesic-antipiretic and Anti-inflammatory Agents and Drugs Employed in the Treatment of Gout. En: Hardman JG, Limbird LE, Gilman AG, editores. New York: Goodman & Gilman´s The Pharmacological Basis of Therapeutics. 10 ed. New York: McGraw-Hill; 2001. pp. 703-705. [ Links ]
2. Rosenstein-Ster E. Diccionario de Especialidades Farmacéuticas. 31a edición. Bogotá: Thompson P.L.M.; 2003. [ Links ]
3. Jiménez JA, Martínez F. Thermodynamic Study of the Solubility of Acetaminophen in Propylene Glycol + Water Cosolvent Mixtures. J Braz Chem Soc 2006; 17(1): 125-134. [ Links ]
4. Sangster J. Octanol-Water Partition Coefficients: Fundamentals and Physical Chemistry. Chichester: John Wiley & Sons; 1997. pp. 1-55. [ Links ]
5. Baena Y, Pinzón JA, Barbosa H, Martínez F. Temperature Dependence of the Solubility of Some Acetanilide Derivatives in Several Organic and Aqueous Solvents. Phys Chem Liquids 2004; 42(6): 603-613. [ Links ]
6. Perlovich GL, Kurkov SV, Kinchin AN, Bauer-Brandl A. Thermodynamics of Solutions III: Comparison of the Solvation of (+)-Naproxen with Other NSAIDs. Eur J Pharm Biopharm 2004; 57(2): 411-420. [ Links ]
7. Perlovich GL, Kurkov SV, Bauer-Brandl A. The Difference between Partitioning and Distribution from a Thermodynamic Point of View: NSAIDs as an Example. Eur J Pharm Sci 2006; 27(2-3): 150-157. [ Links ]
8. Mora CP, Martínez F. Thermodynamic Quantities Relative to Solution Processes of Naproxen in Aqueous Media at pH 1.2 and 7.4. Phys Chem Liquids 2006; 44(5): 585-596. [ Links ]
9. US Pharmacopeia. 23 ed. United States Pharmacopeial Convention, Rockville, MD; 1994. [ Links ]
10. Cevc G. Lipid Properties as a Basis for Membrane Modeling and Rational Liposome Design. En: Gregoriadis G, editor. Liposomes Technology. BocaRaton: CRC Press; 1993. pp. 1-36. [ Links ]
11. Ganong WF. Fisiología Médica. 17 ed. México: El Manual Moderno; 2000. p. 6. [ Links ]
12. Mora CP, Tello ME, Martínez F. Validación de una metodología analítica para la cuantificación de naproxeno en estudios de reparto líquido/líquido mediante espectrofotometría ultravioleta. Rev Col Cienc Quím Farm 2006; 35(1): 81-105. [ Links ]
13. Martin A, Bustamante P, Chun AHC. Physical Pharmacy: Physical Chemical Principles in the Pharmaceutical Sciences. 4 ed. Philadelphia: Lea & Febiger; 1993. pp. 160-161. [ Links ]
14. Betageri GV, Nayernama A, Habib MJ. Thermodynamics of Partitioning of Nonsteroidal Anti-inflammatory Drugs in the n-Octanol/buffer and Liposome Systems. Int J Pharm Adv 1996; 1(3): 310-319. [ Links ]
15. Budavari S, O'Neil MJ, Smith A, Heckelman PE, Obenchain Jr. JR, Gallipeau, et al. The Merck Index, An Encyclopedia of Chemicals, Drugs, and Biologicals. 13 ed. Whitehouse Station (NJ): Merck & Co; 2001. p. 1149. [ Links ]
16. Mora CP, Lozano HR, Martínez, F. Aspectos termodinámicos de la miscibilidad parcial entre el octanol y el agua. Rev Bras Cienc Farm 2005; 41(1): 13-26. [ Links ]
17. CHEMINFO. Chloroform -Record Number 650. Canadian Centre for Occupational Health & Safety. Ontario, Canada. URL: http://www.ccohs.ca. Consultado: enero de 2006.
18. Dallos A, Liszi J. (Liquid + liquid) Equilibria of (octan-1-ol + water) at Temperatures from 288.15 K to 323.15 K. J Chem Thermodyn 1995; 27(4): 447-448. [ Links ]
19. Ávila CM, Martínez F. Thermodynamic Study of the Solubility of Benzocaine in some Organic and Aqueous Solvents. J Solution Chem 2002; 31(12): 975-985. [ Links ]
20. Garzón LC, Martínez F. Temperature-solubility Dependence for Ibuprofen in some Organic and Aqueous Solvents. J Solution Chem 2004; 33(11): 1379-1395. [ Links ]
21. Krug RR, Hunter WG, Grieger RA. Enthalpy-entropy Compensation. 2. Separation of the Chemical from the Statistical Effects. J Phys Chem 1976; 80: 2341-2351. [ Links ]
22. Bustamante P, Romero S, Peña A, Escalera B, Reillo A. Enthalpy- entropy Compensation for the Solubility of Drugs in Solvent Mixtures: Paracetamol, Acetanilide, and Nalidixic Acid in Dioxane-water. J Pharm Sci 1998; 87(12): 1590-1596. [ Links ]
23. Martínez F, Gómez A. Thermodynamic Study of the Solubility of some Sulfonamides in Octanol, Water, and the Mutually Saturated Solvents. J Solution Chem 2001; 30(10): 909-923. [ Links ]
24. Bevington PR. Data Reduction and Error Analysis for the Physical Sciences. New York: McGraw-Hill; 1969. pp. 56-91. [ Links ]
25. Montgomery DC. Diseño y análisis de experimentos. 2 ed. México: Limusa; 2004. pp. 640-644. [ Links ] ]]>