
Aislamiento de Lactobacillus plantarum LPBM10 y caracterización parcial de su bacteriocina
Isolation of Lactobacillus plantarum LPBM10 and partial characterization of its bacteriocin
Sandra ZAPATA1; Juliana MUÑOZ1; Orlando S. RUIZ1; Olga I. MONTOYA1; Pablo A. GUTIÉRREZ1*
1Grupo de Biotecnología Microbiana. Escuela de Biociencias, Facultad de Ciencias, Universidad Nacional de Colombia Sede Medellín. Calle 59A No 63 - 20, Bloque 19A-211, A.A. 3840. Medellín, Colombia
]]>
RESUMEN
Las bacterias acidolácticas (BAL) son un grupo de microorganismos Gram positivos utilizados ampliamente en la preservación de alimentos debido a sus propiedades probióticas y su capacidad para producir bacteriocinas. Las bacteriocinas son compuestos antimicrobianos de naturaleza peptídica y han recibido gran atención por la industria de alimentos debido a su uso potencial como sustitutos de aditivos químicos. En este trabajo reportamos el aislamiento y caracterización de la cepa de Lactobacillus plantarum LPBM10. Esta bacteria fue aislada a partir de leche fermentada, presenta propiedades probióticas y es productora de bacteriocinas. El extracto libre de células de LPBM10 presenta actividad antimicrobiana frente a bacterias Gram positivas y Gram negativas. La bacteriocina LPBM10 es altamente termoestable, presenta mayor actividad a pH ácido y su actividad no se ve afectada por la presencia de proteinasa K, agentes quelantes y detergentes. El compuesto antibacteriano LPBM10 fue purificado mediante diálisis y cromatografía de exclusión. El análisis por espectroscopía ultravioleta e infrarroja sugiere que la bacteriocina LPBM10 es de naturaleza peptídica con presencia de tirosina y cisteína. Pruebas sobre el extracto crudo dializado mediante cromatografía de intercambio iónico indican la presencia de un compuesto aniónico antagonista del compuesto LPBM10.
Palabras clave: Lactobacillus plantarum, Bacteriocinas, Antimicrobianos.
ABSTRACT
Lactic acid bacteria are a group of Gram-positive microorganisms widely used in food preservation due to their probiotic properties and their ability to produce bacteriocins. Bacteriocins are antibiotic compounds of peptide nature which have been studied intensively for their potential use as substitutes of chemical additives in food preservation. In this paper we report the isolation and characterization of Lactobacillus plantarum LPBM10. This bacteriocin was isolated from fermented milk and can be classified as probiotic. The free cell extract was active against Gram positive and Gram negative bacteria. This bacteriocin is highly thermostable, active at low pH and its activity is not affected by proteinase K, chelating agents and detergents. This antibiotic compound was purified by dyalisis and size exclusion chromatography. Its analysis by UV and FT-IR spectroscopy suggests that bacteriocin is a peptide containing some cystein and tyrosine aminoacids. Experiments on dyalized crude extract by ion-exchange chromatography suggest the presence of an anionic inhibitor of LPBM10.
Keywords: Lactobacillus plantarum, Bacteriocins, Antimicrobials.
INTRODUCCIÓN
]]> Las bacterias acidolácticas (BAL) son un grupo de microorganismos Gram positivos de forma bacilar o cocoide, que tienen la característica de producir ácido láctico y otros compuestos como acetato, etanol, CO2, formato y succionato a partir de carbohidratos fermentables. Este grupo de bacterias incluye géneros como Bifidobacterium, Lactococcus, Lactobacillus, Streptococcus y Pediococcus, que pueden ser aisladas a partir de alimentos fermentados, masas ácidas, bebidas, plantas y los tractos respiratorio, intestinal y vaginal de animales de sangre caliente, entre otros (1, 2). Estas bacterias son consideradas probióticas ya que contribuyen de manera benéfica al balance de la flora intestinal (3, 4) y son efectivas en la prevención y control de desordenes gastrointestinales (5, 6).El amplio uso de las bacterias acidolácticas en la preservación de alimentos se debe a que producen ácidos orgánicos y una gran variedad de sustancias antimicrobianas como peróxido de hidrógeno (H2O2), dióxido de carbono (CO2), diacetil y bacteriocinas (7, 8). Las bacteriocinas son compuestos de naturaleza peptídica, sintetizados ribosomalmente y que, generalmente, tienen como blanco la membrana celular. Se clasifican de acuerdo con sus características químicas y espectros de actividad en cuatro clases. Los péptidos de clase I tienen un tamaño entre 2 y 6 kDa y son modificados postraduccionalmente, mediante la deshidratación de serina y treonina y la posterior adición de cisteína, para fomar los aminoácidos lantionina y metillantionina. La clase II corresponde a péptidos no modificados postraduccionalmente, son termoestables y presentan un rango de actividad bastante limitado. A la clase III pertenecen proteínas con un peso superior a 30 kDa y sensibles al calor. La clase IV está conformada por un grupo heterogéneo de proteínas que presentan adiciones de carbohidratos y lípidos (2,9).
Las bacteriocinas han recibido una gran atención de la industria alimentaria debido a su aplicación potencial en la preservación de alimentos como sustitutos de aditivos químicos (10). La primera bacteriocina aislada y aprobada para ser utilizada en alimentos fue la nisina, la cual comenzó siendo aplicada para controlar la proliferación de esporas de Clostridium botulinum en quesos (11). En la actualidad, las únicas bacteriocinas utilizadas comercialmente son la nisina, producida por Lactococcus lactis (NisaplinTM; Danisco, Dinamarca), y la pediocina PA-1, producida por Pediococcus acidilactici (ALTATM 2431; Kerry Bioscience, Carrigaline, Co. Irlanda). Otras bacteriocinas, como las lacticinas 3147 y 481, están a la espera de ser comercializadas (1).
Lactobacillus plantarum es una de las bacterias más utilizadas en las producción de alimentos fermentados y hasta el momento se han descrito una gran cantidad de bacteriocinas producidas por diferentes cepas (12, 13,14). En este trabajo se reporta el aislamiento y caracterización de una cepa nativa de Lactobacillus plantarum a partir de leche cruda fermentada (15), así como el aislamiento, purificación y caracterización parcial de su bacteriocina. El espectro antibacterial de dicho compuesto antibacteriano sugiere que esta cepa o su bacteriocina pueden ser utilizados como sustancia antimicrobiana de amplio espectro en la preservación de alimentos.
MATERIALES Y MÉTODOS
Aislamiento y caracterización de Lactobacillus plantarum LPBM10
La cepa LPBM10 fue aislada en caldo MRS a partir de leche fermentada naturalmente (sin ningún tipo de inóculo) e incubada a 37°C durante 5 días en condiciones de anaerobiosis. Después se tomó 1 mL de caldo MRS, se inoculó en agar MrRS por profundidad y se incubó bajo las mismas condiciones. A los diferentes aislamientos obtenidos se les hicieron las pruebas de la catalasa, coloración de Gram y producción de esporas. La caracterización bioquímica de LPBM10 se realizó con la prueba API 50CHL (bioMérieux, Inc.). Esta presentó el mejor comportamiento durante el análisis de las propiedades probióticas y fue seleccionada para estudios posteriores (15). La microscopía electrónica de barrido (SEM) se llevó a cabo sobre un extendido de cultivo fresco de LPBM10 fijado por calentamiento. La extracción de plásmidos se hizo según la metología descrita por Duan et al. (16). La cepa LPBM10 fue almacenada a -80 °C en caldo MRS con glicerol al 20%.
Pruebas antimicrobianas y estimación de la actividad bactericida
La actividad bactericida se evaluó con el método de difusión en disco en agar Mueller-Hilton inoculado con la cepa indicadora correspondiente. En la superficie del agar se depositaron discos de papel de filtro de 7 mm de diámetro y tamaño de poro de 100 μm, previamente esterilizados. Los discos fueron impregnados con 20 μl de la solución y las cajas incubadas durante 18 h a 37ºC. La actividad se expresó como la diferencia, en milímetros, entre el radio del halo de inhibición y el radio del disco de papel filtro. Las cepas indicadoras utilizadas fueron: Lactobacillus brevis, Klebsiella sp., Bacillus cereus, Bacillus pumilus, Bacillus subtilis y Serratia marcescens, Salmonella tiphy (ATCC 6539), Listeria monocytogenes (ATCC 7644), Staphylococcus aureus (ATCC 1395) y Escherichia coli (ATCC 25922). Todas las cepas fueron recuperadas en medio BHI a 37°C por 24 h., a excepción del L. brevis que fue activado en caldo MRS a 30°C por 48 h.
]]> Cinética de crecimiento y producción de sustancias antimicrobianasSe inocularon 100 mL de un cultivo de L. plantarum LPBM10 en 900 mL de caldo MRS; y se incubó a 30°C y 150 rpm durante 33 h. Se tomaron 10 mL del cultivo cada 3 horas y se monitoreó el crecimiento bacteriano determinando la absorbancia a 600 nm. Para la medición de la actividad del extracto se centrifugaron 9 mL muestra del cultivo durante 20 min (6000 g, 4°C). El sobrenadante fue esterilizado mediante filtración con una membrana de 0.45 μm y se sometió a calentamiento a 80ºC por 10 minutos, con el fin de prevenir la acción de enzimas proteolíticas. La actividad del extracto libre de células fue medida por el método de difusión en disco descrito anteriormente.
Efecto de enzimas, temperatura, pH y surfactantes sobre la actividad bactericida
El extracto libre de células se incubó en presencia de proteinasa K a 37°C (1mg/mL) por 6 horas; después de la incubación, la enzima fue inactivada por calentamiento durante 30 minutos. Las pruebas con SDS, Urea, Tween 20®, Tween 80® y Tritón X-100® se realizaron a una concentración del 1% en el extracto libre de células. El efecto del EDTA fue evaluado a una concentración de 0.1, 2 y 5 mM. La actividad antimicrobiana fue determinada después de un periodo de incubación de 6 horas a 37°C. Para determinar el efecto del pH, se tomaron 10 μL de una fracción de cromatografía concentrada y se mezclaron con 10 μL de solución tampón (0.1 M acetato, pH 3.6, 4.2, 4.8 y 5.4; fosfato de potasio 0.1 M, pH 6.0, 6.6. 7.3 y 7.8; Tris-HCl 0.1 M, pH 8.2 y 8.6). No se observó ningún efecto inhibitorio de las soluciones tampón utilizadas sobre las cepas indicadoras. La prueba de termoestabilidad se realizó mediante incubación a 94°C durante 2 h, se recolectó 1 mL de muestra cada 10 min. Después se determinó la actividad residual de cada una de las pruebas y los halos de inhibición fueron comparados con un control apropiado.
Purificación de sustancias antimicrobianas
El extracto libre de células se dializó utilizando una membrana de diálisis de 3.5 kDa (BioLynx Inc.). El filtrado se pasó por una columna Biogel P10 (Bio-Rad Laboratories, Inc.) de dimensiones 11 x 90 mm, preequilibrada con agua destilada. Se tomaron fracciones de 0.5 mL y se seleccionaron aquellas que presentaron actividad antimicrobiana. Las fracciones activas se unieron, se concentraron y se analizaron por espectroscopía ultravioleta en un espectrofotómetro GENESYS 6 (Thermo Scientific) en un rango de 190-400 nm, tomando datos en intervalos de 1 nm. La bacteriocina fue cuantificada utilizando los coeficientes de extinción a 205 (49.8 mg.ml-1.cm-1) y 280 nm (262 mg.ml1.cm-1), determinados con el método de Scopes (17). El espectro infrarrojo se realizó con una muestra resuspendida en metanol, en un equipo Spectrum BX con transformada de Fourier (Perkin elmer). La cromatografía de capa fina se realizó en placas de Silica gel G60 F254 (Merck, Germany), disolviendo la muestra en metanol y utilizando como eluente metanol/cloroformo (2:1); además el proceso de revelado se realizó por calentamiento después de aplicarle una solución de H2SO4/H2O (1:1).
El filtrado de diálisis se pasó por una columna de intercambio aniónico (Macro-Prep® DEAE support) de dimensiones 28 x 3 mm, preequilibrada con agua destilada. Las sustancias aniónicas se eluyeron con 2 volúmenes de NaCl 50, 200 y 2000 mM y se evaluó la actividad antimicrobiana. La cromatografía de intercambio catiónico se realizó bajo las mismas condiciones descritas para la cromatografía de intercambio catiónico utilizando una resina de carboximetilcelulosa (Macro-Prep® CM support).
RESULTADOS Y DISCUSIÓN
Caracterización bioquímica y morfológica de la cepa LBPM10
]]> La caracterización preliminar de LPBM10 permite establecer que esta cepa corresponde a un microorganismo Gram positivo, catalasa negativa, que forma colonias de tamaño grande, cremosas, de color beige, con bordes homogéneos y cóncavas en agar MRS. LPBM10 tiene potencial probiótico, tal como lo indica su crecimiento a un pH ácido de 2.0 y 0.3% de sales biliares (15). La cepa LPBM10 fue identificada como Lactobacillus plantarum mediante características morfológicas y la fermentación de carbohidratos mediante la prueba API 50CHL (bio-Mérieux, Inc.) (18, 19). La microscopia electrónica de LPBM10 muestra que esta bacteria tiene forma de varilla recta con extremos redondeados y dimensiones de ~ 0.7 μm x 1.6 μm (Véase figura 1). No se encontraron plásmidos asociados a LPBM10.
Figura 1. Microscopia electrónica de barrido de Lactobacillus plantarum LPBM10.
Crecimiento de LBPM10 y producción de bacteriocinas
La producción de sustancias antimicrobianas por la cepa LBPM10 fue determinada mediante la medición de la actividad antimicrobiana del extracto libre de células en diferentes fases de crecimiento (Véase figura 2). LBPM10 presenta actividad antimicrobiana constitutiva con un máximo a las doce horas, correspondientes al final de la fase exponencial. El máximo de actividad se mantuvo constante durante 12 horas y comenzó a decrecer a las 27 horas demostrando que la producción de bacteriocinas depende de la fase de crecimiento y es estable en el medio de producción durante largos periodos. Estos resultados son similares a los obtenidos por Nissen-Meyer et al. (20) y González et al. (21), quienes reportan que la actividad antimicrobiana de L. lactis y L. plantarum comienza a decaer una vez comienza la fase estacionaria.
Espectro antimicrobiano de LPBM10
El extracto libre de células de Lactobacillus plantarum LPBM10 mostró un efecto antibacterial frente a bacterias Gram positivas como Bacillus cereus, Bacillus pumilus, Bacillus subtilis, Listeria monocytogenes (ATCC 7644) y Staphylococcus aureus (ATCC 1395); y bacterias Gram negativas como Salmonella tiphy (ATCC 6539), Escherichia coli (ATCC 25922), Klebsilella sp. y Serratia marcescens. No se encontró actividad frente a Lactobacillus brevis, lo que se explica por la cercanía entre ambas especies que pueden compartir un mecanismo de defensa frente a sus propios compuestos antimicrobianos (9). El efecto bactericida del extracto frente a las bacterias Gram negativas es interesante ya que pocos extractos de bacterias acidolácticas han mostrado actividad antimicrobiana frente a este grupo de bacterias. En L. plantarum se ha reportado actividad frente a bacterias Gram negativas con la plantaricina 35d (22) y las bacteriocinas producidas por las cepas ST194BZ, ST414BZ y ST664BZ (23).
]]>
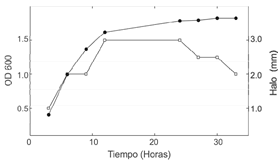
Figura 2. Crecimiento de L. plantarum LPBM10 (•) y producción de bacteriocinas en caldo MRS a 30°C (•).
Efecto de pH, temperatura, enzimas, surfactantes y EDTA
La actividad bactericida asociada al extracto libre de células es muy estable en condiciones extremas de temperatura. El almacenamiento del extracto a -20 y -80°C no tiene ningún efecto sobre su actividad bactericida. El calentamiento durante 2 horas a 95°C tampoco afecta negativamente la actividad, al contrario, se observa que la actividad del extracto aumenta al ser calentado previamente. La estabilidad térmica es una propiedad común en las bacteriocinas de bácterias acidolácticas de bajo peso molecular y muy importante para los compuestos utilizados como bioconservantes ya que muchos de los procesos de la industria alimentaria involucran pasos de calentamiento y preservación a bajas temperaturas (21, 23, 24).
La actividad antimicrobiana del extracto de LPBM10 es mayor entre un pH de 3.6-5.4 con un máximo a pH 4.2 y presenta actividad reducida encima de 6.0. Esta dependencia del pH sobre la actividad puede ser el reflejo de la protonación de un aminoácido titulable, tal como se observa en algunos lantibióticos (25) (Véase figura 3). Estos resultados concuerdan con los obtenidos por González et al. (21) quienes reportaron que la plantaricina C producida por L. plantarum LL41 pierde su actividad a pH alcalino. Resultados similares se han obtenido para algunas sustancias antimicrobianas producidas por otras cepas de Lactobacillus y Lactococcus (12, 22, 23, 26).
Figura 3. Efecto del pH sobre la actividad de la bacteriocina producida por LPBM10.
]]> A diferencia de otros, Lactobacillus, cuya actividad antimicrobiana es sensible al tratamiento con proteasas (23), el extracto libre de células de LPBM10 conserva su actividad luego de una incubación con proteinasa K. Resultados similares fueron obtenidos con la plantaricina 423, la cual pierde su actividad luego de ser tratada con proteinasa K, pepsina, papaína y tripsina (12). Sin embargo, la plantaricina C, pese a ser sensible al tratamiento con pronasa, tripsina y quimotripsina, no pierde su actividad en presencia de pepsina y proteinasa K (21). La resistencia a proteasas es común en compuestos como los lantibióticos, los cuales, al sufrir grandes modificaciones postraduccionales, son altamente resistentes a la acción de estas enzimas hidrolíticas (27).
Se ha demostrado que algunos agentes quelantes como el EDTA ayudan a la potenciación de la actividad de compuestos antimicrobianos, especialmente contra bacterias Gram negativas como Salmonella enterica y E. coli (28). El secuestro de cationes desestabiliza la membrana externa y facilita la formación de poros que permiten la difusión de bacteriocinas hacia la membrana citoplasmática. La actividad del extracto no se afectó en presencia de EDTA, lo que indica que la actividad del péptido es indiferente a la permeabilización de la membrana externa. Las interacciones con la membrana pueden ser simuladas con detergentes como SDS, Tween 20®, Tween 80® y Triton X-100®, los cuales pueden tener un efecto antagónico sobre la actividad de las bacteriocinas. La presencia de detergentes no tuvo ningún efecto sobre la actividad antibacteriana sugiriendo que la partición en un ambiente no polar no es fundamental en el mecanismo de acción de esta bacteriocina. Un efecto similar se observa en algunas bacteriocinas tipo I, las cuales se asocian con los grupos fosfato de precursores de la pared bacteriana, como el lípido II, pero no necesitan insertarse en la región lipídica de la membrana (29).
Caracterización parcial del compuesto antimicrobiano
Con el fin de caracterizar el compuesto responsable de la actividad antimicrobiana de LPBM10, se llevó a cabo su purificación parcial. Con el fin de establecer el peso molecular del compuesto se realizó una diálisis del extracto crudo, utilizando una membrana con un corte de 3.5 kDa. Al tomar la fracción externa se verificó que el compuesto antimicrobiano había traspasado la membrana indicando que su peso molecular debe ser menor a este tamaño de corte. Esta fracción arrojó resultados positivos para la prueba de Bradford (30). El filtrado se concentró y se pasó a través de una columna de exclusión P10, la fracción activa correspondió a un volumen de elución entre 4.5 y 6 mL (Véase figura 4). Las fracciones cromatográficas parecen estar puras al ser analizadas por cromatografía de capa fina (Véase figura 4) y fueron nuevamente positivas para la prueba de Bradford, indicando que el compuesto es de carácter peptídico. La muestra purificada presenta un halo de inhibición frente a E. coli de 7.5 mm en una concentración de 120 mg/mL, comparable al obtenido con el antibiótico ampicilina cuyo halo es de 3 mm a una concentración de 100 mg/mL.
Figura 4. Cromatografía de exclusión del filtrado de diálisis del extracto libre de células de LPBM10 y actividad de la fracción purificada.
La muestra purificada fue analizada mediante espectroscopía ultravioleta e infrarroja (Véase figura 5). El espectro de absorción ultravioleta en el rango 190-320 nm presenta máximos a una λ de 207 y 274 nm con un patrón característico de proteínas. La absorción cercana a una λ de 205 nm es atribuible a los enlaces peptídicos mientras que a una λ de 280 nm se atribuye por lo general a los aminoácidos triptófano (λ max = 280) y tirosina (λ max = 274). El máximo a una λ de 274 nm sugiere la presencia de tirosina. En el espectro infrarrojo se observa una banda a 2664 cm-1 característica de mercaptanos que sugiere la presencia de cisteínas.
]]>
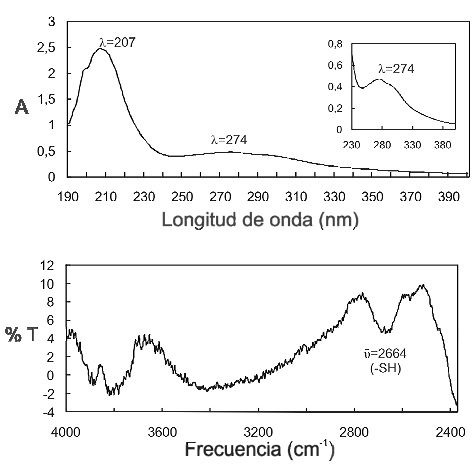
Figura 5. Espectro ultravioleta e infrarrojo de la bacteriocina producida por LPBM10.
Con el fin de determinar la carga del compuesto antimicrobiano, se pasó el filtrado de diálisis por columnas de intercambio aniónico y catiónico. En ambos casos, la actividad antimicrobiana fue detectada en la solución efluente, lo que indica que el compuesto antimicrobiano no posee una carga significativa que le permita adherirse a la columna en las condiciones de corrido (pH 7.0). De manera sorprendente, el efluente de la cromatografía aniónica presentó mucha mayor actividad respecto a la muestra inicial (Véase figura 6). Este resultado sugiere la presencia de un inhibidor de la bacteriocina de carácter aniónico. Si se tiene en cuenta que la mayoría de los péptidos antimicrobianos interactúan con lípidos aniónicos de la membrana bacteriana, es posible que el efecto inhibitorio sea ocasionado por la presencia de remanentes de estos lípidos en el filtrado de diálisis. Este resultado explica el aumento de la actividad antimicrobiana cuando el extracto es sometido a calentamiento.
Pese a que existen varios procesos en la industria de alimentos para prevenir o minimizar la contaminación bacteriana, los casos de intoxicación ocurren aún con frecuencia. En este sentido, las bacterias tienen una importante aplicación práctica en el mejoramiento de la vida útil de alimentos y la prevención de transmisión de enfermedades. Una bacteria cuyo control merece particular atención es L. monocytogenes, ya que este es un microorganismo ubicuo en el ambiente que puede persistir durante largos periodos a temperaturas de refrigeración y altas concentraciones de sal. Son numerosos los casos de listeriosis reportados en el mundo. Por ejemplo, sólo en los Estados Unidos, se estima que L. monocytogenes es responsable de 500 muertes anuales (31). Otros microorganismos responsables de enfermedades transmitidas por alimentos son bacterias Gram negativas como Escherichia coli, Campylobacter y Salmonella entre otros (32). En la industria de alimentos, las bacterias Gram negativas representan un gran problema económico y de salud pública ya que presentan una resistencia inherente a algunos de los compuestos antimicrobianos utilizados. Esto hace que la sustancia antimicrobiana producida por L. plantarum LPBM10 tenga una prometedora aplicación al ser activa frente a bacterias Gram negativas, a diferencia de la gran mayoría de bacteriocinas reportadas hasta el momento.
Las bacteriocinas pueden ser incorporadas en los alimentos en forma pura, mediante adición de un ingrediente previamente fermentado por una cepa productora o mediante la utilización de inóculos bacterianos productores de bacteriocinas in situ. Para examinar el potencial de utilización de la bacteriocina LPBM10 en alimentos será necesario caracterizar en detalle la secuencia de aminoácidos y/o clonar su gen codificante para determinar su similitud con otros compuestos antimicrobianos descritos en la literatura. También será necesario optimizar los métodos de producción y purificación que permitan la obtención de grandes cantidades de este compuesto a costos más reducidos para que sea viable su producción industrial a gran escala.
Figura 6. Efecto del calentamiento (A), intercambio catiónico (B) y aniónico (B) sobre la actividad bactericida del dializado del extracto libre de células de LPBM10.
]]> AGRADECIMIENTOS
Agradecemos al Dr. Carlos Pelaéz y a Giann Peñaloza, del Grupo Interdisciplinario de Estudios Moleculares de la Universidad de Antioquia (GIEM), por su valiosa contribución en la discusión y el desarrollo de experimentos preliminares. A Benjamín Rojano, Tatiana Lobo y Karol Zapata, del Laboratorio de Ciencia de los Alimentos, a Medardo Pérez, del laboratorio de Microscopía Avanzada, a Mauricio A. Marín, del Laboratorio de Biología Celular y Molecular y a Jairo Quijano, del Laboratorio de Fisicoquímica Orgánica. Este proyecto se realizó con financiación de la Dirección de Investigaciones de la Universidad Nacional de Colombia, Sede Medellín (DIME, proyecto 20101006544).
REFERENCIAS BIBLIOGRÁFICAS
1. Deegan LH. Bacteriocins: Biological tools for bio-preservation and shelf-life extension. Int Dairy J. 2006; 16 (9): 1058-1071. [ Links ]
2. Savadogo A, Ouattara CAT, Bassole IHN, Traore AS. Bacteriocins and lactic acid bacteria: a mini review. Afr J Biotechnol. 2006; 5 (9): 678-683. [ Links ]
3. Lilley DM, Stilwell RH. Probiotics growth promoting factors produced by microorganisms. Science. 1965; 147 (3659): 747-748. [ Links ]
4. Schrezenmeir J, de Vrese M. Probiotics, prebiotics and symbiotics: approaching a definition. Am J Clinical Nutr. 2001; 73 (2): 361-364. [ Links ]
5. Bhatnagar S, Singh KD, Sazawal S, Saxena SK, Bhan MK. Efficacity of milk versus yoghurt offered as part of a mixed diet in acute noncholera diarrhea among malnourished children. J Pediatr. 1998; 132 (6): 999-1003. [ Links ]
6. Guandalini S, Pensabene L, Zikri MA, Dias JA, Casali LG, Hoesktra H et al. Lactobacillus GG administered in oral rehydratation solution to children with acute diarrhea : a multicenter European trial. J Pediatr Gastroenterol Nutr. 2000; 30 (1): 54-60. [ Links ]
7. Podolak PK, Zayas JF, Kastner CL, Fung DYC. Inhibition of Listeria monocytogenes and Escherichia coli O157:H7 on beef by application of organic acids. J Food Prot. 1996; 59 (4): 370-373. [ Links ]
8. Smulders FJM, Barendsen P, van Logstestijn JG, Mossel DAA, van der Marel GM. Lactic acid: considerations in favor of its acceptance as a meat decontaminant. J Food Technol. 1986; 21: 419-436. [ Links ]
9. Jack RW, Tagg JR, Ray B. Bacteriocins of Gram-Positive Bacteria. Microbiol Rev. 1995; 171 (2): 171-200. [ Links ]
10. Lewus CB, Kaiser A, Montville TJ. Inhibition of food-borne bacterial pathogens by bacteriocins from lactic acid bacteria isolated from meat. Appl Environ Microbiol. 1991; 57 (6): 1683-1688 [ Links ]
11. Chung K, Dickson J, Crouse J. Effects of nisin on growth of bacteria attached to meat. Appl Environ Microbiol. 1989; 55 (6): 1329-1333 [ Links ]
12. vanReenenCA,DicksLMT,ChikindasML.Isolation,purification and partial characterization of plantaricin 423, a bacteriocin produced by Lactobacillus plantarum. J Appl Microbiol. 1998; 84 (6): 1131-1137. [ Links ]
13. Ruiz-Barba JM, Piard JC, Jiménez-Díaz R. Plasmid profiles and curing of plasmids in Lactobacillus plantarum strains isolated from green olive fermentation. J App Bacteriol. 1991; 71 (5): 417-421. [ Links ]
14. Kato T, Matsuda T, Ogawa E, Ogawa H, Kato H, Doi U et al. Plantaricin-149, a bacteriocin produced by plantaricin NRIC 149. J Ferment Bioeng. 1994; 77 (3): 277-282. [ Links ]
15. Salazar B. Aislamiento de cepas nativas de probióticos y comparación de la viabilidad por efecto de un prebiótico. [Tesis de maestría]. Medellín: Escuela de Biociencias, Facultad de Ciencias, Universidad Nacional de Colombia; 2003. [ Links ]
16. Duan K, Dunn NW, Kim WS. Rapid plasmid DNA isolation from Lactococcus lactis using overnight cultures. Biotechnol Tech. 1999; 13 (8): 519-21. [ Links ]
17. Scopes RK. Measurement of protein by spectrophotometry at 205 nm. Anal Biochem. 1974; 59 (1): 277-282. [ Links ]
18. Schillinger U, Lucke FK. Identification of lactobacilli from meat and meat products. Food Microbiol. 1987; 4 (3): 199-208. [ Links ]
19. Stiles ME, Holzapfel WH. Lactic acid bacteria of foods and their current taxonomy. Int J Food Microbiol. 1997; 36 (1): 1-29. [ Links ]
20. Nissen-Meyer J, Holo H, Havarstein LS, Sletten K, Nes IF. A Novel Lactococcal Bacteriocin whose activity depends on the complementary action of two peptides. J Bacteriol. 1992; 174 (17): 5686-5692. [ Links ]
21. González B, Arca P, Mayo B, Suárez JE. Detection, Purification, and Partial Characterization of Plantaricin C, a Bacteriocin Produces by a Lactobacillus plantarum Strain of Dairy Origin. Appl Environ Microbiol. 1994; 60 (6): 2158-2163. [ Links ]
22. Messi P, Bondi M, Sabia C, Battini R, Manicardi G. Detection and preliminary characterization of a bacteriocin (plantaricin 35d) produced by a Lactobacillus plantarum strain. Int J Food Microbiol. 2001; 64 (1-2): 193-198. [ Links ]
23. Todorov SD, Dicks LMT. Lactobacillus plantarum isolates from molasses produces bacteriocins active against Gram-Negative bacteria. Enzyme Microb Technol. 2005; 36 (2-3): 318-326. [ Links ]
24. Jiménez-Díaz R, Ríos-Sánchez RM, Desmazeaud M, Ruiz-Barba JL, Piard JC. Plantaricins S and T, two newbacteriocins produced by Lactobacillus plantarum LPCO10 isolated from a green olive fermentation. Appl Environ Microbiol. 1993; 59 (5): 1416-1422. [ Links ]
25. Sahl HG, Bierbaum G. Lantibiotics: Biosynthesis and Biological activities of Uniquely Modified Peptides from Gram-Positive Bacteria. Annu Rev Microbiol. 1998; 52 : 41-79. [ Links ]
26. Verellen TLJ, Bruggeman G, van Reenen CA, Dicks LMT, Vandamme EJ. Fermentation optimisation of plantaricin 423, a bacteriocin produced by Lactobacillus plantarum 423. J Ferment and Bioeng. 1998; 86 (2): 174-179. [ Links ]
27. Willey JM, van der Donk WA. Lantibiotics: Peptides of Diverse Structure and Function. Annu Rev Microbiol. 2007; 61 : 477-501. [ Links ]
28. Belfiore C, Castellano P. Vignolo G. Reduction of Escherichia coli population following treatment with bacteriocins from lactic acid bacteria and chelators. Food Microbiol. 2007; 24 (3): 223-229. [ Links ]
29. Martin NI, Breunkink E. The expanding role of lipid II as a target for lantibiotics. Future Microbiol. 2007; 2 (5): 513-525. [ Links ]
30. Bradford MM. A rapid and sensitive method for the quantitation of microgram quantities of protein utilizing the principle of protein-dye binding. Anal Biochem. 1976; 72: 248-254. [ Links ]
31. Centers for Disease Control and Prevention. Atlanta, USA, 2008 [Sitio en Internet]. Disponible en http://www.cdc.gov/nczved/ dfbmd/disease_listing/listeriosis_gi.html. Consultado: 8 de agosto de 2008. [ Links ]
32. Adak GK, Long SM, O"Brian SJ. Trends in indigenous foodborne disease and deaths in England and Wales. Gut. 2002; 51 (6): 832-841. [ Links ]
Recibido: Julio 21 de 2008.
Aceptado: Enero 20 de 2009.
]]>
* Autor a quien se debe dirigir la correspondencia: paguties@unalmed.edu.co
]]>