Esteroles libres de la esponja marina Mycale laevis
Free sterols from the marine sponge Mycale laevis
Hernán A. VALLE Z.1*; Gilmar G. SANTAFÉ P. 2
1Grupo de Investigación, Productos Naturales Marinos, Facultad de Química Farmacéutica, Universidad de Antioquia, Calle 67 53-108, Laboratorio 2-131. Medellín, Colombia
2Grupo de Investigación, Química de los Productos Naturales, Departamento de Química, Universidad de Córdoba, Carrera 6 76-103. Montería, Colombia
]]>
RESUMEN
El desarrollo de las investigaciones en bioprospección marina requiere el fortalecimiento de los inventarios de organismos marinos, lo que implica una clasificación taxonómica exhaustiva de los mismos. La clasificación de las esponjas marinas es compleja desde el punto de vista morfológico y se facilita con el uso de información quimiotaxonómica basada en la composición de sus esteroles. El presente estudio describe la composición de esteroles libres de la esponja Mycale laevis, recolectada en la Bahía de Cispatá (Córdoba, Colombia). A partir del extracto metanólico de la esponja M. laevis, se obtiene el subextracto de diclorometano, que se fracciona mediante cromatografía en columna sobre sílica gel, eluyendo con mezclas de hexano-acetato de etilo con aumento gradual de la polaridad. La obtención de la fracción mayoritaria (Rf = 0.77, sílica gel/ hexano-acetato de etilo 1:1) y su análisis por cromatografía de gases acoplada a espectrometría de masas (CG-EM), permite la identificación de 9 esteroles monohidroxilados con núcleos esteroidales Δ0, Δ5 y Δ7 . Los estanoles (núcleo Δ0) son los más abundantes en la fracción esterólica, con el 71.7 % del total de compuestos presentes. Estos resultados contribuyen a los estudios quimiotaxonómicos de esponjas marinas pertenecientes a la familia Mycalidae.
Palabras clave: Mycale laevis, Esponjas, Esteroles, Cromatografía de gases, Espectrometría de masas.
ABSTRACT
The development of marine bioprospection research requires to fortify of marine organisms inventories, which also implies their exhaustive taxonomic classification. From the morphological point of view, the classification of marine sponges is a complex procedure and it is facilitated with the use of chemotaxonomic information based on the composition of its sterols. This study describes the free sterols composition of the Mycale laevis sponge, collected in the Cispatá Bay (Córdoba, Colombia). The subextract of dichloromethane is obtained from the methanol extract of the sponge; this subextract is fractionated through chromatography in column on silica gel, using hexane-ethyl acetate mixtures with a gradual increase of the polarity as a mobile phase. The obtention of the majoritary fraction (Rf = 0.77, silica gel /hexane: ethyl acetate 1:1) and its analysis by means of gas chromatography coupled to mass spectrometry (GC-MS), allows the identification of 9 monohydroxylated sterols with nuclei steroidal Δ0,Δ5 and Δ7 sterols. Stanols (nucleus Δ0) are the most abundant in the sterolic fraction with 71.7% of the total of the present compounds. These results contribute to chemotaxonomics studies marine sponges in the Mycalidae family.
Key words: Mycale laevis, Sponges, Sterols, Gas Chromatography, Mass spectrometry.
INTRODUCCIÓN
]]> Las esponjas (Filo Porífera) son animales sedentarios reconocidos por producir la mayor cantidad de compuestos inusuales entre los diferentes grupos de organismos marinos. En la actualidad existen 5.500 especies diferentes de esponjas, de las cuales 1.185 han sido estudiadas en busca de compuestos químicos, encontrándose 6.668 compuestos en total (base de datos MarinLit) (1).Las esponjas son la mayor fuente de esteroles con estructuras inusuales en el ambiente marino, lo que puede comprobarse con los 250 esteroles polares descubiertos hasta el año 2002 (2); adicionalmente se identificaron 80 esteroles en esponjas, entre los años 2003 y 2008 (1,3-7). Los esteroles “inusuales” difieren estructuralmente de los este-roles “comunes” (que tienen núcleos 3β-hidroxi-Δ5 o Δ0-colestano y cadenas laterales C8-C10) por presentar una o ambas de las siguientes características: (i) cadenas laterales con tamaños entre C-0 y C-12 que han perdido o ganado átomos de carbono en posiciones diferentes a C-24, y (ii) núcleos y/o cadenas laterales con oxigenación múltiple (2). Las esponjas marinas se caracterizan por su gran plasticidad morfológica y, por lo tanto, resulta complicada la diferenciación entre ciertas especies, géneros e incluso familias. Para resolver este problema, se han realizado estudios quimiotaxonómicos en esponjas basados en la composición de sus esteroles totales, tanto “comunes” como “inusuales” (8). La importancia de los esteroles de esponjas no radica únicamente en el campo de la taxonomía, también existen informes que demuestran la utilidad de estos compuestos como agentes antimicóticos, citotóxicos, anticolonizadores y anticancerígenos (6-9). En lo que concierne a la esponja Mycale laevis se han identificado ácidos grasos monoinsaturados con estructuras nuevas (10); sin embargo, ha sido poco estudiada desde el punto de vista químico. El siguiente trabajo investigativo pretende aportar conocimientos químicos acerca de la esponja Mycale laevis que podrían servir como caracteres químicos de clasificación sistemática a los quimiotaxónomos que estudian la familia Mycalidae. Para lograr este objetivo, se obtuvo la fracción esterólica del extracto metanólico de la esponja por métodos cromatográficos (cromatografía en columna) y luego se analizó mediante la técnica cromatografía de gases acoplada a espectrometría de masas (CG-EM). El análisis de los espectros de masas de los componentes separados, sugiere la presencia de 9 esteroles monohidroxilados, cuyas estructuras fueron confirmadas por comparación de los espectros y tiempos de retención (en Cromatografía de Gases) con los de muestras auténticas reportadas en la literatura especializada.
MATERIALES Y MÉTODOS
Colecta y ubicación taxonómica de la esponja marina
Se recolectaron aproximadamente 1.500 g húmedos de la esponja Mycale laevis, mediante buceo autónomo en el sitio conocido como Piedras de Ararat, del complejo de la Bahía de Cispatá (departamento de Córdoba), a una profundidad de 10 metros. Inmediatamente después de recolectarla se lavó con abundante agua destilada, se refrigeró y transportó al Laboratorio de Productos Naturales de la Universidad de Córdoba (Montería). La ubicación taxonómica fue realizada por personal experto del Instituto de Investigaciones Marinas (INVEMAR) de Santa Marta (Colombia) y se hizo con base en las características del esqueleto de espículas. Una muestra de la esponja está disponible en el Museo de Historia Natural Marina de Colombia con el número de catálogo POR-229.
Obtención del extracto
Después de 24 horas de refrigeración a -15ºC, se cortó la esponja en trozos pequeños y se sometió a extracción con metanol en un recipiente de vidrio (ámbar) a temperatura ambiente por un período de 72 horas; luego se filtró el extracto y se evaporó al vacío (a 45ºC) hasta obtener una suspensión acuosa que posteriormente se extrajo con diclorometano; este procedimiento se repitió dos veces más para garantizar la máxima extracción de los metabolitos secundarios. Las fases en diclorometano se reunieron y se secaron en el rotavaporador (11, 12) y se obtuvieron 4.34 g de un residuo café oscuro de consistencia viscosa, rotulado como “subextracto de diclorometano de Mycale laevis”; el subextracto se mantuvo en condiciones de oscuridad y baja temperatura (-15ºC).
Aislamiento y purificación de compuestos
El subextracto de diclorometano (1.5 g) de la esponja se sometió a fraccionamiento por Cromatografía en Columna (CC) con fase estacionaria de sílica gel 60 (0.063-0.2 mm / 70-230 mallas, Merck) y fase móvil con gradiente de polaridad creciente basado en el siguiente sistema de elución: hexano-acetato de etilo (5:2), hexano-acetato de etilo (1:1), acetato de etilo y acetato de etilo-metanol (1:1). Las fracciones obtenidas se monitorearon por Cromatografía en Capa Fina (CCF) para verificar si se trataba de compuestos puros o de mezclas. Para el monitoreo se utilizaron cromatoplacas de aluminio (20 X 20 cm) con sílica gel 60 F-254 y un espesor de 0.2 mm, usando como eluentes los mismos sistemas de elución con las que se obtuvieron a partir de Cromatografía en Columna (CC). Como reveladores cromatográficos se utilizaron: una lámpara ultravioleta marca CAMAG (254 y 366 nm) y una solución de ácido fosfomolíbdico al 5% en etanol para asperjar la placa, que se calentaba posteriormente. Las fracciones que presentaron entre sí un Rf similar, se reunieron en una sola y se evaporaron al vacío. La fracción mayoritaria (0.411 g) presentó el mismo valor de Rf que un patrón de colesterol con el que se comparó posteriormente. Esta fracción se conservó en la oscuridad a -15ºC para su posterior análisis mediante Cromatografía de Gases acoplada a Espectrometría de Masas (CG-EM).
]]> Elucidación estructuralLa fracción mayoritaria (25 mg) se analizó mediante la técnica de Cromatografía Gaseosa acoplada a Espectrometría de Masas (CG-EM), para adquirir información estructural de sus componentes. El análisis se realizó en un equipo Shimadzu GC-17, utilizando una columna capilar de sílica fundida HP-1 (25 m X 0.2 mm d.i.) y helio como gas de arrastre a 1.0 mL/min. La temperatura de la columna se mantuvo a 270ºC, la relación de split fue de 1:10 y el volumen de inyección fue de 1 a 2 μL. El detector utilizado fue un espectrómetro de masas Shimadzu modelo QP-5050A, con una fuente de ionización de 70 eV, y un filamento de 60 μA mantenido a 300ºC. Como patrón de referencia se utilizó colesterol (tiempo de retención en estas condiciones: 29 min). El espectro de cada componente se analizó y luego se comparó con los de sustancias patrón referenciadas en la bibliografía (13, 14, 15). Los tiempos de retención relativos al colesterol de cada componente, obtenidos experimentalmente (TRR-exp) con la técnica Cromatografía de Gases (CG), fueron comparados con los reportados en la literatura (TRR-lit) (13, 15). El análisis cuantitativo se efectuó por medio del método de normalización de áreas de los cromatogramas que fueron calculadas en el modo analítico de la técnica CG.
RESULTADOS Y DISCUSIÓN
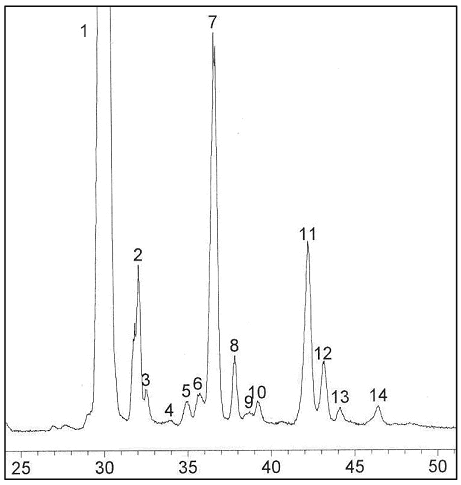
Al finalizar el proceso de fraccionamiento por Cromatografía en Columna (CC) del subextracto de diclorometano, se obtuvieron 6 fracciones, de las cuales llamó la atención la tercera por ser la mayoritaria (0.411 g), además de presentar diminutos cristales en forma de agujas de color verde y un comportamiento cromatográfico similar a un patrón de colesterol con el que fue comparada (Rf = 0.77, en CCF, sílica gel/ hexano : acetato de etilo 1:1); esta información preliminar permitió inferir la presencia de compuestos esterólicos. En el cromatograma obtenido por la técnica CG (Veáse figura 1), se puede observar una mezcla de 14 componentes separados, de los cuales 9 fueron identificados (componentes: 1, 3, 5, 6, 7, 10, 11, 12 y 14). Al finalizar el proceso de identificación, se confirmó la naturaleza esterólica de los 9 componentes mencionados.
Figura 1. Cromatograma de gases de la fracción esterólica mayoritaria presente en el subextracto de diclorometano de la esponja Mycale laevis.
La figura 2 corresponde al espectro de masas del componente 1, en donde se evidencia la señal con valor de m/z 388, que pertenece al ión molecular del compuesto C27H48O. También se presentan los fragmentos generales en los valores de m/z: 373 (M+-CH3 ) y 355 (M+-[CH3 +H2O]) que son característicos de un esterol. Además, son importantes los fragmentos intensos, m/z: 233, 215 y 147, que indican la ausencia de insaturaciones en el núcleo esteroidal, lo que permite concluir que es del tipo Δ0 -3β-hidroxiandrostano. La diferencia entre el ión molecular y la señal m/z 275 determinó la composición de la cadena lateral como C8H17 , la cual es completamente saturada. Las señales m/z: 331 (M+-57) y 303 (M+-85) corresponden a la escisión simple de los fragmentos C4H9 · y C6H13·, a partir de la cadena lateral, e indican que los átomos de carbono que la conforman tienen una disposición igual a la cadena lateral del colesterol. Al comparar el espectro de masas del componente 1 y su tiempo de retención relativo al colesterol, con los provenientes de otros estudios realizados en fracciones esterólicas de esponjas marinas (13), se encontró que correspondía al del esterol: colestan-3β-ol (trr-exp = 1.02 versus trr-lit = 1.02).
]]>Figura 2. Espectro de masas del componente 1.
Figura 3. Espectro de masas del componente 3.
En el espectro de masas de la figura 3 (componente 3) se observa el ión molecular con un valor de m/z 386 correspondiente al compuesto de fórmula C27H46O. También se observan las señales de los fragmentos generales con valores m/z: 371 (M+-CH3) y 353 (M+-[CH3 +H2O]), característicos de los esteroles.
Otros fragmentos presentes tienen valores m/z: 273 (pérdida de la cadena lateral), 255 (pérdida de la cadena lateral-H2O), 246 (típico del núcleo Δ7 ), 231 (fisión del anillo D) y 213 (fisión del anillo D-H2O), que indican la presencia de una insaturación en el C7 del núcleo esteroidal. La diferencia entre el valor de m/z del ión molecular y el ión m/z 273 determinó la existencia de una cadena lateral saturada de composición C8H17 , indicando una cadena lateral igual a la del esqueleto básico de los esteroles. Del análisis precedente se sugiere que el componente 3 tiene una estructura del tipo Δ7-3β-hidroxiandrosteno y cadena lateral saturada de 8 átomos de carbono. Mediante la información obtenida a partir del espectro, la comparación del mismo con algunos existentes en datos bibliográficos y la comparación de los tiempos de retención relativos al colesterol en CG con los reportados en la literatura (13, 14), se pudo determinar la estructura del compuesto como: colest-7-en-3β-ol (trr-exp = 1.11 versus trr- lit = 1.12).
]]>
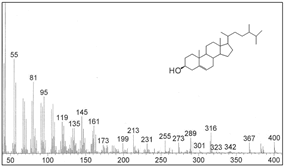
Figura 4. Espectro de masas del componente 6.
En la figura 4 se muestra el espectro de masas del componente 6, donde se aprecia la señal en m/z 400 generada por el ión molecular de fórmula C28H48O. Los fragmentos generales con señales de valores m/z: 385 (M+-CH3 ), 382 (M+-H2O) y 367 (M+-[CH3 +H2O]), indican que este compuesto puede ser un esterol. También pueden observarse los fragmentos con valores de m/z: 273 (pérdida de la cadena lateral), 255 (273-H2O), 231 (fisión del anillo D), 213 (231-H2O), 315 (M+-85) y 289 (M+-111), que sustentan claramente la presencia del núcleo esteroidal Δ5 -3β-hidroxiandrosteno. Este núcleo esteroidal tiene una cadena lateral saturada C9H19 , previamente determinada por la diferencia entre el valor de m/z del ión molecular y el valor de m/z 273. Debido a las señales en m/z: 357 (M+-43), 329 (M+-71), 315 (M+-85) y 301 (M+-99), se puede deducir que la estructura de la cadena lateral es similar a la del colesterol, diferenciándose únicamente por la presencia de un grupo metilo en la posición 24. Este análisis y la comparación del espectro de masas del compuesto en cuestión y su trr (respecto al colesterol) con los de sustancias patrón (13), sugiere la estructura del 24ξ-24-metilcolest-5-en-3β-ol (trr-exp = 1.22 versus trr-lit = 1.22). La identificación de los demás componentes se realizó de manera similar y en la tabla 1 se registraron todos los resultados.
De acuerdo con los resultados que aparecen en la tabla 1 se puede decir que entre los 9 esteroles identificados, los estanoles 1 y 7 son los componentes mayoritarios, que constituyen el 68.8% del total de la fracción; además, se encuentra el estanol 12, con una abundancia relativa del 2.9%. Con excepción del compuesto 5, los demás compuestos presentan cadenas laterales saturadas pertenecientes a tres tipos estructurales caracterizados por poseer 8, 9 y 10 átomos de carbono, siendo los dos primeros derivados alquilados en la posición 24 con grupos etilo y metilo, respectivamente; en cuanto a los núcleos esteroidales, se observa un orden creciente de abundancia entre los tres tipos de núcleos encontrados, dirigido en la forma: Δ7 →Δ5 →Δ0 (6%, 10.1% y 71.7%). Esto se puede explicar por la habilidad que tienen las esponjas para transformar los esteroles, reduciendo (en ese mismo orden) los dobles enlaces de los núcleos, con el fin de satisfacer los requerimientos de sus membranas celulares (15,16). Los nombres de los 9 esteroles identificados son: colestan-3β-ol [1], colest-7-en-3β-ol [3], 24-metilencolesta-7,24(28)-dien-3β-ol [5], 24ξ-24-metilcolest-5-en-3β-ol [6], 24ξ-24-metilcolestan-3β-ol [7], 24ξ-24-metilcolest- 7-en-3β-ol [10], 24ξ-24-etilcolest-5-en-3β-ol [11], 24ξ-24-etilcolestan-3β-ol [12] y 24ξ-24-etilcolest-7-en-3β-ol [14]. Los 5 componentes restantes de la fracción esterólica no pudieron identificarse con la técnica espectroscópica utilizada y corresponden al 12.2% (abundancia relativa) de la fracción.
Tabla 1. Esteroles identificados en la esponja Mycale laevis y sus abundancias relativas.
AGRADECIMIENTOS
]]> Los autores agradecen la financiación de este trabajo a la Universidad de Córdoba (Montería); al profesor Sven Zea (Instituto de Investigaciones Marinas, INVEMAR), por la ubicación taxonómica de la esponja estudiada, y al Grupo de Investigación “Estudio y Aprovechamiento de los Productos Naturales de Colombia” (Universidad Nacional de Colombia Sede Bogotá), por los análisis CG-EM.
REFERENCIAS BIBLIOGRÁFICAS
1. Blunt JW, Copp BR, Hu W-P, Munro M, Northcote PT, Prinsep MR. Marine natural products. Nat Prod Rep. 2008; 25 (1): 35-94. [ Links ]
2. Sarma NS, Sri Rama Krishna M, Ramakrishna Rao S. Sterol ring system oxidation pattern in marine sponges. Mar Drugs. 2005; 3 (1): 84-111. [ Links ]
3. Blunt J, Copp B, Munro M, Northcote P, Prinsep M. Marine natural products. Nat Prod Rep. 2003; 20 (1): 1-48. [ Links ]
4. Blunt J, Copp B, Munro M, Northcote P, Prinsep M. Marine natural products. Nat Prod Rep. 2004; 21 (1): 1-49. [ Links ]
5. Blunt J, Copp B, Munro M, Northcote P, Prinsep M. Marine natural products. Nat Prod Rep. 2005; 22 (1): 15-61. [ Links ]
6. Blunt J, Copp B, Munro M, Northcote P, Prinsep M. Marine natural products. Nat Prod Rep. 2006; 23 (1): 26-78. [ Links ]
7. Blunt J, Copp B, Hu W-P, Munro M, Northcote P, Prinsep M. Marine natural products. Nat Prod Rep. 2007; 24 (1): 31-86
]]>8. Duque C, Puyana M, Osorno O, Zea S. Visión retrospectiva de las investigaciones en productos naturales marinos en Colombia durante los últimos quince años. En: Red de estudios del mundo marino, REMAR. Elmundomarino de Colombia: Investigación y desarrollo de territorios olvidados. Bogotá: Unibiblos; 2003. p. 313-329. [ Links ]
9. Faulkner DJ. Marine natural products. Nat Prod Rep. 2001; 18 (1): 1-49. [ Links ]
10. Carballeira NM, Negron V, Reyes ED. Novel monounsaturated fatty acids from the sponges Amphimedon compressa and Mycale laevis. J Nat Prod. 1992; 55 (3): 333-339. [ Links ]
11. Tanaka J, Higa T, Suwanborirux K, Kokpol U, Bernardinelli G, Jefford C. Bioactive morsesterterpene 1,2-dioxanes from Thai sponge, Mycale sp. J Org Chem. 1993; 58 (11): 2999-3002. [ Links ]
12. Santafé G, Paz V, Rodríguez J, Jiménez C. Novel cytotoxic oxygenated C29 sterols from the Colombian marine sponge Polymastia tenax. J Nat Prod 2002; 65 (8): 1161-1164. [ Links ]
13. Castellanos L. Composición esterólica de esponjas del orden Halichondrida del Caribe colombiano y su significancia como carácter químico de clasificación. [Tesis de Maestría]. Bogotá: Universidad Nacional de Colombia; 1999. [ Links ]
14. Stonik V, Ponomarenko L, Makarieva T, Boguslavsky V, Dmitrenok A, Fedorov S, et al. Free sterol compositions from the sea cucumbers Pseudostichopus trachus, Holothuria (Microtele) nobilis, Holothuria scabra, Trochostoma orientale and Bathyplotes natans. Comp Biochem Physiol B Comp Biochem. 1998; 120 (2): 337-347. [ Links ]
15. De Rosa S, Iodice C, Nechev J, Stefanov K, Popov S. Composition of the lipophilic extract from the sponge Suberites domuncula. J Serb Chem So. 2003; 68 (4-5): 249-256. [ Links ]
16. Silva CJ, Djerassi C. Biosynthetic studies of marine lipids. The origin of common sterol side chains in eleven sponges using [3-3H]-squalene. Comp Biochem Physiol 1992; 101 (1-2): 255 [ Links ]
]]>
Recibido: Junio 4 de 2008.
Aceptado: Octubre 28 de 2008
* Autor a quien se debe dirigir la correspondencia: havalle@unalmed.edu.co
]]>