Se asignó a los pacientes el esquema genérico de tratamiento en estudio: Lamivudina/Zidovudina x 150/300 mg 1 comprimido cada 12 horas + Efavirenz x 600 mg 1 comprimido cada 24 horas (12, 14). Los pacientes fueron seguidos durante 12 meses, determinando al inicio, a los 3, 6 y 12 meses los valores de linfocitos CD4+ como un marcador de la inmunosupresión debida al VIH y, en los mismos períodos, la carga viral, como variables objetivas para evaluar la efectividad. Por su parte, para valorar la seguridad se realizó pruebas hepáticas (alanina aminotransferasa –ALT– y aspartato aminotransferasa –AST–), renales [creatinina sérica y estimación de la depuración de creatinina por la fórmula de Cockcroft–Gault (13)] y hematológicas (glóbulos rojos y recuento diferencial de glóbulos blancos, plaquetas, hemoglobina, hematocrito y citometrías).
Seguimiento y recolección de datos
El seguimiento clínico fue realizado por los médicos de planta de la institución. Esta actividad se realizó antes de la toma de las muestras para las pruebas de laboratorio y después de conocer los resultados de las mismas. Adicionalmente, el paciente podía consultar en el momento que lo considerará necesario. Todos los hallazgos fueron consignados en la historia clínica institucional. Por su parte, para el SFT se utilizó el método DÁDER (15), y fue realizado por un químico farmacéutico entrenado para ello durante 3 meses.
El SFT inició con el consentimiento del paciente, luego se realizó la primera entrevista en la cual se obtuvo la mayor información útil desde la perspectiva farmacéutica, basada en su historia clínica. En esta primera entrevista se efectuó la primera dispensación, se adecuó el horario de toma de los medicamentos, se informó al paciente sobre los posibles efectos adversos que se pueden presentar y se elaboró el primer estado de situación (documento en que se registra la relación entre problemas de salud y medicamentos utilizados para su tratamiento, incluyendo el TARc). Se realizó seguimiento telefónico al iniciar la TARc (a la semanas 1 y 2, y al completar el primer mes de tratamiento). Además, se evaluó la adherencia utilizando un método indirecto y validado en pacientes con VIH (Simplified Medication Adherence Questionnaire–SMAQ-) (16). Posteriormente, se realizó cada mes la dispensación de las dosis de tratamiento para el mismo periodo, la cual se acompañó de la elaboración del respectivo estado de situación, así como la realización de intervenciones cuando fuera necesario, orientadas a la prevención, mantenimiento o modificación de los estilos de vida que pudieran influir desfavorablemente en el control de la enfermedad (alcoholismo, drogadicción, entre otras), y en especial, la adherencia terapéutica.
Variables de estudio
Efectividad
Determinada por el aumento significativo en los recuentos de CD4+ y por la disminución significativa de carga viral en plasma, medidos en la línea base previa al inicio del tratamiento, a los 3, 6 y 12 meses después de iniciar el TARc.
Seguridad
Valorada por los resultados de controles médicos, farmacéuticos y psicológicos. Adicionalmente, se realizó valoración y seguimiento de pruebas hematológicas (glóbulos rojos y recuento diferencial de glóbulos blancos, plaquetas, hemoglobina, hematocrito y citometrías), hepáticas (aspartato y alanino aminotransferasa) y renales [creatinina sérica y estimación de la depuración de creatinina por la fórmula de Cockcroft–Gault (13)], así como la ausencia de otros problemas de seguridad. Estas prueba fueron tomadas en los mismos tiempos en que se tomaron las pruebas virológicas e inmunológicas (inicio, 3, 6 y 12 meses), exceptuando la hemoglobina y hematocrito, valoraciones que fueron repetidas a las 4 y 8 semanas, y a los 3, 6 y 12 meses de iniciado el tratamiento.
]]> AdherenciaEstablecida mediante el cuestionario SMAQ a partir de preguntas como: ¿el paciente ha olvidado tomar los medicamentos?, ¿el paciente toma los medicamentos a la hora indicada?, ¿el paciente deja de tomar los medicamentos cuando se siente mal?, o ¿el paciente olvidó tomar los medicamentos durante el fin de semana?, acompañado de una pregunta semicuantitativa (orientada a establecer el número de dosis no tomadas durante la última semana). La clasificación del paciente como adherente está dada por el criterio: cumple con un 95% o más de las dosis indicadas; y no adherente: cumplimiento menor al 95%.
Para minimizar posibles sesgos de análisis se utilizó las siguientes estrategias: en las determinaciones del recuento de linfocitos CD4+, de los niveles de carga viral y demás variables de interés, las muestras sanguíneas fueron tomadas en las mismas condiciones, usando los mismos equipos para los análisis y utilizando técnicas analíticas validadas para ello en el laboratorio habitual de referencia de la institución prestadora de la atención integral. Los medicamentos necesarios para los tratamientos durante el periodo del estudio fueron aportados por Humax Pharmaceutical S.A. (Medellín, Colombia), los cuales provenían del mismo lote de producción, con certificado de análisis de calidad respectivo y con pruebas de disolución que garantizaban su similitud con los medicamentos innovadores.
Grupo control para la comparación de la efectividad
Con el fin de identificar un grupo control adecuado se realizó una revisión de la literatura biomédica para identificar publicaciones con resultados alcanzados en pacientes con condiciones similares y con el mismo esquema (dosis, frecuencia y tiempo de seguimiento) pero en tratamiento con medicamentos innovadores. En este sentido, se planteó una hipótesis de no inferioridad, para la cual fueron comparados los resultados obtenidos con los reportados en una publicación de referencia que incluyó pacientes con condiciones similares a los del presente estudio y con el mismo esquema de tratamiento Lamivudina/Zidovudina + Efavirenz, pero con medicamentos innovadores. Para la selección del estudio referencia (comparador) se utilizó los siguientes criterios: a) información de las características poblacionales al inicio; b) tiempo de seguimiento de un año; c) reporte de los datos completos de pacientes que lograron metas de tratamiento (carga viral indetectable y aumento promedio de CD4 +); d) posibilidad de inferir o asegurar que el esquema con el que se trató a los pacientes usó medicamentos innovadores; e) publicación en una revista científica con un alto factor de impacto y, por tanto, que garantizara la aplicación de las buenas prácticas clínicas en la realización del estudio.
Análisis estadístico
Para determinar la distribución de cada variable se realizó estadísticos descriptivos y un test de distribución normal. Posteriormente, las características iniciales de la cohorte seguidas de las mediciones clínicas posteriores fueron comparadas mediante test de rango con signo de Wilcoxon para proporciones o porcentajes, y pruebas t-Student o ANOVA de mediciones repetidas para variables continuas. Los análisis fueron realizados utilizando el programa SPSS versión 17.0 (SPSS Inc, Chicago, Ili). La contrastación de la hipótesis de no inferioridad con los datos reportados en la literatura fue realizada a través de métodos de inferencia sobre parámetros, realizando pruebas de significancia por comparación de medias o de proporciones para dos poblaciones independientes. La comparación se apoyó en la herramienta EPIDAT 3,1 (OPS/OMS). Valores de p menores a 0,05 fueron considerados estadísticamente significativos.
Consideraciones éticas
Este proyecto de investigación se ajustó a las normas de ética médica vigentes (17). En Colombia se acogió a lo dispuesto en la Resolución 8430 de 1993 y la Resolución 2378 de 2008, Declaración de Helsinki y sus enmiendas, y la Guía de las Buenas Prácticas Clínicas (ICH E6); en consecuencia, el estudio fue aprobado por el Comité Técnico de Investigaciones de la Facultad de Química Farmacéutica de la Universidad de Antioquia y por el Comité de Ética para Investigación en Humanos de la institución donde se ejecutó el proyecto.
]]> RESULTADOS
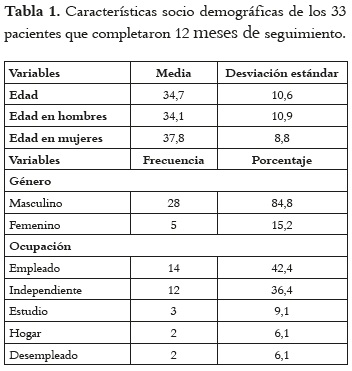
Se invitó a 59 pacientes a participar, de los cuales 47 cumplieron criterios de inclusión, el flujo de los pacientes en el estudio se presenta en la figura 1. En los 47 pacientes que cumplieron criterios de inclusión, la edad media (con desviación estándar [DE]), fue 34,4 años [10,4], y 38 (80,9%) eran hombres. De estos 47 pacientes, 33 (70,2%) cumplieron con el tratamiento durante los doce meses de seguimiento. Por su parte, de las 14 descontinuaciones del tratamiento, 4 (28,6%) fueron atribuibles a problemas de seguridad relacionadas con el esquema de tratamiento: posible anemia grave (valores de hemoglobina de 6,5, 7,1, 7,5 y 7,7 g/dL) por Zidovudina. En la tabla 1 se presenta las características sociodemográficas de los 33 pacientes que finalizaron el estudio.
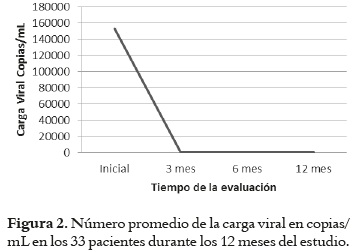
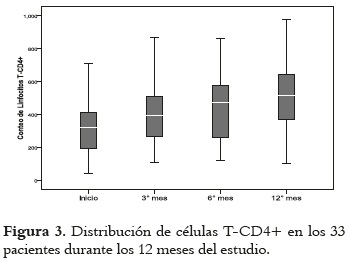
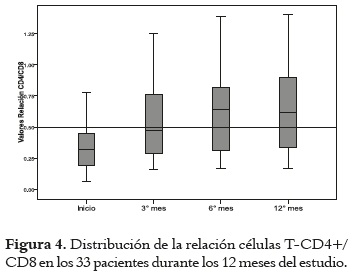
De los 33 pacientes que completaron los doce meses de seguimiento, 23 (69,7%) fueron diagnosticados en estado no avanzado de enfermedad (18). Por su parte, relacionado con los objetivos del estudio, de los 33 pacientes un total de 28 (84,8%) alcanzaron una carga viral indetectable, significativamente diferente al valor inicial del tratamiento (p < 0,001), y 30 (90,9%) presentaron un aumento progresivo y significativo del recuento de células T CD4+ por encima de 200 células/mm3 (p < 0,001). Adicionalmente, se observó un incremento promedio mayor de 0,5 en la relación CD4/CD8 (ver figuras 2, 3, 4).
]]>
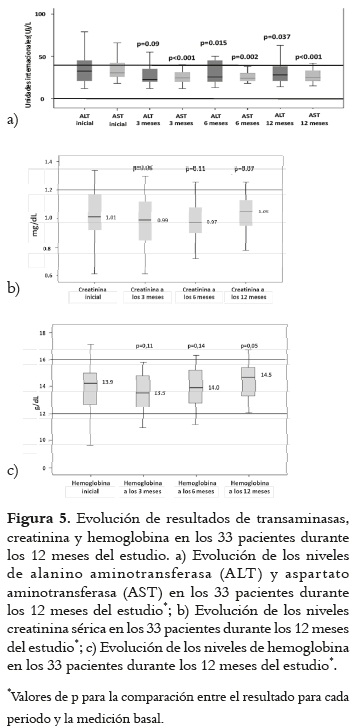
La evolución de resultados de transaminasas, creatinina y hemoglobina en los 33 pacientes durante los 12 meses del estudio se presenta en la figura 5. En el caso de las transaminasas (AST y ALT) se presentó disminuciones estadísticamente significativas en cada período de observación (3, 6 y 12 meses) (ver figura 5-A).
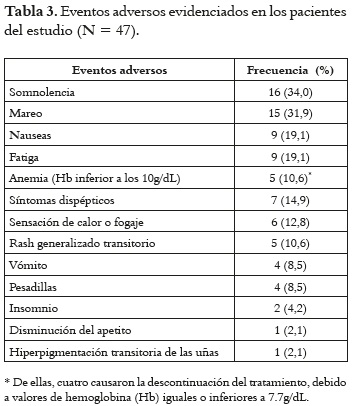
Las reacciones adversas a medicamentos (RAM) presentadas por la totalidad de los 47 pacientes incluidos en el estudio, fueron transitorias y detectadas en el SFT (ver tabla 3). Además, se presentó 45 problemas de proceso con los medicamentos, especialmente la adherencia menor al 95%, los cuales, exceptuando dos casos en los que fue necesario excluir los pacientes, fueron identificados, intervenidos y resueltos mediante el SFT.
Comparación con estudios de referencia
La selección de un estudio para la comparación dio como resultado el trabajo publicado por Staszewski et al., 1999 (19). A continuación se presenta los resultados de las comparaciones en las variables de efectividad:
Valores iniciales
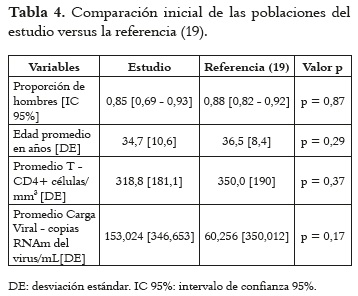
]]> No se encontró diferencias estadísticamente significativas entre la población en estudio con el esquema genérico Lamivudina/Zidovudina + Efavirenz con respecto a la población de estudio de referencia con medicamentos innovadores, en lo que tiene que ver con género, edad, recuento de células T CD4+ y carga viral (ver tabla 4).
Valores finales
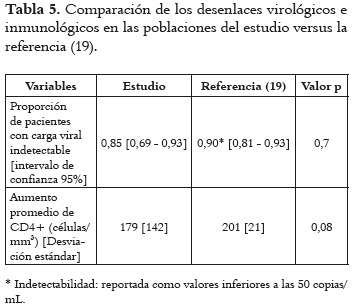
Después de aproximadamente un año de tratamiento (12 meses en el presente estudio y 48 semanas en el estudio control), la diferencia de medias (en los valores de células CD4+) y la diferencia de proporciones (de pacientes con carga viral indetectable) no fueron estadísticamente significativas, y por tanto se prueba la hipótesis de no inferioridad del esquema genérico. En las dos poblaciones, de estudio y de referencia, los resultados del seguimiento muestran diferencia estadísticamente significativa en el incremento de las células CD4+ y en la disminución de la carga viral a niveles de indetectabilidad cuando se comparan los valores basales con los resultados finales en cada uno de los estudios. Las comparaciones se muestran en la tabla 5.
DISCUSIÓN
En este estudio el tratamiento con el esquema genérico Lamivudina/Zidovudina + Efavirenz en pacientes con VIH/SIDA sin resistencias primarias o transmitidas, de un programa de atención integral ambulatoria especializada, no resultó inferior a los datos de eficacia reportados con el esquema innovador (Combivir® + Stocrim®, respectivamente) en condiciones similares (19). En este sentido, la comparación de la efectividad, determinada por los niveles alcanzados en la carga viral y en los recuentos de linfocitos CD4+, no presentó diferencias estadísticas significativas, comprobándose entonces la hipótesis de no inferioridad del esquema genérico respecto al estudio referencia. Adicionalmente, la comparación cualitativa del perfil de seguridad del esquema genérico (establecido por valoraciones realizadas mediante controles médicos, farmacéuticos, psicológicos, hematológicos, hepáticos y renales durante los 12 meses de seguimiento) con el reportado para el esquema innovador en diferentes estudios no muestra diferencias significativas, en especial con la anemia macrocítica asociada a Zidovudina (20-25).
Para la comparación se realizó una búsqueda bibliográfica en la cual se identificó un estudio que cumplió con los criterios de inclusión (pacientes con condiciones similares y con resultados de la combinación con medicamentos innovadores Lamivudina/Zidovudina + Efavirenz), el cual, a pesar de haber sido publicado en 1999, es uno de los estudios que respaldó la recomendación de este esquema como tratamiento de primera línea (19). Además, se identificó otros trabajos, los cuales, aunque no cumplen con todos los criterios de inclusión, utilizan el esquema Lamivudina/Zidovudina + Efavirenz con medicamentos innovadores, y reportan resultados de indetectabilidad en la carga viral cercanos al 85% alcanzado en el presente estudio. Por ejemplo, el estudio de Robbins et al., 2003 (26) reportó una proporción de pacientes con carga viral indetectable del 75%. Similarmente, en el estudio de Gallant et al., 2006 (27), diseñado con el objetivo de comparar un esquema basado en Tenofovir, Emtricitabina y Efavirenz versus el esquema Lamivudina/Zidovudina + Efavirenz, reportó en el brazo de control (Lamivudina/Zidovudina + Efavirenz) una proporción del 73% de los pacientes que lograron indetectabilidad de la carga viral. Por su parte, un estudio abierto con 19 pacientes con el esquema innovador Combivir® + Stocrim® realizado en Londres por Portsmouth S et al., 2004 (20), encontró que el tiempo medio para alcanzar una carga viral indetectable fue de 12 semanas (rango 4-36 semanas); tiempo que es similar al que se obtuvo en el presente estudio (12 semanas) (ver figura 2).
]]> En lo relacionado con la seguridad del TARc en este estudio los 5 casos de anemia asociada al tratamiento que se presentó en los 47 pacientes cursaron con macrocitosis, y su incidencia fue del 10,6%, valor que se encuentra en el límite inferior del rango (10-25%) establecido para este problema de seguridad a partir de varios estudios (20-25), y por consiguiente ligeramente inferior a varios de los reportes de cada estudio; por ejemplo, inferior al 19,4% del estudio de Rajesh et al., 2011 (21), quienes identificaron 19 casos de anemia macrocítica en 98 pacientes en tratamiento con TARc y esquema de Zidovudina. Además, estos autores reportan, gracias a un análisis de regresión logística, que los valores de hemoglobina inferiores a los 10,5 g/dL, al inicio del tratamiento, son un fuerte predictor para la aparición grave de este problema de seguridad. Por su parte, un estudio realizado en el estado de Paraná (Brasil) con 110 pacientes, con respecto a la posibilidad de desarrollar macrocitosis, encontró diferencias estadísticamente significativas en los grupos de pacientes utilizando esquemas de TARc con Zidovudina respecto a los pacientes con esquemas sin este fármaco (22). La anemia macrocítica grave o seria (Hb inferior a 6,5 g/dL) se presentó en uno (2,2%) de los pacientes incluidos; este valor es ligeramente inferior al 6,6% reportado, a las 48 semanas de tratamiento en pacientes VIH (+) que inician tratamiento con Zidovudina (23).Los otros efectos adversos encontrados en el estudio son similares a los reportados en la literatura biomédica para los medicamentos de este esquema de TARc, y proporcionalmente similares a los del estudio de Portsmouth S et al., 2004 (20). En este estudio, aunque las aminotransferasas (AST y ALT) presentaron valores ligeramente elevados al inicio del tratamiento, posteriormente, se presentó una disminución estadísticamente significativa en cada período de observación (3, 6 y 12 meses), lo cual puede ser reflejo de la disminución progresiva de la carga viral y del efecto pro-inflamatorio del virus (28).
La realización del SFT por parte de un Químico Farmacéutico puede ayudar a prevenir abandonos por los efectos adversos que pueden presentar los pacientes al inicio de la TARc; por tanto, el SFT podría haber afectado esta variable. En este sentido, aunque el diseño del estudio no permite generar conclusiones sobre el efecto del SFT, sí se puede inferir que dicho proceso fue una herramienta importante para evaluar la efectividad y seguridad de los medicamentos de la TARc y para gestionar el estudio.
En general, la información que arroja el presente estudio permite evaluar los resultados clínicos de los ARV competidores, lo cual es importante dada la modificación del proceso en la Food and Drug Administration para agilizar la revisión de ARV genéricos disponibles para el plan de emergencia para el manejo del SIDA (29). Similarmente, en los países en desarrollo (2), incluyendo Colombia, el impacto de la política de medicamentos genéricos de primera y segunda línea se ha visto reflejado en la disminución del costo del tratamiento y en un mayor acceso a estos productos (11). En definitiva, este estudio aunque no es novedoso, por su concepción y diseño (ensayo clínico abierto no controlado), coincide con información publicada y aporta elementos importantes para la valoración terapéutica de los ARV genéricos producidos en Colombia, los cuales son una opción siempre y cuando se trabaje simultáneamente sobre la adherencia de los pacientes y la optimización del tratamiento. En este sentido, es importante destacar que el esquema Lamivudina/ Zidovudina + Efavirenz es uno de los esquemas más utilizados en Colombia, incluyendo la institución en la que se realizó el estudio. Adicionalmente, un estudio de uso de medicamentos en condiciones normales de la práctica médica realizado por Gutiérrez F et al., 2007 (11), en una entidad promotora de salud (Medellín, Colombia), en el cual se incluyeron en el análisis a 670 pacientes en TARc, reportó que un 57% de los pacientes estaba en tratamiento con el esquema Lamivudina/Zidovudina + Efavirenz, siendo el primero y único esquema recibido, con niveles de indetectabilidad de la carga viral (carga viral <400 copias/mL) cercanos al 83%.
Las limitaciones del presente estudio son atribuibles a su diseño, debido a que no se realizó un estudio controlado, y la comparación de los resultados obtenidos se realizó con resultados tomados de la literatura científica, que corresponden a pacientes de poblaciones diferentes a los evaluados, por lo tanto se limita la posibilidad de generalizar los hallazgos.
CONCLUSIONES
Al año de tratamiento de pacientes VIH que no han recibido terapia antirretroviral, los resultados de efectividad alcanzados con el esquema genérico Lamivudina/Zidovudina+Efavirez no son inferiores a los alcanzados en un grupo de pacientes con condiciones clínicas similares tratados bajo el mismo esquema con medicamentos innovadores.
AGRADECIMIENTOS
]]> Los autores expresan sus agradecimientos a Humax Pharmaceutical S.A. (Medellín, Colombia) por su apoyo para la realización de este trabajo. El grupo de investigación Promoción y Prevención farmacéutica recibe fondos de la Convocatoria de Estrategia de Sostenibilidad 2013-2014 de la Universidad de Antioquia.Conflicto de intereses: Trabajo patrocinado por Humax Pharmaceutical S.A. (Medellín, Colombia). Francisco J. Gutiérrez H. y Jaime A. Hincapié, son empleados de Humax Pharmaceutical S.A.
REFERENCIAS BIBLIOGRÁFICAS
1. ONUSIDA. Situación de la epidemia de SIDA [en línea]. Ginebra (Suiza); 2007 Dec; [accesado Agosto 2012]. Disponible en: http://data.unaids.org/pub/EPISlides/2007/2007_epiupdate_es.pdf. [ Links ]
2. Waning B, Diedrichsen E, Moon S. A lifeline to treatment: the role of Indian generic manufacturers in supplying antiretroviral medicines to developing countries. J Int AIDS Soc. 2010 Sep 14; 13: 35. [ Links ]
3. Kumet R, Gelenberg AJ. The effectiveness of generic agents in psychopharmacologic treatment. Essent Psychopharmacol. 2005; 6 (2): 104-111. [ Links ]
]]>4. Rheinstein PH. Therapeutic inequivalence. Drug Saf. 1990; 5 (S1): 114-119. [ Links ]
5. Over M, Revenga A, Masaki E, Peerapatanapokin W, Gold J, Tangcharoensathien V, et al. The economics of effective AIDS treatment in Thailand. AIDS. 2007 Jul; 21 (S4): S105-S116. [ Links ]
6. Oluboka O, Stewart S, Landry S, Adams S. Does therapeutic equivalence follow bioequivalence? A randomized trial to assess clinical effects after switching from Clozaril to generic clozapine (gen-clozapine). J Clin Pharmacol. 2010 May; 50 (5): 531-535. [ Links ]
7. Amariles P, Muñoz A, Restrepo M, Villegas A. Eficacia Clínica de la Glicazida Genérica con respecto al medicamento referencia en el tratamiento de la diabetes tipo 2 en afiliados al ISS. Medellin- Colombia 1999. Pharmaceutical Care (Esp). 2001; 3 (5): 370-390. [ Links ]
8. Grissinger M. Eficacia Clínica de la Glicazida Genérica con respecto al medicamento referencia en el tratamiento de la diabetes tipo 2 en afiliados al ISS. Medellin-Colombia 1999. 2006; 31(11): 635-636. [ Links ]
]]>9. Amariles P, Faus MJ, Sabater D, Machuca M, Martinez-Martinez F. Seguimiento Farmacoterapéutico y parámetros de efectividad y seguridad de la farmacoterapia. El farmacéutico. 2006; 362: 84-100. [ Links ]
10. Amariles P. Seguimiento Farmacoterapéutico en pacientes VIH/ SIDA. Aula de Farmacia. 2011; 7 (87): 8-24. [ Links ]
11. Gutiérrez F, Velásquez C, Amariles P, Giraldo N, Ocampo S, Estrada J. Impacto del Seguimiento Farmacoterapéutico en un Programa de VIH/SIDA de la Ciudad de Medellín, 2005-2007. Infectio. 2008; 12 (S1): 124. [ Links ]
12. WHO. Scaling up antiretroviral therapy in resource-limited settings. Guidelines for a public health approach. Geneva: WHO; 2002. [ Links ]
13. Cockcroft DW, Gault MH. Prediction of creatinine clearance from serum creatinine. Nephron. 1976; 16 (1): 31-41. [ Links ]
]]>14. AIDSINFO-NIH. Guidelines for the Use of Antiretroviral Agents in HIV-1-Infected Adults and Adolescents [internet]. NIH; 2011. [citado agosto 2012]. Disponible en: http://aidsinfo.nih.gov/contentfiles/AdultandAdolescentGL.pdf. [ Links ]
15. Sabater Hernández D, Silva Castro MM, Faus MJ. Método Dáder: Guía de Seguimiento Farmacoterapéutico. Tercera Edición. Granada (España): Grupo de Investigación en Atención Farmacéutica; 2007. [ Links ]
16. Knobel H, Escobar I, Polo R, Ortega L, Martín-Conde MT, Casado JL, et al. Recomendaciones GESIDA/SEFH/PNS para mejorar la adherencia al tratamiento antirretroviral (2004). Enferm Infecc Microbiol Clin. 2005 Apr; 23 (4): 221-231. [ Links ]
17. Sarria-Castro M. Bioética, investigación y salud pública, desde una perspectiva social. Rev Cubana Salud Pública. 2007 Ene- Mar; 33 (1). [ Links ]
18. CDC. 1993 Revised Classification System for HIV Infection and Expanded Surveillance Case Definition for AIDS Among Adolescents and Adults. MMWR Recomm Rep. 1992; 41 (RR- 17): 1-19. [ Links ]
]]>19. Staszewski S, Morales-Ramirez J, Tashima KT, Rachlis A, Skiest D, Stanford J, et al. Efavirenz plus zidovudine and lamivudine, efavirenz plus indinavir, and indinavir plus zidovudine and lamivudine in the treatment of HIV-1 infection in adults. Study 006 Team. N Engl J Med. 1999 Dec 16; 341 (25): 1865-1873. [ Links ]
20. Portsmouth S, Imami N, Pires A, Stebbing J, Hand J, Nelson M, t al. Treatment of primary HIV-1 infection with nonnucleoside reverse transcriptase inhibitor-based therapy is effective and well tolerated. HIV Medicine. 2004 Jan; 5 (1): 26-29. [ Links ]
21. Rajesh R, Vidyasagar S, Varma DM, Mohiuddin S, Noorunnisa. Evaluation of incidence of zidovudine induced anemia in Indian human immunodeficiency virus positive patients in comparison with stavudine based highly active antiretroviral therapy. Int J Risk Saf Med. 2011; 23 (3): 171-180. [ Links ]
22. Antunes de Oliveira O, Antunes de Souza R, Do Rosário L. Impacto do tratamento antirretroviral naocorrência de macrocitoseem pacientes com HIV/AIDS do município de Maringá, Estado do Paraná. Rev Soc Bras Med Trop. 2011 Jan- Feb; 44 (1): 35-39. [ Links ]
23. Ssali F, Stöhr W, Munderi P, Reid A, Walker AS, Gibb DM, et al. Prevalence, incidence and predictors of severe anaemia with zidovudine-containing regimens in African adults with HIV infection within the DART trial. Antivir Ther. 2006; 11 (6): 741-749. [ Links ]
]]>24. Zhou J, Jaquet A, Bissagnene E, Musick B, Wools-Kaloustian K, Maxwell N, et al. Short-term risk of anaemia following initiation of combination antiretroviral treatment in HIV-infected patients in countries in sub-Saharan Africa, Asia-Pacific, and central and South America. J Int AIDS Soc. 2012 Jan 30; 15 (1): 5. [ Links ]
25. Severe P, Juste MA, Ambroise A, Eliacin L, Marchand C, Apollon S, et al. Early versus Standard Antiretroviral Therapy for HIVInfected Adults in Haiti. N Engl J Med. 2010; 363 (3): 257-265. [ Links ]
26. Robbins GK, De Gruttola V, Shafer RW, Smeaton LM, Snyder SW, PettinelliC, et al. Comparison of sequential three-drug regimens as initial therapy for HIV-1 infection. N Engl J Med. 2003 Dec 11; 349 (24): 2293-2303. [ Links ]
27. Gallant JE, De Jesus E, Arribas JR, Pozniak AL, Gazzard B, Campo RE, et al. Tenofovir DF, emtricitabine, and efavirenz vs. zidovudine, lamivudine, and efavirenz for HIV. N Engl J Med. 2006 Jan 19; 354 (3): 251-260. [ Links ]
28. Mata-Marín JA, Gaytán-Martínez J, Grados-Chavarría BH, Fuentes-Allen JL, Arroyo-Anduiza CI, Alfaro-Mejía A. Correlation between HIV viral load and aminotransferases as liver damage markers in HIV infected naive patients: a concordance cross-sectional study. Virol J. 2009 Oct 30; 6 (10): 181. [ Links ]
]]>29. Holmes Ch, Coggin W, Jamieson D, et al. Use of generic antiretroviral agents and cost savings in PEPFAR treatment programs. JAMA. 2010 Jul 21; 304 (3): 313-320. [ Links ]
]]>