Estudio de la hidrólisis del crudo de aceite de palma africana empleando como catalizador la lipasa de la levadura C.rugosa
Study of the hydrolysis of crude palm oil using lipase from Candida rugosa as the catalyst
Miguel Molano
Asesor: Ingeniero Químico e Ingeniero Mecánico, Profesor instructor del Departamento de Ingeniería Química de Universidad de los Andes
Diana Riveros
Autor: Estudiante de Ingeniería Química de la Universidad de los Andes
Edgar Vargas
Ingeneiro Químico, Msc. Ing. Química, Profesor instructor del Departamento de Ingeniería Química de Universidad de los Andes
Recibido 9 de septiembre de 2005, aprobado 30 de octubre de 2005.
RESUMEN
En este artículo se presenta el estudio de la hidrólisis del crudo de aceite de palma por medio de la lipasa Candida rugosa. Los factores estudiados en esta investigación fueron el nivel de agitación, el efecto de blanqueo y la cantidad de lipasa. Experimentalmente fueron alcanzados porcentajes de hidrólisis del 79-93% en períodos de tiempo de 2 horas y media. Se pudo obtener un incremento de la reacción al aumentar la rotación del agitador al igual que incrementando la concentración de lipasa. Aunque la literatura cita el blanqueado como una ventaja para la hidrólisis enzimática, este procedimiento parece no tener un efecto benéfico en la reacción.
KEY WORDS
Fatty acids, Lipase, Palm oil, hydrolysis.
ABSTRACT
This paper shows the study of the hydrolysis reaction of crude palm oil giving by lipase from Candida rugosa. The studied factors were agitation level, bleaching effect and lipase concentration. Experimentally 79 - 93% hydrolysis were achieved in 2 and a half hour. The reaction rate was increased with the increment of the impeller rotational speed as well as increasing the lipase concentration. Although the literature cites bleaching as a beneficial advantages to enzymatic hydrolysis, this procedure do not have a significant beneficial effect on the reaction.
1. INTRODUCCIÓN
Los ácidos grasos son una importante materia prima para la industria química. En Colombia, se registra una producción de alguna importancia solamente para el ácido esteárico; por lo cual, para satisfacer la demanda de otros ácidos grasos, el país depende de las importaciones ((Vélez et al. 2002)
]]> Existen diversas tecnologías para la producción de ácidos grasos. Algunos de estas tecnologías son Twitchell y Colgate-Emery, las cuales utilizan presiones y temperaturas altas (alrededor de 700 psi y 480 °F) por períodos de 2 horas para alcanzar un 96-99% de hidrólisis. En este último método, se alimenta el material graso y agua continuamente a un fraccionador (20 m altura), en contracorriente, llegando a ser un proceso de gran eficiencia (Álvarez, 1995).La gran mayoría de industrias productoras de ácidos grasos, en países industrializados, han utilizado tecnologías que requieren un alto consumo de energía, debido a que eran la única forma de producirlos en ese tiempo. La viabilidad de conseguir comercialmente lipasas en este momento, ha hecho la hidrólisis enzimática más atractiva para los nuevos productores.
La patente de Yamada K. (1965) divulga la purificación de una lipasa de gran actividad, obtenida de una especie de levadura llamada Candida cylindracea, ahora llamada Candida rugosa. Benzonana y Esposito (1971) demostraron luego que esta lipasa catalizaba completamente la hidrólisis de diversos aceites, obteniendo ácidos grasos libres y glicerol. Muchas otras lipasas se han utilizado en la industria para este fin, como son las obtenidas a partir de Rhizotus arrhizus, Rhizomucor miehei y Aspergilus niger, las cuales se comercializan fácilmente (Arango, 2004). Como se muestra en el estudio de Samuel Serota (1984), algunas de las anteriores lipasas, como la proveniente de R. arrhizus, son específicas para algunos enlaces en los triglicéridos (no hidroliza posición-2). En cambio, las lipasas provenientes de C. rugosa y A. niger, no son específicas y atacan a cualquier posición.
En el presente artículo, se mostrarán las condiciones óptimas para la producción de ácidos grasos, por medio de una hidrólisis enzimática, catalizada por la enzima producida por la C. rugosa. Los factores analizados fueron: el nivel de agitación, la concentración de lipasa y el nivel de blanqueo. Este último se hace importante ya que la literatura muestra que aparentemente se presentan impurezas en el aceite, las cuales producen una inhibición de la enzima en su proceso catalítico.
Hay que tener en cuenta que una de las fases más importantes en los procesos industriales, es reproducir a mayor escala los resultados encontrados en el laboratorio, siendo esta una etapa crítica para cualquier proceso químico. Debido a su importancia, en el presente estudio se muestra el escalamiento a las condiciones del mejor resultado obtenido de la experimentación a nivel laboratorio, con el objetivo de verificar si el escalamiento realizado puede obtener los mismos porcentajes de hidrólisis que la escala menor.
Hay que tener en cuenta que, para las reacciones de hidrólisis, la agitación es uno de los factores de mayor importancia, ya que de ello depende la buena afinidad entre la fase grasa y acuosa. Como es bien sabido estas dos fases tienen poca solubilidad, por lo que es necesario formar emulsiones para aumentar la interfase de contacto en las primeras etapas de la reacción. Por tal motivo, el escalamiento se enfoca principalmente en la agitación y todos los parámetros que a ella se relacionan, como son el escalamiento del nivel de agitación, influencia del tipo de agitador dentro del mezclado y el análisis de los parámetros de mezclado que permanecen constantes dentro de este proceso.
2. EXPERIMENTACIÓN
2.1 MATERIALES
Se utilizó lipasa de la Candida rugosa 2,820 unidades/mg sólido, (200 g), que fue adquirida en SIGMA Chemical Co. La lipasa fue almacenada a una temperatura de 8°C. Se utilizó la arcilla blanqueadora Tonsil actisil, brindada por Meza Hermanos LTDA, importadora y distribuidora de este material a nivel industrial en Colombia. El crudo de aceite de palma (7 Litros) fue suministrado por la empresa Oleaginosas San Marcos Ltda.
2.3 DISEÑO EXPERIMENTAL
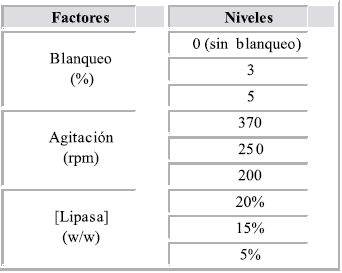
]]> Se utilizó un diseño factorial de 33, en el que se tomaron tres factores con tres niveles independientes. Los factores estudiados con sus respectivos niveles se ilustran en la tabla número 1. Para este diseño se requirieron 27 ensayos, con el objetivo de correlacionar cada uno de los distintos factores con sus diferentes niveles, tomando además para cada combinación una réplica.Tabla 1. Factores analizados en el estudio, con sus distintos niveles.
Otros factores que intervienen en la hidrólisis enzimática ya han sido estudiados por diversos investigadores, y sus reportes se encuentran registrados en la literatura, de donde se tomaron las condiciones óptimas a las cuales trabaja la enzima. Estas condiciones óptimas bajo las que se estudió la hidrólisis fueron: temperatura (37°C) [7], pH (7,2) [8] y relación de reactantes (2:1 agua aceite, 10g aceite y 20 g de agua) [9]. Un nuevo factor fue tomado en cuenta en la reacción, para alcanzar grados de hidrólisis más altos, se utilizó una relación de hexano-aceite óptima, estudiada por H.T. Khor (1986), la cual corresponde a 0,5 ml de hexano por gramo de aceite. El tiempo establecido para que la reacción de hidrólisis se llevara a cabo fue de 2 horas y media, en donde se pudo apreciar porcentajes de hidrólisis elevados.
2.4 METODOLOGÍA DE EXPERIMENTACIÓN
Para poner en marcha la reacción de hidrólisis, se utilizó un beacker de 100 ml, en el que se agregaron 10 g de aceite disueltos en 5 ml de hexano. La cantidad de lipasa correspondiente al ensayo se disolvió en 10 ml de buffer de fosfato de sodio de pH 7.2, más 10ml de agua destilada. Esta fase acuosa se puso en contacto con la fase oleosa, para luego ser agitado con impeller tipo turbina simple de pala recta de 3 cm de diámetro.
Después de dos horas y media, para cada ensayo, se detuvo la agitación y se determinó la cantidad de ácidos libres, para luego establecer el porcentaje de hidrólisis de la muestra, como se ve en la ecuación uno.
Donde, FFA finales son los ácidos libres totales después de la reacción; FFA iniciales son los ácidos libres que tiene la muestra de aceite inicialmente antes de la reacción y I.S es el índice de saponificación del aceite con que se realizó la hidrólisis.
2.4 ESCALAMIENTO
Como se mencionó anteriormente, el escalamiento se realizó como estudio posterior a la experimentación hecha en el laboratorio; este proceso se hizo con relación a la agitación. Debido a las limitaciones de la enzima, fueron posibles tan solo dos escalamientos, realizados con base en los resultados obtenidos a nivel de laboratorio. Para ello, fue necesario determinar cuál de las combinaciones entre niveles de cada uno de los tres factores (tabla 1), fue la que arrojó un mayor porcentaje de hidrólisis, para así tomar sus condiciones y escalarlas.
]]> Para el primer escalamiento (Escala 1), fue pertinente usar el mismo tipo de agitador que se utilizó en la experimentación a nivel de laboratorio, pero con un mayor tamaño; así entonces, se empleó un agitador tipo turbina de pala recta con un diámetro de 5 cm para realizar la reacción de hidrólisis a una escala mayor. Para el segundo escalamiento (Escala 2), se utilizó un agitador diferente con el objeto de comparar su desempeño frente al agitador tipo turbina. El agitador escogido fue el de tipo ancla, el cual es el más utilizado para líquidos con viscosidades altas o sólidos en suspensión. Para cada uno de estos dos experimentos, las condiciones entre reactivos tipo de aceite (condiciones obtenida del análisis de resultados del laboratorio), las condiciones óptimas como pH y temperaturas descritas anteriormente, y así como las dimensiones del recipiente reactante son idénticas; tan solo difieren en el tipo de agitador.Con el fin de determinar el volumen total de reactantes para el escalamiento y de igual forma el recipiente en el que se va realizar la hidrólisis, se tomaron como base algunas medidas del diseño estándar de turbinas (McCabe, 2002), con las que se pudo establecer un volumen total de 785ml. De igual forma, las relaciones de hexano, agua, buffer, lipasa y tipo de aceite siguen constantes para este nuevo volumen (ver tabla 3).
La velocidad de rotación utilizada para la nueva escala se estableció basándose en el concepto de similaridad geométrica, así como lo explica Doble en su publicación (2002).
3. ANÁLISIS Y RESULTADOS
3.1 CARACTERÍSTICAS DE LOS TRES ACEITES
Con el objetivo de proporcionar información necesaria sobre el tipo de aceite con el que se está trabajando y, además, para comprobar la influencia que tiene el proceso de blanqueado sobre el aceite de palma, se han escogido una serie de pruebas proporcionadas por la A.O.C.S (American Oil Chemical Society) (Firestone, 1989). La tabla 2 muestra las pruebas realizadas. El Aceite 5% y 3 % hace referencia a la concentración de arcilla usada para su blanqueado.
Tabla 2. Pruebas de caracterización para los diferentes aceites
En la tabla 2 se establecen los promedios de cada una de las muestras y su desviación estándar. Se puede apreciar que para las pruebas de acidez e índice de saponificación, los valores para los tres tipos de aceites permanecen casi constantes, de esta forma se puede garantizar una homogeneidad en cuanto al cálculo del porcentaje de hidrólisis. Este hecho pudo confirmar la buena efectividad de las arcillas usadas para el blanqueo, dando únicamente un cambio en su coloración, indicando la remoción de algunas impurezas como los β-carotenos y vitaminas que le otorgan la coloración rojiza al aceite crudo de palma.
3.2 RESULTADOS DE EXPERIMENTACIÓN
]]> En las siguientes gráficas se muestra los resultados del análisis de varianza (ANOVA) realizados con la ayuda del software MINITAB® Release 14.20, el cual permite analizar los datos, considerando el efecto de las variables evaluadas sobre los parámetros de porcentaje de hidrólisis que proporciona cada uno de ellos. De esta manera, podemos identificar fácilmente cuáles de los factores (cantidad de enzima, nivel de agitación ó nivel de blanqueo) son determinantes para obtener niveles de hidrólisis altos.Los resultados estadísticos obtenidos mostraron la influencia que tiene cada unos de los factores analizados dentro de la reacción de hidrólisis. En primer lugar se tiene el nivel de agitación con una mayor significancia, seguido de la cantidad de lipasa y dejando por último al nivel de blanqueo como el que produce menor efecto en la reacción (Gráfica 1).
Gráfica 1. Diagrama estandarizado de pareto que refleja el efecto de las variables evaluadas sobre el % de hidrólisis de la reacción
En la gráfica 2 se muestra un análisis estadístico con el que se relaciona cada uno de sus factores y niveles. En su primera sección, se muestra la interacción de la concentración de lipasa vs el nivel de blanqueo. Se puede observar que a mayor concentración de enzima (línea superior, 20%) se pueden obtener porcentajes de hidrólisis más altos, lo que no sucede con los porcentajes de enzima al 5 %. La influencia del blanqueo no tiene gran relevancia aunque sí se exhibe algunas interacciones dentro de los tipos de aceite, haciendo un poco más elevado el porcentaje de hidrólisis para los aceites que no fueron blanqueados. En la segunda sección de esta gráfica, se presenta la concentración de lipasa vs el nivel de agitación, donde se muestra la fuerte influencia que tiene el nivel de agitación frente a la respuesta de hidrólisis. A medida que aumenta la agitación se obtienen mayores porcentajes de hidrólisis; de igual forma, para concentraciones de lipasa más altos, como los exhibidos por la línea superior, se pueden alcanzar porcentajes de hidrólisis hasta de un 93%.
Gráfica 2. Interacción de los factores [lipasa], blanqueo y agitación.
En la tercera y última sección, se aprecia las interacciones entre la agitación y el blanqueado. Aquí se ratifica la gran influencia que tiene la agitación en los tres tipos de aceite. Cada una de las líneas representa un nivel de blanqueado diferente, debido a la proximidad que se presenta una con la otra se encontró que el blanqueo no muestra gran efecto en este estudio.
Gracias a las graficas 3 y 4, se puede ver una interacción por pares de factores representados por líneas de diferentes tonos, los cuales repercuten en la respuesta de hidrólisis. El grado de hidrólisis se presenta desde los niveles alcanzados más altos hasta los más bajos, los cuales se asocian con la intensidad del color, siendo la franja más oscura un porcentaje mayor al 91.5% y la franja más clara, un porcentaje de hidrólisis menor al 85.5%.
]]> Gráfica 3. Comportamiento de la hidrólisis frente al blanqueo y % lipasaGráfica 4. Comportamiento de la hidrólisis frente al nivel de agitación (rpm) y % lipasa
Con la gráfica 3, se puede ver el comportamiento que tiene la concentración de lipasa relacionada con el nivel de blanqueo del aceite, a una agitación constante. Aquí se comprueba que la influencia del blanqueo es muy reducida, ya que el contorno de las líneas están dispuestas de forma horizontal casi perpendiculares unas a otras, lo que para cualquier nivel de blanqueo a una misma cantidad de enzima representará un porcentaje de hidrólisis similar. Esto sugiere que la reacción de hidrólisis puede trabajarse a concentraciones altas de enzima para alcanzar porcentajes elevados de hidrólisis, debido a que una mayor presencia de catalizador tiene la posibilidad de interactuar en la interfase agua-aceite más rápidamente que cuando hay menor cantidad, en un período de tiempo determinado. De igual forma, trabajar con un aceite crudo puede disminuir los costos en los procesos de purificación del aceite, dependiendo de la posterior utilización de los ácidos.
Para la gráfica 4, los factores del nivel de agitación y porcentaje de lipasa utilizados fueron graficados teniendo constante el nivel de blanqueo (0 sin blanquear). Los porcentajes de hidrólisis más elevados, se presentan especialmente en niveles de agitación altos 370 rpm, y porcentajes de lipasa altos. De acuerdo a lo anterior, la esquina superior derecha representa las condiciones en las que se desarrolla la reacción de hidrólisis con mayor éxito, opuesto a lo que sucede con la esquina inferior izquierda, la cual relaciona niveles bajos de agitación y cantidades bajas de enzima; en consecuencia se obtienen grados de hidrólisis bajos. Es importante destacar que la agitación hace parte esencial de la reacción de hidrólisis, ya que es necesario garantizar una afinidad entre la parte acuosa y la oleosa, obteniendo una mejor relación entre reactivos y, por ende, mayor formación del producto.
A medida que avanza la reacción, los ácidos grasos se van liberando, rompiendo sus enlaces éster de la molécula de triglicéridos, obteniendo ácidos grasos libres, glicerol y moléculas de diglicéridos y monoglicéridos. Hay que tener en cuenta que el aceite de palma está constituido principalmente por ácidos palmíticos saturados y oleicos insaturados, los cuales aumentan la viscosidad de la mezcla debido a que su punto de fluidez es alto. Estamos hablando de un sólido disuelto en la mezcla de reactivos lo que hace más difícil el mezclado.
Una de las etapas principales de la reacción es el período de hidrólisis rápida, en el que la agitación juega un papel muy importante, ya que este período se caracteriza por una reacción en fase homogénea debida a un aumento apreciable de la solubilidad del agua en la fase aceite. La grasa y el agua no se encuentran emulsificadas; en este período, se encuentran mezcladas y, por movimientos de agitación, se presenta la dispersión de las dos fases. Por este motivo, es necesario garantizar una buena agitación y estudiar su comportamiento cuando estamos hablando de un proceso a gran escala (Brown 1979).
3.3 ESCALAMIENTO
Como se mencionó anteriormente, el escalamiento se hizo de acuerdo a la mejor combinación de niveles de los tres factores analizados a nivel laboratorio y a las condiciones que proporcionaron un mejor porcentaje de la reacción a nivel laboratorio, como las tomadas para la etapa de escalamiento que se presentan en la tabla 3.
]]> Tabla 3. Condiciones a nivel laboratorio y escalamientoEl porcentaje de hidrólisis a través del tiempo para cada una de las escalas (turbina de 5 cm y agitador tipo ancla), se ve reflejado en la gráfica 5. En ésta, se puede apreciar que el porcentaje de hidrólisis aumenta más cuando se utiliza un agitador de tipo ancla, que al utilizar una agitador de turbina al transcurso de 4 horas y media; es decir, que la hidrólisis enzimática no solo se ve influenciada por el nivel de agitación, sino que también hay una fuerte relación con el tipo de agitador que se utilice para su mezclado.
Gráfica 5. Relación logaritmica del porcentaje de hidrólisis vs. tiempo
La gráfica 5 presenta el porcentaje de hidrólisis alcanzado con respecto al logaritmo del tiempo. Se pudo verificar que la hidrólisis cumple una cinética de primer orden a nivel logarítmico, así como se enuncia en el estudio hecho por Warner, M. Linfield (1984). Los puntos encontrados para cada una de las escalas se acoplan perfectamente a una línea recta, con la que se puede obtener una proyección de la línea para hallar el tiempo necesario para producir un 100 % de hidrólisis.
3.4 RELACIÓN ENTRE AGITADORES DE ESCALAMIENTO
En la escala 1 no se obtuvieron los mismos resultados que a nivel laboratorio, ya que para dos horas y media, las mejores condiciones a nivel laboratorio proporcionaban un valor del porcentaje de hidrólisis del 93%, lo que para el escalamiento con este mismo tipo de turbina fue del 87%. Por otro lado, el agitador tipo ancla (escala 2) reprodujo los resultados a nivel laboratorio de forma casi similar.
Aunque la turbina de pala recta es utilizada para mezclas de líquidos dentro de un rango de viscosidad amplio, el tipo ancla muestra mejores beneficios para la reacción de hidrólisis. Algunas veces el agitador tipo turbina tiende a formar una especie de remolino o vórtice en la parte media del recipiente en que se es realizando el mezclado; este vórtice causa muchas veces zonas de estancamiento del fluido, por lo que la operación de mezclado no se hace de manera satisfactoria. Aunque la presencia del vórtice disminuye con la viscosidad del sistema en agitación, el mecanismo de mezclado sigue siendo el mismo, produciendo así una disminución en el porcentaje de hidrólisis como consecuencia de una disminución de las interacciones entre fase líquida y oleosa.
El agitador de tipo ancla simple tiene como ventaja una superficie amplia, la que produce una disminución en el vórtice y, además, al abarcar una superficie mayor, se proporciona un mejor mezclado de los reactivos, proporcionando así una mayor área de contacto. De esta forma, se ve promovida la disminución de zonas muertas en el mezclado, incrementando así la reacción de hidrólisis (Holland, 1966).
3.5 CRITERIOS CONSTANTES OBTENIDOS PARA EL ESCALAMIENTO
]]> Para la escala 1 y 2, se realizó el análisis de acuerdo a "los resultados de interés" (Doble M., 2002), que en este caso serían proporcionar dos escalas con similaridad geométrica, a diferentes velocidades de agitación, con el fin de obtener un mismo resultado. Para estas dos escalas se evaluó cada uno de los criterios expuestos en la tabla 4.Tabla 4. Criterios de escalamiento
La idea que se tiene con este método de escalamiento es evaluar cada uno de las variables que influyen en el mezclado de un volumen a otro; es decir, de una escala a otra, y determinar cuál de ellas permanece constante, lo que conllevaría a un punto de partida para cualquier escalamiento. Las variables que intervienen son las correspondientes a las fuerzas de viscosidad (número de Reynolds), gravedad (número de Froude), tensión superficial (número de Weber), entre otras.
Evaluando cada uno de los criterios, la potencia por unidad de volumen, fue la que permaneció constante para las dos escalas; es decir, que todos los parámetros restantes pueden cambiar en gran proporción o en menor, pero siempre se tiene que presentar un criterio constante a lo largo de la reacción para distintas escalas de las que se obtiene un mismo resultado, en nuestro caso, un porcentaje de hidrólisis similar.
Aunque la potencia por unidad de volumen fue el criterio de escalamiento encontrado para esta reacción, es necesario hacer ensayos de escalamiento adicionales a diferentes revoluciones y volúmenes, manteniendo la similitud geométrica, para llegar a comprobar si realmente el criterio se sigue cumpliendo: sí el criterio sigue siendo constante para todas las pruebas de escalamiento que obtengan los mismos resultados.
4. CONCLUSIONES
La reacción de hidrólisis enzimática puede llegar a tener altos porcentajes de hidrólisis, entre 87- 96%, en períodos de tiempo cortos, cuando se utilizan mayores cantidades de catalizador y niveles de agitación altos. Esto se presenta debido a que, con una mayor cantidad de enzima, el aceite puede ser hidrolizado en menor tiempo, siempre y cuando se garantice una buena agitación.
Los procedimientos de blanqueo, que se enunciaban en algunos estudios realizados, no son necesarios para el crudo de aceite de palma, sus impurezas no causan inhibición a la enzima de la Candida rugosa.
Uno de los factores que intervienen en la hidrólisis es el nivel de agitación. Es importante tener en cuenta el tipo de agitador que se va a usar para el mezclado de las dos fases, ya que agitadores como el tipo ancla presenta mejores resultados que tipos de agitadores como el de turbina recta, influyendo notoriamente en el producto final de la reacción.
]]> El escalamiento de la reacción de hidrólisis enzimática, catalizador por la lipasa proveniente de la C.rugosa, se podría hacer por medio del criterio de potencia por volumen utilizado P/V (Potencia por unidad de volumen). El escalamiento no es confiable si no se realiza un estudio más detallado, para determinar si realmente hay un patrón de escalamiento para el anterior criterio.5. BIBLIOGRAFÍA
[1] Álvares, C. Producción de ácido esteárico a partir de estearina o grasas Refinadas mediante proceso de hidrólisis. Tesis Pregrado en Ingeniería Química. Universidad Nacional de Colombia, Bogota, Colombia, 1995. [ Links ]
[2] Arango, M. Moreno, N. Pareja, C. Martinez, F. Perea, A. Transesterificación enzimática de la oleica de palma para la producción de grasas especiales en un reactor tipo Batch. Palmas, 26:1, 2004, pp. 370-375. [ Links ]
[3] Benzonana, G, S. Esposito. Biochimi, Biophysics. Acta 231, 1971, pp.15-22 [ Links ]
[4] Brown, H. Fat Splitting. J.AM.Oil Chemists's Soc 56, (1979, November), pp. 729A-732A. [ Links ]
[5] Doble M. Troublefree reaction saclaeup. Chemical Engineering, (January 2002), pp. 345-350. [ Links ]
[6] Firestone, D. Official Methods and Recommended practices of the American Oil Chemists'society, 1989. [ Links ]
[7] Holland, F.A., & Chapman. Liquid Mixing and Processing in Stirred Tanks. Reinhold Publishing Corporation. New York, 1966, pp. 1-88. [ Links ]
[8] H.T. Khor, Aplil. Lipase-Catalyzed Hydrolysis of Palm Oil. JAOCS, 63, 1986, pp. 538-540. [ Links ]
[9] McCabe Warren L. Operaciones unitarias en la ingeniería Química. Mc Graw Hill, Sexta edición, 2002, pp 263. [ Links ]
[10] McCabe, W., Smith, J., Harriott, P. Operaciones Unitarias en Ingeniaría Química. Mc Graw Hill, 2002, 269-299. [ Links ]
[11] S. Bhattacharyya. Biohydrolysis of vegetable oils by Mucor miehei lipase, Oleagineux revue internationale des corps gras. 47, (5). [ Links ]
[12] Serota, S. Enzymatic Fat Hydrolysis and Síntes, JAOCS, 61, (February 1984):191-195. [ Links ]
[13] Vélez, M; Rincón, S; Cuéllar, M; Cendales, J. El mercado de la industria oleoquímica en Colombia. Versión Final, Fedepalma, 2002, Pp. 8,17. [ Links ]
[14] Warner M. Linfield. Ezymatic Fat Splitting JAOCS, 62, pp.131-133. [ Links ]
[15] Yamada, K., H Machida, Meito S. Kabushiki Kaisha. US patent 3, 1965, pp.189,529. [ Links ] ]]>