 MATERIALES Y MÉTODOS
MATERIALES Y MÉTODOS  RESULTADOS Y DISCUSIÓN
RESULTADOS Y DISCUSIÓN  CONCLUSIONES
CONCLUSIONES  AGRADECIMIENTOS ]]>
AGRADECIMIENTOS ]]>
 BIBLIOGRAFÍA
BIBLIOGRAFÍA FOLIAR SUBSTRATES FOR INCREASING CHITINOLYTIC AND GLUCANOLYTIC BACTERIA ON PHYLLOSPHERE OF BANANA
Lina María Salazar Peláez1, Luis Fernando Patiño Hoyos2 y Elkin Bustamante Rojas3
1 Bacterióloga. Instituto Colombiano de Medicina Tropical CES. Carrera 43A # 52S-99. Sabaneta, Colombia. <lmsalazar@ces.edu.co>
2 Profesor. Politécnico Colombiano Jaime Isaza Cadavid. A.A. 4932, Medellín, Colombia. <luisferph@gmail.com>
3 Consultor en Manejo Integrado de Plagas. CATIE. Apartado Postal. 7170 Turrialba, Costa Rica <elkinbustamante@hotmail.com>
Recibido: Agosto 2 de 2005; aceptado: Mayo 19 de 2006.
La Sigatoka Negra, causada por el hongo Mycosphaerella fijiensis Morelet, es considerada la enfermedad de mayor importancia económica para los cultivos de musáceas alimenticias. Su control, se fundamenta en la aplicación de fungicidas sintéticos, cuyo modo de acción viene siendo vulnerado por poblaciones del hongo. La presente investigación, ha explorado la posibilidad de desarrollar una estrategia de regulación biológica, basada en el estudio y manipulación de algunos de los factores bióticos y abióticos que interactúan en la filosfera de banano, con el objetivo de incrementar las poblaciones epifitas naturales de bacterias quitinolíticas y glucanolíticas, las cuales pueden afectar negativamente la germinación del patógeno. Con base en una fase previa a este estudio, en la cual se realizó una caracterización químico-microbiológica parcial de la filosfera de plantas de banano y plátano bajo condiciones del Urabá antioqueño (Colombia), se evaluaron 14 sustratos foliares, compuestos por quitina coloidal (QC) [4 %], harina de cebada (HC) [2,5 %] y urea (U) [1 %], solas ó en combinación, los cuales siempre estuvieron acompañados de una solución mineral base y una solución adherente-dispersante. Aquellos sustratos a base de HC y U, produjeron los mayores incrementos en las poblaciones de bacterias líticas epifitas, con recuentos superiores a las 10.000 veces, con respecto a sus poblaciones iniciales sobre hojas de banano del cultivar Gran Enano, y de hasta 8,6 y 15 veces mayores para las bacterias quitinolíticas y glucanolíticas respectivamente, con relación a la población en el tratamiento sin sustratos foliares. Se discute la influencia de la precipitación sobre las poblaciones de dichas bacterias líticas y la necesidad de ajustar una formulación que mejore las posibilidades de control sobre la sigatoka negra.
Palabras clave: Filosfera, Mycosphaerella fijiensis, sigatoka negra, biorregulación.
ABSTRACT
Black Sigatoka, caused by the fungus Mycosphaerella fijiensis Morelet, is considered the economically most important disease of banana and plantain crops. Its control has been based on the use of synthetic fungicides, whose mode of action becomes overcome by the fungus populations. This research explored the possibility of developing a biological regulation strategy based on the study and manipulation of certain biotic and abiotic factors that interact in the phyllosphere of the banana, with the objective of increase the natural populations of chitinolytic and glucanolytic bacteria, which could negatively affect the germination process of M. fijiensis. On the basis of a previous phase of this study in which a partial chemical and microbiological characterization in the phyllosphere of banana and plantain crops under conditions of Uraba-Antioquia (Colombia), was conducted here 14 foliar substrates were evaluated that consisted of colloidal chitin (CC) [4%], barley flour (BF) [2,5%] and urea (U) [1%], individually or in a combination, always with a mineral base and attachment-dispersant solutions. Those substrates that had a combination of BF and U yielded higher increases in the epiphytic lytic bacterial populations, with counts exceeding 10.000 fold with respect to their their initial populations on banana leaves of the Grande naine variety and 8,6 y 15 fold higher in populations of chitinolytic and glucanolytic bacteria, respectively, with respect to the population without foliar substrate treatments. The effect of rainfall on bacteria populations and the necessity of adjusting a formulation that improves the possibilities of foliar substrates for black sigatoka control are discussed.
Key Words: Phyllosphere, Mycosphaerella fijiensis, Black Sigatoka, biological control.
 MATERIALES Y MÉTODOS
MATERIALES Y MÉTODOS
 RESULTADOS Y DISCUSIÓN
RESULTADOS Y DISCUSIÓN
 CONCLUSIONES
CONCLUSIONES
 AGRADECIMIENTOS ]]>
AGRADECIMIENTOS ]]>
 BIBLIOGRAFÍA
BIBLIOGRAFÍA
La Sigatoka Negra, causada por el hongo ascomiceto Mycosphaerella fijiensis Morelet, se ha constituido en la enfermedad de mayor impacto económico para la industria de banano de exportación en el mundo, en Colombia los costos del control químico de la enfermedad varían entre US$700 y 900/hectárea al año; cifra que representa el 46 % del valor global de los agroquímicos y cerca del 14 % de los costos totales de producción de la fruta (Chica et al. 2004). La enfermedad produce una rápida destrucción del área foliar de la planta, la cual reduce el área fotosintética y produce un efecto detrimental sobre la calidad de la fruta, con una reducción de hasta un 60 % en el peso del racimo, cuando no se implementa una medida química de control (Belálcazar 1991, citado por Chica et al. 2004). Adicionalmente, se presenta una maduración prematura de los racimos, lo cual es la principal causa de pérdidas ocasionadas por la enfermedad (Marín y Romero 1992).
Básicamente, la enfermedad se ha controlado mediante la aplicación de fungicidas sintéticos, cuyo costo varía en Colombia entre 700 y 900 dólares /hectárea al año, cifra que representa el 13,8 % de los costos totales de producción del banano y el 46 % del valor total de los agroquímicos (Chica et al. 2004). Sin embargo, la efectividad de esta medida de control ha disminuido debido a múltiples factores, entre ellos: cambios en la incidencia y severidad de la enfermedad, condiciones particulares en cada una de las fincas que favorecen el establecimiento y diseminación del patógeno, y principalmente al incremento de las poblaciones del hongo con menor sensibilidad a los fungicidas sistémicos empleados (Patiño 2003, Chica et al. 2004). Situación agravada por el número reducido de grupos químicos disponibles actualmente para controlar la enfermedad y la no disponibilidad a corto y mediano plazo de moléculas fungicidas con novedosos modos de acción sobre el patógeno.
La regulación biológica para patógenos foliares, puede ser una alternativa complementaria del control integrado de enfermedades, la cual frecuentemente involucra la aplicación del microorganismo antagonista sobre la superficie de la hoja (Spurr 1981, Blakeman y Fokkema 1982). Sin embargo, el éxito de dicho antagonista depende de su capacidad para establecerse como miembro de la microbiota epifita especialmente cuando se requiere disminuir el inóculo del patógeno (Spurr 1981, Blakeman y Fokkema 1982). Por tal motivo, el uso de antagonistas microbianos aislados de la microbiota epifita debería preferirse al uso de antagonistas aislados de otros ambientes, pues los primeros se encuentran adaptados a las condiciones que determinan el hábitat en la superficie de la hoja (Blakeman y Fokkema 1982, Andrews 1992).
Dentro de la regulación biológica de fitopatógenos, una de las estrategias consiste en el uso de microorganismos antagonistas productores de sustancias antibióticas y/o enzimas líticas que actúen sobre sus esporas o tubos germinativos en su fase epifita de crecimiento (Andrews 1992, Elad et al. 2002). Por ejemplo, el empleo de microorganismos productores de quitinasas y/o glucanasas en la regulación de hongos basidiomicetos y ascomietos ha demostrado ser de utilidad, pues la pared celular de dichos hongos está constituida principalmente por microfibrillas de quitina y b-glucanos, hecho que los hace sensibles al ataque de estas enzimas, especialmente a nivel de la hifa (Sahai y Manocha 1993, Alexopoulos, Mims, y Blackwell 1996, Mahadevan y Crawford 1997, Cohen-Kupiec y Chet 1998). Esta bioregulación mediante el uso de bacterias líticas antagonistas, ha sido estudiada con diversos fitopatógenos como Rhizoctonia solani, Phytophthora fragariae var. rubi, Phytophthora capsici, Sclerotium rolfsii, Fusarium oxysporum f.sp. cucumerinum, Bipolaris sorokiniana y Pseudomonas syringae pv. tomate, entre otros (Chernin et al. 1995, Valois et al. 1996, Ordentlich, Elad and Chet 1998, Sing et al. 1999, Zhang y Yuen 2000, Parra y Ramírez 2002, Ji y Wilson 2003, Sid Ahmed et al. 2003).
Osorio et al. (2004), realizaron pruebas de antagonismo sobre ascosporas de M. fijiensis, con bacterias quitinolíticas aisladas del filoplano de banano en un ensayo in situ sobre discos de hojas también de esta planta, encontrando que algunos de los aislados inhibieron la germinación de las ascosporas o deformaron sus tubos germinativos, hasta en un 40 y 85 % respectivamente. Tal efecto, en parte, fue explicado por la actividad de las enzimas quitinolíticas sobre la pared del patógeno.
En una fase previa a esta investigación, se demostró que las bacterias líticas epifitas podían estar presentes en bajas poblaciones en la filosfera de plantas de banano cultivadas, y que además algunas de estas bacterias producían quitinasas y/o glucanasas en un periodo inferior a las 48 horas de incubación, cuando una fuente de quitina ó b-(1,3) glucanos estuvo presente en el medio de cultivo que soportaba su crecimiento (Salazar 2005). Esta capacidad, les puede permitir a los aislados actuar sobre la quitina y/o b-(1,3) glucanos presentes en la pared celular de los tubos germinativos de M. fijiensis, antes de que estos penetren en el estoma; pues se ha observado que trascurren al menos 48 horas entre la llegada de la ascospora a la hoja y el inicio del proceso de penetración en el estoma (Marín et al. 2003).
Por otro lado, se ha demostrado que las poblaciones del microorganismo antagonista pueden ser incrementadas mediante la aplicación de sustratos foliares que las favorezcan nutricionalmente, aumentando consecuentemente su actividad biorreguladora (Davis et al. 2002, Fokkema et al. 1979, Ploper, Backman y Rodriguez-Kabana 1992, Stadler y Mueller 1996), en lugar de la aplicación directa y masiva de los agentes biológicos de control, evitando los riesgos potenciales asociados a este tipo de aplicación en campo. La quitina ha sido aplicada como sustrato junto con la bacteria Bacillus cereus cepa 304 para el control de la mancha foliar en maní causada por Cercospora arachidicola, incrementándose el tamaño poblacional de la bacteria sobre las hojas y resultando en un control significativo de la enfermedad (Kokalis-Burelle et al. 1992). Los aminoácidos también han sido utilizados como sustratos para incrementar el tamaño poblacional de cepas de bacterias antagonistas no patogénicas sobre frutas de manzana, logrando un control mejorado del moho azul que afecta esta fruta (Janisiewicz, Usall y Bors 1992). Se ha reportado también que la aplicación de metionina incrementó el tamaño poblacional del agente de control biológico Pseudomonas putida AP-1 en el suelo, donde la supresión de la marchitez por Fusarium en tomate fue mayor cuando la bacteria fue aplicada con el aminoácido en relación a su aplicación individual (Yamada y Ogiso 1997).
La habilidad para incrementar selectivamente el tamaño poblacional y la eficacia de un microorganismo biocontrolador, empleando enmiendas nutricionales, se basa en el hecho de que la concentración y diversidad de nutrientes constituye un factor limitante para el crecimiento de las poblaciones microbianas en la planta, especialmente las localizadas en el filoplano; pues dicho lugar constituye un hábitat donde la concentración de fuentes de carbono y nitrógeno es escasa (Andrews 1992, Janisiewicz y Bors 1995, Wilson y Lindow 1994, Wilson et al 1995, Salazar 2005), observándose por ejemplo que la aplicación exógena de carbono incrementa las poblaciones de P. putida y P.syringae en la filosfera de frijol y tomate respectivamente (Wilson y Lindow 1995, Ji y Wilson 2003).
]]> En el caso de las estrategias de regulación biológica para M. fijiensis, se han realizado algunas investigaciones basadas en la aplicación de bacterias antagonistas productoras de quitinasas y/o b-glucanasas aisladas de la filosfera de banano y plátano, solas ó en combinación con sustratos foliares de diversas características nutricionales compuestas por quitina coloidal, leche y melaza, entre otros (González et al. 1996, Ruíz-Silvera et al. 1997, Arango 2000); no obstante, es necesario dirigir la aplicación de estas sustratos con base en una caracterización previa de la filosfera de banano, al menos en sus componentes químico nutricional (minerales, carbohidratos y proteínas) y de poblaciones nativas de bacterias con potencial lítico sobre el hongo causante de la Sigatoka Negra. Con base en lo anterior, el objetivo del presente trabajo consistió en evaluar diversos sustratos foliares a base de quitina coloidal y harina de cebada, como fuentes de quitina y b-(1,3) glucanos, respectivamente, a partir de una caracterización química y microbiológica de la filosfera de banano, para favorecer nutricionalmente, y de manera selectiva, a las poblaciones epifitas de bacterias quitinolíticas y/o glucanolíticas nativas de la filosfera de banano, como punto de partida para formular sustratos foliares con potencial de control sobre la Sigatoka Negra.
Composición de los sustratos. Se evaluaron catorce tratamientos y seis testigos, elaborados a partir de los siguientes compuestos:
Tabla 1. Composición de los sustratos foliares, elaborados para incrementar poblaciones de bacterias quitinolíticas y glucanolíticas sobre hojas de banano.
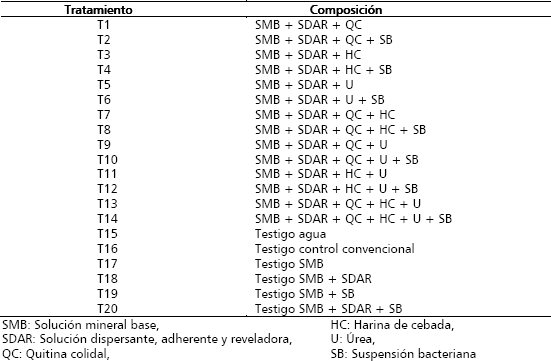
En los números pares de los tratamientos, se incluyó una suspensión bacteriana (SB) preparada a partir de un bacilo gram negativo, aislado de la filosfera de una planta de banano variedad Gran Enano aislado Q3. Dicho aislado, evidenció en ensayos in vitro actividad quitinolítica y glucanolítica antes de las 24 horas de incubación. Para la obtención de la suspensión bacteriana, una colonia pura del aislado fue incubada en medio líquido durante 16 horas, a 25 °C y en agitación constante a 100 rpm. La composición del medio, fue la siguiente: 1 g/l de K2HPO4 (Mallin-ckrodt), 0,5 g/l de MgSO4 (JT Baker), 1 g/l de NaCl (Carlo Erba), 3,5 g/L de extracto de levadura (Merck) y 20ml/l de quitina coloidal. La concentración final de la suspensión en los sustratos que la contenían, fue de 5x108 a 5x109 UFC/ml.
La inclusión de una suspensión bacteriana dentro de los tratamientos, se realizó para verificar si la aplicación foliar del inóculo bacteriano lograba un incremento superior en la población epifita de bacterias quitinolíticas y glucanolíticas, comparado con aquellos tratamientos que no contenían la suspensión bacteriana.
Se evaluaron seis testigos, los cuales no contenían los compuestos quitina coloidal, harina de cebada o urea; e incluían la solución mineral base, la solución dispersante y adherente y la suspensión bacteriana (T17-T20); más otros dos tratamientos, uno a base de agua (T15) y otro que consistió en un sistema estándar de control químico (T16), basado en un programa convencional de control de la enfermedad (Tabla 1).
La totalidad de los tratamientos, a excepción de los testigos 15 y 16, fueron llevados a un pH final de 7,5; esto con el objetivo de favorecer el crecimiento de la población bacteriana epifita y limitar el crecimiento de hongos. Los sustratos fueron preparados dos días antes de su aplicación y fueron almacenados a 4°C, homogenizando la mezcla 15 minutos antes de su aplicación final sobre las hojas de banano. Todos los tratamientos fueron aplicados semanalmente durante 17 semanas consecutivas entre el 26 de enero y el 21 de mayo de 2004, periodo que incluyó dos épocas climáticas, una seca comprendida entre las semanas uno a la ocho; y otra lluviosa, la cual inició en la semana nueve y prosiguió hasta la última semana de evaluación. Las aplicaciones se realizaron mediante un atomizador manual sobre el envés de la primera hoja y las subsiguientes hojas que emergieron después de su iniciación.
Ubicación geográfica. El experimento se llevó a cabo en un lote experimental del Centro de Investigaciones del Banano, Cenibanano, ubicado en el Municipio de Carepa (Antioquia, Colombia), a una altura de 27 msnm, con una temperatura promedia de 28 °C, una precipitación promedio anual de 3.500 mm y una humedad relativa promedio del 88 %.
Diseño experimental, variables evaluadas y análisis estadístico. Se empleó un diseño completamente al azar, con 20 tratamientos 14 tratamientos y 6 testigos y 7 repeticiones, para un total de 140 unidades experimentales las unidades experimentales estuvieron representadas por plántulas de banano variedad Gran Enano, altamente susceptible a la Sigatoka Negra, procedentes de cultivo in vitro, de cinco meses de edad y con una altura aproximada de 80 a 90 cm.
Para la evaluación de la dinámica de crecimiento de las bacterias quitinolíticas y glucanolíticas epifitas, en cada tiempo de evaluación se seleccionaron aleatoriamente dos de las siete repeticiones, haciendo recuentos de las bacterias en la semana de inicio del ensayo antes de la aplicación de los sustratos, para determinar el número inicial de bacterias líticas epifitas y posteriormente a la primera, cuarta, sexta, novena y catorceava semanas después de comenzar con las aplicaciones de los tratamientos.
]]> El procedimiento relacionado con el conteo de las bacterias de interés, fue el siguiente: se realizaron diluciones seriadas de las muestras, previo paso de homogeneización, hasta la dilución de 10-3. A partir de dicha dilución se tomaron 20ml, los cuales fueron sembrados por triplicado mediante la técnica de siembra en superficie en los medios agar nutritivo quitina y agar cebada, para determinar las poblaciones de bacterias quitinolíticas y glucanolíticas, respectivamente. El agar nutritivo quitina, estuvo compuesto por 20 ml/L de quitina coloidal y 15g/L de agar nutritivo (Difco - Becton Dickinson) -pH final de 7,2; mientras que el agar cebada, estuvo compuesto por 1 g/l de K2HPO4 (Mallinckrodt), 0,5 g/l de MgSO4 (JT Baker), 1g/l de NaCl (Carlo Erba), 5 g/l de harina de cebada, 1 g/l de NH4NO3 (Merck) y 15 g/l de agar agar (BactoTM Becton Dickinson) -pH final de 7,2-. El proceso de incubación, se realizó a 25 °C durante 48 horas. En ambos medios, la capacidad para utilizar la quitina coloidal y/o la harina de cebada como fuentes de carbono, era evidenciada por la formación de un halo de consumo alrededor de la colonia (González 1996, y Talavera et al. 1998). Los recuentos, fueron expresados en términos de unidades formadoras de colonia por mililitro de muestra -UFC/ml-.
Bajo condiciones físicas favorables para el crecimiento bacteriano, la diversidad y concentraciones de las fuentes de carbono disponibles en la superficie de la hoja constituyen el determinante principal de los tamaños de las poblaciones de bacterias epifitas (Wilson y Lindow 1994, Mercier y Lindow 2000, Ji y Wilson 2003). De tal manera que, dichas poblaciones pueden ser manipuladas por cambios en el estatus de tales nutrientes (Mercier y Lindow 2000). Ésta, constituyó la premisa a partir de la cual se diseñó la estrategia para potenciar la regulación biológica contemplada en esta investigación. Tal estrategia, consistió en emplear fuentes de carbono específicas quitina coloidal y harina de cebada, como fuentes de quitina y b-(1,3) glucanos, respectivamente; como constituyentes principales de los sustratos foliares, para el incremento selectivo de las poblaciones de bacterias quitinolíticas y glucanolíticas epifitas de plántulas de banano.
El efecto de los sustratos foliares sobre la dinámica de crecimiento de dichas poblaciones, se describe a continuación: El incremento de las poblaciones de bacterias líticas epifitas, empezó a hacerse visible a partir de la cuarta semana de iniciado el ensayo; incremento que llegó a alcanzar su pico máximo hacia la sexta semana (Tabla 2). Después de dicho pico, los recuentos de la población comenzaron a descender hasta alcanzar los niveles encontrados antes del inicio del ensayo, del orden de < 0,05 UFC/ml, los cuales comenzaron a observarse nuevamente en la semana nueve de evaluación y continuaron hasta el final de las aplicaciones.
Tabla 2. Población de bacterias quitinolíticas y glucanolíticas, seis semanas después de la aplicación de sustratos foliares.
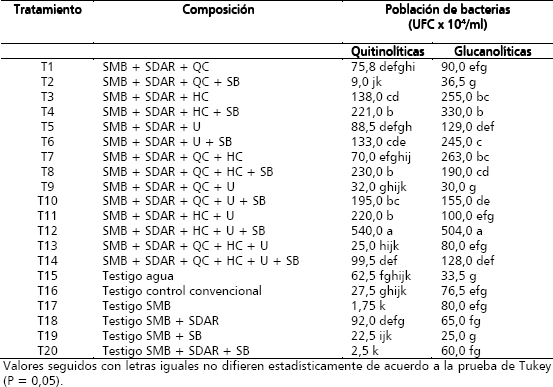
El inicio de la época lluviosa, ocurrió durante el transcurso de la novena semana. Situación que podría explicar la caída en los recuentos allí evidenciada, pues las lluvias ejercen un efecto de lavado sobre los sustratos aplicados y sobre la población lítica establecida semanas antes. Al respecto Butterworth y McCartney (1991), demostraron que las precipitaciones constituyen un mecanismo eficiente de remoción bacteriana de la superficie de las hojas. Estos autores, en ensayos de invernadero, determinaron que la proporción de bacterias que se desplaza por el efecto del golpe de las gotas está directamente relacionada con el número total de bacterias presentes en las hojas. Los resultados de esta investigación concluyeron que el efecto de lavado de las lluvias es complejo y que su efectividad en la remoción de bacterias de la superficie foliar depende de la intensidad de la lluvia y de las características físicas de la hoja. Con base en lo anteriormente planteado, es importante que la estrategia de biorregulación se direccione a alcanzar su máxima capacidad de establecimiento en la época de baja a moderada precipitación, en la cual presenta menos riesgos de remoción de las bacterias antagonistas y mediante formulación sostener estas poblaciones para las épocas de mayor precitación, las cuales son también las épocas de mayor presión de la enfermedad (Chica et al. 2004).
Para determinar cuáles fueron los tratamientos que más incrementaron las poblaciones de bacterias líticas epifitas, se realizó una comparación entre el recuento en la semana seis y el recuento obtenido antes del inicio del ensayo cuyo promedio para todos los sustratos fue menor a 0,05 X 104 UFC/ml, para así calcular el valor del incremento. También se calculó el incremento en la semana seis de los diferentes tratamientos con respecto al testigo agua para esta misma semana.
Los cuatro sustratos foliares que produjeron los mayores recuentos de bacterias quitinolíticas, correspondieron en orden de mayor importancia a los siguientes tratamientos:
Estos cuatro tratamientos resultaron estadísticamente superiores a los seis testigos evaluados (T15-T20) (Tabla 2), donde el componente común es la harina de cebada al 2,5%. La harina de cebada, constituye una fuente rica de b-(1,3) glucanos y es carente de quitina (Holmes 1991, Michniewicz Michnie-wicz, Kołodziejczyk y Obuchowski 2003). A pesar de ello, los b-(1,3) glucanos también pudieron ser utilizados como fuente de carbono por las bacterias quitinolíticas. La anterior situación, no debe ser considerada como irregular, pues en la caracterización microbiológica parcial realizada durante la primera fase de la investigación se encontró que algunas de las bacterias aisladas de la filosfera de musáceas poseían tanto actividad quitinolítica como glucanolítica (Salazar 2005).
Por otro lado, ninguno de los testigos estuvo entre los ocho mejores tratamientos para bacterias quitinolíticas; aunque el testigo compuesto de solución mineral y solución dispersante T18, fue el mejor entre todos los testigos obteniendo un recuento de 92 x 104 UFC/ml, evidenciando un incremento de 1.840 veces con respecto al recuento inicial y de 1,5 veces con relación al tratamiento agua. El testigo a base de solución mineral T17, representó el tratamiento con menor población observada, obteniendo un recuento de 1,75 x 104 UFC/ml en la semana seis, con un incremento de 35 veces con respecto al recuento base y de tan solo 0,03 veces en la semana seis con respecto a la población encontrada en el testigo agua. El comportamiento del testigo agua presentó poblaciones superiores aunque no significativamente a los demás testigos que incluían solución mineral, lo cual puede estar revelando que los niveles de minerales en la filosfera no son tan determinantes para los incrementos poblacionales como si lo son las fuentes de carbono (Wilson y Lindow 1994, Mercier y Lindow 2000, Ji y Wilson 2003).
Arango 2000, evaluó el efecto de diversos sustratos foliares sobre el crecimiento de la población bacteriana quitinolítica de la filosfera del cultivar Gran Enano, en un ensayo de invernadero con etapa de inoculación natural. Dicho estudio, concluyó que la aplicación de quitina coloidal sola, ó en combinación con otras fuentes de carbono y nitrógeno, logra favorecer el crecimiento de la población de bacterias quitinolíticas epifitas.
La inclusión de la suspensión bacteriana dentro de los sustratos, demuestra que la adición de un inóculo extra de la bacteria a las poblaciones naturales epifitas, la cual es mantenida en el laboratorio en medios selectivos cuya fuente de carbono es la misma que la de los sustratos foliares, puede potencializar su propio incremento y el de las poblaciones naturales con actividad lítica, situación similar ha sido reportado para el caso de Stenotrophomonas maltophilia C3 en el control de Bipolaris sorokiniana, donde los aislados de la bacteria preinducidos en medio con quitina mostraban un mejor control de la enfermedad (Zhang y Yuen 2000).
En la presente investigación, el incremento de las poblaciones quitinolíticas en respuesta a la aplicación de quitina coloidal es bastante heterogéneo y evidencia las diferencias en la composición de aquellos sustratos que la contenían. Por ejemplo, el tratamiento 1-solución mineral, solución dispersante y quitina coloidal ocupó el onceavo lugar entre los mejores sustratos; mientras que el tratamiento 2 -solución mineral, solución dispersante, quitina coloidal y suspensión bacteriana, ocupó el tercer lugar entre los sustratos con más bajas poblaciones de las bacterias. Sin embargo, los dos mejores sustratos para estas poblaciones incluían quitina coloidal como uno de sus componentes. Para obtener resultados más consistentes y representativos, es necesario realizar investigaciones, en donde se intensifique el sistema de muestreo utilizado y se utilicen técnicas como el desprendimiento de las bacterias epifitas mediante sonicación (Ji y Wilson 2003, Morris, Monier y Jacques 1998), con la cual se pueden recuperar mayores poblaciones de bacterias a las obtenidas con el sistema de lavado con solución buffer.
]]> Con respecto a las bacterias glucanolíticas, los sustratos que produjeron los mayores recuentos corresponden a los siguientes tratamientos:Estos tres tratamientos al igual que en el caso de las bacterias quitinolíticas, presentaron niveles poblacionales estadísticamente superiores, con respecto a los testigos evaluados (T15-T20) (Tabla 2). Ninguno de estos tratamientos testigo hizo parte de los nueve mejores tratamientos para bacterias glucanolíticas; aunque el tratamiento 17 compuesto de solución mineral, fue el mejor entre todos los testigos obteniendo un recuento de 80 X 104 UFC/ml en la semana seis; evidenciando un incremento de 1.600 veces, con respecto al recuento base y de 2,4 veces con base al testigo agua. El tratamiento 19 solución mineral y suspensión bacteriana representó el tratamiento con menor población bacteriana observada, obteniendo un recuento de 25 X 104 UFC/ml en la semana seis, evidenciando un incremento de 500 veces con respecto al recuento base y de tan solo 0,7 veces con respecto al testigo agua en la semana seis; y en forma similar a lo encontrado con los testigos para las poblaciones de bacterias quitinolíticas, nuevamente las fuentes de carbono son más determinantes, ya que estas si produjeron incrementos significativos (Tabla 2) que los que se pueden obtener a partir de las concentraciones de minerales disponibles para la microbiota epifita (T17-T20).
Al comparar los mejores sustratos para ambos tipos de población lítica, es evidente la importancia de los tratamientos 12 y 4, los cuales tienen como componente en común la harina de cebada, cuya aplicación como sustrato foliar para musáceas alimenticias no ha sido reportada con anterioridad, y la suspensión bacteriana preparada a partir de un aislado de la población nativa de bacterias líticas epifitas. El empleo de la harina de cebada, tiene como ventajas adicionales su bajo costo económico y fácil obtención, con respecto a los altos costos y laboriosa preparación de la quitina coloidal, empleada en estudios previos (González 1996, Arango 2002, Patiño 2002). Se confirma la importancia de una fuente de carbono, en este caso quitina y glucano, como sustratos selectivos para incrementar poblaciones de bacterias capaces de degradar estos carbohidratos (Wilson y Lindow (1994), Ji y Wilson 2003); lo cual plantea un resultado promisorio como base para la elaboración de sustratos foliares diseñados para incrementar poblaciones nativas de microorganismos con potencial antagonista sobre M. fijiensis.
A partir de este estudio exploratorio, se encontró que los sustratos foliares que produjeron los mayores recuentos de bacterias quitinolíticas epifitas, correspondieron a los tratamientos 12, 8, 4 y 11; cuyo constituyente común, además de la solución mineral base y la solución dispersante, fue la harina de cebada al 2,5%. De igual forma, los sustratos que produjeron los mayores recuentos de bacterias glucanolíticas epifitas, correspondieron a los tratamientos 12, 4 y 7; cuyo constituyente común, también fue la harina de cebada al 2,5%; destacándose el componente urea en algunos de estos sustratos el cual puede complementar el efecto de control sobre el patógeno y la presencia de una suspensión bacteriana cuya preinducción en medio con quitina puede también ayudar a incrementar actividad de poblaciones líticas epifitas; lo cual proyecta la importancia de profundizar en investigaciones que ayuden a explicar estos resultados. Finalmente se considera que es prioritario dirigir las futuras investigaciones a lograr una formulación que permita maximizar la expresión en condiciones de campo, del potencial biorregulador sobre M. fijiensis por acción de la microbiota epifita nativa de la filosfera de banano y plátano, al favorecer su colonización y tamaño poblacional mediante la aplicación de sustratos foliares.
]]>Esta investigación se realizó gracias a fondos y apoyo del Instituto Colombiano para el Desarrollo de la Ciencia y la Tecnología Francisco José de Caldas COLCIENCIAS, a través del proyecto: Componentes químicos y microbiológicos de la filosfera de musáceas y su aplicación en el manejo de la Sigatoka Negra, código 842-12-11569; así como el apoyo del Centro de Investigaciones del Banano CENIBANANO-AUGURA Colombia y del profesor Pablo Buriticá Céspedes de la Universidad Nacional de Colombia, Sede Medellín.
Alexopoulos, C. J, Mims, C. W, and Blackwell, M. 1996. Characteristics of fungi. En: Introductory Micology. 4th ed. New York, USA : John Wiley & Sons. p. 26-56. [ Links ]
Andrews, J. H. 1992. Biological control in the phyllosphere. En: Annual Review of Phytopathology. Vol. 30; p.603-635. [ Links ]
Arango, M. E. 2002. Alternativas de manejo para el control biológico de Sigatoka Negra (Mycosphaerella fijiensis Morelet) en el cultivo del banano (Musa AAA). p. 130-134. En: XV Reunión Internacional ACORBAT (15: 2002: Cartagena de Indias, Colombia). Memorias. Medellín: Augura. [ Links ]
Blakeman, J. P. and Fokkema, N .J. 1982. Potencial for biological control of diseases on the phylloplane. En: Annual Review of Phytopathology. Vol. 20; p.167-192. [ Links ]
Butterworth, J. and Mc Cartney, H. A. 1991. The dispersal of bacteria from leaf surfaces by water splash. En: Journal of Applied Bacteriology. Vol 71; p. 484-496. [ Links ]
Chernin, L., Ismailov, Z., Haran, S. and Chet, I. 1995. Chitinolytic Enterobacter agglomerans antagonistic to fungal plant pathogens. En: Applied and Environmental Microbiology. Vol 61, no.5; p.1720-1726. [ Links ]
Chica, R., Herrera, M., Jiménez, I., Lizcano, S., Montoya, J. A., Patiño, L. F., Rodríguez, P. A. y Ruíz, L. H. 2004. Impacto y manejo de la Sigatoka Negra en el cultivo del banano de exportación en Colombia. p. 53-62. EN. XVI Reunión Internacional Acorbat (16: 2004: Oaxaca, México). Memorias. Oaxaca: Acorbat. [ Links ]
Cohen-Kupiec, R. and Chet, I. 1998. The molecular biology of chitin digestion. En: Current Biology. Vol. 9; p. 270-277. [ Links ]
Davis, R. F., Backman, P. A. Rodriguez-Kabana, R. and Kokalis-Burelle, N.1992. Biological control of apple fruit diseases by Chaetomium globosum formulations containing cellulose. En: Biological Control. Vol 2; p.118123. [ Links ]
Elad, Y., Richard, R., Bélanger, R. and Jürgen, K. 2002. Biological control of diseases in the phyllosphere. p.66-78. En: I Curso Taller Internacional Control biológico, componente fundamental del manejo integrado de plagas en una agricultura sostenible. (2002: Bogotá, Colombia). Memorias. Bogotá: CORPOICA. [ Links ]
Fokkema, N. J., den Houter, J. G., Kosterman, Y. J. C. and Nelis, A. L. 1979. Manipulation of yeasts on fieldgrown wheat leaves and their antagonistic effect on Cochliobolus sativus and Septoria nodorum. En: Transactions of the British Mycological Society. Vol 72; p. 1929. [ Links ]
González, R., Bustamante, E., Shannon, E. P., Okumoto, P. S. y Leandro. G. 1996. Evaluación de microorganismos quitinolíticos antagonistas a Mycosphaerella fijiensis en casa de mallas y en campo. En: Manejo Integrado de Plagas (Costa Rica). No. 40; p.12-16. [ Links ]
Holmes, M.G. 1991. Opportunities for research in coarse grains (barley and oats) in the Riverina. Riverina Outlook Conference, Food Processing Workshop. Wagga, Farrer Centre and The Regional Institute Ltd. Disponible en Internet http://www.regional.org.au/au/roc/1991%20food/regional.org.au/au/index.htm#P41_2571food/index.htm#TopOfPage. Consultada: 5 Dic. 2004]. [ Links ]
Janisiewicz, W. J., Usall, J. and Bors, B. 1992. Nutritional enhancement of biological control of blue mold on apples. En: Phytopathology. Vol 82; p. 13641370. [ Links ]
________ and Bors, B. 1995. Development of a microbial community of bacterial and yeast antagonists to control woundinvading postharvest pathogens of fruits. En: Applied and Environmental Microbiology. Vol 61, no. 9; p. 32613267. [ Links ]
Ji, P. and Wilson, M. 2003. Enhancement of population size of a biological control agent and efficacy in control of bacteria speck of tomato through salicylate and ammonium sulfate amendments. En: Applied and Environmental Microbiology. Vol 69, no. 2; p. 1290-1294. [ Links ]
Kokalis-Burelle, N., Backman, P. A., Rodriguez-Kabana, R. and Ploper, L. D. 1992. Potential for biological control of early leafspot of peanut using Bacillus cereus and chitin as foliar amendments. En: Biological Control. Vol 2; p.321328. [ Links ]
Mahadevan, B. and Crawford, D. L. 1997. Propierties of the chitinase of the antifungal biocontrol agent Streptomyces lydicus WYEC108. En: Enzyme and Microbial Technology. Vol. 20, no. 7; p. 489-493. [ Links ]
Marín, D. H. y Romero, C. R. 1992. El combate de la Sigatoka Negra. Costa Rica: Corporación Bananera Nacional, Departamento de Investigaciones. 22p. (Boletin no. 4). [ Links ]
Marín, D. H., Romero, R. A., Guzmán, M. and Sutton T. B. 2003. Black Sigatoka: An increasing threat to banana cultivation. En: Plant Disease. Vol. 87, no. 3; p. 208-223. [ Links ]
Mercier, J. and Lindow, S. E. 2000. Role of leaf surface sugars in colonization of plants by bacterial epiphytes. En: Applied and Environmental Micro-biology. Vol. 66, no.1; p. 369-374. [ Links ]
Michniewicz, J.; Kołodziejczyk, P. and Obuchowski, W. 2003. Betaglucan enzymatic hydrolysis in cereal grains and cereal products. Electronic Journal of Polish Agricultural Universities, 6 (1). Disponible en internet http://www. ejpau.media.pl/series /volume6/issue1 /food/art03.html. [Consultada: 5 Dic. 2004]. [ Links ]
Mondal, S. N. and Timmer, L. W. 2003. Effect of urea, CaCO3, and dolomite on pseudothecial development and ascospore production of Mycosphaerella citri. En: Plant Disease. Vol 87, no.5; p. 478-482. [ Links ]
Morris, C. E., Monier, J. M. and Jacques, M. A. 1998. A technique to quantify the population size and composition of the biofilm component in communities of bacteria in the phyllosphere. En: Applied and Environmental Microbiology. Vol 64, no. 12; p. 4789-4795. [ Links ]
Ordentlich, A., Elad, Y. and Chet, H. 1998. The role of chitinase of Serratia marcescens in biocontrol of Sclerotium rolfsii. En: Phytophatology. Vol 78, no.1; p. 84-88. [ Links ]
Osorio, I., Patiño, L. F., Bustamante, E. y Rodríguez. P. 2004. Selección y evaluación de bacterias quitinolíticas provenientes de la zona de Urabá, para el control de la Sigatoka Negra. En. Boletín Técnico de Cenibanano. No.6; p. 8-13. [ Links ]
Parra, Y. y Ramírez, R. A. 2002. Efecto de diferentes derivados de la quitina sobre el crecimiento in vitro del hongo Rhizoctonia solani Kuhn. En: Cultivos Tropicales. Vol. 23, no. 2; p. 73-75. [ Links ]
Patiño, L. F. 2002. Efecto de una fuente de energía, tres inductores de resistencia y un sustrato foliar sobre Sigatoka Negra en banano. p. 135-142. En: XV Reunión Internacional ACORBAT (15: 2002: Cartagena de Indias, Colombia). Memorias. Medellín: AUGURA. [ Links ]
________. 2003. La resistencia a fungicidas, una continua amenaza al control de Sigatoka Negra. En. Boletín Técnico de Cenibanano. No. 4; p. 5-2. [ Links ]
Ploper, L. D., Backman, P. A. and Rodriguez-Kabana, R.. 1992. Enhanced natural biological control of apple fruit diseases by applications of biopolymers. En: Biological Control Tests. Vol 7; p. 3. [ Links ]
Ruíz-Silvera, C., Bustamante, E., Jiménez, F., Saunders, J., Okumoto, S. y González, R. 1997. Sustratos y bacterias antagonistas para el manejo de Mycosphaerella fijiensis en banano. En: Manejo Integrado de Plagas (Costa Rica). No. 45; p. 9-17. [ Links ]
Sahai, A. S. and Manocha, M. S. 1993. Chitinases of fungi and plants: their involvement in morphogenesis and hostparasite interaction. En: FEMS Microbiology Reviews. Vol. 11, no. 4; p. 317-338. [ Links ]
Salazar, L. M. 2005. Estudio de la filosfera de musáceas alimenticias en el Urabá antioqueño. Medellín. 103 h. Tesis Magíster en Biotecnología. Universidad Nacional de Colombia. Facultad de Ciencias. [ Links ]
Sid Ahmed, A., Ezziyyani, M., Pérez Sánchez, C. and Candela, M. E. 2003. Effect of chitin on biological control activity of Bacillus spp. and Trichoderma harzianum against root rot disease in pepper (Capsicum annuum) plants. En: European Journal of Plant Pathology. Vol. 109; p. 633637. [ Links ]
Sing, P. P., Shin, Y. C., Park, C. S. and Chung, Y. R. 1999. Biological control of Fusarium wilt of cucumber by chitinolytic bacteria. En: Phytophatology. Vol 89, no.1; p. 92-99. [ Links ]
Spurr, H. W. 1981. Experiments on foliar disease control using bacterial antagonists. En: Blakeman, J. P., ed. Microbial ecology of the phylloplane. London Academic Press. p. 369-381. [ Links ]
Stadler, B., and T. Mueller. 1996. Aphid honeydew and its effect on the phyllosphere microflora of Picea abies (L.) Karst. En: Oecologia. Vol 108, no. 44; p. 771776. [ Links ]
Talavera, S. M. E., Bustamante, E., González, R. y Sánchez, V. 1998. Selección y evaluación en laboratorio y campo de microorganismos glucanolíticos antagonistas a Mycosphaerella fijiensis. En: Manejo Integrado de Plagas (Costa Rica). No. 47; p. 2430. [ Links ]
Valois, D.; Fayad, K.; Barasubiye, T.; Garon, M.; Dery, C.; Brzezinski, R. and Beaulieu, C. 1996. Glucanolytic actinomycetes antagonistic to Phytophtora fragariae var. rubi, the agent causal of raspberry root rot. En: Applied and Environmental Microbiology. Vol 62, no. 5; p. 1630-1635. [ Links ]
Wilson, M., and Lindow, S. E. 1994. Ecological similarity and coexistence of epiphytic icenucleating (Ice+) Pseudomonas syringae strains and a nonicenucleating (Ice-) biological control agent. En: Applied and Environmental Microbiology. Vol. 60; p. 31283137. [ Links ]
________ and S. E. Lindow. 1995. Enhanced epiphytic coexistence of nearisogenic salicylate-catabolizing and non-salicylate-catabolizing Pseudomonas putida strains after exogenous salicylate application. En: Applied and Environmental Microbiology. Vol 61; p. 10731076. [ Links ]
Wilson, M., Savka, M. A. Hwang, I. Farrand, S. K. and Lindow, S. E. 1995. Altered epiphytic colonization of mannityl opine producing transgenic tobacco plants by a mannityl opinecatabolizing strain of Pseudomonas syringae. En: Applied and Environmental Microbiology. Vol 61; p. 21512158. [ Links ]
Yamada, M. and Ogiso, M. 1997. Control of soilborne diseases using antagonistic microorganisms. Part IV. Study on the available substrates for antagonistic bacterial strains to control Fusarium wilt of tomatoes. En: Research Bulletin of the Aichiken Agricultural Research Center No. 29; p. 141144. [ Links ]
Zhang, Z. and Yuen, G. Y. 2000. Effects of culture fluids and preinduction of chitinase production on biocontrol of Bipolaris leaf spot by Stenotrophomonas maltophilia C3. En: Biological Control. Vol 18; p. 277-286. [ Links ] ]]>