 MATERIALES Y MÉTODOS
MATERIALES Y MÉTODOS  RESULTADOS Y DISCUSION
RESULTADOS Y DISCUSION  CONCLUSIONES ]]>
CONCLUSIONES ]]>
 BIBLIOGRAFÍA
BIBLIOGRAFÍAMULTIPLICACIÓN Y TUBERIZACIÓN in vitro DE ÑAME (Dioscorea alata L.) EN SISTEMA DE INMERSIÓN TEMPORAL
MULTIPLICATION AND in vitro TUBERIZATION OF YAM (Dioscorea alata L.) IN TEMPORARY IMMERSION SYSTEM
Robinson Salazar Díaz1 y Rodrigo Alberto Hoyos Sánchez2
1 Profesor Ciencias Naturales y Educación Ambiental. Institución Educativa Héctor Abad Gómez. Calle 50 Nº 39-65. Medellín, Colombia <conjuro_ g@yahoo.com> <rsalaza@unalmed.edu.co>
2 Profesor Asociado. Universidad Nacional de Colombia, Sede Medellín. Facultad de Ciencias Agropecuarias. A.A. 1779. Medellín, Colombia. <rhoyos@unalmed.edu.co>
Recibido: Mayo 5 de 2007, aprobado: Agosto 14 de 2007.
]]>RESUMEN
Se realizó la estandarización de la multiplicación y tuberización in vitro de ñame (Dioscorea alata L.) utilizando el sistema de inmersión temporal conocido como RITA®. Se evaluó inicialmente el porcentaje de brotación de segmentos nodales en medio de cultivo semisólido utilizando dos tipos de citoquininas (BAP y Kinetina). Las plantas obtenidas fueron subcultivadas cada cuatro semanas y luego utilizadas para la obtención de meristemos y plántulas para llevar a cabo los diferentes experimentos en sistema de inmersión temporal. Se obtuvo un mayor porcentaje de explantes brotados al utilizar Kinetina. Con el sistema RITA® se evaluó el efecto de la densidad de explantes sobre la tasa de multiplicación y sobre la inducción, formación y desarrollo de microtubérculos, no encontrándose diferencias estadísticamente significativas entre las densidades evaluadas. De igual manera, se evaluó el efecto de diferentes frecuencias y tiempos de inmersión sobre la tasa de multiplicación, encontrándose que a una frecuencia de inmersión cada 12 horas y durante 10 minutos se obtenía la formación de mayor número de nudos y mayor tamaño de las plantas a las cuatro semanas de cultivo. Al utilizar el sistema de inmersión temporal se alcanzaron mayores tasas de multiplicación y tuberización in vitro comparadas con el sistema de cultivo convencional. Demostrándose así, el potencial de estos sistemas para implementar un programa de producción de semillas de ñame.
Palabras claves: Dioscorea alata, sistemas de inmersión temporal, microtuberización, tiempo de inmersión, frecuencia de inmersión.
ABSTRACT
Multiplication rate and in vitro tuberización of yam (Dioscorea alata L.) was made using the temporary immersion system RITA®. Shoot percentage of nodal segments was initially evaluated in semisolid medium using two cytokinin types ((BAP and Kinetin). The obtained plants were subcultured every four weeks and then used to obtain meristems and plantlets to carry out different experiments in temporary immersion system. A higher sprouted explants percentage was obtained when using Kinetin. With the system RITA® the effect of explants density was evaluated on the multiplication rate and on the induction, formation and microtubers development, not find statistically significant differences among the evaluated densities. On the same way, the effect of different frequencies and immersion times on the multiplication rate were evaluated, finding that to an immersion frequency every 12 hours and during 10 minutes the formation of more number of knots and higher size of plants was obtained to four weeks of culture. When using temporary immersion system higher multiplication and in vitro tuberization rates were reached compared with the conventional culture system. This fact demonstrated the potential of these systems to implement a program of yam seeds production.
Key words: Dioscorea alata, temporary immersion systems, micro-tubing, immersion time, immersion frequency.
 MATERIALES Y MÉTODOS
MATERIALES Y MÉTODOS
 RESULTADOS Y DISCUSION
RESULTADOS Y DISCUSION
 CONCLUSIONES ]]>
CONCLUSIONES ]]>
 BIBLIOGRAFÍA
BIBLIOGRAFÍA
Con el fin de establecer o implementar los procesos de propagación vegetal más simples y de un mejor costo-beneficio, se han diseñado diferentes sistemas semi-automatizados (biorreactores), los cuales han dado un éxito regular en los diferentes cultivos en los cuales se han aplicado. Los medios líquidos ofrecen condiciones más homogéneas haciendo los nutrientes más accesibles al tejido. Además, se elimina el agente gelificante, que es uno de los insumos utilizados más costosos. En los últimos años se ha comenzado a implementar un nuevo tipo de biorreactor en el cual el tejido vegetal es sumergido en el medio líquido por cortos períodos de tiempo (Etienne y Berthouly, 2002). Este sistema conocido como RITA® (récipient á immersion temporaire automatique) ha producido rendimientos substanciales en producción y calidad en varias especies cultivadas, como café, rábano, banano, palma de aceite, cítricos, aumentando los niveles de mecanización de algunas etapas de la micropropagación, lo cual ha implicado una reducción en los costos de producción, coeficientes de multiplicación incrementados, mejor porcentaje de enraizamiento y supervivencia de las plantas en la etapa de aclimatización, comparada con la micropropagación convencional (Alvard, Cote y Teisson, 1993). El establecimiento de una metodología para multiplicación y tuberización in vitro de cultivo de ñame, tiene un gran impacto en diferentes áreas como producción de plantas libres de virus o promoción de la producción de este cultivo particularmente el área de producción de semilla de alta calidad y conservación de germoplasma. Estos tópicos hacen relevante profundizar en los estudios sobre el cultivo de ñame y así lograr un manejo adecuado y optimizar su rendimiento. El objetivo principal de esta investigación fue evaluar un sistema eficiente de micropropación y tuberización in vitro de ñame (Discorea alata L.) variedad Pico de Botella, basado en el sistema de inmersión temporal, evaluando el efecto de este sistema sobre la calidad de las plantas y el tamaño y peso de microtubérculos, durante las fases de multiplicación y tuberización in vitro.
Material vegetal. Tubérculos de ñame provenientes de selecciones en campo de plantas sin aparente sintomatología viral, se lavaron con detergente y se enjuagaron con abundante agua destilada estéril, se cortaron en trozos de 100,0 g aproximadamente y luego se colocaron en solución del funguicida Benomil a una concentración de 2,0 g · L durante media hora, finalmente se sembraron en suelo envuelto en bolsas de polietileno y se llevaron a invernadero. El material sembrado se regó mensualmente con una solución nutritiva compuesta de 4,0 g · L de sulfato de amonio, 2,0 mg · L de cloruro de potasio y 0,5 ml · L de ácido fosfórico.
Micropropagación
Establecimiento in vitro de segmentos nodales. De las plantas obtenidas de los tubérculos sembrados en vivero, se tomaron segmentos nodales de 2,0 cm aproximadamente. Las plantas tenían de 8 10 semanas de cultivo. A los segmentos nodales se les hizo tratamientos de desinfección, los cuales consistieron en un lavado con detergente (una gota de Tween 20/100 mL de agua corriente), luego se enjuagaron 3 veces con abundante agua. Seguidamente y dentro de la cabina de flujo laminar se dejaron 30 segundos en alcohol al 70%, luego se enjuagaron 3 veces con agua destilada estéril, después se les adicionó peróxido de hidrógeno al 2% durante dos minutos, se enjuagaron tres veces con agua destilada estéril, y finalmente se adicionó hipoclorito de sodio al 2% durante 10 minutos, pasado este tiempo, se enjuagaron tres veces con agua destilada estéril.
Los segmentos nodales se cortaron a una longitud de aproximadamente 0,5 cm, y se establecieron en el medio de cultivo MS (Murashige and Skoog 1962), suplementado con 30,0 g · L de sacarosa,0,1 mg · L de tiamina HCl y 100.0 mg · L de mioinositol, 20,0 mg · L de cisteina y 1,8 g · L de phytagel, pH 5,7 - 5,8. El medio de cultivo fue esterilizado previamente en autoclave a 121°C, 15 kg · cm2 por 20 minutos. Se utilizaron frascos de cultivo de 120,0 mL en los cuales se adicionaron 20,0 mL de medio de cultivo por frasco, estos se sellaron con papel aluminio y Vinilpelâ. Finalmente los explantes se llevaron al cuarto de incubación a una temperatura de 28±2°C bajo un fotoperiodo de 12 horas y una intensidad lumínica de aproximadamente 1200 1500 lux.
Con base en estudios preliminares, se evaluaron dos tipos de regulador de crecimiento (0, mg · L de Kinetina y 0, mg · L de BAP), a los 30 días de cultivo se evaluó el número y porcentaje de explantes brotados. Se utilizó un diseño completamente al azar con 50 repeticiones por tratamiento T1 (0, mg · L de Kinetina) y T2 (0, mg · L de BAP), utilizando un segmento nodal como unidad experimental.
]]> De acuerdo a los resultados del experimento anterior y luego del análisis estadístico donde se determinó el mayor porcentaje de explantes brotados y mejor respuesta de los brotes, se introdujo nuevo material vegetal, que luego de la brotación en el mejor tratamiento obtenido, fue pasado a un medio de multiplicación consistente de 30 g · L de sacarosa, 0,1 mg · L de tiamina, 20.0 mg · L de cisteína, 100.0 mg · L de mioinositol, 0,5 g · L de carbón activado, 4,0 mg · L de BAP, 0,5 mg · L de ANA y 1,8 g · L de Phytagel, pH 5,7-5,8 medio de multiplicación de ñame (MMÑ) para así contar con material suficiente para los diferentes ensayos a evaluar incluyendo la obtención de meristemos.Cultivo de meristemos. Se tomaron explantes procedentes del experimento anterior y se establecieron en un medio de cultivo para multiplicación MMÑ. El medio de cultivo se esterilizó bajo las ya descritas. Este material se incubó a una temperatura de 28± 2°C bajo un fotoperíodo de 12 horas luz y una intensidad lumínica de aproximadamente 1200-1500 lux durante 30 días. A partir de segmentos nodales de plantas desarrolladas in vitro se extrajeron meristemos ( 0,5 cm. aprox.) Se escindieron utilizando un estereomicroscopio, la disección se llevó a cabo en cabina de flujo laminar estéril.
Medios de cultivo. Para la evaluación del crecimiento y diferenciación de los meristemos se realizaron observaciones preliminares utilizando los medios de cultivo para ñame detallados por Mantell y Hugo (1989) y Perea y Buitrago (2000), Estos protocolos fueron modificados para esta investigación evaluándose seis (6) diferentes medios de cultivo, así: M1: ANA 0,5 mg/L + BAP 0,2 mg · L +GA3 0,5 mg · L, M2: ANA 0,25 mg · L + BAP 0,1 mg · L +GA3 0,05 mg · L, M3: ANA 0,2 mg · L + BAP 0,12 mg · L +GA3 0,08 mg · L, M4: ANA 0,75 mg · L + BAP 0,15 mg · L, M5: ANA 0,75 mg · L + BAP 0,15 mg · L + GA3 0,1 mg · L, M6: GA3 0,1 mg · L), suplementados con sales básicas MS, 30,0 g · L de sacarosa, 0,1 mg · L de tiamina, 20,0 mg · L de cisteína, 100,0 mg · L de mioinositol, 0,5 g · L de carbón activado, 80,0 mg · L de sulfato de adenina, 1,8 g · L de Phytagel, pH 5,7-5,8. Cada uno, tuvo 10 repeticiones. Para la evaluación del desarrollo de los meristemos se tuvieron en cuenta dos aspectos: crecimiento y desarrollo directo (desarrollo de plántulas a partir del meristemo) e indirecto (desarrollo de plántulas a partir de callos formados del meristemo inicial).
Las plantas regeneradas a partir de meristemos se propagaron en medio de multiplicación para ñame (MMÑ). Las vitroplantas obtenidas, se evaluaron para determinar si presentaban la sintomatología viral típica en ñame caracterizadas por manchas cloróticas, bandeo o moteado, finalmente se seleccionaron plantas para ser aclimatadas y evaluar sintomatología viral.
Efecto de la densidad de explantes sobre la tasa de multiplicación en el sistema RITAâ. Luego de la fase de establecimiento de 30 días en medio sólido se utilizaron segmentos nodales de aproximadamente 0,5 cm de longitud, para la evaluación de multiplicación masiva en RITAâ de 1 litro con un volumen de medio de 200 mL y en medio semisólido. Las unidades experimentales (10) fueron distribuidas utilizando diseño completamente al azar con tres repeticiones, el factor a evaluar fue la densidad de explantes (5,10 y 15 segmentos nodales por recipiente de cultivo), para un total de tres tratamientos. Se preparó el medio de cultivo para multiplicación de ñame (MMÑ) antes mencionado. La frecuencia de inmersión fue establecida para cada 8 horas con un tiempo de inmersión de 10 minutos teniendo en cuenta evaluaciones preliminares. Este material fue incubado a una temperatura de 22- 24°C bajo un fotoperiodo de 12 horas luz y una intensidad lumínica de aproximadamente 1.200-1.500 lux.
A los 30 días se evaluó el coeficiente de multiplicación, expresado como el número de explantes originados del tejido empleado inicialmente.
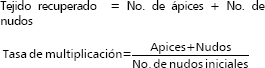
Optimización del tiempo y la frecuencia de inmersión en el sistema RITAâ . Se empleó un arreglo factorial en un diseño completamente al azar con tres repeticiones, evaluando los siguientes factores: tiempo de inmersión (5 y 10 min) y frecuencia de inmersión (8 y 12 h) para un total de cuatro (4) tratamientos por un período de 4 semanas. El medio de cultivo utilizado fue el MMÑ. La incubación se hizo a una temperatura de 22- 24°C bajo un fotoperíodo de 12 horas luz y una intensidad lumínica de aproximadamente 1200-1500 lux.
El volumen total de medio de cultivo fue de 200 mL y el número de explantes utilizado fue el encontrado como óptimo en la evaluación del experimento anterior (10 explantes). Se evaluó el coeficiente de multiplicación.
Para evaluar la eficiencia relativa del sistema de cultivo convencional (medio semisólido MMÑ) sobre la tasa de multiplicación se sembraron a partir de segmentos nodales de ñame de aproximadamente 0,5 cm. Se realizó el seguimiento a 5, 10 y 15 explantes a partir de tres repeticiones por tratamiento. A las cuatro semanas se evaluó el coeficiente de multiplicación. Los datos generados fueron comparados con los obtenidos en el sistema RITA®.
]]> MicrotuberizaciónEfecto del número de explantes sobre la producción de microtubérculos en sistema RITAÒ. Se evaluaron dos densidades (10 y 15 explantes) en inmersiones de 10 minutos cada 8 horas en frascos RITAÒ de 1 L con un volumen de MMÑ de 200 mL. Los explantes se dejaron en este medio de cultivo durante 30 días, pasado este tiempo el medio de cultivo fue cambiado por el medio de tuberización compuesto por macrosales de White y microsales de Heller (Mantell and Hugo, 1989) suplementado con 0,1 mg · L de tiamina, 20 mg · L de cisteína, 100 mg · L de mioinositol,0,5 g · L de carbón activado, 60 g · L de sacarosa, 1,0 mM de ABA (Salazar y Beltrán, 2002).
La incubación se hizo a una temperatura de 22- 24°C bajo un fotoperíodo de 12 horas luz y una intensidad lumínica de aproximadamente 1200-1500 lux. Se utilizó un diseño completamente al azar con cuatro repeticiones por tratamiento. La calidad de microtubérculos obtenidos fue determinada por medición de la longitud y diámetro de los microtubérculos, número de microtubérculos por planta y el peso fresco promedio y biomasa total de los microtubérculos obtenidos.
Para la evaluación de la microtuberización en medio de cultivo semisólido, se utilizó un segmento nodal de 0,5 cm. por frasco de cultivo, provenientes de plántulas desarrolladas in vitro. Los explantes se incubaron bajo un fotoperiodo de 12 horas luz y para su crecimiento se empleó el MMÑ adicionando 1,8 g · L de Phytagel, como fase de inducción de crecimiento (30 días) previo a la incubación bajo las condiciones de tuberización. Para la evaluación de la microtuberización se utilizaron las plántulas establecidas in vitro las cuales se incubaron bajo las siguientes condiciones de cultivo ( 60 g · L de sacarosa, 1,0 mM de ABA (Salazar y Beltrán, 2002). La incubación se realizó bajo un fotoperiodo de 12 horas luz y una temperatura de 29- 31°C). Se utilizaron 10 y 15 vitroplantas como control, se evaluaron cuatro repeticiones por tratamiento.
Los microtubérculos cosechados fueron pesados, medidos el largo y ancho (diámetro) y luego se almacenaron en cajas de Petri con papel absorbente húmedo.
Los recipientes RITAâ utilizados en los diferentes experimentos tenían una capacidad de 1,0 L, se adicionaron 200,0 mL de medio de cultivo líquido a cada uno, el soporte inerte sobre el cual se colocaron los explantes, fue reemplazado por un círculo de malla de polisombra.
Análisis estadístico. Se utilizó un diseño completamente al azar con estructura de los tratamientos unifactorial con el factor densidad de explantes, tanto para multiplicación como para tuberización en sistema RITAÒ, para la evaluación del efecto del tiempo y frecuencia de inmersión sobre la tasa de multiplicación en RITAÒ se utilizó un diseño completamente al azar con estructura de los tratamientos multifactorial (2 x 2).
Para el análisis de los datos experimentales se utilizó el sofware SASÒ versión 8,2. El supuesto de normalidad se evaluó con la prueba Shapiro-Wilk (W) usando el PROC UNIVARIATE. La separación de medias se realizó mediante la prueba de Duncan. Para la digitalización de los datos y construcción de los gráficos se empleó el programa EXCEL XPÒ. Todas las pruebas se trabajaron con un nivel de confianza del 95%.
]]> Micropropagación
Establecimiento in vitro de segmentos nodales. El protocolo de desinfección fue efectivo debido a que los segmentos nodales sembrados no presentaron contaminación. Se hizo evaluación semanal para determinar el tiempo de brotación de los explantes, teniendo en cuenta que en trabajos preliminares se había observado brotación a la semana de iniciados los explantes. Se encontró que los explantes en medio de cultivo con kinetina presentaron un 60% de brotación a los 6 días de sembrados, mientras que los nudos sembrados en medio con BAP no presentaron brotación. Sin embargo, 20 días más tarde los explantes en medio de cultivo con BAP (0,5 mg · L) presentaron una brotación del 70% y los establecidos en medio con kinetina (0,5 mg · L) permanecieron igual. Al comparar la apariencia de los explantes provenientes de los dos medios de cultivos se encontró que los explantes brotados en medio de cultivo con kinetina presentaron además de menor tiempo de brotación, mayor tamaño que los iniciados en BAP, encontrándose, entonces, que para la iniciación y brotación de explantes de ñame es recomendable utilizar 0,5 mg · L de kinetina.
Estos resultados coinciden con los de Cabrera et al. (2003) quienes encontraron resultados favorables al utilizar 0,5 mg · L de kinetina después de 45 días de cultivo, resultados similares fueron obtenidos por Ng (1992), quien estudió el efecto de tres tipos de citoquininas en la multiplicación de segmentos nodales de ñame blanco, encontrando a las seis semanas de cultivo mayor número de brotes al utilizar Kinetina como regulador de crecimiento. Lo anterior indica el papel que juegan las citoquininas en relación con el genotipo utilizado y especialmente el tipo de citoquinina en el proceso de inducción de multiplicación axilar según lo descrito por Bancroft y Mcdonald (1998).
Es importante resaltar que en las condiciones en las que se hizo esta investigación se logró acortar los periodos de subcultivo con respecto a los tiempos mencionados por Cabrera et al. (2003), 45 días y Ng (1992), 42 días. El tiempo de subcultivo logrado en este trabajo fue de 20 días para obtener el número de plantas necesarias en los diferentes experimentos.
Cultivo de meristemos. Los meristemos (menores de 0,5 mm aprox.) de plantasin vitro no presentaron ningún tipo de contaminación (hongos o bacterias), contrario a lo ocurrido cuando se obtenían meristemos de plantas de invernadero. Además, las plantas provenientes de los meristemos obtenidos de plantas in vitro no presentaron ningún tipo de sintomatología viral. En la evaluación solo se presentaron diferencias altamente significativas entre los medios evaluados para el porcentaje de formación y desarrollo de plántulas (crecimiento directo), encontrándose que el M6 (0,1 mg · L GA3) presentó el mayor promedio de crecimiento y desarrollo de los meristemos. También, se presentó un porcentaje de 0,1 a 0,3% de plántulas formadas a partir de callos (crecimiento indirecto). El porcentaje de formación de callos fue de 0,1 a 0,4%, como se puede observar en la Figura 1.
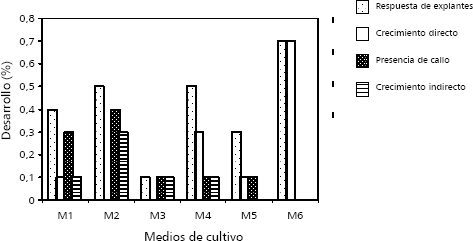
Figura 1. Efecto de diferentes medios de cultivo sobre el desarrollo de meristemos en ñame.
En el caso del crecimiento y desarrollo directo, después de 15 días se comenzó a observar el crecimiento de las plántulas, esto se logró utilizando el medio de cultivo MS suplementado con 0,1 mg/L de GA3, (M6). Perea (2000), informa sobre un crecimiento y desarrollo de meristemos de ñame a los 20 días utilizando 0,08 mg/L de GA3..
Las plantas obtenidas a partir de meristemos se aclimataron y evaluaron, no se observó ningún tipo de sintomatología viral como: manchas cloróticas, bandeo o moteado, indicando que el material y procedimiento utilizado podrían ser adecuados pero no definitivos para obtener el material vegetal con estas características (Figura 2).
 ]]>
Figura 2. Plántula de ñame de dos meses de edad y sin sintomatología viral obtenida a partir de meristemos.
]]>
Figura 2. Plántula de ñame de dos meses de edad y sin sintomatología viral obtenida a partir de meristemos.
Efecto de la densidad de explantes sobre la tasa de multiplicación en el sistema RITAâ. No se evidenciaron diferencias estadísticamente significativas entre las densidades evaluadas, por lo cual se recurre a un análisis descriptivo de los resultados que permitan explicar este comportamiento. Los resultados también podrían explicarse por la frecuencia y tiempo de inmersión utilizados que podrían no haber sido los más adecuados para el desarrollo de las plantas, teniendo en cuenta que estos son factores críticos para una alta eficiencia biológica como lo indican Etienne y Berthouly (2002). Por lo anterior y partiendo de una densidad determinada se recurre entonces a evaluar tiempos y frecuencias de inmersión óptimos para el desarrollo de los explantes.
La tasa de multiplicación promedio más alta encontrada fue de 7,13 y se obtiene al emplear una densidad de 10 explantes. Aunque no hubo diferencias significativas en los tratamientos evaluados, 10 explantes son una buena alternativa para una correcta utilización de los vasos RITA® (Figura 3). Una densidad de siembra de cinco explantes sería inadecuada porque se subutilizarían los frascos de cultivo y se ocasionaría pérdida de medio de cultivo, por otro lado, si se opta por la siembra de 15 explantes/frasco se podría generar un crecimiento limitado de los brotes y una baja en su proliferación.
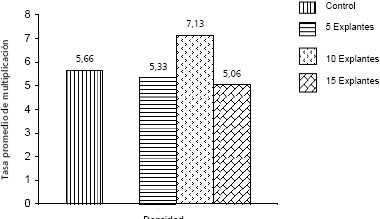
Figura 3. Efecto de la densidad de explantes sobre la tasa de multiplicación de ñame.
Etienne y Berthouly (2002), destacan a la densidad como un factor determiminante en un protocolo de micropropagación, pero que ha sido poco estudiado en sistemas de inmersión, en este trabajo se pudo observar que a medida que se incrementaba o disminuía el número de explantes, la tasa de multiplicación disminuía con relación a la encontrada cuando se emplearon 10 explantes por recipiente. Cabrera et al. (2003), informan sobre una tasa de multiplicación de 8,6 al emplear 10 explantes de ñame por recipiente de cultivo, similares resultados son encontrados en yuca por Basail 2001, al usar 10 explantes por frasco de cultivo, estableciéndose con esta densidad, la tasa de multiplicación es mayor al compararla con la obtenida al utilizar el medio de cultivo semisólido. Por otra parte, Roels et al. (2005), no encontraron diferencias significativas entre frecuencias y tiempos de inmersión para las tasas de multiplicación dentro de los rangos evaluados.
Optimización del tiempo y la frecuencia de inmersión en el sistema RITAâ. No se encontraron diferencias significativas entre las frecuencias y la interacción tiempo de inmersión y frecuencia de inmersión. Sin embargo, si se encontraron diferencias estadísticamente significativas entre los tiempos de inmersión al que fueron sometidos los explantes (Tabla 1).
Tabla 1. Efecto de los tiempos y frecuencia de inmersión sobre la tasa promedio de multiplicación en explantes de ñame en el sistema RITAâ.

Cuando se realiza el análisis estadístico para el tiempo de inmersión se encuentra que a 5 minutos la tasa de multiplicación es de 5,7 y a 10 minutos es de 9,75, evidenciando diferencias estadísticas entre los niveles de este factor. Las tasas de multiplicación promedio encontradas a 5 y 10 minutos de inmersión, fueron mayores que las obtenidas en el medio de cultivo semisólido (Control).
]]> Teniendo en cuenta los resultados anteriores, se ven reflejadas las ventajas del sistema RITAâ que permite aumentar las tasas de multiplicación en relación con el método de cultivo convencional. Los ciclos de inmersión varían considerablemente dependiendo de la especie evaluada e incluso de la clase de tejido utilizado y del tipo de sistema de cultivo empleado, Al respecto, Akita y Takayama (1994), aprovecharon periodos de inmersión cortos (1 min.) para estimular la producción de embriones en café, la misma técnica ha sido evaluada en banano y plátanos por Escalona et al. (1999), mientras que periodos largos de inmersión (1 h cada 6 h), han sido efectivos para tuberización en papa (Ethiene y Berthouly, 2002).Los efectos de los tiempos de inmersión en la respuesta morfogenética de los tejidos pueden estar relacionados con las relaciones hídricas, el intercambio gaseoso y el incremento de la toma de nutrientes que se logra en esta forma de cultivo (Escalona et al. 1999), aspectos que de alguna forma favorecen el crecimiento y desarrollo del material vegetal. Se puede encontrar que el tamaño y vigorosidad de las vitroplantas se vea favorecido por el medio de cultivo líquido, además, de encontrar mayor número de ápices y entrenudos por plantas como lo plantean Jiménez et al. (1999) (Figura 4).
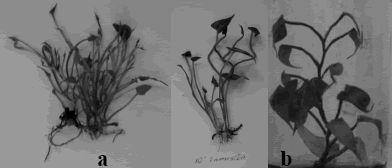
Figura 4. Vitroplantas de ñame a los 30 días de cultivo. a) en vasos RITA®. b) medio de cultivo semisólido.
Los resultados obtenidos al utilizar inmersión temporal se relacionan con la forma de empleo del medio de cultivo líquido. Debido a que éste combina las ventajas de inmersión constante con las de inmersión parcial con un soporte inerte, evitándose así hiperhidricidad y falta de oxígeno por inmersión constante (Alvard, Cote y Teisson, 1993).
Castro y González (2001), indican que el intercambio gaseoso proporciona una mejor asimilación de los nutrientes, adicionalmente, se da una mejor difusión de sustancias y disminución de la humedad relativa, aspectos que reducen la condición de estrés, obteniéndose así tasas de multiplicación más altas y vitroplantas de mejor calidad. Es importante anotar que en ninguno de los experimentos realizados, se encontró material vegetal con síntomas de hiperhidricidad. La superficie del material vegetal en este sistema está en contacto uniforme con los nutrientes del medio del cultivo, aún cuando no está sumergido, ya que el medio de cultivo queda sobre los explantes adherido, formando una película que no inhibe el intercambio gaseoso y es renovada su composición química en cada inmersión (Cabasson et al.1997).
Los siguientes son algunos de los coeficientes de multiplicación establecidos en diferentes trabajos donde se ha utilizado el sistema de inmersión temporal, lo que demuestra la eficiencia del sistema con relación al convencional en medio semisólido.
Castro et al. (1999), encontraron 10,5 brotes a las 6 semanas de cultivo en eucalipto, Montoya (2006), 7,25 brotes en 100 días en papa, Medero et al. (1997), 6,6 brotes en malanga, Teisson et al. (1996), 5,2 brotes en musa.
Microtuberización
Efecto del número de explantes sobre la producción de microtubérculos en sistema RITAÒ. No se presentaron diferencias estadísticamente significativas entre las densidades evaluadas para cada una de las variables, por lo cual se hace un análisis descriptivo con base en el promedio y la desviación estándar de cada tratamiento en cada variable. Se encontró, una variabilidad alta entre los tratamientos, en tanto que la formación y desarrollo de microtubérculos, se llevó a cabo en ambas densidades evaluadas (10 y 15 explantes). Otros valores de interés fueron: mayor número de explantes que tuberizó 0,62, número promedio de microtubérculos por explante 0,85, longitud promedio 9,52 mm, diámetro promedio 3,91 mm y peso fresco promedio total 0,2421 g. También se encontró a una densidad de 10 explantes por vaso RITA® a las 12 semanas de cultivo (Figura 5).
]]>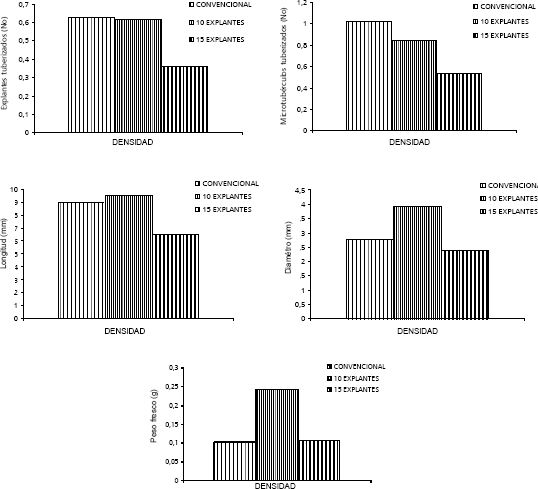
Según Forti Mandolino y Ranalli (1991), a bajas densidades de cultivo el peso de los microtubérculos formados in vitro se incrementa, mientras que a densidades altas la competencia por nutrientes es mayor y por consiguiente el peso de los microtubérculos es menor. Jiménez et al. (1999), explican que al haber mayor asimilación de nutrientes por haber mayor contacto explante medio de cultivo, el tamaño y peso de los microtubérculos es mayor que en medio sólido. Los mismos autores encontraron mayor producción de microtubérculos de papa al utilizar sistemas de inmersión temporal, al igual que lo determinado por Cabrera et al. (2005).
Se demuestra que se forman microtubérculos de mayor tamaño, diámetro y peso con relación a los obtenidos en medio de cultivo semisólido (Figura 6). Estos resultados concuerdan con los obtenidos por Jiménez et al. (1999) en papa y para Cabrera et al. (2003) en ñame, quienes explican que el mayor contacto del medio de cultivo con las yemas de las vitroplantas, favorece la inducción y formación de microtubérculos. Obtener microtubérculos de mayor peso y tamaño permite aprovechar mejor las ventajas de éstos, porque pueden ser almacenados o llevados a campo directamente sin un proceso de aclimatación previa (Mantell y Hugo 1989).
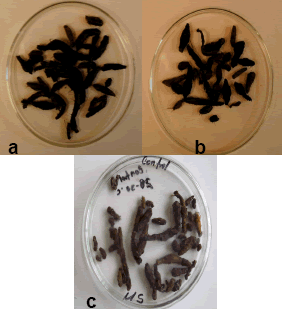
Figura 6. Efecto de la densidad sobre la inducción, formación y desarrollo de microtubérculos en ñame en el sistema RITA®. a) Microtubérculos obtenidos a una densidad de 10 explantes. b) Microtubérculos obtenidos a una densidad de 15 explantes. c) Control en medio de cultivo semisólido. Fotoperíodo de 12 horas luz y temperatura de 28- 30 °C.
En el sistema RITA® no se presentan diferencias entre las densidades evaluadas para la tasa de multiplicación y la inducción, formación y desarrollo de microtubérculos de ñame.
El tiempo de inmersión donde se producen las mejores tasas promedio de multiplicación de microtubérculos de ñame (9,75) fue el de una duración de 10 minutos de inmersión.
]]> El uso del sistema de inmersión temporal con los vasos RITA® permite lograr una mayor eficiencia biológica, traducida en la obtención de mejores tasas de multiplicación y tuberización en ñame, comparadas con el método convencional. Se destaca así el potencial del sistema para implementar un programa de producción de semillas de la especia.Con el incremento del conocimiento de los factores que afectan la tuberización en sistemas de inmersión temporal, tanto para la inducción como para la acumulación de peso, se permitirá que las técnicas de producción de microtubérculos tengan mayor aplicabilidad.
Akita, M. and S. Takayama. 1994. Stimulation of potato (Solanum tuberosum L.) tuberization by semicontinuos liquid medium surface level control. Plant Cell Rpt. 13(3):184-187. [ Links ]
Alvard, D. F. Cote and C. Teisson. 1993. Comparison of methods of liquid medium culture for banana micropropagation: effects of temporary immersion of explants. Plant Cell Tissue Org. Cult. 32(1):55-60. [ Links ]
Basail, M. 2001. Propagación de la yuca (Manihot esculenta, Crantz), en sistemas de inmersión temporal. Trabajo de grado Ingeniero Agrónomo. Facultad de Ciencias Agropecuarias. Universidad Central de las Villas Marta Abreu, Santa Clara, Cuba. 80 p. [ Links ]
Cabasson, C., D. Alvard, D. Dambie, and C. Teisson. 1997. Improvement of citrus somatic embryo development by temporary immersion. Plant Cell Tissue Org. Cult. 50(1):33-37. [ Links ]
Cabrera, J.M., K.R. Gómez, P.M. Basail, N.Y. Torres, J.A. Robaina, P.A. Santos, V. Medero, C.A. Rayas, T.J. López, G.M. García, J. Ventura, y M.O. Valdez. 2005. Multiplicación en sistemas de inmersión temporal de segmentos nodales de (Dioscorea alata L.). p. 81. En: Resúmenes Taller Internacional sobre Biotecnología Vegetal y Agricultura Sostenible. 2005. Bioveg Centro de Bioplantas, Ciego de Ávila, Cuba. [ Links ]
Cabrera, M., Y. Torres, A. Santos, M. Basail, A. Rayas, V. Medero, A. Robaina, J. López, G.M. García, J. Ventura, E. Espinosa, V. Gutiérrez, E. Otero, M. Berta, y M. Álvarez. 2003. Establecimiento y multiplicación in vitro del clon de ñame blanco de guinea (Dioscorea rotundata Poir). Instituto de Investigaciones en Viandas Tropicales, INIVIT, Villa Clara, Cuba. 7 p.www.agronet.uclu.edu.cu/eventos/agrocentro/ac2003/simposios/agronom/trabajos/a-89.doc [ Links ]
Castro, D.C. y J.l. González. 2001. Control de condiciones ambientales y medio de cultivo para la propagación de Eucalyptus grandis en el sistema de inmersión temporal. Actualidades Biolog. 23(75): 13-18. [ Links ]
Escalona, M., J. Lorenzo, B. González, M. Daquinta, C. Barroto, J. González, and Y. Desjardines. 1999. Pineapple (Ananas comosus Merr) micropropagation in temporary immersion systems. Plant Cell Rpt. 18(9):743-748. [ Links ]
Etienne, H. and M. Berthouly. 2002. Temporary immerssion systems in plant micropropagation. Plant Cell Tissue Org. Cult. 69(3): 215-231. [ Links ]
Forti, E., G. Mandolino and P. Ranalli. 1991. In vitro tuber induction: influence of the variety and of the media. Acta Hort. 300:127132. [ Links ]
Jiménez, E., N. Pérez, M. Feria, R. Barbón, A. Capote, M. Chavez, E. Quiala and J. Pérez. 1999. Improved production of potato microtubers using a temporary immersion system. Plant Cell Tissue Org. Cult. 59(1): 19-23. [ Links ]
Mantell, S. and S. Hugo. 1989. Effects of photoperiod, mineral medium strength, inorganic ammonium, sucrose and cytokinin on root, shoot and microtuber development in shoot cultures of Dioscorea alata L. and D. bulbifera L. yams. Plant Cell Tissue Org. Cult. 16(1):23-37. [ Links ]
Montoya, P.N. 2006. Tuberización in vitro de papa (Solanum tuberosum L). variedad Diacol Capiro en biorreactores de inmersión temporal y evaluación de su comportamiento en campo. Tesis de Maestría en Biotecnología. Facultad de Ciencias Agropecuarias. Universidad Católica de Oriente. Escuela de Formación Avanzada. Universidad Pontificia Bolivariana. Rionegro, Colombia. 66 p. [ Links ]
Ng, S.Y.C. 1992. Micropropagation of white yam (Dioscorea rotundata Poir). p. 135-159. En: Bajaj, Y.P.S. ed. Biotechnology in agriculture and forestry. Part III. High tech and micropropagation. v. 19. Springer-Verlag, Berlin, Germany . [ Links ]
Perea, D.M. y H.G. Buitrago. 2000. Aplicación de la biotecnología agrícola al cultivo de ñame. p. 17-19. En: Guzmán, M. y G. Buitrago (eds.). Ñame: producción de semillas por biotecnología. Universidad Nacional de Colombia Unibiblos, Bogotá, Colombia. [ Links ]
Roels, S., M. Escalona, J. Cejas, C. Noceda, R. Rodríguez, M.J. Canal, J. Sandoval and P. Deberg. 2005. Optimization of plantain (Musa AAB) micropropagation by temporary immersion system. Plant Cell Tissue Org. Cult. 82(1):57-66. [ Links ] ]]>