
STRATEGIES FOR THE IMPROVEMENT OF SECONDARY METABOLITES PRODUCTION IN PLAN CELL CULTURES
Mario Arias Zabala1; Mónica Juliana Angarita Velásquez2; Ana Maria Aguirre Cardona3; Juan Manuel Restrepo Flórez4 y Carolina Montoya Vallejo5
1 Profesor Asociado. Universidad Nacional de Colombia, Sede Medellín. Facultad de Ciencias. A.A. 3840. Medellín, Colombia. <marioari@unalmed.edu.co>
2 Investigadora. Universidad Nacional de Colombia, Sede Medellín. Facultad de Ciencias. A.A. 3840. Medellín, Colombia. <mjangari@unalmed.edu.co>
3 Estudiante Maestría en Biotecnología. Universidad Nacional de Colombia, Sede Medellín. Facultad de Ciencias. A.A. 3840. Medellín, Colombia. <amaguir@unalmed.edu.co>
4 Investigador. Universidad Nacional de Colombia, Sede Medellín. Facultad de Ciencias. A.A. 3840. Medellín, Colombia. <jmrestr1@unalmed.edu.co>
5 Investigadora. Universidad Nacional de Colombia, Sede Medellín. Facultad de Ciencias. A.A. 3840. Medellín, Colombia. <cmontoy0@unalmed.edu.co>
Recibido: Mayo 12 de 2008; Aceptado: Abril 15 de 2009
Resumen. El cultivo de células vegetales ha surgido como una alternativa para la obtención de metabolitos de alto valor agregado, producidos en las plantas en bajas concentraciones y para los cuales, no existen procesos de síntesis química conocidos; sin embargo, para la implementación de esta tecnología es necesario el desarrollo de estrategias que permitan incrementar la productividad de los cultivos in vitro. En este trabajo se discuten diferentes alternativas planteadas para lograr este objetivo: en la primera parte se presentan las formas para obtener líneas celulares sobreproductoras, abordando las estrategias clásicas de selección y la ingeniería genética; posteriormente se discuten los efectos que sobre el crecimiento y la producción de metabolitos secundarios pueden tener la composición química del medio de cultivo y las condiciones físicas en las que se conduce el proceso; finalmente, se presenta la elicitación como alternativa para inducir la síntesis de metabolitos secundarios en cultivos de células vegetales.
]]> Palabras claves: Producción de metabolitos secundarios, células vegetales, metabolismo secundario, cultivo in vitro, optimización de producción.Abstract. The strategy of plant cell culture has become an alternative for the production of high value metabolites that are normally produced in low levels in plants and for which there is not chemical synthesis processes known. However, for the implementation of this technology it is necessary to develop strategies that let us improve the productivity of the in vitro cultures. In this work, different alternatives in order to fulfill that objective are presented: in the first part, the strategies to obtain overproducer cell lines are discussed, showing the clasic strategies for cell line selection and genetic engineering as alternatives; after that, the efect over the growth and secondary metabolite productition of the chemical medium composition and physical conditions of the process are reviewed; finally, the elicitation is presented as an alternative to induce the synthesis of secondary metabolites in plant cell cultures.
Key words: Secondary metabolites production, plant cells, secondary metabolism, in vitro culture, production optimization
Por mucho tiempo los seres humanos han usado las plantas como fuente de fragancias, saborizantes y medicinas; usualmente estos compuestos cumplen un rol ecológico mediando la interacción de la planta con su ambiente, encontrándose generalmente en muy bajas concentraciones, por lo cual se hace necesario utilizar gran cantidad de material vegetal para obtener cantidades significativas del compuesto de interés (Foley y Moore, 2005).
Tradicionalmente el aprovechamiento de estos compuestos ha estado determinado por la capacidad de diseñar procesos de extracción efectivos para las moléculas de interés; sin embargo, durante la última mitad del siglo pasado surgió la alternativa del cultivo de células vegetales para obtener estas moléculas sin necesidad de utilizar la planta completa. La utilización de esta estrategia para la producción de metabolitos secundarios, requiere la determinación de las condiciones de producción óptimas, así como el empleo de metodologías como la ingeniería genética y/o la elicitación con el fin de incrementar la producción de los metabolitos de interés. Sin embargo, dificultades asociadas con el escalado, han hecho que la utilización comercial de esta tecnología esté aun limitada a unos pocos procesos (Tabla 1).
Tabla 1. Algunos metabolitos producidos industrialmente por cultivo de células vegetales

En este trabajo se presentan las principales estrategias empleadas para incrementar la producción de metabolitos secundarios en un cultivo in vitro de células vegetales, el material presentado recoge los resultados de investigaciones publicadas durante los últimos 10 años.
Estrategias para incrementar la producción de metabolitos secundarios.
Selección y mejoramiento de la línea celular. La primera estrategia para lograr una línea celular altamente productora de un metabolito es la selección adecuada de la fuente de explante; recomendándose el uso de una parte de la planta en donde normalmente se halla observado la acumulación del metabolito, pues se ha demostrado que líneas obtenidas de diferentes partes de la planta, presentan productividades diferentes de metabolitos secundarios (Oncina et al., 2000; Fedoreyev et al., 2000). Una vez establecido el cultivo in vitro se debe seleccionar la línea celular con base en su velocidad de crecimiento, niveles de producción y estabilidad (Dörnenburg y Knorr, 1995), subcultivando sólo aquellas que presentan la característica de interés (Qu et al. , 2006;Trejo, 2008).
]]> Ingenierías genética y metabólica. Las ingenierías genética y metabólica son estrategias efectivas para optimizar la producción de metabolitos secundarios; en la Tabla 2, se nota el importante efecto de aplicar este tipo de metodologías en la producción de ciertos metabolitos, logrando incrementos importantes en la producción como puede verse en el caso de la apigenina por Saussurea involucrata donde se logra un incremento del 542% (Dörnenburg y Knorr, 1995); el desarrollo de estas técnicas ha venido cobrando un papel cada vez mas importante en la producción de metabolitos secundarios y es de esperarse una creciente aplicación de las mismas. Las estrategias tradicionales son fundamentalmente tres: el incrememento del flujo por una ruta biosintética, el incremento en el número de células productoras y la inhibición de la degradación de los productos de interés.Tabla 2. Efecto de la ingeniería metabólica en el incremento de la producción de metabolitos secundarios.

El incremento en el flujo a través de la ruta biosintética puede lograrse insertando promotores fuertes a las enzimas de la ruta, lo cual lleva a una sobreexpresión de las mismas y eventualmente a una mayor producción del metabolito de interés (sin embargo a veces lo que se logra es disminuir la viabilidad celular debido a una perturbación del metabolismo) (Petersen, 2007); otra forma de incrementar el flujo es modificando las enzimas de la ruta de interés para que éstas no presenten inhibición feedback, este hecho requiere un conocimiento estructural de la enzima involucrada y del mecanismo de acción de la misma, anteriormente era por tanto considerablemente difícil tener esta información disponible, sin embargo, cada vez más la disponibilidad de datos estructurales es mayor, lo que permite con más facilidad tomar decisiones de mutagénesis encaminadas a la disminución de la inhibición de una enzima o inclusive al incremento de la rata de reacción de la misma; finalmente otra forma de aumentar el flujo por una ruta, es bloqueando las rutas competitivas; por ejemplo, mediante ARN antisentido, una tecnología basada en el hecho de que las células no reconocen como propio un ARN de doble cadena, tal que cuando detectan la presencia del mismo lo destruyen; de manera muy sucinta, en esta metodología lo que se hace es insertar un plásmido tal que cuando se realiza la transcripción del mismo, se forma un dímero de ARN (el cual tiene la secuencia de la enzima que se quiere bloquear), este ARNdc es reconocido por una enzima conocida como "dicer" la cual lo corta en pequeños fragmentos de longitud entre 21 y 25 pares de bases (ARNsi) estos fragmentos se enlazan con un complejo proteico de silenciamiento llamado RISC el cual tiene la habilidad de reconocer secuencias de RNA mensajero (similares a las de ARNsi asociado que tiene) y degradarlas, de este modo se ha logrado la inhibición de la síntesis de la proteína para la que codifica el ARN antisientido. Esta metodología ha sido probada con éxito en especies como Coffea arabica y Papaver somniferum; la desventaja del uso de esta técnica, es el desconocimiento del metabolismo vegetal, de modo que un cambio pequeño puede acarrear consigo importantes consecuencias.
La segunda estrategia es incrementar el número de células productoras, lo que podría lograrse a través de la manipulación de la diferenciación celular; sin embargo, este conocimiento es aún muy precario lográndose apenas la diferenciación en raíces (como se discute más adelante), lograr diferenciación en otro tipo de especializaciones celulares, es aún una tarea compleja y de poca aplicación industrial en el corto plazo.
La tercera estrategia consiste en inhibir la degradación de los productos, lo que se logra provocando un descenso en el catabolismo, siendo particularmente efectivo el bloqueo de enzimas relacionadas con la degradación del metabolito de interés (Yeoman y Yeoman, 1996); la estrategia para bloquear estas enzimas puede igualmente ser el ARN antisentido.
Recientemente se ha comenzado a explorar la posibilidad de utilizar factores de transcripción como blancos de la ingeniería metabólica, los factores de transcripción son proteínas ADN específicas que interactúan con las regiones promotoras de los genes, modulando la tasa de iniciación de la transcripción por la ARN polimerasa II, lo importante es que genes que se regulan coordinadamente frecuentemente tienen sitios similares de enlace para los factores de transcripción en sus promotores, de este modo, al usar un factor de transcripción como blanco se está afectando toda la ruta pues usualmente estos controlan múltiples pasos de la misma (Petersen, 2007; Verporte y Mamelink, 2002) evitando de este modo el problema de identificar los pasos limitantes (Broun, 2004). Es importante anotar que a la fecha, ya son conocidos factores de transcripción relacionados con ciertas rutas metabólicas, es por ejemplo sabido que los factores de la familia proteinca ORCA, están relacionados con la biosíntesis de alcaloides indólicos en Catharanthus roseus.
Otra estrategia que se sale de las aproximaciones tradicionales es la transgénesis de genes de plantas en Escherichia coli y Saccharomyces cerevisiae, esto tiene importantes ventajas sobre el cultivo de células vegetales, fundamentalmente por las altas tasas de crecimiento, la baja sensibilidad al estrés de corte y el conocimiento tanto de las condiciones de cultivo como para la expresión de genes heterólogos en las mismas; aproximaciones importantes en esta perspectiva, se han logrado en la producción de paclitaxel, en este caso se intentó realizar la expresión de 5 enzimas consecutivas en la ruta en S. cerevisiae a pesar de que no se logró una producción elevada de los metabolitos involucrados en la ruta, es importante que en este experimento se obtuvo la expresión de todas las proteínas involucradas la mayoría de ellas de manera funcional (Broun, 2004); un caso es la producción de ácido artemisico en el cual se logró la producción exitosa por S. cerevisiae del mismo tal que la producción fue de 115 mg•l-1, cerca de dos órdenes de magnitud mayor que en el cultivo de in vitro de Artemisa annua.
Nutrientes para el medio de cultivo. La dilucidación de los requerimientos nutricionales de las células vegetales se inició el siglo pasado, lo que permitió el desarrollo de medios de cultivo de composición definida. En todos ellos se encuentran macroelementos, microelementos, vitaminas y fitohormonas; estos componentes son suficientes para garantizar el metabolismo de las células, que en condiciones de cultivo in vitro son generalmente heterótrofas. Algunos de los medios más comúnmente utilizados son el Murashige-Skoog (MS), Linsmaier-Skoog (LS), Gamborg (B5) y Schenk-Hildebrandt (SH).
Dado que el metabolismo se ve afectado por la composición y concentración de los diferentes nutrientes, es posible inducir cambios en el crecimiento y en la producción, manipulando el medio de cultivo; cuando se encuentra que las condiciones óptimas de estos procesos son diferentes, es posible desarrollar cultivos en dos etapas, en los que en la primera se utiliza un medio de crecimiento, mientras que en la segunda se emplea uno que induzca la producción (Raval et al., 2003). A continuación se detallan diversos efectos que tiene la manipulación de algunos componentes del medio de cultivo tiene sobre el crecimiento y la producción de metabolitos secundarios.
Fuente de carbono. Existen dos formas de manipular la fuente de carbono: variando su naturaleza o su concentración. En general se utiliza la sacarosa como fuente principal, aunque es posible usar para este mismo fin otros azúcares (Chattopadhyay et al., 2002; Prakash y Srivastava, 2005). Se ha encontrado que la concentración inicial de sacarosa afecta el crecimiento, el consumo de nutrientes y la producción de metabolitos secundarios (Akalezi et al. , 1999); sin embargo, estos efectos son especie específicos y dependen de la línea celular con la que se esté trabajando. En cultivos en suspensión de Taxus chinensis y Panax notoginseng se ha observado que altas concentraciones iniciales de sacarosa alargan la fase de adaptación de la curva de crecimiento, debido al estrés causado por el incremento en la presión osmótica; mientras que bajas concentraciones iniciales incrementan la velocidad de crecimiento (Wang et al., 1999, Zhang et al., 1996).
]]> La sacarosa además de actuar como principal fuente de carbono, también puede afectar la producción de metabolitos secundarios, ya sea incrementando el contenido intracelular o la concentración final del metabolito; su efecto se debe tanto al estrés osmótico que se genera cuando está a altas concentraciones (teniendo en cuenta que las condiciones normales para el medio de cultivo mas comunmente utilizado (MS) son una osmolaridad de alrededor de 140 mmol•kg-1 y considerándose altas concentraciones condiciones superiores a los 170 mmol/kg) como al estrés nutricional que ocurre cuando se agota en el medio; efecto observado entre otras especies en T. chinensis y P. notoginseng (Wang et al., 1999, Zhang et al., 1996, Sato et al. , 1996; Zhong, 2001).Fuente de fosfato. El fosfato es un componente limitante del crecimiento mientras se mantiene en una proporción menor a la estequiométrica (Liu y Zhong, 1998). Éste está directamente relacionado con el crecimiento y el metabolismo energético, pues participa en la biosíntesis de nucleótidos, fosfolípidos y otras biomoléculas (Sato et al., 1996). Las concentraciones bajas de fosfato (en las cuales el fosfato esta por debajo de 1,04 mM) pueden llegar a estimular el metabolismo secundario ya sea por la disminución de la tasa de crecimiento que favorece el flujo de nutrientes hacia la producción de metabolitos secundarios (Raval et al., 2003, Sato et al., 1996), o por la activación de enzimas relacionadas con la biosíntesis de estos metabolitos (Ramachandra y Ravishankar, 2002).
Fuente de nitrógeno. Al igual que el fósforo, el nitrógeno es un componente fundamental para el crecimiento celular pues es utilizado en la síntesis de proteínas y ácidos nucleicos; éste puede agregarse en forma de fuentes inorgánicas u orgánicas (Yeoman y Yeoman, 1996; Schlatmann et al. , 1996). Las fuentes inorgánicas de nitrógeno más comúnmente utilizadas son el nitrato y el amonio que pueden suministrarse simultáneamente o de forma individual (Schlatmann et al., 1996; Ramachandra y Ravishankar, 2002); éstos afectan el pH del medio, ya que el consumo de nitrato implica una acidificación, contrario a lo que ocurre cuando se consume el amonio (Schlatmann et al. , 1996).
Dos variables que pueden manipularse son la concentración total y la relación nitrato/amonio; se ha encontrado que ambas afectan tanto el crecimiento como la producción de metabolitos secundarios (Yeoman y Yeoman, 1996; Ramachandra y Ravishankar, 2002). En P. quinquefolium (Zhong y Wang, 1998) y en Azadirachta indica (Prakash y Srivastava, 2005) se ha visto que altas relaciones nitrato/amonio (encima de la relación 1 a 1), favorecen tanto el crecimiento como la producción de metabolitos, encontrándose el mejor resultado cuando el nitrato es la única fuente de nitrógeno, pues el amonio resulta inhibidor del crecimiento y de la producción; diferente a lo que se ha observado en la obtención de antocianinas a partir de F. ananassa, donde la presencia tanto de nitrato como de amonio resulta indispensable para obtener altos niveles de crecimiento y producción antocianinas (Sato et al., 1996).
El nitrógeno puede actuar como un nutriente limitante del crecimiento hasta una concentración crítica en el medio de cultivo (alrededor de 10 mM pero con cambios entre especies), como se observa en F. ananassa, donde además estimula la producción de antocianinas cuando sus niveles se mantienen en un rango cercano a dicha concentración (10 mM) (Sato et al., 1996), probablemente porque los nutrientes del metabolismo primario se desvían a la formación de metabolitos secundarios (Raval et al., 2003); sin embargo, también se ha observado que altas concentraciones de éste (alrededor de 80 mM) pueden resultar inhibitorias para el crecimiento y/o la producción de metabolitos secundarios (Zhong y Wang, 1998).
Microelementos. Existen muchos iones inorgánicos importantes para el metabolismo celular que son agregados al medio de cultivo en forma de sales y que pueden afectar de manera diferente el crecimiento y la acumulación de metabolitos secundarios. Se han encontrado tres mecanismos por los cuales estos compuestos pueden estimular la producción cuando es incrementada su concentración en el medio de cultivo: favoreciendo el aumento en la concentración de biomasa, si el micronutriente limita el crecimiento (Liu y Zhong, 1996); elicitando la síntesis del metabolito de interés mediante el incremento de la presión osmótica en el medio (Kartosentono et al., 2002) y/o incrementando la disponibilidad de cofactores enzimáticos cuando actúa como grupo prostético, observándose en los dos últimos casos, un incremento en el contenido intracelular del metabolito (Huang et al., 1995); sin embargo, es importante tener en cuenta que el incremento en la presión osmótica puede tener en algunas ocasiones efectos negativos sobre el crecimiento celular y/o la producción de metabolitos secundarios, en la Tabla 3 se muestra el resultado de modificar la concentración de ciertos micronutrientes en la producción de metabolitos secundarios y el crecimiento de ciertas especies, nótese que al hacer uso de esta estrategia se observan incrementos de cómo máximo el 58% con respecto al valor de referencia, un incremento mucho mas moderado que el que se puede lograr haciendo uso de ingeniería genética en el que se logran incrementos de hasta el 542%; sin embargo, este tipo de experimentos son sencillos de conducir y pueden formar parte de una estrategia combinada para obtener un determinado metabolito de interés.
Tabla 3. Resultados obtenidos en la producción de metabolitos secundarios, al aumentar la concentración de algunos micronutrientes. En la tabla se muestran las concentraciones en las que se obtuvieron los máximos de producción.
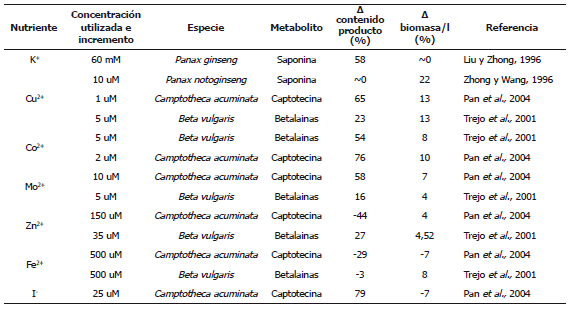
En el caso del hierro, además de su concentración, se ha estudiado el efecto de diferentes fuentes del mismo; éste se suministra generalmente en forma de Fe-Na-EDTA, pero también existen formas alternativas para agregarlo al medio, como el citrato y el sulfato férricos. Al ser suministrado como Fe-Na-EDTA se observa que favorece el crecimiento, pues en esta forma es más asimilable por la célula; sin embargo, el EDTA actúa como agente quelante disminuyendo la disponibilidad de cofactores iónicos y por lo tanto, en ocasiones se obtiene un mayor contenido intracelular de metabolitos secundarios con suplementos alternativos como el citrato (Huang et al., 1995).
D contenido producto (%): cambio porcentual en la concentración del metabolito en comparación con el cultivo antes de aumentar el micronutriente señalado.
D biomasa/l (%): cambio porcentual en la concentración de biomasa en comparación con el cultivo antes de aumentar el micronutriente señalado.
Fitohormonas. Las fitohormonas son compuestos sintetizados por la planta que pueden actuar a bajas concentraciones, mediando procesos de señalización relacionados con el crecimiento, la diferenciación o la respuesta a factores ambientales. Éstas tienen diversos efectos que pueden llegar a afectar el crecimiento, el patrón de consumo de nutrientes, la acumulación intracelular y la producción de metabolitos secundarios (Zhong et al., 1996). Estudiando la composición hormonal del medio se han logrado en P. quinquefolium incrementos en el contenido de metabolitos superiores hasta en un 70% con respecto a cultivos control y en otras especies como se señala mas adelante incrementos de hasta un 500%, el problema en este tipo de estrategia es encontrar el tipo de hormona que afecta la producción del metabolito de interés; otro factor importante es que el efecto hormonal depende también del medio de cultivo y de la presencia de otras hormonas, tal que para ser exitoso deben combinarse todos estos factores para obtener un efecto significativo.
]]> Auxinas. Las auxinas sintetizadas por la planta se derivan del triptófano y cumplen diversas funciones en la regulación del crecimiento y el metabolismo; la más destacada de ellas es la estimulación de la elongación celular. En cultivos in vitro son utilizadas en la inducción de callos y suelen agregarse en el medio de mantenimiento de suspensiones, donde dependiendo de su tipo, concentración y de la especie y línea celular, afectan el crecimiento y el metabolismo secundario (Kim et al., 2007).En algunos casos las auxinas pueden inhibir el metabolismo secundario, como el 2,4-D en la producción de saponinas y alcaloides indólicos en cultivos de P. quinquefolium (al agregarlo cae la producción 85%) (Zhong et al. , 1996) y C. roseus (al agregar 2,4 D cae la producción 70%) (Yahia et al., 1998) respectivamente; mientras que en otros casos lo pueden favorecer, como el IBA en la biosíntesis de saponinas en P. quinquefolium (incremento de aproximadamente un 5%) (Zhong et al., 1996), el IAA en la biosíntesis de L-DOPA por Stizolobium hassjoo (Huang et al., 1995) y el 2,4-D en la producción de antocianinas por Camptotheca acuminata (al agregarlo se logra un incremento cercano al 40 en la producción) (Pasqua et al., 2005).
Citoquininas. Las citoquininas son fitohormonas que regulan, a través de una compleja red de interacciones con las auxinas, con el ambiente y con otras moléculas de la planta, diversos eventos entre los que se destaca la mitosis. En cultivos celulares se utilizan, al igual que las auxinas, en la inducción de callos y en los medios de mantenimiento de suspensiones. Éstas pueden afectar el metabolismo secundario (Zhong et al., 1996), como se ha encontrado en la producción de alcaloides indólicos por Catharanthus roseus y antocianinas por C. acuminata donde la adición de BAP (Yahia et al., 1998) y quinetina (Pasqua et al., 2005), han mostrado incrementos en la producción de 500 y 100% comparados con los controles establecidos en los experimentos.
Giberelinas. Las giberelinas se caracterizan por estimular la elongación y la división celular en la planta, no siendo muy utilizadas en cultivos celulares; sin embargo, en su estudio se ha encontrado que pueden inhibir el metabolismo secundario (Yosihikawa et al., 1986) y promover el crecimiento de brotes, razón por la cual han sido utilizadas en embriogénesis somática.
Ácido abscísico. El ácido abscísico es una molécula que se sintetiza en la planta, mediando la respuesta a situaciones de estrés ambiental; éste puede estimular la producción de metabolitos secundarios como es el caso del paclitaxel en cultivos de T. chinensis (Luo et al., 2001).
Etileno. El etileno es una molécula pequeña que difunde fácilmente a través de la membrana celular; en la planta participa en fenómenos de maduración, abscisión y respuesta a patógenos. En los cultivos celulares se utiliza para inducir la producción de metabolitos secundarios; puede suministrarse para que actúe extracelularmente cuando es alimentado con la fase gaseosa o para que actúe a nivel intracelular cuando se agrega al medio, el precursor ácido 1-aminociclopropano-1carboxílico (ACC) que es transformado en el citoplasma a etileno por la enzima ACC oxidasa (Jeong et al., 2006, Bae et al., 2006).
En cultivos de C. roseus (Yahia et al., 1998) y Lithospermum erythrorhizon se ha observado que el etileno extracelular induce la producción de alcaloides indólicos y shiconina respectivamente, proponiéndose que actúa a través de una red de señalización en la que intervienen proteínas receptoras de membrana, que pueden activar enzimas del metabolismo secundario como la polifenol oxidasa (importante en la biosíntesis de shiconina) (Touno et al., 2005). Además, en suspensiones de T. chinensis se encontró que el etileno suministrado en la aireación es un factor determinante para el escalado de la producción de taxanos (Pan et al., 2000). El etileno intracelular actúa en los cultivos de células vegetales induciendo o inhibiendo el metabolismo secundario; en C. roseus, se ha observado una disminución en la producción de alcaloides indólicos (Yahia et al., 1998), contrario a lo que ocurre en L. erythrorhizon donde, al igual que el etileno extracelular, estimula la acumulación de shiconina (Touno et al., 2005).
Óxido nítrico. El óxido nítrico es una molécula que también difunde fácilmente por la membrana celular (Crawford y Guo, 2005). Éste afecta la producción de metabolitos secundarios, por ejemplo, en C. roseus media la activación de proteínas quinasas necesarias para la producción de alcaloides indólicos (Xu y Dong, 2005).
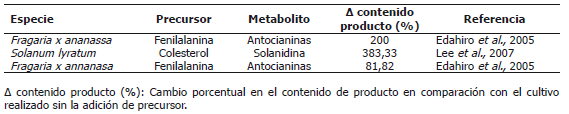
Precursores. Un precursor es una molécula que interviene en la ruta biosintética de un metabolito, por tanto puede agregarse al medio de cultivo para incrementar el rendimiento del proceso. En la Tabla 4 se nota como si se seleciona un precursor adecuado, se pueden lograr incrementos en el contenido de metabolitos secundarios de hasta un 380%; es importante anotar que un precursor es más eficiente mientras su estructura más se asemeje a la del producto de interés; sin embargo, hacer muy similar un precursor a su producto resulta también mas costoso (Yeoman y Yeoman, 1996). Además de las desventajas económicas que implica la adición de precursores específicos, en algunos casos no se da su absorción por las células, no se logra su ubicación intracelular adecuada o resultan tóxicos, aún en bajas concentraciones (Yeoman y Yeoman, 1996). Un ejemplo del uso exitoso de precursores por su efectividad y bajo costo es la L-fenilalanina (Phe), para la producción de fenilpropanoides y flavonoides (Edahiro et al., 2005). Los precursores pueden alimentarse una sola vez al principio del cultivo o de manera repetida, esta última estrategia permite mantener la concentración de éste constante y ha mostrado ser más eficiente que la primera en la inducción de la producción de metabolitos secundarios, en la producción de antocianinas en Fragaria x ananasa se observó que aplicando alimentación repetida del precursor se obtenía una acumulación 81% mayor que cuando la aplicación se hacía solo al proncipio del cultivo (Edahiro et al., 2005).
Tabla 4. Efecto de algunos precursores sobre la producción de metabolitos secundarios en cultivos celulares cuando se agregan al principio del cultivo
El oxígeno es un componente fundamental para los cultivos aerobios pues actúa como aceptor final de electrones en la fosforilación oxidativa (Schlatmann et al., 1996, Zhong, 2002). Se ha encontrado que favorece el crecimiento celular, cuando es empleado hasta cierto valor de su concentración, después del cual tiene efectos inhibitorios debido al estrés oxidativo (este valor es de 36 kPa en P. notoginseng pero puede variar entre especies y líneas celulares) (Han y Zhong, 2003; Trung et al. , 2006), que se caracteriza por un incremento en la producción de H2O2 y especies reactivas de oxígeno (ROS), las cuales activan endonucleasas encargadas de degradar el ADN (Han y Zhong, 2003); sin embargo, en algunos casos este efecto ha favorecido la acumulación de metabolitos secundarios ya que las ROS también pueden desencadenar reacciones que simulan la respuesta a patógenos, como sucede en la producción de paclitaxel por T. chinensis y alcaloides indólicos por C. roseus (Han y Zhong, 2003). Cuando el oxígeno es suministrado a concentraciones que están por debajo de los requerimientos del cultivo, tanto el crecimiento como la producción de metabolitos secundarios se ven disminuidos (Han y Zhong, 2003; Trung et al., 2006, Honda et al., 2002).
El CO2 por su parte se considera el principal producto gaseoso resultante del crecimiento, el cual puede actuar como nutriente esencial en cultivos fotomixotróficos o fotosintéticos (Han y Zhong, 2003). En algunos casos el CO2 no tiene efecto alguno sobre el crecimiento y la producción, mientras que en otros, actúa como una hormona (Lee y Shuler, 2005). A pesar de que no se conoce su mecanismo de acción, se ha observado que el aumento en su concentración puede disminuir el crecimiento, alargar la fase de adaptación, o causar la fenolización de las células. Sin embargo, su efecto puede depender también de la concentración de oxígeno en el medio, disminuyendo la acumulación y producción de metabolitos secundarios (Lee-Parsons y Shuler et al. , 2005 ).
Condiciones físicas para cultivos celulares. Además del ambiente químico del cultivo, es importante conocer los efectos que las condiciones físicas tienen tanto sobre el crecimiento como sobre la producción de metabolitos secundarios.
Temperatura. La temperatura es un factor importante en el cultivo de células vegetales, pues juega un papel fundamental en la estabilidad de las proteínas, en la activación de la transcripción de genes y en los procesos de transferencia de calor y masa (Yeoman y Yeoman, 1996, Schlatmann et al., 1996). El rango de temperaturas generalmente empleado está entre 15-35 ºC. La temperatura afecta diferentes variables relacionadas con el crecimiento, como la velocidad específica de crecimiento, la acumulación de compuestos intracelulares de reserva (biomasa inactiva) y la velocidad de consumo de oxígeno. La primera es máxima a la temperatura óptima del cultivo (Tabla 5) (Yeoman y Yeoman, 1996; Schlatmann et al., 1996) y las demás variables se han visto favorecidas por el incremento de la temperatura (Schlatmann et al., 1996; Choi et al. , 2000).
Tabla 5. Temperaturas óptimas de crecimiento y producción de metabolitos secundarios de algunos cultivos de células vegetales en suspensión.

Se sabe que la temperatura afecta la producción de metabolitos secundarios, aunque no se conocen con claridad los mecanismos bioquímicos por los que esto ocurre. En primer lugar se ha propuesto que el estrés térmico estimula la producción (Georgiev et al., 2004), generando cambios en los procesos de transducción de señales al interior de la célula que activan tanto la transcripción de genes, como enzimas específicas involucradas en la síntesis de estos metabolitos. En segundo lugar, se ha planteado que en los casos en los que se trabaja a una temperatura óptima de producción diferente a la de crecimiento (Tabla 5), lo que ocurre es un desvío de precursores desde el metabolismo primario hacia el secundario (Georgiev et al., 2004).
Es importante anotar que una selección adecuada de la temperatura puede tener efectos claves en la acumulación de metabolitos secundarios, en F. ananasa (Zhang et al. , 1997) al seleccionar la temperatura de proceso óptima se logró un mejoramiento en un 300% en producción de antocianinas y en C. roseus (Hoopen et al. , 2002) un incremento del 100% en producción de ajmalicina.
Presión osmótica. La regulación de la presión osmótica es importante en cultivos de células vegetales ya que además de mantener el balance hídrico (Kim et al. , 2001), afecta el crecimiento y la producción de metabolitos secundarios. Ésta puede regularse agregando al medio agentes osmóticos metabolizables como sacarosa o no metabolizables como manitol, sorbitol y polietilenglicol (PEG). Varios estudios han mostrado que el incremento en la presión osmótica genera tanto la disminución en la velocidad de crecimiento, como el aumento en la acumulación intracelular de metabolitos secundarios, probablemente por que el estrés osmótico, imita el estrés por deshidratación (Kim et al., 2001; Kurata et al., 1998).
pH. El crecimiento óptimo de las células vegetales en suspensión se encuentra entre un pH de 5,0-6,0, el cual puede cambiar durante el curso del cultivo ya que generalmente no se controla (Ramachandra y Ravishankar, 2002) y como se explicó anteriormente, depende del consumo de nitrato y amonio. Se ha demostrado que cambios en el pH inicial del medio de cultivo pueden afectar la acumulación de metabolitos secundarios, como es el caso de la producción de indirubina por suspensiones de Polygonum tinctorium en las cuales la producción en el pH óptimo alcanza a ser mayor entre un 20% y un 30% comparada con otros pH evaluados (Marero et al., 1997).
]]> Iluminación. Las características de la irradiación luminosa, como longitud de onda, intensidad y fotoperiodo, influyen sobre el crecimiento y la producción de metabolitos secundarios en cultivos celulares heterótrofos de manera especie-específica (Yeoman y Yeoman, 1996; Chattopadhyay et al., 2002; Zhang et al. , 2002; Yu et al., 2005). En algunos casos la luz puede actuar como una señal tipo hormonal, requiriéndose pequeñas cantidades para observar su efecto (Zhang et al., 2002); éste puede estar relacionado con fotorreceptores que actúan de forma reversible o irreversible, como interruptores que controlan la expresión de genes específicos. Dependiendo de la longitud de onda aplicada se han observado diferentes efectos: por ejemplo, la luz roja estimula el crecimiento de "hairy roots" de P. ginseng, mientras que otras longitudes de onda como la azul lo desfavorecen. A nivel de la producción se ha propuesto que diferentes longitudes de onda activan rutas de señalización específicas, lo cual se ha comprobado en cultivos de P. ginseng y de F. ananassa (Yu et al., 2005). La intensidad lumínica puede tener diferentes efectos sobre cultivos irradiados continuamente; así por ejemplo, en suspensiones de Vitis vinifera y C. arabica (Zhang et al. , 2002) se observan cambios significativos en la densidad de biomasa con el incremento de esta variable; además en esta última especie, se observan cambios morfológicos sobre las células por la formación de cloroplastos cuando la intensidad lumínica es incrementada (Zhang et al., 2002). La producción de metabolitos secundarios también puede verse afectada por este factor; por ejemplo, altas intensidades lumínicas (5 Klux) favorecen la acumulación de antocianinas en cultivos de F. x ananassa, Perilla frutescens, Daucus carota y V. vinifera, mientras que en cultivos de C. arabica este efecto se mantiene hasta cierto valor de intensidad (3 Klux) después del cual la producción decae (Zhang et al., 2002). Los efectos del fotoperiodo, han sido estudiados con respecto a la relación luz/oscuridad y a la duración del periodo, variables que pueden afectar el crecimiento, la producción y la acumulación interna de metabolitos secundarios como se ha encontado en cultivos de C. arabica (Zhang et al., 2002) y Podophyllum hexandrum (Chattopadhyay et al., 2002). Finalmente es importante tener en cuenta que la luz puede afectar la inducción y friabilidad de callos, así como la producción de metabolitos secundarios a partir de éstos; por ejemplo en cultivos de P. hexandrum, fotoperiodos luz/oscuridad de 16/8 aumentan el crecimiento y la friabilidad de los callos (Chattopadhyay et al., 2002) y en cultivos de C. acuminata es necesario un estímulo lumínico para activar la producción de antocianinas (Pasqua et al., 2005).Elicitación. La elicitación es un conjunto de técnicas en las que se somete las células a factores externos, induciendo mecanismos de defensa que en ocasiones incrementan la síntesis de metabolitos específicos. Dichos factores son llamados elicitores y se clasifican de acuerdo a su naturaleza, en bióticos (quitosano, metiljasmonato, alginato, extractos fúnjicos) (Dong y Zhong, 2002; Conceicao et al., 2006; Ignatov et al., 1999; Wang y Zhong, 2002) y abióticos (metales pesados, estrés térmico, estrés osmótico) (Yu et al., 2005; Wu et al., 2001) o de acuerdo a la interacción planta-elicitor, en generales (metiljasmonato, ácido salicílico), si desencadenan una respuesta de defensa en cualquier planta, y específicos (extractos fúnjicos), cuando sólo actúan sobre una especie en particular (Vasconsuelo y Boland, 2007 ).
Aspectos moleculares. Los elicitores específicos activan un sistema genético de la planta conocido como "gen a gen", en el que una proteína de avirulencia (Avr) de un patógeno determinado es reconocida por una proteína de reconocimiento (R) de la planta, desencadenando la transcripción de genes específicos que median la respuesta de defensa. Las proteínas R pueden ser transmembranales o citoplasmáticas. La gran variabilidad de estos tipos de proteínas implica que confieren resistencia a unos u otros patógenos. Así, patógenos que liberan proteínas Avr al citoplasma son reconocidos por proteínas R citoplasmáticas, mientras que productos Avr extracelulares son reconocidos por proteínas R transmembranales (Zhao et al., 2005).
De manera general, la secuencia de eventos en la respuesta de defensa impulsada por el elicitor comprende los siguientes pasos: reconocimiento, fosforilación y desfosforilación de proteínas de membrana y citoplasma, aumento en la concentración de iones Ca2+ en el citoplasma, despolarización de la membrana, flujo de iones (Cl-, K+ y H+), alcalinización extracelular, acidificación citoplasmática, activación de proteínas quinasas activadas por mitógeno (MAPK), activación de la NADPH oxidasa, producción de ROS, expresión de genes de defensa tempranos, producción de etileno y jasmonato, expresión de genes de defensa tardíos y finalmente acumulación de metabolitos secundarios (Vasconsuelo y Boland, 2007, Zhao et al., 2005).
Utilización de elicitores en cultivos de células vegetales. La elicitación de una especie para la obtención de un metabolito particular, requiere la determinación de la dosis óptima y el tiempo adecuado de aplicación del elicitor, así como la respuesta en el tiempo del cultivo y los efectos combinados de distintos elicitores. Para determinar la dosis óptima del elicitor que maximiza la producción del metabolito de interés, se debe evaluar el efecto de la concentración de éste sobre el crecimiento y la producción. En general los elicitores inhiben el crecimiento, debido probablemente a que en su presencia las células activan mecanismos de defensa desviando los nutrientes y la energía hacia el metabolismo secundario (Thanh et al., 2005, Zhao et al., 2004). En cuanto al efecto sobre la producción, se ha encontrado que hay un incremento en ésta a medida que aumenta la concentración del elicitor hasta un valor máximo, después del cual decrece nuevamente, probablemente por la saturación de los receptores o por que dicha molécula puede ser tóxica para la célula. Estos efectos han sido estudiados en diferentes especies, en las que se muestra un incremento en la producción como resultado del proceso de elicitación (Tabla 6). Debido a que los elicitores afectan el crecimiento, se ha planteado como alternativa el cultivo en dos etapas.
Tabla 6. Efecto de la elicitación en el crecimiento y la acumulación de metabolitos secundarios en cultivos en suspensión de diferentes especies.
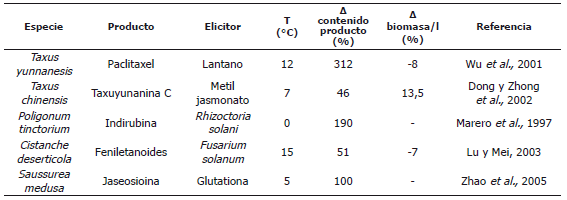
El tiempo de aplicación del elicitor al cultivo es importante, ya que los efectos pueden variar dependiendo de la fase de crecimiento al momento de aplicar el tratamiento (Zhao et al., 2005). Además es importante estudiar el comportamiento del cultivo con el tiempo, ya que el incremento en la productividad se observa cierto tiempo después de la adición del elicitor (Gala et al., 2005, Sánchez et al., 2005). Una técnica muy exitosa en células de T. chinensis es la elicitación repetida, en donde se agrega metiljasmonato al medio en diferentes días del cultivo, obteniéndose un incremento progresivo en el contenido de taxuyunanina C hasta alcanzar un valor significativamente mayor que con una sola elicitación (Hoopen et al., 2002). El acoplamiento de un tipo de elicitor con otros factores aumenta la producción, generándose un efecto sinérgico (Qu et al., 2006). Es importante tener en cuenta el incremento en el costo del proceso a la hora de elegir el elicitor.
CONCLUSIONES
El cultivo de células vegetales para la producción de metabolitos secundarios se plantea como una estrategia interesante para la obtención de compuestos con alto valor agregado, que normalmente son producidos en bajas concentraciones por la planta; sin embargo, la productividad de estos procesos es muy baja, por lo que es necesario aplicar las metodologías de optimización descritas en la presente revisión como una manera de estimular e incrementar la producción del metabolito de interés a escala de laboratorio.
]]> Un país megadiverso como Colombia, debe aprovechar el material vegetal con que cuenta para el desarrollo de este tipo de metodologías, con el fin de obtener compuestos con diversas aplicaciones.
BIBLIOGRAFÍA
Akalezi, C., S. Liu, Q. Li, J. Yu and J. Zhong. 1999. Combined effects of initial sucrose concentration and inoculum size on cell growth and ginseng saponin production by suspension cultures of Panax ginseng. Process Biochemistry 34(6): 639-642. [ Links ]
Bae, K.H., Y.E. Choi, C.G. Shin, Y.Y. Kim and Y.S. Kim. 2006. Enhanced ginsenoside productivity by combination of ethephon and methyl-jasmoante in ginseng (Panax ginseng C.A Meyer) adventitious root cultures. Biotechnology Letters 28(15):1163-1166 [ Links ]
Broun, P. 2004. Transcription factors as tools for metabolic engineering in plants. Current Opinion in Plant Biology 7(2): 202-209. [ Links ]
Chattopadhyay, S., A. Srivastava, S. Bhojwani and V. Bisaria. 2002. Production of podophyllotoxin by plant cell cultures of Podophyllum hexandrum in bioreactor. Journal of Bioscience and Bioengineering 93(2): 215-220. [ Links ]
Choi, H., S. Kim, J. Son, S. Hong, H.S. Lee and H.J. Lee. 2000. Enhancement of paclitaxel production by temperature shift in suspension culture of Taxus chinensis. Enzyme and Microbial Technology 27(8): 593-598. [ Links ]
Conceicao, L.F.R., F. Ferreres, R.M. Tavares and A.C.P. Dias. 2006. Induction of phenolic compounds in Hypericum perforatum L. cells by Colletotrichum gloeosporioides elicitation. Phytochemistry 67(2): 149-155. [ Links ]
Crawford, N. and F. Guo. 2005. New insights into nitric oxide metabolism and regulatory functions. Trends in Plant Science 10(4): 195-200. [ Links ]
Deavours, B. and R.A. Dixon. 2005. Metabolic engineering of isoflavonoid biosynthesis in alfalfa. Plant Physiology 138(4): 2245-2259. [ Links ]
Dong, H.D. and J.J. Zhong. 2002. Enhanced taxane productivity in bioreactor cultivation of Taxus chinensis cells by combining elicitation sucrose feeding and ethylene incorporation. Enzyme and Microbial Technology 31(1): 116-121. [ Links ]
Dörnenburg, H. and D. Knorr. 1995. Strategies for the improvement of secondary metabolite production in plant cell cultures. Enzyme and Microbial Technology 17(8): 674-684. [ Links ]
Edahiro, J., M. Nakamura, M. Seki and S. Furusaki. 2005. Enhanced accumulation of anthocyanin in cultured strawberry cells by repetitive feeding of L-Phenylalanine into the medium. Journal of Biosciences and Bioengineering 99(1): 43-47. [ Links ]
Fedoreyev, S.A., T.V. Pokushalova, M.V. Veselova, L.I. Glebko, N.I. Kulesh, T.I. Muzarok, L.D. Seltskaya, V.P. Bulgakov and Y.N. Zhuravlev. 2000. Isoflavonoid production by callus cultures of Maackia amurensis. Fitoterapia 71(4): 365-372 [ Links ]
Foley, W. and B. Moore. 2005. Plant secondary metabolites and vertebrate herbivores-from physiological regulation to ecosystem function. Current Opinion in Plant Biology 8(4): 430-435. [ Links ]
Gala, R., G. Mita and S. Caretto. 2005. Improving a-tocopherol production in plant cell cultures. Journal of Plant Physiology 162(7): 782-784 [ Links ]
Georgiev, M., A. Pavlov and M. Ilieva. 2004. Rosmarinic acid production by Lavandula vera MM cell suspensions: the effect of temperature. Biotechnology Letters 26(10): 855-856. [ Links ]
Han, J. and J.J. Zhong. 2003. Effects of oxygen partial pressure on cell growth and ginsenoside and polysaccharide production in high density cell cultures of Panax notoginseng. Enzyme and Microbial Technology 32(3): 498-503. [ Links ]
Honda, H., K. Hiraoda, E. Nagamori, M. Omote, Y. Kato, S. Hiraoka and T. Kobayashi. 2002. Enhanced anthocyanin production from grape callus in an air lift type bioreactor using a viscous additive supplemented medium. Journal of Bioscience and Bioengineering 94(2): 135-139. [ Links ]
Hoopen, H.J.G., J.L. Vinke, P.R.H. Moreno, R. Verpoorte and J.J. Heijnen. 2002. Influence of temperature on growth and ajmalicine production by Catharanthus roseus suspension cultures. Enzyme and Microbial Technology 30(1): 56-65. [ Links ]
Huang, S.Y., S.Y. Chen, K.L. Wu and W-T. Taung. 1995. Strategy for inducing pertinent cell line and optimization of the medium for Stizolobium hassjoo producing L DOPA. Journal of Fermentation and Bioengineering 79(4): 342-347. [ Links ]
Hughes, E., S.B. Hong, S. Gibson, V. Shanks and K.Y. San. 2004. Metabolic engineering of the indole pathway in Catharanthus roseus hairy roots and increased accumulation of tryptamine and serpentine. Metabolic Engineering 6(4): 268-276. [ Links ]
Ignatov, A., G. Clark, S. Cline, M. Psenak, R. Krueger and C. Coscia. 1999. Elicitation of dihydrobenzophenanthridine oxidase in Sanguinaria canadensis cell cultures. Phytochemistry 43(6): 1141-1144. [ Links ]
Jeong, C.S., D. Chakrabarty, E.J. Hahn, H.L. Lee and K.Y. Paek. 2006. Effects of oxygen, carbon dioxide and ethylene on growth and bioactive compound production in bioreactor culture of ginseng adventitious roots. Biochemical Engineering Journal 27(3): 252-263. [ Links ]
Kartosentono, S., G. Imdrayanto and N.C. Zaini. 2002. The uptake of copper ions by cell suspension cutures of Agave amaniensis, and its effect on the growth, amino acids and hecogenin content. Plant Cell Tissue and Organ Culture 68(3): 287-292. [ Links ]
Kim, S, H. Choi, J. Kim, H. Lee and S. Hong. 2001. Effect of osmotic pressure on paclitaxel production in suspension cell cultures of Taxus chinensis. Enzyme and Microbial Technology 28(2-3): 202-209. [ Links ]
Kim, Y.S., E.C. Yeung, E.J. Hahn and K.Y. Paek. 2007. Combined effects of phytohormone, indole-3-butyric acid, and methyl jasmonate on root growth and ginsenoside production in adventitious root cultures of Panax ginseng C.A. Meyer. Biotechnology Letters 29(11): 1789-1792. [ Links ]
Kurata, H., T. Achioku and S. Furusaki. 1998. The light/dark cycle operation with an hour-scale period enhances caffeine production by Coffea arabica cells. Enzyme and Microbial Technology 23(7-8): 518-523. [ Links ]
Lee, M.H., J.J. Cheng, C.Y. Lin, Y.J. Chen and M.K. Lu. 2007. Precursor-feeding strategy for the production of solanine, solanidine and solasodine by a cell culture of Solanum lyratum. Process Biochemistry 42(5): 899-903. [ Links ]
Lee, C. and M. Shuler. 2005. Sparge gas composition affects biomass and ajmalicine production from immobilized cell cultures of Catharanthus roseus. Enzyme and Microbial Technology 37(4): 424-434. [ Links ]
Li, F.X., Z.P. Jin, D.X. Zhao, L.Q. Cheng, C.X. Fu and M. Fengshan. 2006. Overexpression of the Saussurea medusa chalcone isomerase gene in S. involucrata hairy root cultures enhances their biosíntesis of apigenin. Phytochemistry 67(6): 553-560. [ Links ]
Liu, S. and J.J. Zhong. 1998. Phosphate effect on production of ginseng saponin and polysaccharide by cell suspension cultures of Panax ginseng and Panax quinquefolium. Process Biochemistry 33(1): 69-74. [ Links ]
Liu, S. and J.J. Zhong. 1996. Efects of potasium ion on cell growth and production of ginseng saponin and polysaccharide in suspension cultures of Panax ginseng. Journal of Biotechnology 52(2): 121-126. [ Links ]
Lu, C.T. and X.G. Mei. 2003. Improvement of phenylethanoid glycosides production by a fungal elicitor in cell suspension culture of Cistanche deserticola. Biotechnology Letters 25(17): 1437-1439. [ Links ]
Luo, J., L. Liu and C.D. Wu. 2001. Enhancement of paclitaxel production by abscisic acid in cell suspension cultures of Taxus chinensis. Biotechnology Letters 23(16): 1345-1348. [ Links ]
Marero, L., J.H. Jin, J. Shin, H.J. Lee, I.S. Chung and H.J. Lee. 1997. Effect of fungal elicitation on indirubin production from a suspension culture of Polygonum tinctorium. Enzyme and Microbial Technology 21(2): 97-101. [ Links ]
Oncina, R., J.M. Botía, J.A. Del Río and A. Ortuño. 2000. Bioproduction of diosgenin in callus cultures of Trigonella foenum-graecum L. Food Chemistry 70(4): 489-492. [ Links ]
Pan, X.W., Y.Y. Shi, X. Liu, X. Gao and Y.T. Lu. 2004. Influence of inorganic microelements on the production of camptothecin with suspension cultures of Camptotheca acuminata. Plant Growth Regulation 44(1): 59-63. [ Links ]
Pan, Z.W., H.Q. Wang and J.J. Zhong. 2000. Scale-up study on suspension cultures of Taxus chinensis cells for production of taxane diterpene. Enzyme and Microbial Technology 27(9): 714-723. [ Links ]
Pasqua, G., B. Monacelli, N. Mulinacci, S. Rinaldi, C. Giaccherini, M. Innocenti and F. Vinceri. 2005. The effect of growth regulators and sucrose on anthocyanin production in Camptotheca acuminata cell cultures. Plant Physiology and Biochemistry 43(3):293-298. [ Links ]
Petersen, M. 2007. Current status of metabolic phytochemustry. Phytochemistry 68(22-24): 2847-2860. [ Links ]
Prakash, G. and A. Srivastava. 2005. Statistical media optimization for cell growth and azadirachtin production in Azadirachta indica (A. Juss) suspension cultures. Process Biochemistry 40(12): 3795-3800. [ Links ]
Qu, J.G., W. Zhang, M.F. Jin and X.J. Yu. 2006. Effect of homogeneity on cell growth and anthocyanin biosynthesis in suspension cultures of Vitis vinifera. Chinese Journal of Biotechnology 22(5): 805-810. [ Links ]
Ramachandra, S. and G. Ravishankar. 2002. Plant cell cultures: Chemical factories of secondary metabolites. Biotechnology Advances 20(2): 101-153. [ Links ]
Raval, K., S. Hellwing, G. Prakash, A. Ramos, A. Srivastava and J. Büchs. 2003. Necessity of two stage process for the production of azadirachtin related limonoids in suspension cultures of Azadirachta indica. Journal of Bioscience and Bioengineering 96(1): 16-22. [ Links ]
Sánchez, S.M., T.J. Fernandez and P. Corchete. 2005. Yeast extract and methyl jasmonate-induced silymarin production in cell cultures of Silybum marianum (L.) Gaertn. Journal of Biotechnology 119(1): 60-69. [ Links ]
Sato, K., M. Nakayama and J.I. Shigeta. 1996. Culturing conditions affecting the production of anthocyanin in suspendend cell cultures of strawberry. Plant Science 113(1): 91-98. [ Links ]
Schlatmann, J., H. Hoopen and J. Heijnen. 1996. Large-scale production of secondary metabolites by plant cell cultures. pp. 11-52. En: Dicosmo, F., M. Misawa, (eds.). Plant cell culture secondary metabolism toward industrial application. New Cork: CRS Press. 232 p. [ Links ]
Thanh, N., H. Murthy, K. Yu, E. Hahn and K. Paek. 2005. Methyl jasmonate elicitation enhanced synthesis of ginsenoside by cell suspension cultures of Panax ginseng in 5-l balloon type bubble bioreactors. Applied Microbial and Biotechnology 67(2): 197-201. [ Links ]
Touno, K., J. Tamaoka, Y. Ohashi and K. Shimomura. 2005. Ethylene induced shikonin biosynthesis in shoot culture of Lithospermum erythrorhizon. Plant Physiology and Biochemistry 43(2): 101-105. [ Links ]
Trejo, T.G., A.J.B. Balcazar, B.B. Martínez, M.G. Salcedo, F.M. Jaramillo, O.M.L. Arenas and A.A. Jiménez. 2008. Effect of screening and subculture on the production of betaxanthins in Beta vulgaris L. var. ''Dark Detroit' callus culture. Innovative Food Science and Emerging Technologies 9(1): 32-36. [ Links ]
Trejo, T.G., A.A. Jiménez, M.M. Rodríguez, D.J. Sánchez and L.G. Gutierrez. 2001. Influence of cobalt and other microelements on the production of betalains and the growth of suspension cultures of Beta vulgaris. Plant Cell, Tissue and Organ Culture 67(1): 19-23. [ Links ]
Trung, N., H.N. Murthy, K. Yu, C.S. Jeong, E.J. Hahn and K.Y. Paek. 2006. Effect of oxygen supply on cell growth and saponin production in bioreactor cultures of Panax ginseng. Journal of Plant Physiology 163(12): 1337-1341. [ Links ]
Vasconsuelo, A. and R. Boland. 2007. Molecular aspects of the early stages of elicitation of secondary metabolites in plants. Plant Science 172(5):861-875. [ Links ]
Verporte, R. and J. Mamelink. 2002. Engineering secondary metabolite production in plants. Current Opinion in Biotechnology 13(2): 181-187. [ Links ]
Wang, H., J. Yu and J. Zhong. 1999. Significant improvement of taxane production in suspension cultures of Taxus chinensis by sucrose feeding strategy. Process Biochemistry 35(5): 479-483. [ Links ]
Wang, Z. and J. Zhong. 2002. Combination of conditioned medium and elicitation enhances taxoid production in bioreactor cultures of Taxus chinensis cells. Biochemical Engineering Journal 12(2): 93-97. [ Links ]
Wu, J., C. Wang, X. Mei. 2001. Stimulation of taxol production and excretion in Taxus spp cell cultures by rare earth chemical lanthanum. Journal of Biotechnology 85(1): 67-73. [ Links ]
Xu, M. and J. Dong. 2005. Nitric oxide stimulates indole alkaloid production in Catharanthus rosesus cell suspension cultures through a protein kinase-dependent signal pathway. Enzyme and Microbial Technology 37(1): 49-53. [ Links ]
Yahia, A., C. Kevers, T. Gaspar, J.C. Chénieux, M. Rideau and J. Créche. 1998. Cytokinins and ethylene stimulate indole alkaloid accumulation in cell suspension cultures of Catharanthus roseus by two distinct mechanisms. Plant Science 133(1): 9-15.
Yeoman, M. and C. Yeoman. 1996. Manipulating secondary metabolism in cultured plant cells. New Phytologist 134(4): 553-569. [ Links ]
Yosihikawa, N., H. Fukui and M. Tabata. 1986. Effect of gibberellin A3 on shikonin production in Lithospermum callus cultures. Phytochemistry 25(3): 621-622. [ Links ]
Yu, K.W., H.N. Murthy, C.S. Jeong, E.J. Hahn and K.Y. Paek. 2005. Organic germanium stimulates the growth of ginseng adventitious roots and ginsenoside production. Process Biochemistry 40(9): 2959-2961. [ Links ]
Zhang, W., C. Curtin, M. Kikuchi and C. Franco. 2002. Integration of jasmonic acid and light irradiation for enhancement of anthocyanin biosynthesis in Vitis vinifera suspension cultures. Plant Science 162(3): 459-468. [ Links ]
Zhang, W., M. Seki and S. Furusaki. 1997. Effect of temperature and its shift on growth and anthocyanin production in suspension cultures of strawberry cells. Plant Science 127(2): 207-214. [ Links ]
Zhang, Y., J. Zhong, J. Yu. 1996. Enhancement of ginseng saponin production in suspension cultures of Panax notoginseng: manipulation of medium sucrose. Journal of Biotechnology 51(1): 49-56. [ Links ]
Zhao, Z., Y. Xu, Z. Qian, W. Tian, X. Qian and J.J. Zhong. 2004. Novel fluoro-and hydroxyl-containing jasmonate derivatives as highly efficient elicitors in suspension cultures of Taxus chinensis. Bioorganic & Medicinal Chemistry Letters 14(18): 4755-4758. [ Links ]
Zhao, J., L. Davis, R. Verpoorte. 2005. Elicitor signal transduction leading to production of plant secondary metabolites. Biotechnology Advances 23(4): 283-333. [ Links ]
Zhao, D.X., C.X. Fu, Y.S. Han and D.P. Lu. 2005. Effects of elicitation of jaceosidin and hispidulin production in cell suspension cultures of Saussurea medusa. Process Biochemistry; 40(2): 739-745. [ Links ]
Zhong, J. 2001. Biochemical engineering of the production of plant-specific secondary metabolites by cell suspension cultures. Advances in Biochemical Engineering/Biotechnology 72: 1-30. [ Links ]
Zhong, J.J., Y. Bai and S.J. Wang. 1996. Effects of plant growth regulators on cell growth and ginsenoside saponin production by suspension cultures of Panax quinquefolium. Journal of Biotechnology 45(3): 227-234. [ Links ]
Zhong, J.J. and S.J. Wang. 1998. Effects of nitrogen source on the production of ginseng saponin and polysaccharide by cell cultures of Panax quinquefolium. Process Biochemistry 33(6): 671-675. [ Links ]
Zhong, J. and D. Wang. 1996. Improvement of cell growth and production of ginseng saponin and polysaccharide in suspension cultures of Panax notoginseng: Cu2+ effect. Journal of Biotechnology 46(1): 69-72. [ Links ]
Zhong, J. 2002. Plant cell culture for production of paclitaxel and other taxanes. Journal of Bioscience and Bioengineering 94(6): 591-599. [ Links ] ]]>