
Molecular Identification of Polyhydroxyalkanoate-Producing Bacteria Isolated from Dairy and Sugarcane Residues
Ana Carolina Cardona Echavarría1; Amanda Lucía Mora Martínez2 y Mauricio Marín Montoya3
1Ingeniera Biológica. Universidad Nacional de Colombia - Sede Medellín - Facultad de Ciencias - Laboratorio de Biología Celular y Molecular. A.A. 3840, Medellín, Colombia. <accardone@unal.edu.co>
2Profesora Asociada. Universidad Nacional de Colombia - Sede Medellín - Facultad de Ciencias - Laboratorio de Procesos Ambientales. A.A. 3840, Medellín, Colombia. <almora@unal.edu.co>
3Profesor Asociado. Universidad Nacional de Colombia - Sede Medellín - Facultad de Ciencias - Laboratorio de Biología Celular y Molecular. A.A. 3840, Medellín, Colombia. <mamarinm@unal.edu.co>
Resumen. Los polihidroxialcanoatos (PHAs) son bioplásticos termoestables sintetizados por algunas bacterias, que los acumulan como reservas de carbono en forma de inclusiones citoplasmáticas. Estos compuestos se constituyen en una opción para la sustitución de polímeros sintéticos no biodegradables. En este trabajo se evaluó la presencia de bacterias productoras de PHAs en lactosueros derivados de la producción de quesos, y en melaza, cachaza y bagazo de caña de azúcar. El aislamiento bacteriano se realizó en medio mínimo de sales suplementado con glucosa al 2% y 1 mL mL-1 de rojo Nilo (0,1%). Las colonias que presentaron fluorescencia a 340 nm en este medio, se evaluaron nuevamente mediante microscopía de fluorescencia con azul Nilo. Aquellas cepas que resultaron positivas para ambas pruebas fueron consideradas como potenciales productoras de PHAs e identificadas por secuenciación de la región 16S del ADN ribosomal. Seguidamente se evaluó, en algunas de éstas, la presencia del gen phaC mediante PCR con cebadores específicos. Se detectaron 38 cepas productoras de PHAs, representando 18 morfotipos bacterianos. Fueron identificadas en los sustratos de lactosuero cepas pertenecientes a los géneros Lactococcus, Klebsiella, Pseudomonas, Enterobacter y Enterococcus; mientras que en los subproductos de caña de azúcar se encontraron cepas de los géneros Bacillus, Enterobacter, Pantoea, Klebsiella y Gluconobacter. El gen phaC se detectó por PCR en 16 bacterias que presentaron los arreglos genéticos I y IV. Este trabajo abre la posibilidad de emplear las bacterias obtenidas en procesos alternativos, ambientalmente sostenibles y generadores de valor agregado, para la disposición final de subproductos y residuos agroindustriales.
Palabras clave: ADNr 16S, bagazo, lactosuero, melaza, PCR, phaC.
Abstract. Polyhydroxyalkanoates (PHAs) are thermostable bioplastics produced by bacteria and stored as inclusion bodies to serve as a reserve carbon source. These compounds are a good alternative to non-biodegradable synthetic plastics. In this work, the presence of PHAs-producing bacteria in whey, sugar-cane molasses, cachaza and bagasse was investigated. Bacteria were isolated using a minimal medium supplemented with 2% glucose and 1 mL mL-1 Nile red (0.1%). Colonies exhibiting fluorescence at 340 nm were further analyzed by fluorescence microscopy with Nile blue. When positive for both tests, bacterial isolates were classified as PHAs producers and their 16S rDNA sequenced. For selected isolates, the presence of the phaC gene was confirmed by PCR. A total of 38 strains, grouped into 18 different morphotypes, were identified as PHA producers. Bacteria belonging to Lactococcus, Klebsiella, Pseudomonas, Enterobacter and Enterococcus genera were isolated from whey and Bacillus, Enterobacter, Pantoea, Klebsiella and Gluconobacter from sugar cane residues. The phaC gene was detected by PCR in 16 bacteria with type I and IV arrangements. This work opens up the possibility of using the isolated bacteria as an environmentally sustainable alternative for the disposal of agro-industrial residues as well as an additional income source.
Key words: 16S rDNA, bagasse, molasses, PCR, phaC, whey.
Los polihidroxialcanoatos (PHAs) son polímeros biodegradables sintetizados por bacterias que los acumulan en forma de inclusiones citoplasmáticas cuando crecen en sustratos ricos en fuentes de carbono y con desbalances de nitrógeno, fósforo y/o azufre (Reddy et al., 2003). Los PHAs fueron descubiertos a principios del siglo pasado en la bacteria Bacillus megaterium y a la fecha, se han reportado en más de 300 especies bacterianas (Keshavarz y Roy, 2010).
Los PHAs se clasifican, dependiendo del número de carbonos presentes en cada monómero, en PHAs de cadena corta (scl, short-chain-lenght) con 3-5 átomos de carbono, como el Poli-3-hidroxivalerato ([P(3HV)] y el Poli-3-hidroxibutirato [P(3HB)]); PHAs de cadena media (mcl, medium-chain-lenght) con 6 a 14 carbonos, como el copolímero poli-3(HB-co-HV); y PHAs de cadena mixta (PHAMCM), que combinan los dos anteriores, como el Poli (3HB-co-3HV-co-3HHx) (Stubbe y Tian, 2003). Dependiendo del número de carbonos, los PHAs presentan diferentes niveles de cristalinidad y elasticidad, siendo dichas propiedades clave para sus aplicaciones en los campos industriales, farmacéuticos, médicos y agrícolas (Ciesielski et al., 2006). El PHB y el Poli 3(HB-co-HV) son los PHAs de mayor utilización comercial (Stubbe y Tian, 2003).
La síntesis de PHAs bacterianos requiere de la enzima polihidroxialcanoato sintasa, codificada por el gen phaC. Dicho gen y otros involucrados en el metabolismo de biosíntesis de estas moléculas, están organizados en operones, siendo hasta ahora identificados cuatro arreglos básicos (Stubbe y Tian, 2003, Lau y Sudesh, 2012). El primer arreglo (Sintasas tipo I) está representado por la bacteria Cupriavidus necator (antes Ralstonia eutropha) y se caracteriza por presentar un operón phaCAB que incluye los genes PHA sintasa (phaC), b-cetotiolasa (phaA) y acetoacetil-CoA reductasa (phaB). Las sintasas PHA tipo II, representadas por Pseudomonas aeruginosa, contienen dos genes sintasas (phaC1 y phaC2) separados por el gen phaZ, cuyo producto enzimático actúa en la despolimerización de éstos compuestos (Solaiman et al., 2000). Las sintasas PHA tipos I y II comprenden enzimas que consisten de un solo tipo de subunidad (PhaC) con masas moleculares entre 61 y 68 kDa. En el tercer sistema (tipo III), la enzima PHA sintasa consiste de dos subunidades codificadas por los genes phaE y phaC, siendo propio de bacterias de los géneros Chromatium, Synechocystis y Thyocystis (Rehm y Steinbuchel, 1999). Finalmente, el cuarto arreglo (tipo IV) es típico de bacterias del género Bacillus, que presentan una PHA sintasa conformada por dos subunidades, phaC y phaR y codificadas por el operón phaRBC (McCool y Cannon, 2001).
]]> Debido a su naturaleza lipídica, la detección y aislamiento de bacterias productoras de PHAs se fundamenta en la utilización de colorantes lipofílicos como el negro Sudán (Schlegel et al., 1970), el azul Nilo (Ostle y Holt, 1982) y su oxazona fluorescente, rojo Nilo (Spiekermann et al., 1999). En los últimos años, su utilización para detectar bacterias productoras de PHAs es acompañada de pruebas moleculares confirmatorias basadas en PCR que detectan la presencia de uno o varios de los genes de biosíntesis de PHAs (Solaiman et al., 2000; Ciesielski et al., 2006).En Colombia, el sector agropecuario ha sido uno de los principales motores del desarrollo económico, con aportes del 9% del PIB, 21% de las exportaciones y 19% del empleo total del país (Proexport, 2011a); siendo dos de las principales actividades agroindustriales, la obtención de azúcar a partir de caña (Saccharum officinarium L.) y la producción de leche y derivados lácteos. Estas dos agroindustrias se caracterizan por generar una gran cantidad de subproductos y residuos en sus procesos de transformación. En el caso de la caña, se estima que por cada tonelada cosechada se producen 330 kg de bagazo, 30-50 kg de cachaza y 800 L de vinaza (Basanta et al., 2007). El lactosuero por su parte, es la sustancia líquida obtenida por separación del coágulo de leche en la elaboración de queso y representa cerca del 90% del total de la leche utilizada en el proceso de producción de quesos y otros derivados lácteos (Londoño et al., 2008). A pesar de que el lactosuero se usa en forma líquida (ca. 10%), en polvo (30%), o como lactosa y otros subproductos en la industria de alimentos y de concentrados de animales (15%), cerca del 45% se desecha como aguas residuales o directamente al suelo, lo que representa serios problemas de contaminación ambiental (Parra, 2009).
Debido a los altos volúmenes de subproductos que generan las agroindustrias de la caña de azúcar y de lácteos en el país, es posible su utilización alternativa como sustrato para la producción microbiana de PHAs. En este estudio se evalúo la presencia de bacterias productoras de PHAs en melaza, bagazo y cachaza de caña de azúcar, así como en lactosueros bovinos y caprinos, a partir de pruebas de preselección con tinción lipídica y de la confirmación por PCR, de la presencia del gen phaC en un subgrupo de las bacterias aisladas. Los microorganismos que resultaron positivos para la producción de PHAs, fueron identificados molecularmente mediante secuenciación del ADNr 16S.
MATERIALES Y MÉTODOS
Subproductos agroindustriales. Las bacterias fueron aisladas a partir de subproductos de la agroindustria de la caña de azúcar y de la producción de derivados lácteos. En el primer caso se utilizaron dos muestras de melaza de caña: una del Ingenio Incauca (Miranda, Cauca), y la otra, de una fuente comercializada en el municipio de Sopetrán (Antioquia). Además, una muestra de bagazo y una de cachaza de caña, del ingenio Incauca (Miranda, Cauca).
Los subproductos lácteos estuvieron representados por tres muestras de lactosuero, dos de estas se generaron, por separado, durante la producción de quesos de leche bovina (raza Holstein), en la Estación Agraria de la Universidad Nacional de Colombia, Sede Medellín "Paysandú" (Santa Elena, Medellín, Antioquia) y en la vereda San José del municipio de Santa Rosa de Osos (Antioquia); y la otra, durante la elaboración de queso caprino (raza Mestiza) en un aprisco del municipio de Sopetrán (Antioquia).
Aislamiento y detección de bacterias productoras de PHAs. A partir de cada una de las siete muestras obtenidas, se realizó un procedimiento de dilución seriada, siguiendo la metodología de Capuccino y Sherman (2007), sembrando 100 mL de las diluciones 1x10-3, 1x10-5 y 1x10-7, por esparcimiento con asa de vidrio, sobre cajas Petri con medio mínimo de sales minerales (MMS), pH 7,0, suplementado con 2% de glucosa, 0,2% de extracto de levadura y 1 mL L-1 (0,1% en acetona) del colorante rojo Nilo (Spiekermann et al., 1999). Las cajas Petri fueron incubadas bajo condiciones aeróbicas, a temperatura ambiente, por 72 h y las colonias resultantes, expuestas a un transiluminador ultravioleta a 340 nm, para seleccionar aquellas que presentarán fluorescencia. Dichas colonias fueron transferidas individualmente a cajas Petri con MMS y rojo Nilo, para reconfirmar su fluorescencia.
Las cepas que resultaron nuevamente positivas, fueron transferidas a medio agar nutritivo (AN), y evaluadas bajo tinción con el colorante azul Nilo, siguiendo la metodología de Ostle y Holt (1982) y utilizando un microscopio de fluorescencia Axiolab-Zeiss® (Alemania) a una longitud de onda de 450 nm y aumento de 1.000X. Las bacterias que presentaron fluorescencia rojo-naranja, indicativa de la producción de PHAs, se sometieron al proceso de tinción de Gram (Capuccino y Sherman, 2007), como base de selección del método de extracción de ADN, preservándose cada una de éstas a -20 °C en crioviales con glicerol al 30%.
Identificación molecular de bacterias. Las bacterias seleccionadas en las pruebas de tinción, fueron cultivadas durante 24 h en medio líquido Luria Bertani (LB), a 150 rpm y 30 ºC. Los cultivos fueron centrifugados a 4.000 rpm por 3 min, para obtener precipitados celulares y dar inicio a la extracción de ADN. Para las bacterias Gram negativas, se utilizaron 500 mL del buffer de extracción SDS (NaCl 10 mM, EDTA 25 mM, Tris-HCl 10 mM pH 8,0 y 100 mL de SDS 20%); mientras que, en aquellas Gram positivas se realizó un pre-tratamiento con 50 mL de lisozima (10 mg mL-1) a 37 ºC por 30 min, seguida por la adición del buffer de extracción de SDS. La integridad del ADN obtenido fue evaluada por electroforesis en gel de agarosa al 1% con buffer TBE 1X y 3 mL de bromuro de etidio (10 mg mL-1), visualizándose bajo luz ultravioleta con el sistema digital Bio Doc Analyze (Biometra®, Alemania).
]]> Identificación molecular de bacterias. Los aislamientos bacterianos fueron identificados a partir de secuenciación de regiones 16S del ADNr. Para esto, se amplificaron mediante PCR cerca de 1.440 pb de este gen, con los cebadores PA (5' AGAGTTTGATCCTGGCTCAG 3') y PC5B (5' TACCTTGTTACGACTT 3') (Kuske et al., 1997). Las condiciones de PCR y la secuenciación fueron similares a las reportadas por Sánchez et al. (2012). Las secuencias obtenidas con cada cebador, fueron editadas mediante el programa Bioedit 6.0.6. (Hall, 1999), construyéndose secuencias consenso y confirmándose su identidad por comparación con las bases de datos moleculares, mediante BLASTN (http://www.ncbi.nlm.nih.gov/BLAST/Blast.cgi). En adición, se obtuvieron del GenBank secuencias 16S del ADNr de bacterias relacionadas taxonómicamente con los microorganismos putativamente identificados mediante el BLASTN, realizándose un alineamiento con Clustal W (Hall, 1999) y construyéndose árboles filogenéticos por los métodos de Neighbor-Joining (NJ) y Máxima verosimilitud (ML), con 1000 iteraciones para determinar los valores de bootstrap. Las distancias genéticas se calcularon por el método de Kimura 2-parámetros, utilizándose el programa Mega 5.0 (Tamura et al., 2011).Detección del gen phaC. Para evaluar mediante PCR la presencia del gen phaC, se seleccionó al menos una cepa de cada género identificado por secuenciación del ADNr 16S, utilizándose cebadores dirigidos a los arreglos genéticos tipo I, II y IV (Tabla 1). No se evaluó la presencia del arreglo tipo III, por cuanto las bacterias que lo contienen generalmente habitan ambientes extremos y requieren medios selectivos para su aislamiento (Reddy et al., 2003). Con fines confirmatorios, se seleccionaron al menos dos amplicones por cada tipo de arreglo detectado, para proceder a su secuenciación directa, tal como se indicó anteriormente.
RESULTADOS Y DISCUSIÓN
Aislamiento y detección de bacterias productoras de PHAs. En este estudio se detectaron, mediante doble tinción con rojo Nilo en medio MMS suplementado con 2% de glucosa, 49 cepas bacterianas productoras de PHAs, que fueron agrupadas en 22 morfotipos por sus caracteríticas en medio AN (Tabla 2); siendo el sustrato de cachaza de caña, el que presentó el mayor número de aislamientos y morfotipos bacterianos (8 aislamientos/5 morfotipos), seguido por la melaza del Ingenio Incauca (8/4) y Sopetrán (7/4) y el lactosuero de la Estación Agraria Paysandú (8/3). Los sustratos que presentaron menor número de morfotipos productores de PHAs fueron el lactosuero caprino (3 aislamientos y 2 morfotipos) y el bagazo de caña, pues a pesar de presentar ocho aislamientos, éstos sólo representaban dos morfotipos bacterianos (Tabla 2). Treinta y ocho de estas cepas, distribuidas en 18 morfotipos, fueron reconfirmadas como productoras de PHAs con la prueba de tinción con azul Nilo. Las colonias de dichos aislamientos emitieron fluorescencia rojo-naranja cuando fueron expuestas a una longitud de onda de 450 nm, siendo evidentes las diferencias en sus patrones de acumulación de PHAs (Figura 1).
Estos resultados indican que ambos tipos de sustratos evaluados, presentan una alta diversidad de flora bacteriana con capacidad de síntesis de PHAs, lo que puede deberse a sus altos contenidos de carbono y bajos niveles de nitrógeno (residuos de caña de azúcar) o de fósforo (lactosueros). Trabajos previos realizados por De Lima et al. (1999) habían identificado los suelos de cultivo y los derivados de la caña de azúcar como nichos ecológicos óptimos para el aislamiento de bacterias productoras de PHAs, dado sus altos desbalances de C: N. Esta situación fue confirmada en Colombia por Moreno et al. (2007), quienes realizaron un proceso de aislamiento de bacterias productoras de PHAs, en la rizosfera de caña de azúcar cultivada en diferentes departamentos, y encontraron que al menos 291 de 440 aislamientos evaluados, podían acumular estos biopolímeros a partir de alguna de las tres fuentes de azúcar evaluadas (glucosa, fructosa y sacarosa). En forma similar, Naheed et al. (2012) aislaron de diversos residuos agroindustriales, bacterias del género Enterobacter con capacidad de acumular PHB en un 57% de su peso celular seco, utilizando como medio de fermentación melaza de caña de azúcar suplementada con 0,2% de sulfato de amonio. En el presente trabajo, se logró la obtención de un amplio número de morfotipos bacterianos a partir de subproductos de caña de azúcar, obteniéndose tanto bacterias Gram negativas, como Gram positivas; aunque fue evidente que los sustratos de bagazo y cachaza de caña de azúcar favorecieron el aislamiento de estas últimas, destacándose el alto número de morfotipos identificados como Bacillus megaterium (Tabla 2).
Con respecto a los lactosueros resultantes de la agroindustria de producción de quesos, se han realizado diferentes evaluaciones biotecnológicas que incluyen el uso de lactosa, su principal carbohidrato, como fuente de bioetanol, vinagre y de diferentes aditivos alimenticios (Koller et al., 2012). Young et al. (1994) reportaron por primera vez, la posibilidad de usar lactosueros como fuente de carbono para la síntesis de PHAs, utilizando la bacteria Pseudomonas cepacia (antes Burkholderia cepacia). Dicha bacteria demostró la capacidad de acumular a partir de lactosa, hasta 56% de PHB en peso seco celular, lo que representaba una eficiencia de conversión de 5 g L-1 de lactosuero. Posteriormente, Ahn et al. (2000, 2001) propusieron la utilización de cepas genéticamente modificadas de Escherichia coli con el operón de biosíntesis de PHAs de Alcaligenes latus, para la síntesis de bioplásticos a partir de lactosueros, alcanzando hasta 4 g/L/h de PHAs en procesos fermentativos por lotes y con altas concentraciones de lactosa (hasta 280 g L-1). Estos reportes coinciden con los resultados encontrados en este estudio, en los que fue posible la identificación de bacterias especialmente Gram negativas a partir de los sustratos de lactosueros bovinos y caprinos, destacándose en este sustrato la presencia de un morfotipo representante del género Pseudomonas, cuyos miembros son ampliamente utilizados a nivel biotecnológico para la síntesis y acumulación de PHAs (Reddy et al., 2003; Keshavarz y Roy, 2010).
]]> Identificación molecular de bacterias. Las amplificaciones por PCR con los cebadores PA y PC5B permitieron obtener amplicones de 1.440 pb (Figura 2) en las 27 bacterias seleccionadas para su identificación, que incluían al menos un representante de cada morfotipo (Tabla 2). El análisis por BLASTN indicó que diez de las cepas pertenecen al género Bacillus, tres a los géneros Lactococcus, Klebsiella y Enterobacter, dos a Pantoea; mientras que se identificó un representante en los géneros Enterococcus, Neisseria, Pseudomonas, Leuconostoc, Gluconobacter y Acinetobacter. Además, de una bacteria sólo determinada a nivel de la familia (Enterobacteriaceae). Estos resultados de BLASTN corresponden a un alineamiento local que conduce a identificaciones genéricas y putativas, pues dependen de la validez taxonómica de las accesiones depositadas en las bases de datos moleculares. Por lo tanto, para tener mayor confiabilidad en la identificación, se realizó un análisis filogenético con secuencias de referencia que presentan respaldo en la literatura científica (Patel, 2001; Janda y Abbott, 2007). Los dendrogramas resultantes presentaron topologías similares con ambos algoritmos (NJ y ML), lo que ofrece un soporte adicional a las inferencias taxonómicas realizadas. Por lo anterior, sólo se presenta el dendrograma de ML (Figura 3).El análisis filogenético incluyó además de 27 secuencias obtenidas en este estudio, 55 secuencias representativas de diferentes especies y como grupo externo (outgroup) se utilizó una secuencia de Deinococcus sp. (Accesión KC49323). El dendrograma resultante presentó dos clados principales que separaron las bacterias Gram negativas (I) de las Gram positivas (II). El primer clado se subdividió a su vez en tres subclados soportados por valores de bootstrap de 100%, que diferenciaron las Gamma (IA), Beta (IB) y Alfa (IC) proteobacterias, siendo el subclado IA el que incluyó mayor número (11) de bacterias Gram negativas obtenidas de todos los subproductos, con excepción de bagazo de caña. Este subclado, dividió a su vez las bacterias productoras de PHAs entre las familias Enterobacteriaceae, Moraxellaceae y Pseudomonadaceae, siendo identificadas a nivel genérico las cepas 11-lactosuero y 13-lactosuero (Klebsiella sp.), 34-cachaza, 12-lactosuero y 14-lactosuero (Enterobacter sp.), 6-melaza (Pantoea sp.), 26-melaza (Acinetobacter sp.) y 19-suero (Pseudomonas sp.); mientras que fue posible inferir la identificación a nivel de especie en este subclado IA, de los aislamientos 33-cachaza (Enterobacter oryzae) y 30-cachaza (Enterobacter cloacae). Lo anterior, fue, además, soportado por la matriz de identidad genética, en donde dichos aislamientos compartieron valores de 98 y 100%, con cepas de referencia de ambas especies (matriz no mostrada).
El subclado IB alojó a la cepa 16-lactosuero en conjunto con dos secuencias de referencia de Neisseria mucosa; sin embargo, al compartir niveles de identidad de 87%, no fue posible identificar dicha bacteria a nivel de especie. Por su parte el subclado IC, agrupó la cepa 24-melaza con acetobacterias del género Gluconobacter, aunque sólo compartió con estas 81% de identidad.
Por otra parte, el clado II representando las bacterias Gram positivas, presentó cuatro subclados con soportes de bootstrap superiores al 98%. El subclado IIA incluyó al aislamiento 20-melaza con diferentes especies del género Leuconostoc, mientras que el IIB presentó tres cepas obtenidas de lactosuero (8, 9 y 10) en conjunto con diferentes secuencias de Lactococcus lactis, subsp. lactis y subsp. cremoris. El subclado IIC representa el género Enterococcus e incluyó el aislamiento 15-lactosuero. Finalmente, el subclado IID agrupó todas las especies del género Bacillus, que se subdividieron en tres grupos soportados por valores bootstrap de 100% y que representan los complejos de especies B. subtilis, B. cereus y B. megaterium; siendo las cepas 37-melaza y 35-cachaza, representantes de los dos primeros complejos; mientras que siete cepas se identificaron como B. megaterium, lo cual se soportó, adicionalmente, por altos niveles en la matriz de identidad (>99%) con cepas de referencia de dicha especie (matriz no mostrada).
De las bacterias identificadas en este trabajo, ya se habían mencionado en la literatura como productoras de PHAs miembros de los géneros Enterobacter (Naheed et al., 2012), Klebsiella (Zhang et al., 1994); Pantoeae (Gasser et al., 2009), Acinetobacter (Reddy et al., 2003), Pseudomonas (Reddy et al., 2003), Neisseria (Kalia et al., 2007), Lactococcus (Tanaka et al., 1995) y Bacillus (Reddy et al., 2003); mientras que, hasta donde se conoce, dichos reportes no se han realizado para especies de los géneros Leuconostoc, Gluconobacter y Enterococcus, por lo que el estudio de dicha característica en las cepas aquí aisladas e identificadas, resultará prioritario en el futuro próximo. Para esto será necesario realizar procesos fermentativos con diferentes fuentes de carbono y condiciones operacionales, además de detectar, clonar y secuenciar los genes responsables de la biosíntesis de PHAs en dichas bacterias, de tal manera que se evalúe el tipo de su operón.
A nivel mundial, las bacterias Gram negativas productoras de PHAs más recurrentemente aisladas y utilizadas corresponden a las especies C. necator, A. latus, P. oleovorans, P. putida, E. coli recombinante y Azotobacter vinelandii; siendo C. necator la más empleada por su capacidad de acumular grandes cantidades de PHB, en un porcentaje cercano al 80% del peso seco celular, a partir de medios simples con fuentes de carbono económicas (Reddy et al., 2003; Keshavarz y Roy, 2010). Para el caso de las bacterias Gram positivas, B. megaterium es la bacteria más registrada como productora de PHAs (Reddy et al., 2003; Shamala et al., 2003). Esta bacteria ha sido aislada de una gran variedad de sustratos y desechos agroindustriales, así como utilizada en procesos fermentativos con diferentes fuentes de carbono, siendo posible a partir de la manipulación de las condiciones de crecimiento, reducir su esporulación y por tanto, inducir la acumulación de altas cantidades de bioplásticos (López et al., 2012). En Colombia se han adelantado diferentes estudios tendientes a detectar la presencia de bacterias productoras de PHAs a partir de diferentes sustratos y residuos de procesos agroindustriales (Moreno et al., 2007; Revelo et al., 2007; Franco et al., 2009; Sánchez et al., 2012). Recientemente, éstos últimos autores aislaron a partir de suelos contaminados con residuos del beneficio de fique (Furcraea bedinghausii) en el municipio de Guarne (Antioquia), cuatro cepas con potencial para producir PHAs, siendo identificadas como B. megaterium (dos cepas), B. mycoides y Gordonia sp. El gen PhaC fue detectado en los dos aislamientos de B. megaterium y mediante cromatografía de gases con detector selectivo de masas, fue posible develar al polihidroxibutirato (PHB) como el principal biopolímero acumulado en dichas bacterias. Ya que en el presente estudio, también se identificaron varias cepas de B. megaterium, su utilización en pruebas posteriores que evalúen diferentes sustratos y desechos agroindustriales como fuentes de síntesis de PHAs, resultará altamente promisorio para su posible escalado industrial en Colombia, más aún cuando existen reportes recientes de la posibilidad de aumentar la eficiencia en la producción de PHAS por parte de cepas de esta especie (hasta 65% de PHB), mediante el control de la concentración de amonio (0,2-0,4 g L-1) en sistemas de fermentación por lotes (Sabra y Aboud-Zeid, 2008).
Por otra parte, en el presente estudio, los lactosueros de origen bovino y caprino se caracterizaron por mostrar la mayor diversidad de morfotipos bacterianos productores de PHAs, seguramente como resultado de su riqueza nutricional, siendo identificadas en estos sustratos las bacterias Lactococcus lactis, Klebsiella sp., Enterobacter sp. y Pseudomonas sp. La utilización de dichas bacterias representa un potencial importante para Colombia, que ha logrado establecerse como el cuarto productor de lácteos en América Latina, con cerca de 6500 millones de litros/año (Proexport, 2011b). Diferentes trabajos han confirmado la utilidad de bacterias para transformar lactosueros en PHAs, incluyendo E. coli, Hydrogenophaga psedoflava, Azotobacter spp., LactoBacillus spp., C. necator, Haloferax mediterranei y P. hydrogenovora (Koller et al., 2012). En adición, existen informes sobre el mejoramiento en la eficiencia de síntesis de PHAs a partir de este sustrato y que pueden ser evaluados con las cepas obtenidas en el presente estudio. En este sentido, Ahn et al. (2000) registraron concentraciones finales de 92,6 g L-1 de PHB y altas productividades en su síntesis (2,57 g/L/h), a partir de lactosuero sometido a fermentación Fed Batch con la bacteria recombinante E. coli CGSC 4401, transformada con los genes de la biosíntesis de PHAs de A. latus. Durante el proceso los autores, estratégicamente, disminuyeron la concentración de oxígeno disuelto en el medio (DOC) por etapas, del 40% al 30% y luego al 15%. Cada vez que el DOC se redujo durante la fase activa síntesis de PHB, la tasa de síntesis de PHB aumentó de forma pronunciada.
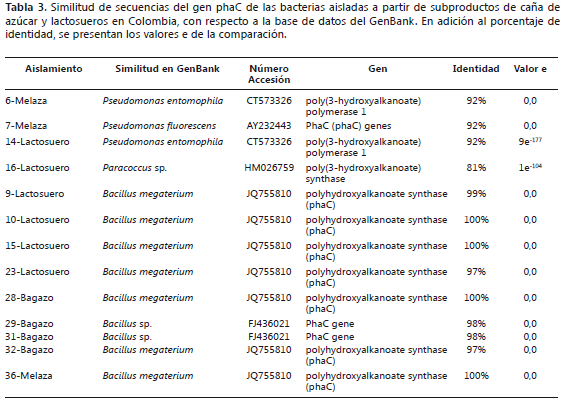
Detección del gen phaC. La identificación molecular de las bacterias bajo estudio, sirvió de base para realizar la selección de los cebadores más apropiados para la detección del gen phaC, siendo posible su confirmación en un subgrupo de siete de las cepas (Tabla 2) mediante la PCR anidada que utiliza los cebadores GD/G1R/G2R, y que generó amplicones de 491 pb (Figura 2). Adicionalmente, la utilización de los cebadores B1F/R dirigidos a amplificar una porción del gen phaC del tipo IV, permitió la obtención de amplicones de 590 pb en nueve cepas identificadas molecularmente como B. megaterium. La naturaleza de dichos amplicones fue confirmada mediante secuenciación directa en dos cepas, representando los morfotipos 1 y 13 y conteniendo el arreglo genético de biosíntesis de PHAs tipo II, y en cuatro cepas de los morfotipos 2, 9, 16 y 17, que presentaron el operón tipo IV; obteniéndose, con excepción de la cepa 16-lactosuero, valores de identidad en GenBank superiores al 92% con respecto al gen phaC de bacterias del género Pseudomonas y Bacillus sp., respectivamente (Tabla 3). La cepa 16-lactosuero, identificada como asociada filogenéticamente al género Neisseria, fue la excepción al presentar tan sólo un 82% de identidad con el gen phaC de la bacteria Paracoccus sp. (Accesión HM26759), lo cual no permite su ubicación en uno de los cuatro tipos de operones de biosíntesis de PHAs.
]]>
Este estudio abre la posibilidad de realizar un amplio rango de investigaciones y aplicaciones futuras, para la evaluación de sustratos y condiciones fermentativas, utilizando las bacterias aisladas e identificadas a partir de residuos de la caña de azúcar y lactosueros en Colombia. De gran interés resultará evaluar, no sólo su capacidad para metabolizar los mismos residuos a partir de los cuales fueron aisladas, sino también, otros subproductos y desechos agroindustriales producidos en Colombia y otros países tropicales, como aquellos generados en el procesamiento de palma de aceite, pulpa de frutas y de concentrados de animales.
CONCLUSIONES
Se logró el aislamiento de 38 cepas bacterianas que presentan potencial como productoras de PHAs, siendo identificadas 27 cepas, a nivel de género o especie, mediante secuenciación de regiones 16S del ADNr. Los lactosueros de bovinos y caprinos fueron los que presentaron mayor diversidad de bacterias, con miembros de los géneros Enterobacter, Klebsiella, Pseudomonas, Enterococcus, Lactococcus y Bacillus; mientras que, en los residuos de caña de azúcar se destacó el aislamiento repetido de B. megaterium.
Fue posible la detección del gen phaC, mediante PCR específica en aislamientos seleccionados que presentaron tinción positiva de PHAs con rojo y azul Nilo. Las secuencias obtenidas confirmaron los altos niveles de identidad de dicho gen, con respecto a la región correspondiente en los operones de biosíntesis de PHAs de los tipos II y IV depositados en las bases de datos moleculares.
AGRADECIMIENTOS
Esta investigación fue financiada por el proyecto DIME 20101007214. Se agradece a Catalina Pineda Molina del Laboratorio de Cultivo Tisular del CES, por su asistencia con las observaciones de microscopia de fluorescencia y al Ingenio Incauca por proveer los subproductos de la caña de azúcar.
]]> BIBLIOGRAFÍA
Ahn, W.S, S.J. Park and S.Y. Lee. 2000. Production of Poly(3-Hydroxybutyrate) by fed-batch culture of recombinant Escherichia coli with a highly concentrated whey solution. Applied and Environmental Microbiology 66(8): 3624-3627. [ Links ]
Ahn, W.S., S.J. Park and S.Y. Lee. 2001. Production of poly(3-hydroxybutyrate) from whey by cell recycle fed-batch culture of recombinant Escherichia coli. Biotechnological Letters 23(3): 235-240. [ Links ]
Basanta, R., M.A. García, J.E. Cervantes, H. Mata y G. Bustos. 2007. Sostenibilidad del reciclaje de residuos de la agroindustria azucarera: una revisión. Ciencia y Tecnología Alimentaria 5(4):293-305. [ Links ]
Capuccino, J. and N. Sherman. 2007. Microbiology: A Laboratory Manual. Benjamin Cummings, New York. 544 p. [ Links ]
Ciesielski, S., A. Cydzik-Kwiatkowska, T. Pokoj and E. Klimiuk. 2006. Molecular detection and diversity of medium-chain-length polyhydroxyalkanoates-producing bacteria enriched from activated sludge. Journal of Applied Microbiology 101(1): 190-199. [ Links ]
De Lima, T.C.S., B.M. Grisi and M. Bonato. 1999. Bacteria isolated from sugarcane agro ecosystem: their potential production of polyhydroxyalkanoates and resistance to antibiotics. Revista de Microbiología 30(1): 241-224. [ Links ]
Franco, M., D. Gómez, N. Castro y M. Rendón. 2009. Polihidroxialcanoatos en actinomicetos nativos de suelos colombianos. Revista Peruana de Biología 16(1): 115-118. [ Links ]
Gasser, I., H. Muller and G. Berg. 2009. Ecology and characterization of polyhydroxyalkanoate producing microorganisms on and in plants. FEMS Microbiology Ecology 70(1): 142-150. [ Links ]
Hall, T.A. 1999. BioEdit: a user-friendly biological sequence alignment editor and analysis program for Windows 95/98/NT. Nucleic Acids Symposium Series 41: 95-98. [ Links ]
Janda, J.M. and L.S. Abbott. 2007. 16S rRNA gene sequencing for bacterial Identification in the diagnostic laboratory: pluses, perils, and pitfalls. Journal of Clinical Microbiology 45(9): 2761-2764. [ Links ]
Kalia, V., S. Lal and S. Cheema. 2007. Insight in to the phylogeny of polyhydroxyalkanoate biosynthesis: Horizontal gene transfer. Gene 389(1): 19-26. [ Links ]
Keshavarz, T. and P. Roy. 2010. Polyhydroxyalkanoates: bioplastics with a green agenda. Current Opinion in Microbiology 13(3): 321-326. [ Links ]
Koller, M., A. Salerno, A. Muhr, A. Reiterer, E. Chiellini, S. Casella, P. Horvat and G. Braunegg. 2012. Chapter 2: Whey lactose as a raw material for microbial production of biodegradable polyester. pp. 19-60. In: Saleh, H. (ed.). Polyesters. InTech, China. 420 p. [ Links ]
Kuske, C.R., S.M. Bams and J.D. Busch. 1997. Diverse uncultivated bacterial groups from soils of the arid Southwestern United States that are present in many geographic regions. Applied Environmental Microbiology 63(9): 3614-3621. [ Links ]
Lau, N. and K. Sudesh. 2012. Revelation of the ability of Burkholderia sp. USM (JCM 15050) PHA synthase to polymerize 4-hydroxybutyrate monomer. AMB Express 2(41): 2-9. [ Links ]
Londoño, M., J. Sepúlveda, A. Hernández y J. Parra. 2008. Bebida fermentada de suero de queso fresco inoculada con LactoBacillus casei. Revista Facultad Nacional Agronomía Medellín 61(1): 4409-4421. [ Links ]
López, J.A., J.M. Naranjo, J.C. Higuita, M.A. Cubitto, C.A. Cardona and M.A. Villar. 2012. Biosynthesis of PHB from a new isolated Bacillus megaterium strain: outlook on future developments with endospore forming bacteria. Biotechnology and Bioprocess Engineering 17(2): 250-258. [ Links ]
McCool, G. and M. Cannon. 2001. PhaC and PhaR are required for polyhydroxyalkanoic acid synthase activity in Bacillus megaterium. Journal of Bacteriology 183(14): 4235-4243. [ Links ]
Moreno, N., I. Gutiérrez, D. Malagón, V. Grosso, D. Revelo, D. Suárez, J. González, F. Aristizábal, A. Espinosa and D. Montoya. 2007. Bioprospecting and characterization of poly-b-hydroxyalkanoate (PHAs) producing bacteria isolated from Colombian sugarcane producing areas. African Journal of Biotechnology 6(13): 1536-1543. [ Links ]
Naheed N., N. Jamil, S. Hasnain and G. Abbas. 2012. Biosynthesis of polyhydroxybutyrate in Enterobacter sp. SEL2 and Enterobacteriaceae Bacterium sp. PFW1 using sugar cane molasses as media. African Journal of Biotechnology 11(16): 3321-3332. [ Links ]
Ostle, A.G. and J.G. Holt. 1982. Nile Blue A as a fluorescent stain for poly-beta-hydroxybutyric acid. Applied and Environmental Microbiology 44(1): 238-241. [ Links ]
Parra, R.A., 2009. Lactosuero: importancia en la industria de alimentos. Revista Facultad Nacional de Agronomía Medellín 62(1): 4967-4982. [ Links ]
Patel, J.B. 2001. 16S rRNA gene sequencing for bacterial pathogen identification in the clinical laboratory. Molecular Diagnosis 6(4): 313-321. [ Links ]
PROEXPORT. 2011a. Sector Agroindustrial Colombiano, http://www.proexport.com.co; consulta: febrero 2013. [ Links ]
PROEXPORT. 2011b. Sector lácteo en Colombia. En: http://www.botschaft-kolumbien.de/descargas_proexport/berlin_2011/espanol/inversion/agroindustria/perfil_lacteo.pdf. 18 p.; consulta: abril 2013. [ Links ]
Reddy, C.S.K., R. Ghai, R. Rashmi and V.C. Kalia. 2003. Polyhydroxyalkanoates: an overview. Bioresource Technology 87(2): 137-146. [ Links ]
Rehm, B.H. and A. Steinbuchel. 1999. Biochemical and genetic analysis of PHA synthases and other proteins required for PHA synthesis. International Journal of Biological Macromolecules 25(1): 3-19. [ Links ]
Revelo, D., M.V. Grosso, N. Moreno and D. Montoya. 2007. A most effective method for selecting a broad range of short and medium chain-length polyhidroxyalkanoate producing microorganisms. Electronic Journal of Biotechnology 10(3): 348-357. [ Links ]
Sabra, W. and D.M. Aboud-Zeid. 2008. Improving feeding strategies for maximizing polyhydroxybutyrate yield by Bacillus megaterium. Research Journal of Microbiology 3(5): 308-318. [ Links ]
Sánchez, S., M. Marín, A. Mora y M. Yepes. 2012. Identificación de bacterias productoras de polihidroxialcanoatos (PHAs) en suelos contaminados con desechos de fique. Revista Colombiana de Biotecnología 14(2): 89-100. [ Links ]
Schlegel, H.G., R. Lafferty and I. KraussI. 1970. The isolation of mutants not accumulating poly-beta-hydroxybutyric acid. Archives of Microbiology 71(3): 283-294. [ Links ]
Shamala, T.R., A. Chandrashekar, S.V.N. Vijayendra and L. Kshama. 2003. Identification of polyhydroxyalkanoate (PHA)-producing Bacillus spp. using the polymerase chain reaction (PCR). Journal of Applied Microbiology 94(3): 369-374. [ Links ]
Sheu, D.S., Y.T. Wang and C.Y. Lee. 2000. Rapid detection of plyhydroxyalkanoate-accumulating bacteria isolated from the environment by colony PCR. Microbiology 146(8): 2019-2025. [ Links ]
Solaiman, D.K., R.D. Ashby and T.A. Foglia. 2000. Rapid and specific identification of medium-chain-length polyhydroxyalkanoate synthase gene by polymerase chain reaction. Applied Microbiology and Biotechnology 53(6): 690-694. [ Links ]
Spiekermann, P., B.H. Rehm, R. Kalscheuer, D. Baumeister and A. Steinbuchel. 1999. A sensitive, viable-colony staining method using Nile Red for direct screening of bacteria that accumulate poly-lyhydroxyalkanoic acids and other lipid storage compounds. Archives of Microbiology 171(2): 73-80. [ Links ]
Stubbe, J. and J. Tian. 2003. Polyhydroxyalkanoate (PHA) homeostasis: the role of the PHA synthase. Natural Products Reports 20(5): 445-457. [ Links ]
Tamura K., D. Peterson, N. Peterson, G. Stecher, M. Nei and S. Kumar. 2011. MEGA5: Molecular evolutionary genetics analysis using máximum likelihood, evolutionary distance, and máximum parsimony methods. Molecular Biology and Evolution 28(10): 2731-2739. [ Links ]
Tanaka, K., K. Katamune and A. Ishizaki. 1995. Fermentative production of poly(b-hydroxybutyric acid) from xylose via L-lactate by a two-stage culture method employing Lactococcus lactis IO-1 and Alcaligenes eutrophus. Canadian Journal of Microbiology 41(13): 257-261. [ Links ]
Young, F.K., R. James, K. Sheldon and W. May. 1994. Microbial Production of poly-b-hydroxybutyric acid from d-xylose and lactose by Pseudomonas cepacia. Applied and Environmental Microbiology 60(11): 4195-4198. [ Links ]
Zhang, H., V. Obias, K. Gonyer and D. Dennis. 1994. Production of polyhydroxyalkanoates in sucrose-utilizing recombinant Escherichia coli and Klebsiella strains. Applied and Environmental Microbiology 60(4): 1198-1205. [ Links ]
]]>