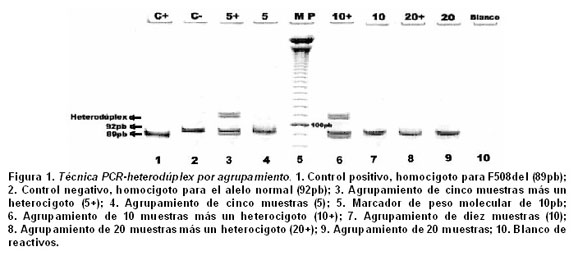
PCR-heterodúplex por agrupamiento: Implementación de un método de identificación de portadores de la mutación más común causal de fibrosis quística en Colombia
Lina Manuela Jay, Lic. Quim.1, Heidi Mateus, M.D.2, Dora Fonseca, Biol.2, Carlos Martín Restrepo, M.D.3, Genoveva Keyeux, Biol., Ph.D.4
1. Licenciada en Química, Universidad Distrital Francisco José de Caldas, Facultad de Ciencias y Educación, Bogotá, Colombia.
2. Profesora Titular, Unidad de Genética, Facultad de Medicina, Universidad del Rosario, Bogotá, Colombia. e-mail: hmateus@urosario.edu.co dfonseca@urosario.edu.co
3. Coordinador Unidad de Genética, Facultad de Medicina, Universidad del Rosario, Bogotá, Colombia. e-mail: cmrestre@urosario.edu.co
4. Profesora Asociada, Unidad de Genética, Universidad Nacional de Colombia, Bogotá. e-mail: gkeyeuxb@unal.edu.co
Recibido para publicación mayo 31 de 2005 Aceptado para publicación junio 15 de 2006
RESUMEN
]]> Introducción: La fibrosis quística (FQ) es una enfermedad autosómica recesiva frecuente, con una incidencia de 1 en 2,500 recién nacidos. La causan más de 1,300 mutaciones distintas en el gen regulador de la conductancia transmembranal de la fibrosis quística (CFTR). Sin embargo, la mutación F508del es la más común en la mayoría de las poblaciones.Objetivos: Desarrollo de una técnica rápida, de bajo costo y confiable que permita filtrar con rapidez a los portadores o afectados por esta mutación que mediante el asesoramiento genético, contribuya a disminuir la aparición de nuevos casos y a un diagnóstico temprano de los enfermos y así lograr un descenso en la morbilidad y la mortalidad asociadas con la fibrosis quística en Colombia.
Metodología: En el presente estudio se aplicó la técnica PCR-heterodúplex por agrupamientos, gracias al análisis de 400 muestras de sangre en papel filtro obtenidas de individuos asintomáticos para la FQ.
Resultados: En las pruebas de validación de la técnica PCR-heterodúplex por agrupamiento se obtuvo una eficiencia, reproducibilidad y especificidad de 100% y una sensibilidad de 92%.
Conclusiones: Se demostró la sensibilidad y reproducibilidad de la técnica PCR Directa-heterodúplex por agrupamientos de hasta 10 muestras, que se pueden emplear en programas para filtrar heterocigotos y afectados de F508del.
Palabras clave: Fibrosis quística; CFTR; Análisis heterodúplex; Mutación; Filtrado genético; Colombia.
PCR-heteroduplex by grouping: Rapid screening carrier method for cystic fibrosis F508del mutation in Colombia
SUMMARY
Background: Cystic fibrosis (CF) is the most frequent autosomal recessive disorder in the Caucasian population with an incidence of 1 in 2,500 newborns. More than 1,300 mutations in the cystic fibrosis transmembrane conductance regulator (CFTR) gene that causes CF have been described. However, mutation F508del is the most common mutation in different populations around the world.
Objective: To develop a fast, reliable and low-cost technique to screen carriers and affected individuals for the F508del mutation. This kind of analysis will have an impact on genetic counselling to decrease the incidence of new cases, in the early diagnosis and instauration of appropriate treatment to decrease morbidity and mortality associated to CF in Colombia.
]]> Methods: The reliability of the PCR-heteroduplex by grouping technique by analysis of 400 blood spot samples from asymptomatic CF patients was defined.Results: Using PCR-heteroduplex by grouping technique 100% efficiency, reproducibility and specificity and 92%sensitivity were found.
Conclusions: The sensitivity and reproducibility of the PCR-heteroduplex by grouping technique up to pooling of 10 samples were demonstrated. This kind of analysis could be used in heterozygotes and affected screening programs.
Key words: Cystic fibrosis; CFTR; Heteroduplex analysis; Genetic screening; Colombia.
La fibrosis quística (FQ) es la enfermedad genética autosómica recesiva de mayor frecuencia en la población caucásica, con una incidencia de 1 en 2,500 recién nacidos vivos. Los afectados con FQ presentan enfermedad pulmonar crónica, alteraciones digestivas como insuficiencia pancreática y elevación de los electrólitos en el sudor. La FQ se debe a mutaciones en el gen regulador de la conductancia transmembranal de la fibrosis quística (CFTR)1, localizado en el cromosoma 7q31.2, del que se conocen hasta la fecha más de 1,300 mutaciones o polimorfismos en este gen2; la mutación F508del es la más frecuente y se observa en 66% de los afectados a nivel mundial3. La frecuencia de portadores sanos (heterocigotos) en la población caucásica se ha estimado en 1 de cada 25 personas4.
En América Latina pocos países han informado estudios sobre el tema. Cuba es el país con la mayor incidencia de FQ (1/3,862)5 y en México se presenta en 1/9,000 nacimientos6; Costa Rica es el de menor frecuencia de la mutación F508del con 22.9%7 y Argentina el de mayor frecuencia (59.5%)8. En un estudio en hispanos de los Estados Unidos, que agrupa personas de casi toda América Latina, esta mutación se encontró en 48% de los afectados9.
En Colombia hasta el momento no se conoce la incidencia real de la enfermedad ni la frecuencia de portadores; algunos estudios previos hallaron en la mutación F508del una cifra cercana a 40%, con amplias variaciones regionales (25%-60%)10,11 y una frecuencia de portadores de 1 en 65, que se debe tomar a título indicativo, pues los estudios se hicieron en un pequeño número de controles sanos11,12.
La mutación F508del se encuentra en el exon 10 del gen CFTR y se produce por la deleción de tres pares de bases que llevan a la pérdida de un codon de fenilalanina en la proteína. Como es alta su prevalencia, es importante realizar estudios de portadores que permitan identificar las personas en riesgo de tener un hijo afectado por la enfermedad. Esta mutación convencionalmente se había diagnosticado mediante la reacción en cadena de la polimerasa (PCR) amplificando la región específica del exon 10 donde esta se encuentra. Sin embargo, como la mutación I507del, se encuentra muy cercana a la F508del y corresponde también a la deleción de tres pares de bases, este abordaje metodológico no permitiría diferenciar estas dos mutaciones, lo que puede llevar a errores diagnósticos. La PCR seguida del análisis de heterodúplex permite distinguir estas mutaciones, gracias a la formación, por complementariedad de las cadenas de ADN, de bandas específicas para cada una ellas. La ejecución de esta metodología ha permitido el estudio individual de portadores en otras poblaciones. Para llevar a cabo estudios poblacionales exhaustivos en personas sanas que permitan conocer indicadores epidemiológicos de una enfermedad que se presume común en el medio colombiano, se hace necesario poner en funcionamiento una técnica rápida, de bajo costo, eficiente y confiable que permita identificar los portadores o los afectados por la mutación F508del. En el presente estudio se practicó la técnica de PCR-heterodúplex, aplicada en el análisis simultáneo de varias muestras de sangre, para descubrir la mutación F508del en especímenes tomados sobre papel de filtro S&S903, a fin de ser utilizada en estudios poblacionales futuros y determinar la frecuencia de la mutación en el país o en pruebas diagnósticas de portadores y afectados por tal mutación.
MATERIALES Y MÉTODOS
]]> Muestras empleadas. El estudio se presentó al Comité de Ética de la Facultad de Medicina de la Universidad del Rosario para su aprobación. Se utilizó una colección de 400 muestras de sangre, tomadas del banco del laboratorio de biología celular y molecular, de personas sanas que antes firmaron un consentimiento informado aceptando participar anónimamente en estudios poblacionales; las muestras se habían conservado en papel filtro S&S903. Se incluyeron como controles muestras de 68 pacientes heterocigotos para la mutación F508del, provenientes del Banco de ADN de fibrosis quística y además muestras de 50 personas voluntarias, homocigotas para el alelo normal, estos genotipos se verificaron previamente con el estuche comercial de detección de mutaciones de Roche Molecular Systems21 y la técnica PCR-heterodúplex simple descrita por Raskin et al.13; esta última prueba se considera como el «método de referencia» para identificar la mutación F508del en el presente estudio.Técnica PCR-heterodúplex por agrupamiento. En cada papel de filtro se ubicaron más o menos 15 ml de sangre total (1 gota depositada directamente de la jeringa), volumen que permitía una saturación completa del papel, se secaron y almacenaron a temperatura ambiente. De cada muestra se extrajo un fragmento de 1 mm2, que se identificaron y agruparon en conjuntos de 5, 10 ó 20 muestras. En seguida se realizó una amplificación del ADN mediante la técnica de reacción en cadena de la polimerasa (PCR de la sigla en inglés), y se agregó a cada grupo de muestras una mezcla maestra que contenía: amortiguador 10X (Tris Base 10 mM pH 8.0 y KCl 50 mM), MgCl2 2.5 mM, Chelex 100X al 0.09%, dNTPs 0.07mM, 0.6 pmol/µl de cada uno de los primers, para un volumen final de 50 µl. Los primers utilizados fueron: -forward- 5’ GTT TTC CTG GAT TAT GCC TGG 3’ y -reverse-: 5’ ATG CTT TGA TGA CGC TTC TGT 3’1. Al comienzo de la reacción de PCR se hizo un choque térmico, pues se sometieron las muestras a tres ciclos de desnaturalización inicial (94°C por 6 minutos, luego desnaturalización a 96°C por 3 minutos y por último 3 minutos de renaturalización a 55°C), estos ciclos se utilizan para producir liberación del ADN e inactivar proteínas y metales pesados según la técnica descrita por Raskin et al.13, y Makowski et al.14 Después, se agregó una unidad de enzima TaqDNA polimerasa y se utilizó un programa de amplificación compuesto por desnaturalización prolongada a 94°C por 5 minutos, seguida por 40 ciclos de desnaturalización a 94°C por 45 segundos, alineamiento a 60°C por 45 segundos y extensión a 72°C por 45 seg y se culminó con un período de extensión prolongada de 72°C por 10 minutos.
Para el análisis de los productos amplificados por PCR se requiere la formación de un heterodúplex (híbrido de ADN que contenga una copia normal y una mutante en una doble hebra in vitro). El heterodúplex se obtuvo al desnaturalizar las cadenas amplificadas de ADN a 94°C por 10 minutos y luego una fase de renaturalización a 55°C por 25 minutos en las mezclas de muestras amplificadas. Posteriormente, las muestras se separaron con electroforesis en gel de poliacrilamida al 10%, durante 90 minutos a 120 voltios. Para cada corrido se incluyó un control positivo que correspondía a un paciente homocigoto para la mutación F508del, un control negativo homocigoto para el alelo normal y un blanco de reactivos. Los geles se visualizaron bajo luz ultravioleta teñidos con bromuro de etidio y los resultados se documentaron mediante fotografía en medio digital.
Determinación de la sensibilidad de la técnica. Se hicieron agrupamientos aleatorios de 5, 10 y 20 muestras de sangre obtenida en papel de filtro S&S903 de controles homocigotos para el alelo normal. A cada agrupamiento se le adicionó un control heterocigoto para la mutación F508del.
Además de identificar el número mínimo óptimo de muestras en un agrupamiento que permitiera identificar la presencia de un solo cromosoma portador de la mutación, se analizó la sensibilidad de la técnica mediante la relación S=a/(a+b), donde a son los verdaderos positivos y b son los falsos negativos15.
La sensibilidad obtenida se comparó con la determinada en la técnica PCR-heterodúplex simple descrita por Raskin et al.13
Determinación de la especificidad de la técnica. La especificidad se evaluó mediante la identificación de resultados falsos positivos, en diez agrupamientos compuestos por muestras de los controles sanos, negativos para la mutación F508del. Los resultados obtenidos se compararon con la especificidad determinada para la PCR heterodúplex sin agrupamientos.
Determinación de la reproducibilidad de la técnica. Un agrupamiento compuesto por 10 muestras de controles homocigotos para el alelo normal más un heterocigoto para la mutación F508del, se evaluó bajo las mismas condiciones de PCR-heterodúplex por agrupamiento en 10 ensayos independientes.
Comparación de los métodos. Una vez estandarizada la técnica, se tipificaron 400 muestras de sangre en papel de filtro organizadas en 40 agrupamientos (de 10 muestras cada uno) y se procedió a su análisis mediante PCR-heterodúplex por agrupamiento, además, estas 400 muestras habrían sido previamente tipificadas como homocigotas para el alelo normal, en forma individual con la técnica de PCR-heterodúplex simple descrita por Raskin et al.13
En cada uno de los ensayos se incluyó un control heterocigoto para la mutación y los hallazgos de los ensayos de agrupamiento se compararon con la técnica PCR-heterodúplex simple.
]]> La estrategia para identificar a los portadores de la mutación F508del en un programa masivo de filtrado, se basa en la formación de heterodúplex en los agrupamientos de muestras que contienen por lo menos un cromosoma mutante. Durante la reacción de denaturación y renaturación de estos grupos, se forman dos tipos de moléculas, los homodúplex y los heterodúplex. Los homodúplex corresponden a la hibridación de dos cadenas normales o de dos cadenas mutadas, mientras que los heterodúplex se forman por la hibridación estocástica de una cadena de ADN normal y una cadena mutada, que lleva a la formación de un bucle en una de las cadenas, cuya movilidad electroforética es diferente a la de los homodúplex16,17.Determinación de la sensibilidad de la PCR heterodúplex por agrupamiento. El análisis de los geles de poliacrilamida para los agrupamientos de 5 y 10 muestras demostró la presencia de las bandas correspondientes al alelo normal (92pb), al alelo mutante (89pb) y a los heterodúplex. En el agrupamiento de 20 muestras no fue posible descubrir la muestra heterocigota (Figura 1), lo que permitió establecer el límite de sensibilidad de la técnica en máximo 10 muestras (20 cromosomas). Se observó una mayor intensidad de la banda correspondiente al alelo normal con respecto a las otras, lo que es consecuencia de la mayor concentración de ADN del alelo normal (10 ó 20 cromosomas) con respecto al mutado (1 cromosoma).
De 40 agrupamientos (de 9 muestras homocigotas para el alelo normal más una muestra de un control heterocigoto para la mutación F508del), no se detectó el cromosoma mutado en tres. Estos resultados permiten estimar que la sensibilidad de la técnica fue 92.5%. Para la PCR-heterodúplex simple se determinó una ausencia total de falsos negativos, e indicó una sensibilidad de 100%. Con el programa Epi-Info 6 se determinó un valor predictivo positivo de 100% y un valor predictivo negativo de 92%.
Determinación de la especificidad de la técnica. En el análisis de 10 agrupamientos de personas con genotipo normal mediante PCR heterodúplex por agrupamiento no se encontró ningún resultado falso positivo, pues se obtuvo en todos los agrupamientos una única banda correspondiente al alelo normal de 92pb. Esto permite determinar que esta técnica tiene una especificidad de 100%, si se tiene en cuenta que los primers o cebadores sólo amplificaron el segmento de interés.
Determinación de la reproducibilidad de la técnica. Este parámetro se evaluó mediante repeticiones de montajes de PCR seguidos de la formación de heterodúplex empleando agrupamientos de muestras idénticas. El análisis fue realizado 10 veces independientes, y se obtuvieron los mismos resultados en cada proceso, luego se utilizó la prueba de concordancia Kappa no ponderada, y se alcanzó un valor de concordancia de 100%, Kappa de 1 y un valor p<0.000001 (Cuadro 1).
Comparación de los métodos. En las 400 muestras analizadas se compararon los resultados obtenidos mediante la técnica PCR-heterodúplex por agrupamiento y otros métodos ya validados como PCR-heterodúplex simple e hibridización con sondas alelo específicas (ASO) para la identificación de la mutación F508del. Se procedió al análisis estadístico mediante una prueba de concordancia Kappa no ponderada, con valores de concordancia entre 99.2% y 100%, respectivamente, con un valor p<0.00001 en ambas comparaciones (Cuadro 2).
DISCUSIÓN
]]> La FQ es una enfermedad autosómica recesiva letal que afecta gran cantidad de poblaciones alrededor del mundo. En Colombia no se conoce su frecuencia real, ni la de los portadores de la mutación F508del, que es la más frecuentemente asociada con esta entidad. Un par de estudios preliminares informaron una frecuencia de portadores cercana a 1 en 6511,12, valor que justifica la necesidad de emprender estudios en un mayor número de personas en diversas regiones del país para lograr así dar conclusiones precisas sobre esta frecuencia e incluso obtener cálculos del número probable de nuevos casos de afectados con la enfermedad.El análisis molecular de la F508del se ha visto como un método diagnóstico de portadores y afectados en varias poblaciones del mundo para descubrir en el primer caso, las parejas en riesgo de tener hijos afectados, ofrecer adecuados asesoramientos genéticos y en el segundo caso conseguir un diagnóstico temprano que permita establecer medidas que mejoren la calidad y el pronóstico de vida de los afectados.
Por lo general, los estudios moleculares se han hecho a través de PCR seguida de análisis electroforético, que permite identificar portadores gracias a la visualización de las bandas de amplificación del alelo normal y el mutado, que muestran 3 bases de diferencia, y de la banda del heterodúplex, que migra más lentamente. Dada la cercanía de la mutación I507del al sitio de la mutación F508del, no es posible mediante PCR diferenciar homocigotos para una u otra mutación, lo que podría llevar a errores de genotipificación molecular. En el presente trabajo, se efectuó un análisis de heterodúplex posterior a la PCR, mediante desnaturalización de los productos amplificados obtenidos, que permite diferenciar las personas hetero y homocigotas para estas dos mutaciones, debido a la formación de bandas de migración lenta, producto de interacciones no covalentes entre fragmentos distintos de ADN, con cambios en su conformación que resultan de la complementariedad incompleta de las hebras no idénticas. Esta metodología, tiene también ventajas sobre otras, como la PCR alelo especifica, pues en esta última se usa mayor cantidad de primers (tres en total, para identificar el alelo normal y el mutado) y requiere de montaje de tubos de PCR que por separado identifiquen el alelo normal y el mutado, además, se correría el riesgo similar al uso de PCR de no diferenciar las mutaciones F508del e I507del.
Si se tienen en cuenta las consideraciones de la aplicación masiva de análisis moleculares para identificar mutaciones como la F508del, es importante buscar alternativas que permitan disminuir costos en los procesos manteniendo estándares de calidad adecuados en términos de sensibilidad y especificidad. El uso de agrupamientos de muestras, permite en un solo paso analizar varias personas en búsqueda de los portadores, y aun de los afectados, disminuye hasta en 80% la cantidad de reactivos necesarios para la amplificación y en 90% el costo de los procesos de post-PCR. De igual forma, el tiempo necesario para el procesamiento de las muestras en una forma masiva es considerablemente inferior, porque para procesar 1000 muestras por métodos convencionales se necesitarían 3 meses aproximadamente, mientras que por la técnica PCR-heterodúplex por agrupamiento todo el proceso tardaría alrededor de 5 días.
Para evitar los pasos de la extracción del ADN convencional que aumentan los costos y el tiempo de procesamiento, se ejecutó la técnica de liberación de ADN basada en calor y el empleo de reactivos como el Chelex, al que se le ha atribuido una gran capacidad quelante para extraer ácido nucleico; aun así la sensibilidad que se informa en este estudio fue 92.5%, ya que en tres de 40 agrupamientos (que corresponden al análisis de 400 muestras) a los que se había introducido un heterocigoto tipificado antes molecularmente, no se detectó el cromosoma mutado; esto pudo ser el reflejo de una inadecuada liberación de ADN o de la presencia de impurezas en la muestra analizada, principalmente hemoglobina, compuesto que se ha asociado como un inhibidor de procesos de amplificación; este riesgo, es inherente a la metodología propuesta, pues al no usar técnicas de extracción convencionales de ADN, la calidad y cantidad de ADN liberado se afecta. Una posible solución a esta limitante, que podría disminuir los inhibidores es el uso de limpiezas previas al paso de liberación de ADN por calor y chelex, mediante el uso de detergentes como el dodecil sulfato de sodio (SDS), cuya función se ha asociado con el rompimiento de bicapas lipídicas de las membranas y con la unión a las cargas positivas de las proteínas cromosómicas liberando el ADN a la solución acuosa.
Mediante la técnica de PCR-heterodúplex por agrupamientos, se obtuvieron bandas de amplificación específicas para la mutación F508del en el exón 10 del gen CFTR, lo que se evidenció mediante electroforesis, por la visualización de bandas de peso molecular acorde con lo esperado; este hallazgo permite atribuir a la metodología una especificidad total, que evitaría falsos positivos. El análisis posterior con heterodúplex, obvia el riesgo metodológico más grande que se tiene, por la cercanía de la mutación I507del.
La realización de PCR «in situ», y como no se efectuó un protocolo convencional de extracción de ADN, demostró una excelente reproducibilidad, pues al analizar diferentes sacabocados de 1 mm de las mismas muestras en 10 ensayos distintos, se obtuvieron los mismos resultados, lo que indica que, bajo análisis estandarizados, la liberación de ADN y la eficacia de amplificación se mantienen constantes; este punto es de gran importancia porque en análisis masivos, es indispensable mantener valores de sensibilidad y especificidad que repercutan en un óptimo costo-beneficio de la prueba en la identificación de portadores de esta enfermedad genética.
En relación con el futuro, la puesta en marcha de esta metodología, permitirá llevar a cabo estudios masivos en búsqueda de los portadores de la mutación F508del en las diferentes regiones del país, con el fin de conocer en cuáles zonas se presenta un mayor número de portadores de esta mutación y por ende un mayor riesgo de nuevos casos de afectados con fibrosis quística. Así podría incluso justificarse la ejecución de un filtrado genético neonatal en recién nacidos, más aún si se tiene en cuenta que está plenamente confirmado que el costo para la identificación de portadores y afectados es menor que los costos del tratamiento de la enfermedad19.
Con este objetivo, esta estrategia molecular, representa un complemento a la medición de tripsina inmuno-reactiva, que no permite identificar portadores sanos y además genera muchos falsos positivos que van en contravención del costo beneficio necesario en un programa de filtrado20. Sin embargo, se debe tener en cuenta que aunque la mutación F508del es la más frecuente en Colombia, estos programas de filtrado neonatal se deberían complementar con el estudio de mutaciones adicionales seleccionadas según las frecuencias mutacionales informadas para cada una de las regiones del país12.
La realización de la PCR-heterodúplex por agrupamiento a partir de manchas de sangre en papel filtro, el mismo que se utiliza en los programas de filtrado neonatal para hipotiroidismo congénito, facilita la ejecución de esta prueba para identificar portadores y afectados por la mutación F508del. En este trabajo se demuestra que por la alta sensibilidad, reproducibilidad y especificidad de la técnica empleada, se convierte en una herramienta adecuada que cumple con los criterios técnicos que se deben considerar en su aplicación como método de filtrado. La correlación obtenida entre los resultados que se alcanzaron con esta técnica y las metodologías ya validadas, hace que esta prueba sea confiable, con un porcentaje de falsos positivos y negativos muy bajo, lo que garantiza así que no se presenten errores de diagnóstico.
]]> REFERENCIAS1. Riordan J, Kerem B, Rommens JM. Identification of cystic fibrosis gene: cloning and characterization of complementary DNA. Science 1989; 245: 1066-1072. [ Links ]
2. Fibrosis genetic analysis consortium. Online cystic fibrosis mutation data. [fecha de acceso noviembre 16, 2005]. URL disponible en: http://www.genet.sickkids.on.ca/cftr/
3. Bobadilla J, Macek M, Fine J, Farrell PM. Cystic fibrosis: A worldwide analysis of CFTR mutations-correlation with incidence data and application to screening. Hum Mutat 2002; 19: 575-606. [ Links ]
4. Lemna W, Feldman G, Kerem B. Mutation analysis for heterozygote detection and the prenatal diagnosis of cystic fibrosis. N Engl J Med 1990; 322: 291-296. [ Links ]
5. Collazo T, Magarino C, Chávez R, Suardiaz B, Gispert S, Gómez M, et al. Frequency of delta-F508 mutation and XV2C/KM19 haplotypes in Cuban cystic fibrosis families. Hum Hered 1995; 45: 55-57. [ Links ]
6. Orozco L, Velásquez R, Zielenski J. Spectum of CFTR mutations in Mexican cystic fibrosis patients: identification of five novel mutations (W1098C, 846delT, P750L, 4160insGGGG and 297-1G’!A). Hum Genet 2002; 106: 360-365.
7. Venegas PB, Novak JM, Oscar CA, Sánchez FL, Gutiérrez IG, Rivera JM, et al. Cystic fibrosis mutations in Costa Rica. Hum Biol 2003; 75: 179-188. [ Links ]
8. Visich A, Zielenski J, Castanos C. Complete screening of the CFTR gene in Argentine cystic fibrosis patients. Clin Genet 2002; 61: 207-213. Erratum in: Clin Genet 2002; 62: 343. [ Links ]
9. Grebe T, Seltzer WK, de Marchi X. Genetic analysis of Hispanic individuals with cystic fibrosis. Am J Hum Genet 1994; 54: 443-446. [ Links ]
10. Restrepo CM, Pineda L, Rojas-Martínez A. CFTR mutations in three Latin American countries. Am J Med Genet 2000; 91: 277-279. [ Links ]
11. Keyeux G, Sánchez D, Garavito P. Estudios moleculares en pacientes colombianos con fibrosis quística. Acta Med Colomb 1997; 22: 167-173. [ Links ]
12. Keyeux G, Rodas C, Bienvenu T. CFTR mutations in patients from Colombia: implications for local and regional molecular diagnosis programs. Hum Mutat 2003; 644: 1-7. [ Links ]
13. Raskin S, Phillips JA, Krishnamani MR, Vnencak-Jones C, Parker RA, Rozov T, et al. Cystic fibrosis genotyping by direct PCR analysis of Guthrie blood Sports. Am J Med Genet 1993; 46: 665-669. [ Links ]
14. Makowski GS, Davis EL, Hopfer SM. Enhanced direct amplification of Guthrie card DNA following selective elution of PCR inhibitors. Nucleic Acids Res 1995; 23: 3788-3789. [ Links ]
15. Cuckle HS, Wald N. Test using single markers. In: Antenatal and neonatal screening. 2nd ed. Wold N (ed.). Oxford: Oxford University Press; 2000. p. 3-22.
16. Nagamine C, Chan K, Lau Y-F C. A PCR artifact: Generation of heteroduplex. Am J Hum Genet 1989; 45: 337-339. [ Links ]
17. Anglani F, Picci L, Camporese C, Zacchello F. Heteroduplex formation in polymerase chain reaction. Am J Hum Genet 1990; 47: 169-170. [ Links ]
18. National Committee for Clinical Laboratory Standards. Blood collection on filter paper for neonatal screening programs. 2nd ed. (document LA4-A2). Approved standard. Vol. 12, N° 13. Villanova: NCCLS; 1992. [ Links ]
19. Huber KH, Mirkovic B, Nersesian R, Myers A, Saiki R, Bauer K. Survey of CF mutations in the clinical laboratory. BMC Clin Pathol 2002; 2: 1-8. [ Links ]
20. Schoos R, Verloes A, Bourguignon JP, Koulischer L. Programs of systematic screening in neonatology. Pharmaco-economic aspects. Rev Med Liege 1998; 53: 311-315. [ Links ] ]]>