10 U/l) que disminuyó significativamente con el tiempo de aplicación de la última dosis de la vacuna (p<0.01) y con la edad del trabajador (p<0.001), presentó mayor protección en 4.7% de los trabajadores que se habían aplicado 4 dosis si se comparan con los de 3 dosis y en sus medianas (209.8 vs. 130.07) (p<0.001), los otros factores no se encontraron asociados, género (p=0.463), consumo de cigarrillo (p=0.331) y exposición a sangre y/o hemoderivados (p=0.433). En el análisis multivariante la no protección acumulativamente se encontró asociada sólo con la edad, 40-44 (RRI=2.37, IC 95%:1.18, 4.78), >45 (RRI=3.58, IC 95%:1.83, 6.99) con respecto a <40 años. Conclusión: La vacuna recombinante Hepavax-Gene anti-HBs tiene alta efectividad en los trabajadores de la salud (90.7%) aunque presenta disminución de protección a mayor tiempo de aplicación de la última dosis y al aumentar la edad del trabajador.]]>
10 U/l), decreasing significantly with the worker’s age (p<0.001) and with the vaccine last dose administration time (p<0.01). Health workers with four doses compared to those with three doses had a 4.7% higher protection (antibody median 209.8 vs. 130.07, p<0.001). No association was found with gender (p=0.463), smoking (p=0.331) and blood exposure (p=0.433). Multivariate analyses found that no protection associated only with age (40-44 years HR=2.37, CI 95%:1.18,4.78 and >45 years HR=3.58, CI 95%:1.83,6.99). Conclusions: Although Hepavax-Gene recombinant hepatitis B vaccine (anti-HBs) has a high effectiveness in the health workers (90.7%) it presents a decrease in protection levels related to a higher worker’s age and a long vaccine last dose administration time.]]>
Inmunogenicidad de una vacuna recombinante anti-HBs en trabajadores de la salud, del Instituto de Medicina Legal de Colombia
Heber Siachoque, M.Sc.1, Milcíades Ibáñez, M.Sc.2
1. Coordinador de la Unidad de Inmunología, Facultad de Medicina, Universidad del Rosario, Bogotá, D.C., Colombia.
e-mail: hever.siachoque@urosario.edu.co
2. Profesor Universitario, Epidemiología, Facultad de Medicina, Universidad del Rosario, Bogotá, D.C., Colombia.
e-mail: mibanez@urosario.edu.co
Recibido para publicación febrero 22, 2007 Aceptado para publicación octubre 8, 2007
RESUMEN
]]> Objetivo: Evaluar la inmunogenicidad de la vacuna recombinante Hepavax-Gene para hepatitis B desde la última dosis administrada en trabajadores del INML.Materiales y métodos: Estudio de corte transversal en 603 trabajadores de la salud con mínimo 3 dosis de vacuna recombinante (0, 1, 6 meses) donde se midieron los niveles de anticuerpos anti-HBs con la técnica de ELISA entre diciembre de 2000 y enero de 2001 desde la aplicación de la última dosis de la vacuna, que varió entre 1 y 6 años.
Resultados: El grupo de estudio lo conformaron 344 hombres y 259 mujeres, con un promedio de edad de 38.8±7.3 años. El nivel de protección fue 90.7% (>10 U/l) que disminuyó significativamente con el tiempo de aplicación de la última dosis de la vacuna (p<0.01) y con la edad del trabajador (p<0.001), presentó mayor protección en 4.7% de los trabajadores que se habían aplicado 4 dosis si se comparan con los de 3 dosis y en sus medianas (209.8 vs. 130.07) (p<0.001), los otros factores no se encontraron asociados, género (p=0.463), consumo de cigarrillo (p=0.331) y exposición a sangre y/o hemoderivados (p=0.433). En el análisis multivariante la no protección acumulativamente se encontró asociada sólo con la edad, 40-44 (RRI=2.37, IC 95%:1.18, 4.78), >45 (RRI=3.58, IC 95%:1.83, 6.99) con respecto a <40 años.
Conclusión: La vacuna recombinante Hepavax-Gene anti-HBs tiene alta efectividad en los trabajadores de la salud (90.7%) aunque presenta disminución de protección a mayor tiempo de aplicación de la última dosis y al aumentar la edad del trabajador.
Palabras clave: Hepatitis B; Inmunogenicidad; Vacunación.
Immunogenicity of Hepavax-Gene recombinant hepatitis B vaccine in INML workers, Colombia
SUMMARY
Objective: To evaluate the immunogenicity of Hepavax-Gene recombinant hepatitis B vaccine in INML workers since the last administered doses.
Methods: Cross-sectional study on 603 health workers with at least three administered recombinant vaccine doses. Antibody levels (anti-HBs) were measured using the ELISA technique during December 2000 and January 2001, taking into account that the last dose in the vaccination varied between 1 and 6 years.
Results: A total of 344 men and 259 women with an age mean of 38.8±7.3 years were studied. Protection levels were found in 90.7% (>10 U/l), decreasing significantly with the worker’s age (p<0.001) and with the vaccine last dose administration time (p<0.01). Health workers with four doses compared to those with three doses had a 4.7% higher protection (antibody median 209.8 vs. 130.07, p<0.001). No association was found with gender (p=0.463), smoking (p=0.331) and blood exposure (p=0.433). Multivariate analyses found that no protection associated only with age (40-44 years HR=2.37, CI 95%:1.18,4.78 and >45 years HR=3.58, CI 95%:1.83,6.99).
]]> Conclusions: Although Hepavax-Gene recombinant hepatitis B vaccine (anti-HBs) has a high effectiveness in the health workers (90.7%) it presents a decrease in protection levels related to a higher worker’s age and a long vaccine last dose administration time.Keywords: Hepatitis B; Immunogenicity; Vaccination.
La hepatitis B es un problema de salud pública a nivel mundial, pues en áreas altamente endémicas, la tasa de portadores crónicos alcanza entre 15% y 25% de la población. Se calcula que hay aproximadamente 2 millardos de personas con evidencia serológica de haber desarrollado enfermedad hepática, una tercera parte de la población mundial, de la que 400 millones desarrollan infección crónica HBV: Se estima que anualmente la infección crónica y aguda causa más de 1’000,000 de muertes al año. La infección puede causar cirrosis y hepatocarcinoma; se han identificado 4 serotipos (adw, ayw, adr, ayr) y siete genotipos de la A a la G. En Suramérica los serotipos predominantes son adw4q, adw2 y ayw4 y el genotipo F1,2.
Colombia se considera una zona moderadamente endémica y mostró entre 1976 y 2001 un aumento en la tasa de incidencia3. Lurman en Bremen, Alemania en 1883 documentó la vía de transmisión del virus de la hepatitis B, que se realiza con mayor frecuencia por inoculación de sangre o hemoderivados4 y por exposición a secreciones de pacientes que tienen la infección, por lo que se relaciona mucho con empleos como los trabajadores de la salud que están expuestos a la sangre y a los hemoderivados4-6.
El descubrimiento de una vacuna contra el agente etiológico del virus de la hepatitis B constituye uno de los acontecimientos científicos más importantes del siglo XX y desde hace dos décadas es posible el empleo de la proteína recombinante del antígeno de superficie de la hepatitis B (HBsAg) como vacuna y por tanto la Organización Mundial de la Salud recomendó a partir de 1992, su uso rutinario a nivel mundial en los niños7-9. La ejecución de esta medida por parte de los países con alta endemia ha permitido observar un descenso en la infección aguda y en la cifra de portadores sanos9,10. Sin embargo, permanece en controversia la necesidad de dosis de refuerzo para mantener la protección contra la enfermedad, pues no se encuentran bien establecidas las bases del grado de memoria inmunológica que genera esta vacuna11,12.
A pesar de que la vacuna contra la HB se ha utilizado masivamente desde hace 20 años, y que en los individuos que responden esta vacuna genera altos títulos de anticuerpos, hay un grupo de la población vacunada que no contesta o que origina títulos bajos de anticuerpos; la explicación a este comportamiento puede ser la falta de memoria inmunológica que se asocia con disminución de la respuesta inmune celular T ayudadora mediada por linfocitos T CD411,13. La efectividad de las distintas vacunas recombinantes anti-HBs ha mostrado ser mayor de 95% con esquema completo (3 dosis) y un costo aproximado de cada dosis de US$7.00, actualmente en Colombia. Esta alta efectividad llevó a revacunar a las poblaciones más expuestas al riesgo de infección por el virus, como los trabajadores de la salud, y a establecer factores asociados que explicarían la pérdida de la protección como sufrir exposiciones a sangre o derivados, aumento de la edad, género masculino, el tabaquismo, tiempo de aplicación de la última dosis y número de dosis14.
La inmunidad protectora de la vacuna se ha medido en títulos de anticuerpos inmediatamente después de aplicar la última dosis pero no se ha hecho un seguimiento en el tiempo, asociado con variables como edad, género, exposición a sangre y hemoderivados.
En este estudio se muestra el nivel protector de la vacuna recombinante anti-HBs desde la aplicación de la última dosis que varió entre 1 y 6 años en los trabajadores del Instituto Nacional de Medicina Legal, INML; en Colombia y la evaluación de algunos factores asociados con la no respuesta.
MATERIALES Y MÉTODOS
]]> Estudio de corte transversal entre diciembre de 2000 y enero 2001 de una cohorte vacunada del INML de las diferentes regionales y seccionales de Colombia donde se generó un estudio serológico con el cual se determinaron los títulos de anticuerpos anti-HBs después de haber recibido el esquema completo de vacunación.Los criterios para incluir los trabajadores de la cohorte fueron, que cada persona tuviera como mínimo las tres dosis de la vacuna recombinante coreana Hepavax-Gene (0, 1, 6 meses), que apareciera en la base de datos de la oficina de Salud Ocupacional del INML en diciembre de 2000, con estudio serológico para títulos de anticuerpos anti-HBs y firma de aceptación del consentimiento informado; los criterios de exclusión fueron, antecedente de haber padecido HB o alguna de sus complicaciones, infección viral con medición de anticuerpos o bacteriana medida con cuadro hemático (PCR, proteína C reactiva). A los trabajadores que no presentaron niveles de anticuerpos protectores (<10 Ul) se les hizo un nuevo esquema de vacunación por parte del INML y la ARP del seguro social.
De los 714 funcionarios de la salud que trabajaban en las diversas regionales y seccionales del país, cumplieron los criterios de selección 603 personas. A cada uno de los trabajadores el personal de laboratorio de cada seccional le tomó una muestra de sangre total, previamente se firmó el consentimiento informado y después se aplicó el cuestionario para obtener datos por medio de entrevista directa con el trabajador.
A la muestra tomada a cada individuo se le determinaron los niveles de anticuerpos anti-HBs con la técnica de ELISA; los reactivos se adquirieron a ORGANON TEKNICA, cuyo personal efectuó la asesoría técnica para el montaje de las pruebas y establecer los niveles de protección según la siguiente lista: no protectores, si eran menos de 10 U/l; débilmente protectores, entre 10 y 99 U/l; protectores entre 100 y 209 U/l, y altamente protectores, títulos >210 U/l.
Análisis estadístico. La sistematización de datos se hizo con los paquetes SPSS 13.0 y STATA 8.0. Para describir las variables cualitativas se utilizó estadística descriptiva mediante distribuciones de frecuencia y porcentuales y en las variables cuantitativas el promedio y la desviación estándar. En la evaluación de normalidad de los niveles de anticuerpos se siguieron las pruebas de Kolmogorov-Smirnov y Shapiro Wilks a un nivel de significancia de 10% (p<0.10).
Para evaluar las diferencias entre los niveles de titulación de anticuerpos con edad, género, tabaquismo frecuente y exposición laboral a sangre y hemoderivados, se utilizó la prueba chi2 con corrección por continuidad de Yates (valores esperados >5) o la prueba exacta de razón de verosimilitud (valores esperados <5); de la misma forma se evaluaron estas relaciones con las pruebas no-paramétricas de Kruskall-Wallis y Mann Whitney. La tendencia en el tiempo y la edad se evaluó mediante la prueba chi2 para tendencia y con la razón de disparidad (OR), a un nivel de significancia de 5% (p<0.05).
Se calculó la probabilidad acumulativa de no protección para HB con el método de Kaplan Meier teniendo en cuenta el tiempo de última dosis con los factores de edad, género, exposición a sangre y número de dosis; las comparaciones entre los grupos se hicieron con la prueba no-paramétrica Log Rank a un nivel de significancia de 1% (p<0.01) por tratarse de pruebas independientes que elevan el nivel de significancia.
Para analizar los factores en conjunto que expliquen la no protección de anticuerpos para HB desde el tiempo de la última dosis, se utilizó el modelo de riesgos proporcionales instantáneos (RRI) de Cox, donde previamente se evaluó la proporcionalidad de los riesgos mediante la prueba de bondad de ajuste de Schonfeld (Biométrica, 1982)15, a un nivel de significancia de 5% (p<0.05).
RESULTADOS
Características demográficas. El grupo de estudio lo conformaron 603 personas que cumplieron con los criterios de selección, donde el promedio de edad ± la desviación estándar del grupo de estudio fue 38.8±7.3 años, la mínima edad fue 21 años y la máxima, 63 años; el género más frecuente fue el masculino (57%). Las ocupaciones más comunes fueron: patología, (40.8%); clínica, (11.3%); toxicología, (7.1%); y administrativos, (5.5%); las otras ocupaciones fueron menores de 5%.
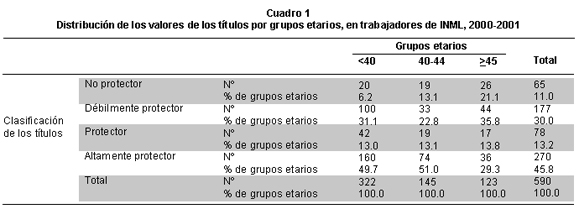
]]> Niveles de titulación de anti-cuerpos de protección al virus de HB. En la evaluación de los niveles de titulación de anticuerpos en el personal del INML se encontró: No protector, 9.3% (n=55); débilmente protector, 29.9% (n=180); protector, 59.5% (n=359); y altamente protector, 1.3% (n=8). La no protección se encontró relacionada de manera significativa en forma directa con la edad (p<0.001, prueba exacta de razón de verosimilitud), con una tendencia significativa, menor en los <40 años y en aumento en el grupo de 40 a 44 años (OR=3.12) y de 45 y más años (OR=5.1) (p<0.001, chi2 de tendencia) (Cuadro 1).Por género no se encontraron diferencias significativas en los niveles de anticuerpos, se mostraron sin protección 9.9% de los hombres y 8.5% en las mujeres (p=0.463, razón de verosimilitud exacta), tampoco hubo diferencias significativas con consumo de cigarrillo (11.3% vs. 8.9%) (p=0.331, razón de verosimilitud exacta), ni con la frecuencia de consumo (p=0.891, razón de verosimilitud exacta), ni con exposición a sangre y/o hemoderivados por parte de los trabajadores (p=0.433, razón de verosimilitud exacta). En general el número de cuatro dosis mostró mayor protección significativamente que con tres dosis (94.4% vs. 89.7%) (p<0.001), de la misma forma con sus medianas de niveles de anticuerpos anti-HBs (209.8 vs. 130.07) (p<0.001, Mann Whitney).
Niveles de titulación de anti-cuerpos en relación con la última dosis. Se encontró menor protección a medida que el tiempo de aplicación de la última dosis fue mayor. Inicialmente de 7.6% al primer año y hasta valores de 23.1% a los 5 años y 17.1% a los 6 años; siendo muy similar en los primeros 4 años, al comparar con los 5 años (OR=4.3) y con los 6 años (OR=2.36) mostrando tendencia significativa (p=0.00245, chi2 de tendencia), y de la misma forma año por año entre las medianas (p=0.006, Kruskall-Wallis), siendo significativa entre el primer año (186) con el quinto (59.1) y sexto año (65) (Gráfica 1).
El riesgo acumulativo de no protección desde el tiempo de aplicación de la última dosis de la vacuna de HB fue mayor con el aumento de edad de los trabajadores, y significativo entre los menores de 40 años con el grupo etario de 40 a 44 años (p=0.0094, prueba Log Rank) y con los de 45 y más años (p<0.0001, prueba Log Rank) (Gráfica 2).
El la distribución de la probabilidad acumulativa de no protección, no se hallaron diferencias significativas por número de dosis, siendo muy similar para los últimos tres años de aplicación de la última dosis de la vacuna y con algunas diferencias entre los 4 y 6 años con respecto a los primeros 3 años (p=0.1640, prueba Log Rank) (Gráfica 3).
De la misma forma no se vieron diferencias significativas con género (p=0.5662, prueba Log Rank), ni exposición a sangre o derivados (p=0.6769, prueba Log Rank).
]]> En el modelo de análisis multivariante de riesgos proporcionales instantáneos (RRI) de Cox se encontró un riesgo mayor significativo en los trabajadores de 40 a 44 años de 1.4 y en los de 45 años y más de 2.6 con respecto a los menores de 40 años de no protección de anticuerpos de HB desde el tiempo de aplicación de la última dosis que varió entre 1 y 6 años, ajustando por las otras variables del modelo (Cuadro 2).DISCUSIÓN
El personal de salud es una de las poblaciones con mayor riesgo ocupacional de desarrollar HB y por tanto es de vital importancia hacer la vacunación con esquema completo mediante vacuna recombinante que ha mostrado una alta eficacia en el nivel de protección15-17.
A pesar del nivel de efectividad de los productos biológicos utilizados con antígeno de superficie se encontraron con alguna frecuencia niveles de no protección en las personas vacunadas con esquema completo. En este estudio se evaluaron 603 trabajadores de la salud con una edad promedio de 38.8±7.3 y mayor frecuencia de hombres (57%); se encontró una cifra de no protección de 9.3% (<10 U/l) entre 1 y 6 años de la última aplicación de la dosis, más que la informada en un estudio similar en 485 trabajadores de la salud en Chile, cuya edad promedio fue 35.8 años y hubo mayor frecuencia de mujeres. En Chile se utilizó la vacuna recombinante anti-HB (Engerix B ®, Glaxo Smith-Kline) con aplicación de 3 dosis del esquema completo por primera vez (0, 1 y 6 meses) y al evaluar los niveles de anticuerpos postvacunación entre los 3 y 6 meses, se encontró una no-protección de 4.3%16. En otro estudio en 165 trabajadores de la salud en Perú, con un promedio de edad de 41±8 años y mayor frecuencia de género femenino (60%) con un esquema completo con la vacuna recombinante anti HB (Engerix B) a 0, 1 y 2 meses el nivel de anticuerpos se midió a los 3 meses postvacunación y hubo 5.5% de no-protección17. El presente estudio mostró un nivel de menor protección explicado por el mayor tiempo desde cuando se aplicó la última dosis de vacunación que varió entre 1 y 6 años siendo para el último año de aplicación, 7.6% y 19.4% entre los 5 y 6 años de aplicación de manera similar como se mostró también con las medianas de los niveles de anticuerpos anti-HB (Gráfica 1).
Esto concuerda con lo visto en los diferentes estudios, que a mayor tiempo de aplicación del esquema completo, hay menor protección anti-HB. Otros factores que se informaron en estudios epidemiológicos de observaciones como asociados para explicar la no-protección postvacunación completa son el género masculino, el aumento de la edad, el tabaquismo y obesidad16,17. En los trabajadores de la salud del INML por género no se encontraron diferencias significativas, tampoco el consumo de cigarrillo al contrario de los informes en los trabajadores de la salud del Perú donde sí hubo esas asociaciones16. Tampoco se encontró relacionado con exposición a sangre y/o hemoderivados; el índice de masa corporal para evaluar obesidad no se midió en este estudio por los problemas de validez y confiabilidad que se pueden generar al obtener la talla y peso mediante entrevista; se apreciaron diferencias significativas con la madurez, pues fue mayor la probabilidad de no protección con el incremento de la edad, en el grupo de 40 a 44 años (OR=3.12) y de 45 y más años (OR=5.1) con respecto a los menores de 40 años, de la misma forma al evaluar el riesgo acumulativo entre 1 y 6 años de aplicación de la última dosis se encontró mayor riesgo de no-protección en los trabajadores de 40 y más años del INML como los informes sobre los y trabajadores de salud de Chile y Perú16,17.
El número de dosis de la vacuna recombinante como esquema completo es de tres aunque se aplica una dosis de refuerzo y completa cuatro en total. En los diversos estudios no ha habido diferencias significativas con el refuerzo y por esto lo recomendable es aplicar sólo el esquema completo; en este estudio en general fue mayor la protección con cuatro dosis en 4.7% que con tres dosis y alta diferencia en sus niveles; al analizar el riesgo acumulativo de no protección desde la última dosis que varió entre 1 y 6 años fue muy similar para los últimos tres años pero mostró diferencias a los 4, 5 y 6 años y con tendencia de mayor protección para los trabajadores con aplicación de cuatro dosis.
En el análisis multivariado que incluía como factores el género, la edad, el tabaquismo, la exposición a sangre y el número de dosis para evaluar la no-protección durante el período de 1 a 6 años de aplicación de la última dosis de la vacuna, apenas la edad se encontró asociada significativamente, pues hubo notable riesgo proporcional instantáneo de no-protección anti-HB en los trabajadores de 40 a 44 años (RRI=2.4) y fue superior en los mayores de 45 años y más (RRI=3.6) en comparación con los menores de 40 años. Esta apreciación es semejante para lo obtenido en el personal de salud en Chile16. En efecto, hubo una tendencia no significativa de menor protección con tres dosis comparada con cuatro dosis (OR=1.9) (p=0.118).
En los trabajadores de la salud del INML en Colombia, la vacuna recombinante anti-HB dio un efecto protector alto (90.7%) aunque sus niveles sí muestran disminución significativa desde la aplicación de la última dosis del esquema que fue mayor entre los 4 y los 6 años. Como los precios son altos se debe medir con prioridad en trabajadores de la salud mayores de 40 años y aplicar la última dosis antes de 3 años, cuando empieza a disminuir la protección, aunque es importante medir después del suministro de la ultima dosis (1-3 meses) para identificar grupos de riesgo e intervenir en ellos a fin de disminuir el riesgo de adquirir HB. A pesar de que la cuarta dosis eleva los costos de la vacunación, se sugiere administrarla debido a que ésta aumenta los niveles de anticuerpos protectores durante los años que siguen a la aplicación.
AGRADECIMIENTOS
]]> Al Departamento de Salud Ocupacional del INML, por su valiosa asistencia en la obtención de las muestras para cuantificar los anticuerpos séricos. A la ARP del Seguro Social por permitir la titulación de anticuerpos.REFERENCIAS
1. Fattovich G. Natural history of hepatitis B. J Hepatol 2003; 39: 50-58. [ Links ]
2. Horng J, Shinn D. Global control of bepatitis B virus infection. Lancet Infect Dis 2002; 2: 395-403. [ Links ]
3. Instituto Nacional de Salud, Dirección General de Salud Pública Subdirección de Epidemiología y Laboratorio Nacional de Referencia. Sistema de Vigilancia en Salud Pública. Boletín Epidemiológico Semanal, Semana Epidemiológica Nº 49, diciembre 1 a 7 de 2002. [ Links ]
4. Mahoney J. Update on diagnosis, management, and prevention of hepatitis B virus infection. Clin Microbiol Rev 1999; 12: 351-366. [ Links ]
5. Hesham R, Zamberi S, Tajunisah ME, Ariza A, Ilina I. Hepatitis B immunization status among health care workers in two Kuala Lumpur hospitals. Med J Malaysia 2005; 4: 407-410. [ Links ]
6. Kermode M. Healthcare worker safety is a pre-requisite for injection safety in developing countries. Int J Infect Dis 2004; 8: 325-327. [ Links ]
7. Dienstag JL, Stevens CE, Bhan AK, Szmuness W. Hepatitis B vaccine administered to chronic carriers of hepatitis B surface antigen. Ann Intern Med 1982; 96: 575-579. [ Links ]
8. Pol S, Driss F, Michel ML, Nalpas B, Berthelot P, Brechot C. Specific vaccine therapy in chronic hepatitis B infection. Lancet 1994; 344: 342. [ Links ]
9. Dikici B, Kalayci AG, Ozgenc F, Bosnak M, Davutoglu M, Ece A, et al. Therapeutic vaccination in the immunotolerant phase of children with chronic hepatitis B infection. Pediatr Infect Dis J 2003; 22: 345-349. [ Links ]
10. Yalcin K, Acar M, Degertekin H. Specific hepatitis B vaccine therapy in inactive HBsAg carriers: a randomized controlled trial. Infection 2003; 31: 221-225. [ Links ]
11. Ren F, Hino K, Yamaquchi Y, Funatsuki K, Hayashi A, Ishiko H, et al. Cytokine-dependent anti-viral role of CD4-positive T cells in therapeutic vaccination against chronic hepatitis B viral infection. J Med Virol 2003; 71: 376-384. [ Links ]
12. Bauer T, Jilg W. Hepatitis B surface antigen-specific T and B cell memory in individuals who had lost protective antibodies after hepatitis B vaccination. Vaccine 2006; 24: 572-577.. [ Links ]
13. Zhuang GH, Yan H, Wang XL, Hwang LY, Wu Q, Wang LR, et al. Hepatitis B revaccination in healthy non-responder Chinese children: five-year follow-up of immune response and immunological memory. Vaccine 2006; 24: 2186-2192.. [ Links ]
14. Dannetun E,Tegnell A, Torner A, Giesecke J. Coverage of hepatitis B vaccination in Swedish healthcare workers. J Hosp Infect 2006; 63: 201-204[ [ Links ]STANDARDIZEDENDPARAG]
15. Kleinbaum D. Survival analysis A self learning text. New York: Springer; 1996. [ Links ]
16. García P, De la Cerda G, Calvo M,Godoy R, Covarrubias C, Potin M, et al. Inmunogenicidad de una vacuna recombinante anti-hepatitis B en personal de la salud. Rev Chil Infectol 2002; 19: 133-139. [ Links ]
17. Lozano A, Caycho J, Antúnez A, Vera D, Posadas D. Inmunogenicidad y eficacia de una nueva vacuna recombinante de hepatitis B en el Perú. Rev Gastroenterol (Perú) 2003; 23:259-264. [ Links ] ]]>