Células madre hematopoyéticas, generalidades y vías implicadas en sus mecanismos de auto-renovación
Hematopoietic stem cells, overview and pathways implied on their self-renewal mechanisms
Claudia Mera Reina,1 Angélica Roa Lara2 y Sandra Ramírez Clavijo3
1. MD, MSc Investigadora, Laboratorio de Biología Celular y Molecular, Departamento de Ciencias Básicas, Facultad de Medicina, Universidad del Rosario. claudiamera@gmail.com.
2. BSc, MSc (Asp), Estudiante de Maestría Ciencias Biomédicas, Facultad de Medicina-Facultad de Ingeniería Mecánica Universidad del Rosario-Universidad de Los Andes. anyeliro@gmail.com.
3. MSc, PhD Directora Departamento de Ciencias Básicas, Facultad de Medicina, Universidad del Rosario. sramire@urosario.edu.co. Correspondencia: Claudia Mera Reina: Carrera 24 63C-69 Tel. 571 3474570 ext. 380.
Recibido: noviembre de 2006 Aceptado: marzo de 2007
Resumen
El tejido sanguíneo está compuesto en un 45% aproximadamente por células y derivados de éstas, con una vida media que oscila entre 120 días para los eritrocitos y alrededor de 3 años para ciertos tipos de linfocitos. Esta pérdida es compensada gracias a la actividad del sistema hematopoyético y a la presencia de una población de células primitivas inmaduras conocidas como Células Madre Hematopoyéticas (CMHs) encargadas del proceso de hematopoyesis, activo desde el inicio de la vida fetal y que genera cerca de 2 x 1011 eritrocitos y 1010 células blancas por día (1). Las CMHs poseen la capacidad de auto-renovarse y diferenciarse a múltiples linajes, se ubican en un nicho particular y tienen marcadores de superficie que las identifican, como por ejemplo el antígeno CD34. Recientemente se ha podido avanzar en el entendimiento de la biología básica de los procesos celulares que rigen los mecanismos de auto-renovación, diferenciación y proliferación de las CMHs, y de la participación de diferentes vías de señalización (Hedgehog, Notch y Wnt) en estos procesos, los cuales controlan el comportamiento in vivo e in vitro de las CMHs. Todo esto es de vital importancia para la implementación y generación de alternativas terapéuticas con CMHs, para diversas enfermedades entre ellas las hematológicas, como por ejemplo las leucemias.
]]> Palabras clave: Célula Madre Hematopoyética, quiescencia, auto-renovación, notch, wnt, hedgehog.Abstract
Blood tissue is composed approximately in 45% by cells and its derivatives, with a life span of around 120 days for erythrocytes and 3 years for certain type of lymphocytes. This lost is compensated with the hematopoietic system activity and the presence of an immature primitive cell population known as Hematopoietic Stem Cells (HSCs) which perform the hematopoiesis, a process that is active from the beginning of the fetal life and produces near to 2 x 1011 eritrocytes and 1010 white blood cells per day (1). Hematopoietic Stem Cells are capable of both self-renewal and differentiation into multiple lineages, are located in a particular niche and are identified by their own cell surface markers, as the CD34 antigen. Recently it has been possible to advance in the understanding of self-renewal, differentiation and proliferation processes and in the involvement of the signaling pathways Hedgehog, Notch and Wnt. Studying the influence of these mechanisms on in vivo and in vitro behavior and the basic biology of HSCs, has given valuable tools for the generation of alternative therapies for hematologic disorders as leukemias.
Key words: Hematopoietic Stem Cells, quiescence, self-renewing, notch, wnt, hedgehog.
INTRODUCCIÓN
Las células madre son un grupo de células que se caracterizan por su capacidad de autorenovación a lo largo de la vida de un individuo y por responder a señales o estímulos generados en el micro ambiente donde se encuentran, para comprometerse en la diferenciación hacia linajes celulares con características y funciones especializadas (2). Estas células se pueden clasificar de dos maneras: i) Según el tejido de origen en células madre embrionarias o adultas ii) Según su potencial de diferenciación en células totipotenciales, pluripotenciales, multipotenciales y unipotenciales. Las células totipotentes son aquellas capaces de dar origen a un organismo completo y a un tejido extraembrionario; las células madre pluripotentes producen células derivadas de cualquiera de las tres capas embrionarias, mesodermo, endodermo y ectodermo; las células multipotentes generan todos los tipos celulares derivados de una sola capa embrionaria (3). Entre este tipo de células se encuentran las células madre neuronales, hematopoyéticas y mesenquimales. Por último, las células madre con un menor potencial para diferenciarse son conocidas como unipotenciales. Un ejemplo de éstas son las células madre epidérmicas encontradas en la capa basal de la piel y que únicamente producen escamas queratinizadas (4).
Cada día son más los estudios realizados sobre células madre hematopoyéticas, dado que pueden mantener su carácter primitivo cuando son manipuladas en el laboratorio, preservando su capacidad de proliferación y diferenciación in vitro hacia todos los linajes hematopoyéticos. Por esta razón han sido usadas exitosamente en el tratamiento de pacientes con alto riesgo de enfermedades hematológicas recurrentes, síndromes con falla de médula ósea, estados inmunodeficientes hereditarios y desórdenes metabólicos. A pesar de saber con certeza que la médula ósea y la sangre de cordón umbilical son fuentes adecuadas para su obtención, la cantidad de células aisladas es muy limitada lo que imposibilita su uso a gran escala, de ahí la necesidad de contar con condiciones óptimas de cultivo que permitan expandirlas in vitro para obtener una cantidad suficiente para ser usadas en transplantes. Para que estas técnicas de cultivo en el laboratorio sean exitosas primero es necesario adelantar investigaciones básicas que permitan entender los procesos de proliferación y diferenciación que conducen a la obtención tanto de un mayor número de células como de diversos linajes de las mismas, para simularlos en el laboratorio. El propósito de este artículo es realizar una revisión acerca de los conceptos básicos sobre las CMHs, sus principales características, la manera de identificarlas molecularmente, así como de los mecanismos implicados en procesos de auto-renovación.
GENERALIDADES
El sistema hematopoyético tiene como función retirar de la circulación las células viejas o las defectuosas, eliminarlas y reemplazarlas por nuevas. Este sistema está constituido por un conjunto de células de la médula ósea, de la sangre y del sistema linfoide que dan origen a todos los tipos de células sanguíneas a partir de una célula madre hematopoyética (CMH). Las CMHs poseen tres características básicas: primero, son multipotentes, es decir, tienen el potencial de generar los linajes sanguíneos: la línea roja que produce los eritrocitos, la línea blanca que produce células de diferentes tipos como el de tipo linfoide: linfocitos B y T, y el tipo mieloide: basófilos/mastocitos, eosinófilos, neutrófilos/ granulocitos, y monocitos/macrófagos, también genera la línea trombocítica que da origen a megacariocitos/plaquetas. Segundo, las CMHs tienen un alto potencial proliferativo, es decir que son capaces de dividirse y producir un gran número de células maduras durante la vida del individuo. Tercero, las CMHs tienen alta capacidad de generación de nuevas células madre idénticas, manteniendo una división de tipo simétrico, capacidad conocida como auto-renovación. Esta propiedad es muy importante debido a que múltiples procesos producen estrés fisiológico en el organismo, con un consumo exagerado de determinadas poblaciones celulares sanguíneas, que de no ser por la capacidad de auto-renovación de las CMHs y su posterior compromiso hacia precursores más maduros se verían reducidas (5, 6).
En el sistema hematopoyético, las células madre son heterogéneas con respecto a su habilidad de auto-renovarse, para distinguirlas se clasifican en células madre hematopoyéticas a largo plazo (CMH-LP) y células madre hematopoyéticas a corto plazo (CMH-CP).
]]> Las CMH-LP son capaces de producir todos los tipos de células maduras de la sangre durante la vida de un individuo y de generar progenitores que al ser transplantados pueden reconstituir el sistema hematopoyético. Éstas CMH-LP constituyen menos del 0.1% de CMHs contenidas en la médula ósea. Las CMH-CP son las encargadas de generar células progenitoras comprometidas con linaje bien sea linfoide o mieloide (6, 7, 1). Parece ser que hay un compromiso progresivo de las CMH-LP en la generación de CMH-CP y de éstas a su vez en la generación de progenitores multipotentes (PMP) pasando por varios estadios de diferenciación que implican cambios funcionales irreversibles y que caracterizan el proceso de maduración celular (8, 9).A medida que las CMHs maduran, progresivamente van perdiendo su potencial de auto-renovarse pero se vuelven mitóticamente más activas, es decir, que en los compartimentos de células progenitoras hay muy poca capacidad de auto-renovación y una alta actividad mitótica (10,11).
NICHO DE LAS CÉLULAS MADRE HEMATOPOYÉTICAS
La médula ósea es un tejido graso y suave que yace al interior del hueso trabecular, y son en conjunto la trabécula y el estroma de la médula ósea los elementos que físicamente soportan y fisiológicamente mantienen el tejido hematopoyético (12). Durante los dos primeros años de vida, la médula ósea activa (médula roja) se localiza en todos los huesos y gradualmente es reemplazada por tejido medular inactivo (médula amarilla o grasa). El microambiente hematopoyético de la médula ósea contiene células de la estroma cuyo origen puede ser mesenquimal, como es el caso de las células endoteliales, los fibroblastos, los adipocitos y los osteoblastos o puede ser hematopoyético no-mesenquimal como los macrófagos y las células dendríticas. Todas estas células de la estroma producen y depositan elementos en la matriz extracelular (MEC), además de esto son capaces de producir y concentrar citoquinas locales hematopoyéticas que pueden inducir o inhibir la proliferación y diferenciación de células progenitoras, formando así el nicho de la célula madre/ progenitora (13). Se cree que la diferenciación hacia un linaje específico puede depender de interacciones especializadas entre células del estroma y células progenitoras (14).
Los procesos de auto-renovación y diferenciación de las CMHs son controlados por un conjunto de mecanismos reguladores extrínsecos e intrínsecos en los nichos hematopoyéticos, que se pueden establecer a través de interacciones entre las células. Un ejemplo de ello son las interacciones de las células progenitoras hematopoyéticas con diferentes tipos celulares como los fibroblastos, los cuales actúan sobre los procesos de crecimiento y diferenciación; las células endoteliales, que facilitan la migración de los precursores hematopoyéticos desde la médula hacia el torrente sanguíneo, y los osteoblastos que mantienen la hematopoyesis gracias a la producción de factores estimulantes de colonias granulocíticas y monocíticas, y al igual que los fibroblastos y las células endoteliales, permiten la adhesión de células primitivas hematopoyéticas CD34+ (15).
Conceptualmente el nicho hematopoyético está dividido en tres partes: i) una zona osteoblástica (localizada cerca de los osteoblastos), ii) una zona medular de CMHs quiescentes y proliferantes y iii) una zona vascular (cerca de los sinusoides) que permite la salida a la circulación de las células maduras (16). El nicho osteoblástico está conformado por osteoblastos cuya función principal es ser formadores de hueso induciendo la diferenciación de las CMHs en osteocitos. En este nicho se han identificado diversas moléculas de adhesión celular que favorecen la interacción de los osteoblastos con las CMHs, entre las que se encuentran la N-caderina que se expresa tanto en osteoblastos como en las CMHs quiescentes, y la ß-1 integrina que se une a la fibronectina y promueve la adhesión a las células estromales de la médula ósea (16).
Las células progenitoras hematopoyéticas que se encuentran cerca de las células madre quiescentes constituyen un segundo tipo de nicho celular conocido como nicho medular. Las células progenitoras producen factores que inhiben la proliferación de las células madre adyacentes, pero cuando el número de estas células progenitoras disminuye dentro del nicho, por ejemplo a causa de una terapia mieloablativa, las CMHs quiescentes son liberadas de su inhibición y comienzan a dividirse (16).
Las CMHs quiescentes ubicadas en primer lugar en el nicho osteoblástico, al recibir estímulos y señales que inducen su proliferación, maduración y diferenciación según los requerimientos del organismo, migran desde este primer nicho hacia el nicho medular y posteriormente, antes de ser liberadas a la circulación, se desplazan al nicho vascular para culminar los procesos de proliferación o diferenciación. Este nicho además de suplir de oxígeno a las CMHs en división, produce factores angiogénicos indispensables para el mantenimiento celular, como el Factor de Crecimiento Vascular Endotelial (VEGF) (16).
PROPIEDADES FUNCIONALES DE LAS CÉLULAS MADRE HEMATOPOYÉTICAS
Estudios realizados con el fin de identificar algunas de las propiedades funcionales de las CMHs han arrojado resultados diversos aun que complementarios entre sí, probablemente debido a la gran heterogeneidad entre las diferentes subpoblaciones de CMHs.
]]> El primer estudio cuantitativo de CMHs fue realizado por Till y McCulloch en 1961 (17), quienes obtuvieron células hematopoyéticas de la médula o del bazo de ratones donadores y las transplantaron por vía intravenosa a ratones previamente irradiados con dosis letales, con el fin de destruir la hematopoyesis endógena y prevenir la generación de CMHs del hospedero. Algunas células inyectadas (aproximadamente 10%) se alojaron en el bazo del receptor y allí proliferaron y formaron colonias macroscópicas que pudieron ser contadas y a las cuales se les llamó unidades formadoras de colonia de bazo (UFC-B).Varios estudios mostraron que aunque las UFC-B hacia los días 12/13 después de ser retransplantadas son capaces de auto-renovarse, son incapaces de mantener una hematopoyesis a largo plazo, lo que permite pensar que realmente no son verdaderas CMHs. Estos resultados fueron la base para implementar la prueba que se utiliza actualmente para definir a una CMH, la cual consiste en demostrar su capacidad de completar y mantener por más de 6 meses la regeneración del sistema linfo-hematopoyético después de haber sido transplantada (18).
Los cultivos a largo plazo de médula (LTC del inglés long-term cultures) fueron desarrollados en 1977 por Dexter et al. (19), quienes cultivaron médula ósea humana o de ratón en un medio suplementado con suero fetal bovino. Las células del estroma formaban una capa alimentadora adherente en la cual las CMHs y las células progenitoras del inóculo proliferaron y se diferenciaron por semanas y meses en ausencia de factores exógenos (20). Las células iniciadoras de cultivo a largo plazo (LTC-IC del inglés long-term culture initiating cells) son células progenitoras más primitivas que las células formadoras de colonia (CFC), se pueden encontrar entre o bajo las células del estroma, son capaces de iniciar y mantener la hematopoyesis por largos períodos de tiempo en cultivo y pueden reiniciar LTC secundarios. Menos del 0.1% de las CMHs de la médula ósea son capaces de proliferar a largo plazo y de auto-renovarse (18). La proporción de LTC-IC con respecto a CFC en sangre periférica es de 1:50 mientras que en médula ósea es de 1:20 (7). Sin embargo, no se han encontrado diferencias significativas en el potencial de proliferación o diferenciación de las LTC-IC de médula ósea y de sangre en estado normal (21).
IDENTIFICACIÓN DE LAS CÉLULAS MADRE HEMATOPOYÉTICAS
Durante el proceso de maduración, las CMHs expresan o dejan de expresar moléculas o antígenos en la membrana celular, lo cual ha sido muy útil para la caracterización de los linajes celulares. La detección de estos marcadores facilita la identificación y aislamiento de grupos celulares particulares. A pesar del gran número de estudios realizados, aún no se ha podido encontrar un único marcador específico de las CMHs, sin embargo, el uso de combinaciones de marcadores permite agrupar en subgrupos mezclas de células funcionalmente heterogéneas con algunas características en común.
Las células hematopoyéticas primitivas no expresan marcadores de linaje (lin) propios. Esta ausencia permite distinguir las células inmaduras del resto de células diferenciadas, siendo éstas últimas más abundantes (22). La selección y aislamiento de células utilizando los marcadores de linaje puede proporcionar un enriquecimiento típico de subpoblaciones de CMHs de 20 a 500 veces en una muestra, dependiendo de la combinación de marcadores usados. A continuación se citan algunos ejemplos de marcadores de diferentes linajes: del linaje eritroide la glicoforina A, el antígeno leucocitario humano- DR (HLA-DR) y el TER-119; del linfoide CD45, CD2, CD3, CD4, CD8, CD19, CD20 y del mieloide CD14, CD56 y CD33 (22).
Las CMHs y otras subpoblaciones de células madre se pueden obtener de diversas fuentes como por ejemplo de la médula ósea, de la sangre periférica y de la SCU (Sangre de Cordón Umbilical). Para identificar, aislar y cuantificar la población de CMHs con frecuencia se utiliza el marcador de linaje conocido como antígeno CD34, el cual se ha identificado en la mayoría de células iniciadoras de cultivo de largo término (CI- CLT), en gran parte de las células formadoras de colonias (CFC) y en células progenitoras linfoides y mieloides. Este marcador sin embargo no está presente en la mayoría de células terminalmente diferenciadas (18). Las células que expresan este marcador de diferenciación linfoncitaria se caracterizan por poseer un gran potencial de repoblación in vivo y por tener la capacidad de generar progenie eritroide y mieloide a partir de células formadoras de colonias. El antígeno CD34 es una proteína monomérica de peso molecular entre 110 y 120 KDA con una región amino terminal extracelular que contiene un dominio proximal de 66 aminoácidos conformado por seis residuos de cisteína y al parecer con una forma globular. De manera significativa, de los 145 aminoácidos que componen el dominio N-terminal, 35% son residuos serina o treonina; este dominio también incluye 7 de 9 sitios potenciales de glicosilación (23). Esta sialomucina, fue el primer marcador de diferenciación reconocido en las células hematopoyéticas primitivas humanas y se continúa usando para aislar progenitores y CMHs para uso clínico (22). Este marcador también se expresa en células endoteliales de vasos pequeños y en fibroblastos embrionarios. El antígeno CD34 es codificado por un gen ubicado en el cromosoma 1q32, región que contiene a su vez varios genes codificadores para moléculas de adhesión celular tales como la selectina L, selectina P, selectina E y laminina B2. Aunque su función no está completamente dilucidada, se ha considerado que puede servir como ligando de la selectina-L, dependiendo de su adecuada glicosilación y sulfatación. También se cree que el antígeno CD34 juega un papel importante tanto en la adhesión intercelular como en la de las células con la matriz extracelular, induciendo la polimerización de actina. Así mismo, se ha demostrado que la regulación de la expresión del antígeno CD34 está implicada en el mantenimiento de la actividad hematopoyética normal gracias a la inhibición de la proliferación de células progenitoras, mediada por contacto y agregación celular (23).
La expresión del antígeno CD34 es mucho mayor en células progenitoras tempranas y disminuye progresivamente a medida que las células maduran, hasta no detectarse en células terminalmente diferenciadas (24,25).
El antígeno CD34 se expresa entre el 1-4% de las células nucleadas presentes en la médula ósea humana de individuos sanos (7). En sangre periférica, aproximadamente un mililitro de sangre contiene en promedio 4 x 103 células/µl CD34+ las cuales corresponden al 0.06% de las células nucleadas totales; y conforman entre el 0.1-1% de células nucleadas de SCU (26).
Las células CD34+ purificadas son capaces de reconstituir la hematopoyesis multilinaje en ratones diabéticos no-obesos con inmunodeficiencia combinada severa (NOD/SCID) irradiados, para hacerlos inmunodeficientes y hacer que no rechacen las células humanas que les son implantadas (27) y que además presentan un potencial de implantación de células humanas en transplantes autólogos y alogénicos (28; 29). Sin embargo, la frecuencia de células con actividad de progenitoras es <20%, la frecuencia de LTCICs es <1% y de CMHs <0.1%, en poblaciones de células CD34+ altamente purificadas (>90%) (22). Es posible hacer la distinción entre la población de CMHs, células progenitoras y células más maduras CD34+, gracias al patrón de expresión de otros marcadores como el CD38, un antígeno que se expresa entre niveles intermedio y alto (>90%) en CMHs CD34+, entre las que se encuentran las células formadoras de colonia, y en el 60% de LTC-ICs (22). Las células CD34+CD38+ son más abundantes que las CD34+CD38-, pero se ha comprobado que estas últimas pueden reconstituir y mantener la hematopoyesis multilinaje en ratones inmunodeficientes después de realizar el transplante (30).
]]> A pesar de ser el CD34 un marcador de CMHs primitivas, se han detectado células CD34- con potencial linfopoyético en el cordón umbilical humano y en fuentes hematopoyéticas adultas, capaces de reconstituir la hematopoyesis multilinaje en ratones inmunodeficientes y además de generar células CD34+ in vitro e in vivo. Sin embargo, las células con fenotipo CD34- también se caracterizan por la ausencia de CD38, de marcadores específicos de linaje y de CD133 (22, 31, 32, 33, 34). Al comparar células CD34-CD38- lin- con células CD34+CD38-lin-, solo una pequeña fracción de las primeras (0.2%) expresa el marcador CD133 y precisamente esas células son capaces de repoblar ratones NOD/SCID, a pesar de que la densidad celular y el nivel de repoblamiento fuese 100 veces menor que el de las células con fenotipo CD34+CD38-lin- (35). Esto sugiere que las células CD34- son incapaces de alcanzar la médula ósea después de haber sido transplantadas por vía intravenosa, ya que se ha demostrado que la inyección directa de células CD34-lin- en la medula ósea de ratones NOD/ SCID resulta en niveles elevados de implantación, en comparación con células CD34+ (36).Otro antígeno que se expresa en la mayoría de las células CD34+ es el CD133, también conocido como AC133 (37,38). Este antígeno es una proteína glicosilada que se ha detectado en células repobladoras, progenitoras inmaduras y progenitoras de monocitos/granulocitos, pero no en la mayoría de progenitores eritroides (22). Su función se ha relacionado con el mantenimiento de los estados primitivos de diferenciación. Las células CD133+ están presentes en la sangre de cordón umbilical (SCU) y en la medula ósea (MO) (39, 40). Se ha mostrado la presencia de células CD133+CD34-CD38-Lin- en sangre periférica de adultos, provenientes posiblemente de la médula ósea y movilizadas por acción del Factor Estimulante de Colonia Granulocítica (FECG) y del Factor de Célula Madre (FCM) también conocido como stem cell factor, con potencial de diferenciación a células CD34+ similar al de células derivadas de SCU (41). Aunque el CD133 representa un importante marcador de superficie celular para la identificación de células madre y células progenitoras humanas, aún no es claro si el uso de este marcador otorga alguna ventaja sobre el uso del CD34 para el aislamiento o la expansión celular de las CMHs y las células progenitoras hematopoyéticas (42).
Otro marcador de linaje es el C-KIT, conocido también como CD117, que corresponde al receptor para el FCM, el cual promueve la proliferación y diferenciación de células progenitoras primitivas hematopoyéticas a células progenitoras comprometidas (43). El C-KIT se expresa en las dos terceras partes de las células CD34+, incluyendo las células progenitoras más comprometidas con linaje, pero está ausente en las células sanguíneas maduras circulantes. Sin embargo a menudo su nivel de expresión es lo suficientemente alto como para ser usado como marcador en técnicas de aislamiento de células hematopoyéticas (22).
Por último el marcador CDCP1 (proteína que contiene el dominio cub), fue identificado recientemente y tiene un patrón de expresión similar al de CD133 (44). El dominio o región estructural cub se ha identificado principalmente en proteínas relacionadas con las inmunoglobulinas (estructura globular) y tiene un papel importante en la adhesión celular. El CDCP1 es una proteína transmembranal inicialmente encontrada en células tumorales de colon y de seno. Su expresión sobre células hematopoyéticas normales está restringida a las células CD34+, incluyendo aquellas con actividad repobladora NOD/SCID y no se ha detectado en células sanguíneas maduras. Al igual que el CD34 y el CD133, el CDCP1 puede ser útil para el enriquecimiento en CMHs y en células progenitoras de las muestras de cordón umbilical y médula ósea, pero no para su discriminación (22).
CRECIMIENTO Y PROLIFERACIÓN DE LAS CMHS
Para proteger al individuo del agotamiento celular, las CMHs deben generar todas las líneas celulares de la sangre requeridas durante su existencia, para lo que es muy útil su multipotencialidad y capacidad de auto-renovarse. Se propone también, que las CMHs utilizan el mecanismo de sucesión clonal, que consiste en la diferenciación de unos pocos clones de CMHs y en la generación de células sanguíneas maduras cuando se requieren, como por ejemplo en los procesos infecciosos en donde se activan los mecanismos celulares de defensa que implican a la mayor parte de las células sanguíneas, o cuando por algún motivo las reservas de glóbulos rojos no son suficientes para suplir las necesidades del cuerpo. Mientras tanto las CMHs restantes permanecen en estado de quiescencia sin contribuir a la hematopoyesis, hasta que la capacidad proliferativa de las células activas se agota (45).
Una característica que comparten las células madre adultas con varios tejidos es su relativa quiescencia. Las células madre generalmente tienen una baja tasa de recambio, en tanto que su descendencia, denotada como células progenitoras en el sistema hematopoyético, prolifera a gran escala. Estas células progenitoras proveen billones de células sanguíneas por día que son necesarias para mantener la homeostasis en el individuo (46). Se ha comprobado que, aunque la mayoría de CMHs permanecen quiescentes en fase G0, en algún momento pueden entrar al ciclo celular para dividirse (47). La baja tasa de proliferación característica de las CMHs, es esencial para el mantenimiento de la población de células madre durante la vida de un individuo. La dinámica que regula cuáles células se auto-renuevan para mantener la población, y cuáles proliferan y llegan a comprometerse para producir células diferenciadas, aún no es clara (3), aunque se cree que unas sustancias llamadas citoquinas, producidas por las células, pueden tener un papel decisorio importante en la regulación de la activación de las CMHs. Esta activación, conlleva una serie de cambios celulares que inducen el paso de fase G0 a fase G1 indicando el inicio de la división celular y conduciendo la expresión de CD34 y a una pérdida gradual de la multipotencialidad con las sucesivas divisiones celulares (3). Las células activadas retienen su multipotencialidad durante un número definido de ciclos y cuando llegan a un estado de mayor compromiso en la diferenciación, proliferan a una mayor velocidad (3). Por el contrario, las células destinadas a la auto-renovación son capaces de retornar a un estado prolongado de quiescencia o G0 después de cada ciclo celular y entrar nuevamente al ciclo celular cuando son estimuladas adecuadamente, aún después de un largo período de tiempo de quiescencia.
Mecanismos moleculares involucrados en procesos de auto-renovación, proliferación y diferenciación de las CMHs
Cualquier célula, puede tener diferentes opciones durante su existencia. Si se trata de una célula eucariota elegirá aquella que sea más conveniente para el individuo del cual forma parte, o si se trata de una célula procariota tomará la opción que le permitirá sobrevivir bajo las condiciones ambientales en que se encuentre. En ambos casos, la elección se hace en respuesta a las diferentes señales que se encuentran en el entorno celular. Estas opciones son proliferar, diferenciarse, permanecer en quiescencia o morir. En el caso de las CMHs la proliferación está relacionada con la capacidad de auto-renovarse y de generar un linaje celular por división clonal, es decir que a partir de un progenitor por división celular y diferenciación se obtengan células con características funcionales y morfológicas prácticamente idénticas. En el caso del tejido sanguíneo el proceso de auto-renovación es crucial para que las células madre persistan a lo largo de la vida de los individuos y se mantengan en el número adecuado, y el proceso de diferenciación es necesario para que se mantenga el número de células sanguíneas requeridas para el correcto funcionamiento del organismo. Estos dos procesos deben estar equilibrados, de lo contrario pueden surgir enfermedades. Se ha encontrado que hay mecanismos moleculares de señalización que participan como reguladores de la auto-renovación, proliferación y diferenciación de las CMHs. Estos mecanismos se conocen como vías de señalización, y en particular se han asociado con la actividad de las CMHs las vías Hedgehog (Hh), Notch y Wingless (Wnt), además de las proteínas morfogénicas de hueso o BMPs y otros factores que regulan la expresión de los genes activándolos o reprimiéndolos.
Las vías de señalización celular corresponden a sistemas de comunicación, constituidos por una serie de proteínas que actúan en respuesta a estímulos extracelulares o intracelulares y cuya activación o inhibición se puede dar en cascada, es decir una actúa sobre otra de manera sucesiva. El estímulo puede ser de naturaleza química o física, y se constituye en una señal portadora de un mensaje. Cuando es de naturaleza química puede recibir el nombre de ligando. La señal es captada por receptores moleculares que son proteínas con tres regiones: una extracelular, una trasnmembranal y otra intracelular. El receptor actúa como decodificador del mensaje y forma un complejo con el ligando, sufre un cambio estructural que generalmente conduce a la activación del receptor y a su vez, transmite el mensaje a otras moléculas intermedias, que pueden ser efectoras o transmisoras del mensaje activando otras moléculas, entre ellas los segundos mensajeros. Los segundos mensajeros inducen la activación o desactivación de otros blancos moleculares que participan en la generación de una respuesta a la señal recibida. Esta cadena de eventos puede llegar o no hasta el núcleo de la célula y según el caso, puede darse la activación o represión de programas genéticos. Cuando el objetivo se cumple la vía se desactiva. Cada vía de señalización tiene sus propios componentes moleculares, aunque pueden ser compartidos con otras vías conformándose una verdadera red de información. La activación o desactivación de los componentes de las vías de señalización se da generalmente por cambios estructurales inducidos por transferencia de grupos químicos como el fósforo (fosforilación), el metilo (metilación) y el acetilo (acetilación), entre otros.
]]> Vía Hedgehog (Hh)Esta vía de señalización se relaciona con la activación de la proliferación de las CMHs, y con la inducción de patrones morfogenéticos claves para el desarrollo embrionario. Está constituida principalmente por proteínas codificadas por los genes hedgehog, que contienen colesterol. Estas proteínas son secretadas y pueden mediar la señalización de dos maneras diferentes: a través del contacto célula-célula entre células adyacentes y de manera alterna, produciendo un ligando soluble capaz de difundirse a través del microambiente para interactuar con células distantes. En ambos casos la señal o ligando se capta a través de receptores conocidos como proteínas supresoras de tumor Patched (Ptc) (48).
Las moléculas que actúan como señal o ligando en mamíferos, son codificadas por tres genes Hedgehog: Sonic hedgehog (Shh), Indian hedgehog (Ihh) y Desert hedgehog (Dhh) y son conocidas como morfógenos por jugar un papel importante durante el desarrollo embrionario. Ellas pueden dirigir la diferenciación celular hacia diversos tejidos por medio de umbrales de concentración específicos.
El receptor funcional para la señal Hh está conformado por dos proteínas transmembranales independientes, la proteína supresora de tumor Patched (Ptc) y el proto-oncogen Smoothed (Smo). Ptc inhibe la activación de Smo en ausencia de su ligando Hh, es decir, en células que no han sido estimuladas por Hh (49). Smoothed es un componente de la vía de señalización Hh que se activa cuando las proteínas Hh se unen al receptor Ptc. La unión del ligando (Hh) al receptor (Ptc), ocasiona un cambio en la estructura del complejo liberando a Smo de la influencia represora de Ptc y dando inicio a la activación de la vía transmitiendo el mensaje hacia el interior de la célula (50).
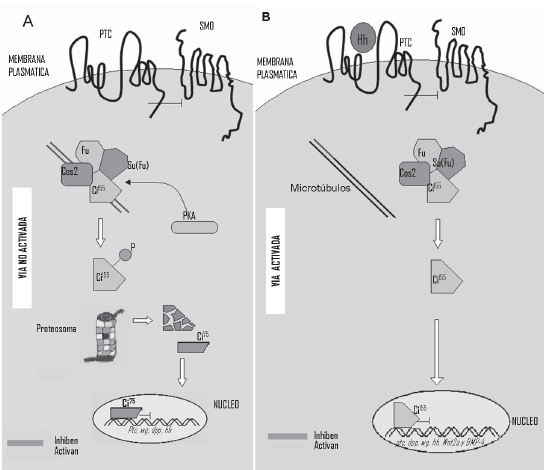
En el citoplasma celular el mensaje es recibido por proteínas llamadas quinasas, que transfieren grupos fosfato sobre proteínas que contienen en su estructura regiones ricas en aminoácidos serina/treonina. Entre ellas están la proteína quinasa Fused (Fu), el Supresor de Fused (Su(Fu)), la proteína Costal-2 (Cos2) (51), y el factor de transcripción Cubitus interruptus (Ci o Gli en mamíferos). Estas proteínas forman un complejo citoplásmico de alto peso molecular que está anclado a estructuras del citoesqueleto celular conocidas como microtúbulos. En ausencia de Hh, el factor de transcripción Ci (Ci155) es fosforilado por la proteína quinasa A (PKA) y subsecuentemente destruido en el proteosoma permitiendo la liberación de un péptido con actividad represora de la transcripción ubicado en la región amino-terminal (Ci75) de la misma molécula Ci155. Con la estimulación por Hh, el gran complejo citoplasmático se disocia de los microtúbulos y Ci155 ingresa al núcleo y allí actúa como activador de la expresión de los genes blanco de Hh, tales como ptc, dpp (Decapentaplegic) , wg (Wingless) , y el propio hh, produciendo finalmente una respuesta que conduce a la inhibición de la vía (52). Otros genes cuya expresión se modifica son Wnt2a y un inhibidor específico de BMP-4 llamado Noggin (Figura 1) (48).
Shh, Ptc y Smo se expresan en células humanas primitivas CD34+CD38-Lin-, células mieloides maduras (CD33+), linfocitos B (CD19+) y T (CD3+), células de la estroma de médula ósea, y células endoteliales de vena umbilical (HUVEC). Las células CD34+CD38-Lin-, las de estroma y las HUVEC, pero no las células comprometidas de linaje mieloide y linfoide, también expresan tres factores transcripcionales Gli-1, Gli-2 y Gli-3, que actúan corriente abajo de la cascada de señalización Hh (48), sugiriendo que posiblemente la señalización Hh no es esencial para la maduración hematopoyética.
Se ha comprobado que la proliferación inducida por citoquinas, de células sanguíneas purificadas, puede ser inhibida por la adición de un anticuerpo que reconozca y se una a Hh para bloquear su acción. Esto muestra que las proteínas Hh producidas endógenamente juegan un papel importante en la expansión de células hematopoyéticas humanas primitivas (48). Así mismo, la adición de formas solubles de Shh incrementa el número de células sanguíneas humanas detectables con capacidad de repoblar ratones NOD-SCID, lo que indica que estas células han conservado el carácter pluripotente (48).
En la mosca Drosophila, la actividad Shh está asociada con el control de señalización de la proteína morfogénica de hueso (BMP). Noggin, una proteína inhibidora específica de BMP-4, es capaz de inhibir la proliferación inducida por Shh de células hematopoyéticas primitivas de una forma similar a un anticuerpo anti-Hh. Así, Shh parece funcionar como regulador de CMHs, aunque en combinación con otros factores de crecimiento, a través de mecanismos dependientes de señales BMP que se activan posteriormente en la cascada (53, 18).
Vía Notch
La vía de señalización Notch se ha asociado con los procesos de proliferación, diferenciación y muerte celular en casi todos los estadios del desarrollo (54). En general, la activación de Notch conduce a la supresión transcripcional de los genes específicos de linaje, inhibiendo la diferenciación en respuesta a señales inductivas de la misma (55).
]]> Esta vía está constituida principalmente por cuatro genes Notch (Notch1, Notch2, Notch3 y Notch4), que se expresan ampliamente durante la embriogénesis (fig. 2). Las proteínas NOTCH son grandes polipétptidos transmembranales con diferentes regiones o dominios estructurales. El dominio extracelular de Notch contiene un número variable de repeticiones que además de atravesar la membrana celular son importantes para que el ligando se una al receptor y active la vía. Una vez formado el complejo ligando-receptor, se produce un cambio estructural que favorece la activación y liberación del dominio intracelular del receptor (Notch-IC) al interior de la célula (fig 1.2) (55, 56, 57, 54). El dominio intracelular de Notch contiene una región que favorece las interacciones proteína-proteína, necesarias para continuar con la transmisión del mensaje. A pesar de no tener una actividad enzimática conocida, la proteína Notch, transmite las señales a través de interacciones moleculares directas. Las proteínas Notch-IC de Drosophila y Notch 1, 2, y 3 en mamíferos, contienen señales de localización nuclear (nls) y secuencias OPA que constituyen un dominio rico en glutamina, con función de transactivador de la transcripción. Otras regiones descritas incluyen el dominio RAM, el cual se une a los efectores o potencializadores de la actividad de la vía, CSL (CBF1/Supressor de Hairless/Lag-1) asociados con diversos efectos de Notch 1,2 y 3 sobre la diferenciación mieloide (55, 56, 57).La familia de proteínas Notch, está integrada por receptores transmembranales con múltiples ligandos identificados en mamíferos como Delta o Delta-like (Dll), y Serrate o Jagged (55, 54).
Una vez se forma el complejo receptor-ligando, el receptor pierde un fragmento del dominio intracelular denominado Notch-IC (figura 1. 2), se libera en el citoplasma y activa la molécula efectora CSL (CBF1/RBP-Jk en mamíferos). Esta proteína interactúa físicamente con Notch-IC y media la transducción de señal del citoplasma hacia el núcleo, donde el complejo se une de manera específica a secuencias del ADN específicas llamadas promotoras cuya función es la de regular la expresión de genes blanco como por ejemplo Hairy/Enhancer of split (HES). El efecto final es la represión de la transcripción de los genes HES, los cuales funcionan como reguladores negativos de la expresión génica específica de linaje (55, 56).
La vía de señalización Notch es un importante regulador de la auto-renovación de las CMHs por inhibición de la diferenciación. A lo largo de la maduración hematopoyética los receptores Notch-1 y Notch-2 se expresan y cualquiera de los dos es capaz de inhibir la diferenciación mieloide en células 32D, Notch-1 en respuesta a G-CSF y Notch-2 en respuesta a GM-CSF (57,58). En conclusión, la vía Notch puede jugar un papel de gran importancia como regulador de la proliferación y de la capacidad de auto-renovación de las CMHs, y es capaz de influir directamente en la determinación celular de las mismas.
Vía WNT
La vía Wnt ha sido de gran importancia en el estudio del desarrollo animal, sin embargo sólo hasta hace pocos años se le ha prestado atención desde el campo de la inmunología, debido a que varios estudios indican que la proliferación y diferenciación de la mayoría de progenitores más primitivos comprometidos con linaje está regulada in vitro por moléculas señalizadoras que tienen un papel instructivo durante el desarrollo embrionario. Al parecer, la vía WNT proporciona señales de mantenimiento y/o proliferación para las poblaciones de células madre y células progenitoras.
Aunque se han propuesto al menos tres vías de señalización intracelular para Wnt (59), la mayoría de estudios del sistema hematopoyético están restringidos a la vía canónica de la β-catenina y el factor de transcripción terciario TCF/LEF, en donde el evento final es la translocación nuclear de la β-catenina y su unión física y activación de los factores de transcripción TCF y/o LEF (fig. 3).
Las proteínas Wnt son secretadas al medio extracelular y actúan como ligandos uniéndose a receptores de la membrana celular ya sea sobre las mismas células productoras de Wnt o sobre células adyacentes, para determinar el destino celular u otros parámetros de diferenciación. Las proteínas Wnt (60), contienen palmitato que les confiere propiedades hidrofóbicas y generalmente están glicosiladas en el extremo amino-terminal. El aminoácido que contiene el palmitato es la cisteína C77, un aminoácido que está presente en todas las proteínas Wnt y que es esencial para su función.
Los receptores más importantes de la vía de señalización Wnt son los pertenecientes a la familia Frizzled (Fz), aunque se han identificado otros como la proteína relacionada con el receptor de lipoproteína de baja densidad (LRP). Las proteínas Wnt se pueden unir a LRP para formar un complejo tetramérico con Frizzled (Nusse R 2003). Además, la cola citoplasmática de LRP puede interactuar con Axina, uno de los componentes de la vía Wnt (63).
Las FRPs (proteínas relacionadas con Frizzled) son proteínas estructuralmente rela cionadas con el dominio rico en cisteína de las Frizzleds y actúan como antagonistas de Wnts que también son secretados, se cree que las FRPs pueden unirse directamente a las proteínas Wnt para bloquear su acción (61). En estudios recientes se ha asociado la presencia de proteoglicanos en la matriz extracelular con el agrupamiento de los receptores de Wnt en la membrana plasmática (62).
]]> Entre las proteínas efectoras implicadas en la cascada de activación de la vía de regulación Wnt se encuentran la β-catenina, DVL (Dishevelled), GSK3β (proteína quinasa glicógeno sintasa-3βaxina, APC (adenomatous polyposis coli). En ausencia de estimulación de la vía Wnt, la proteína β-catenina es desestabilizada por un complejo citoplasmático compuesto por los productos del gen supresor de tumor Axina y APC, por la quinasa caseína 1 (CK1), la cual es una quinasa de tipo serina/treonina, y por GSK3β (64). Después de que se unen Axina y APC, la β-catenina es fosforilada de forma secuencial por CK1 y GSK3β al menos en cuatro residuos conservados del extremo amino-terminal. CK1 fosforila a β?catenina en el aminoácido Ser45, creando así un sitio de preparación para que GSK3β fosforile a los otros residuos, Thr41, Ser37 y Ser33. Esto crea un motivo de reconocimiento para el complejo E3-ubiquitin-ligasa, el cual está compuesto de β-TRCP (proteína que contiene la repetición β-transducina). Esta proteína marca a la β- catenina con moléculas de ubiquitina, marcaje esencial para la degradación de las proteínas por el complejo proteosomal (59). La acción de este complejo es antagonizada por Dishevelled (DVL), proteína citoplasmática que se activa por un mecanismo desconocido cuando Wnt se une con su receptor. DVL se transfiere a la membrana celular, permitiendo que GSK3β se disocie de la Axina, cuando GSK3β ya no está unida a la β- catenina, ésta no se fosforila. Gracias a ello la β- catenina no fosforilada puede acumularse y translocarse al núcleo (Figura 3).Una vez en el núcleo, la β-catenina actúa como un co-activador transcripcional asociándose con los factores de transcripción de la familia TCF/ LEF (52). El mecanismo mediante el cual realiza esta labor es por el reemplazo de los co-represores que pertenecen a la familia del gen relacionado con groucho (GRG), los cuales se unen a TCFs (65). El extremo C-terminal de la β-catenina provee un dominio de transactivación que está unido al ADN y al TCF (62). Luego, la β-catenina recluta a diversas proteínas que pueden modificar localmente las regiones reguladoras de los genes, entre ellas CBP (proteína de unión al elemento de respuesta al AMP cíclico), BRG1 (gen relacionado con brama 1) y/o a p300 (66), para que se unan a los promotores de genes relacionados con la proliferación celular y de esta manera poderlos activar (59). En ausencia de estimulación de la vía, los niveles reducidos de β-catenina conducen a la represión de los genes blanco de Wnt mediante la asociación de co-represores transcripcionales a través del mismo complejo TCF/LEF (52, 68). Todo este complejo mecanismo conduce a la inducción de la proliferación de células progenitoras inmaduras, incluyendo las CMHs. De igual manera la vía de señalización Wnt juega un papel importante en la regulación de la auto-renovación de las CMHs. Por otro lado, el aumento de la cantidad de β-catenina a niveles no normales, en CMHs de ratón, en cultivos a largo plazo expande el pool de células madre transplantables.
En la mayoría de modelos, la principal función de la vía de señalización Wnt es la regulación de las opciones para la determinación celular hacia un tejido específico mediante la activación o inactivación de programas genéticos. Por otro lado, mutaciones en genes Wnt o su expresión inapropiada por lo general conducen a cambios de linaje celular como consecuencia de una expresión génica alterada. Muchos genes directa o indirectamente regulados por Wnt son factores de transcripción o moléculas de señalización secretadas que parecen tener un rol clave en la jerarquía de los genes reguladores (62).
Otros factores implicados en el mecanismo de auto-renovación
Proteínas BMP
Las proteínas morfogenéticas de hueso o BMPs, son miembros de la superfamilia de los factores transformantes de crecimiento (TGFs), a la cual pertenecen TGF-ß, las inhibinas y las activinas. Esta familia participa en gran cantidad de respuestas biológicas como crecimiento celular, apoptósis o muerte celular y diferenciación en diversos tipos celulares. Uno de los miembros de la familia BMP es BMP-4, esta proteína se expresa en el mesodermo ventral e induce la diferenciación hematopoyética en embriones de Xenopus (70). En humanos, las BMPs se expresan en medula ósea adulta y son esenciales en la remodelación del hueso y el crecimiento. Se ha demostrado que BMP-4 juega un papel importante en el crecimiento, diferenciación y capacidad de repoblar de las CMHs humanas CD34+CD38-Lin-, mientras que altas concentraciones de BMP-2 y BMP-7 actúan de forma similar al TGF-β, inhibiendo la proliferación de estas células (71).
Hoxb4
Miembros de la familia de genes homeobox Hox fueron los primeros implicados en la regulación de la especificación de linaje y el desarrollo de las células madre en varios tejidos, incluyendo el sistema hematopoyético. El factor de transcripción HOXB4 es el que más se ha estudiado, sus niveles de expresión se encuentran elevados en células de médula ósea CD34+ CD38-/loCD45RA-CD71- que contienen gran cantidad de células iniciadoras de cultivo a largo plazo (LTC-ICs), pero no se ha encontrado HOXB4 en la mayoría de poblaciones de células progenitoras adultas (72). La diferenciación de células Lin- en los linajes eritroide y granulocítico está acompañada por un aumento en el ARNm de HOXB4. Así mismo, un descenso en los niveles de HOXB4 inhibe la formación de colonias de crecimiento para estos linajes (73).
Se ha demostrado que al manipular células de estroma para que secreten HOXB4 y co-cultivarlas con células humanas CD34+CD38lo hay un incremento en el número de células madre (74, 75) . Además, las células de medula ósea de ratón que sobre-expresan HOXB4 aumentan el número de CFU-S (unidades formadoras de colonia de bazo) y CFCs (células formadoras de colonia) capaces de generar gran cantidad de colonias en cultivos primarios y secundarios siendo indicativas de expansión celular. Al transplantar estas células con HOXB4 expresado a altos niveles en ratones irradiados letalmente, se observó que el compartimento de CRU (unidad repobladora competidora) se regenera hasta alcanzar niveles normales (76). Un hallazgo importante es que las CMHs a que se les transfiere el gen que expresa HOXB4 no se expanden por encima de los niveles observados en ratones no manipulados, lo cual indica que la sobre-expresión no supera los mecanismos reguladores que mantienen el tamaño del pool de CMHs dentro de los niveles normales (77).
Bmi-1
]]> Bmi-1 es un proto-oncogen o gen que al alterarse su función participa en la transforma ción de células normales en tumorales, su función normalmente se relaciona con la represión de la expresión de genes blanco. Se expresa en CMHs de ratones y humanos y se ha encontrado que los embriones de ratón que carecen de Bmi- 1 tienen un menor número de células y mueren antes de alcanzar los 2 meses de vida debido a una disminución progresiva de todas las células sanguíneas, incluyendo las más primitivas. Las células de médula ósea o de hígado fetal obtenidas de estos ratones, al ser transplantadas a ratones irradiados letalmente tienen una capacidad disminuida de repoblar todos los linajes hematopoyéticos (78). Esto indica que Bmi-1 juega un papel importante en el mantenimiento del pool de CMHs posiblemente por defectos en el mecanismo de auto-renovación. (79) La manipulación del Bmi-1 con el fin de alterar la proliferación celular podría ser de gran utilidad en el manejo de células madre leucémicas (79).Integración de Wnt, Hedgehog, Notch y BMP en las células madre hematopoyéticas.
Las primeras CMHs que se producen durante el desarrollo son derivadas del mesodermo, por lo tanto, sería de esperarse que genes que son importantes en el diseño y formación del mesodermo como los componentes de las vías de señalización Hedgehog, Notch y Wnt, también sean esenciales en el compromiso, diferenciación y auto-renovación de las CMHs. A pesar de saber qué señales influyen en los procesos relacionados con la auto-renovación, proliferación o inhibición de la diferenciación, aún no es completamente claro de qué manera se integran unas con otras.
Wnt y Shh comparten el tener como señales o ligandos moléculas modificadas por lípidos, ambas tienen palmitatos unidos covalentemente y son secretadas, por lo tanto, pueden actuar sobre células lejanas; también tienen en común la participación de los receptores de superficie Frizzled y Smoothened en la transmisión del mensaje.
Los receptores Frizzled para Wnt están relacionados a la proteína Smoothened, ambos receptores tienen siete dominios transmembranales y un dominio rico en cisteína en el extremo N terminal. Estas moléculas están más cercanamente relacionadas entre sí que otras familias de receptores serpenteantes. Sin embargo, aunque los receptores están relacionados, los mecanismos de activación de Fz y Smo son fundamentalmente diferentes (61).
Adicionalmente, tanto las señales Wnt como las señales Hh usan las proteínas quinasas GSK3 y Ck1á para facilitar la proteólisis de los efectores transcripcionales: β-catenina para Wnt y Cubitus interruptus para Shh (80).
Wnt y Notch también se relacionan, porque en CMHs a las cuales se les transfiere el gen que codifica para β-catenina expresan de tres a cuatro veces más niveles de HOXB4 y Notch1, genes reguladores de la auto-renovación de CMHs indicando su posible relación (69). En otro estudio, se detectaron señales Wnt y Notch activas en la mayoría de células del nicho de CMHs y una gran fracción de estas células usaban ambas vías simultáneamente. En el mismo estudio, se determinó que la estimulación con proteínas Wnt aumenta la expresión de genes blanco de la vía Notch en CMHs, lo cual demuestra que Wnt contribuye a la expresión diferencial de genes blanco de la vía Notch. Al inhibir la señal de Notch, en presencia de Wnt3a y SLF (Steel factor), la capacidad de las CMHs de mantener un estado indiferenciado disminuye pero la proliferación y supervivencia son normales, es decir, que la señalización de Notch es dominante con respecto a las proteínas Wnt y SLF (81).
También se ha visto relación entre Shh y BMP, en donde Shh regula la proliferación de células sanguíneas primitivas a través de mecanismos que dependen de señales BMP (48).
Entender cómo se relacionan funcionalmente estas vías de señalización con el fin de controlar la regulación de las células madre y explorar las similitudes entre ellas y la manera como operan en diferentes organismos, puede ser un punto crítico para dilucidar el papel de estos factores de señalización en el desarrollo y renovación de células oncogénicas.
Con el desarrollo de la ciencia y la tecnología durante las ultimas décadas, ha sido posible identificar, aislar y estudiar un grupo heterogéneo de células, conocidas como células madre, troncales o stem cells, cuyo potencial de diferenciación se basa en su capacidad para generar desde un organismo completo y su tejido extraembrionario, hasta células con funciones especializadas dentro de un tejido u órgano, como es el caso de las CMHs, siendo esta población una de las más estudiadas dada su potencial aplicación en la medicina clínica en pacientes que padecen trastornos hematológicos malignos.
]]> En conclusión las CMHs se caracterizan por su alta capacidad de proliferación y diferenciación in vivo e in vitro; sin embargo, aunque se ha demostrado la participación de diferentes vías moleculares en los procesos de auto-renovación, proliferación y en los mecanismos que direccionan los patrones de diferenciación y función de estas células, aún no se conocen la totalidad de los procesos y la manera como ellos interactúan para permitir que la CMH preserve su multipotencialidad. Sólo el conocimiento generado a partir de estudios que extrapolen lo que sucede in vivo en el laboratorio, permitirá desarrollar y mejorar técnicas de cultivos celulares que realmente cumplan con el objetivo de expandir CMHs en cantidades suficientes sin presentar alteraciones malignas, para su uso terapéutico.Figura 1. Vía de señalización Hedgehog

Vía Hedghog (Hh): reguladora de la proliferación de las CMHs. Sobre la superficie de las CMHs se encuentra el receptor que reconoce el ligando Hh implicado en la activación de esta vía. Este receptor esta constituido por un complejo transmembranal formado por dos subunidades proteícas, denominadas PTC (Patched) y SMO (Smoothed). La subunidad PTC reprime la actividad de la subunidad SMO en ausencia de la unión de un ligando específico del receptor. En el interior de la célula se encuentra un complejo citoplasmático anclado a los microtúbulos del citoesqueleto, compuesto por 4 proteínas entre ellas la proteína quinasa Fused (Fu), el Supresor de Fused (Su(Fu)), la proteína Costal-2 (Cos2) (51), y el factor de transcripción Cubitus interruptus (Ci o Gli en mamíferos). Cuando la vía Hh no es activada por un ligando especifico la proteina quinasa A (PKA) fosforila a Ci155, el cual es liberado del complejo y destruído en el proteosoma, con la posterior liberación de un represor transcripcional ubicado en la región aminoterminal (Ci75) de Ci155. Si el receptor funcional Ptc es estimulado por un ligando específico Hh, Ci155 es liberado del complejo molecular, se trasloca al núcleo y allí actúa como activador de la expresión de los genes blanco de la vía entre ellos ptc, Wnt2a y un inhibidor específico de BMP-4 llamado Noggin (48).
Figura 2. Vía de señalización Notch
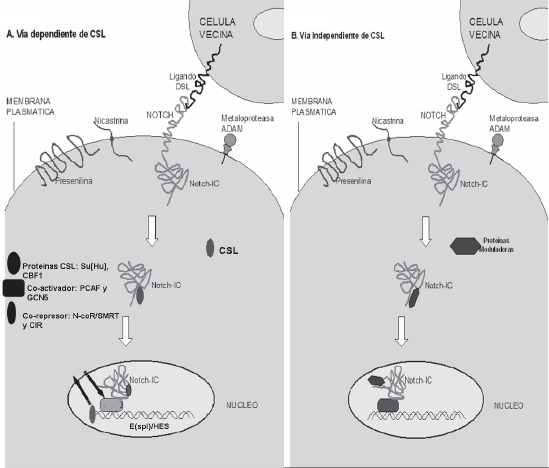
Via Notch: su activación esta implicada en la supresión transcripcional de los genes específicos de linaje, Inhibiendo la diferenciación en respuesta a señales inductivas (55). El grupo de proteínas Notch son receptores transmembranales, cuyos ligandos en mamíferos son denominados Delta o Delta-like (Dll), y Serrate o Jagged (55, 54). El dominio extracelular de Notch se activa cuando los ligandos DSL ubicados sobre células adyacentes se unen a Notch.Esta activación da como resultado el rompimiento proteolítico de Notch, mediado por una metaloproteasa y por proteínas de membrana como Presenilina y Nicastrina, con la posterior liberación y translocación al núcleo del dominio intracelular de Notch (Notch-IC). Notch-IC actúa con diferentes proteínas citoplásmicas y nucleares y la el mensaje puede seguir dos vía diferentes, una dependiente de proteínas CSL (Su[H], CBF1) y otra independiente de éstas. Al interactuar Notch-IC con las proteínas CSL se produce la activación transcripcional dependiente de CSL por el desplazamiento de co-represores (N-CoR/SMRT y CIR) y su reemplazo co-activadores (PCAF y GCN5) moduladores de la estructura del ADN que facilitan la activación de los genes blanco E(spl)/HES, los cuales son reguladores negativos de la expresión génica específica de linaje (55, 56).Por otro lado, en la vía independiente de CSL el resultado también es la regulación transcripcional, mediada por la interacción de Notch-IC con otras proteínas también moduladoras de la estructura de los genes, EMB5, SKIP y Deltex (55,56).
Figura 3. Vía de señalización WNT
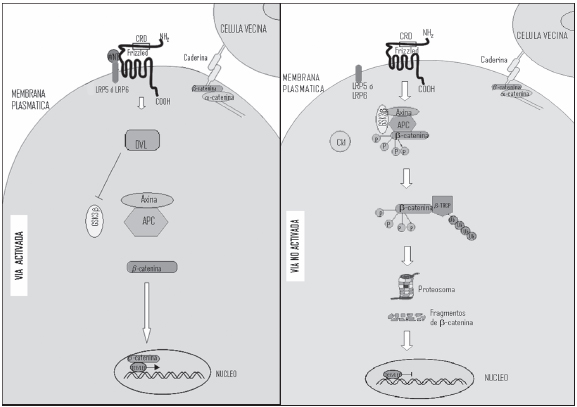
Vía WNT: proporciona importantes señales de mantenimiento y/o proliferación para las poblaciones de células madre y células progenitoras. Las proteínas efectoras implicadas en la cascada de activación de la vía de regulación Wnt son: β-catenina, DVL (Dishevelled), GSK3 β (proteína quinasa glicógeno sintasa-3 βaxina, APC (adenomatous polyposis coli). En ausencia de estimulación de la vía Wnt, la proteína β-catenina es desestabilizada por un complejo citoplasmático compuesto por los productos del gen supresor de tumor Axina y APC, por la quinasa caseína 1 (CK1) la cual es una quinasa de tipo serina/treonina y por (GSK3β) (61). Después de que se unen Axina y APC, la β-catenina es fosforilada de forma secuencial por CK1 y GSK3β al menos en cuatro residuos conservados del extremo amino-terminal. CK1 fosforila a β−catenina en el aminoácido Ser45, creando así un sitio de preparación para que GSK3β fosforile a los otros residuos, Thr41, Ser37 y Ser33. Esto crea un motivo de reconocimiento para el complejo E3-ubiquitin-ligasa, el cual está compuesto de β-TRCP (proteína que contiene la repetición β-transducina), esta proteína marca a la β-catenina con moléculas de ubiquitina, dejándola lista para la degradación proteosomal (82). La acción de este complejo es antagonizada por Dishevelled (DVL), proteína citoplasmática que se activa por un mecanismo desconocido cuando Wnt se une con su receptor., en este caso DVL es reclutada a la membrana celular, permitiendo que GSK3β se disocie de la Axina. Cuando GSK3β ya no está unida a la β-catenina, ésta no se fosforila. Gracias a ello la β-catenina no fosforilada puede acumularse y translocarse al núcleo. Una vez en el núcleo, la β-catenina actúa como un co-activador transcripcional asociándose con los factores de transcripción de la familia TCF/LEF (52). El mecanismo mediante el cual realiza esta labor es desplazando los co-represores y atrayendo coactivadores para finalmente activar genes que favorecen la proliferación y auto-renovación de las CMHs (62).
1. Bellantuono I. Haemopoietic stem cells. Int. J Biochem. Cell Biol. 2004; 36: 60720. [ Links ]
2. Horwitz E. Stem Cell Plasticity: The growing Potential of Cellular Therapy. Arch Med Res 2003; 34: 600-06. [ Links ]
3. Marone M, De Ritis D, Bonanno G, Mozzetti S, Rutella S, Scambia G, et al. Cell Cycle Regulation in Human Hematopoietic Stem Cells: From Isolation to Activation. Leuk. Lymphoma. 2002; 43: 493-501. [ Links ]
4. Niesler C. Old dogmas and new hearts: a role for adult stem cells in cardiac repair? Cardiovasc J S Afr 2004; 15: 184-9. [ Links ]
5. Hoffman R, Benz EJ, Shattil SJ, Furie B, Cohen HJ, Silberstein LE. Stem cell model of hematopoiesis. En: Hematology: Basic principles and practice. Philadelphia, EE.UU.: Churchill Livingstone. 2000. p 126 138. [ Links ]
6. Ivanova N, Dimos JT, Schaniel C, Hackney JA, Moore KA, Lemischka IR. A stem cell molecular signature. Science. 2002; 298: 601-4. [ Links ]
7. Mayani H, Alvarado-Moreno JA, Flores-Guzmán P. Biology of human hematopoietic stem and progenitor cells present in circulation. Arch. Med. Res. 2003; 34: 476-88. [ Links ]
8. Weissman IL. Stem cells: units of development, units of regeneration and units in evolution. Cell. 2000; 100: 157-168. [ Links ]
9. Morrison SJ, Wandyez AM, Hemmati HD, Wright DE, Weissman IL. Identification of a lineage of multipotent hematopoietic progenitors. Development. 1997; 124: 1929-39. [ Links ]
10. Hoffman R, Benz EJ, Shattil SJ, Furie B, Cohen HJ, Silberstein LE, McGlave P. Stem cell model of hemtopoiesis. En: Hematology: Basic principles and practice Philadelphia, EE.UU. Churchill Livingstone. 2000. p 126-38. [ Links ]
11. Reya T, Morrison SJ, Clarke MF, Weissman IL. Stem cells, cancer, and cancer stem cells. Nature. 2001; 414: 105-11. [ Links ]
12. Panoskaltsis N, Mantalaris A, Wu D. Engeneering a mimicry of bone marrow tissue ex vivo. J. Biosci. Bioeng. 2005; 100: 28-35. [ Links ]
13. Quesenberry PJ, Crittenden RB, Lowry P, Kittler EW, Rao S, Peters S, et al. In vitro and in vivo studies of stromal niches. Blood Cells. 1994; 2: 97-104. [ Links ] Citado por: Hoffman R, Benz EJ, Shattil SJ, Furie B, Cohen HJ, Silberstein LE, McGlave P. Anatomy and physiology of hematopoiesis. En Hematology: Basic principles and practice. Philadelphia, EE.UU.: Churchill Livingstone. 2000. p 139-54.
14. Hoffman R, Benz EJ, Shattil SJ, Furie B, Cohen HJ, Silberstein LE, McGlave P. Anatomy and physiology of hematopoiesis. En Hematology: Basic principles and practice. Philadelphia, EE.UU.: Churchill Livingstone. 2000. p 139-54. [ Links ]
15. Hoffman R. Benz EJ, Shattil SJ, Furie B, Cohen HJ, Silberstein LE, McGlave P. Chronic Myelogenous Leukemia. En: Hematology: Basic principles and practice. Philadelphia, EE.UU.: Churchill Livingstone. 2000. p 1155-71. [ Links ]
16. Toshio S, Arai F, Atsushi H. Hematopoietic stem cells and their niche. Trends immunol. 2005; 26: 426-33. [ Links ]
17. Till JE, McCulloch EA. A direct measurement of the radiation sensitivity of normal mouse bone marrow cells. Radiat. Res. 1961; 14: 213-22. [ Links ]
18. Szilvassy S. The Biology of hematopoietic stem cells. Arch Med Res 2003; 34: 446-60. [ Links ]
19. Dexter TM, Allen TD, Lajtha LG. Conditions controlling the proliferation of haemopoietic stem cells in vitro. J. Cell. Physiol. 1997; 91: 335-44. [ Links ]
20. Coloumbel L, Eaves AC, Eaves CJ. Enzymatic treatment of longterm marrow cultures reveals the preferential location of primitive hematopoietic progenitors in the adherent layer. Blood.1983; 62: 291-97. [ Links ] Citado por: Hoffman R, Benz EJ, Shattil SJ, Furie B, Cohen HJ, Silberstein LE, McGlave P. Anatomy and physiology of hematopoiesis. En Hematology: Basic principles and practice. Philadelphia, EE.UU.: Churchill Livingstone. 2000. p 139-54.
21. Benboubker L, Binet C, Cartron G, Bernard MC, Clement N, Delain M et al. Frequency and differentiation capacity of circulating LTC-IC mobilized by G-CSF or GM-CSF following chemotherapy: a comparison with steady-state bone marrow and peripheral blood. Exp. Hematol. 2002; 30: 74-81. [ Links ]
22. Wognum AW, Eaves AC, Thomas TE. Identification and isolation of hematopoietic stem cells. Arch. Med. Res. 2003; 34: 461-75. [ Links ]
23. Lanza F, Healy L, Sutherland DR. Structural and functional features of the CD34 antigen: an update. J. Biol. Regul. Homeost. Agents. 2001; 15: 1-13. [ Links ]
24. Sutherland DR, Keating A. The CD34 antigen: structure, biology, and potential clinical applications. J Hematother. 1992; 1: 115-29. [ Links ] Citado por Hoffman R, Benz EJ, Shattil SJ, Furie B, Cohen HJ, Silberstein LE, et al. Anatomy and physiology of hematopoiesis. En: editors. Hematology: Basic principles and practice. Philadelphia: Churchill Livingstone; 2000. p 139-54.
25. Young PE, Baumhueter S, Lasky LA. The sialomucin CD34 is expressed on hematopoietic cells and blood vessels during murine development. Blood. 1995; 85: 96-105. [ Links ] Citado por Hoffman R, Benz EJ, Shattil SJ, Furie B, Cohen HJ, Silberstein LE, McGlave P. Anatomy and physiology of hematopoiesis. En Hematology: Basic principles and practice. Philadelphia, EE.UU.: Churchill Livingstone. 2000. p 139-54.
]]>26. Wognum B. Hematopoietic Stem Cells. [Mini-review en internet] 2003; 1-6 Disponible de: www.stemcelltechnologies.com [ Links ]
27. Larochelle A, Vormoor J, Hanenberg H, Wang JCY, Bhatia M, Lapidot T et al. Identification of primitive human hematopoietic cells capable of repopulating NOD/SCID mouse bone marrow: implications for gene therapy. Nat. Med. 1996; 2: 1329-36. [ Links ]
28. Civin CI, Trischmann T, Kadan NS, Davis J, Noga S, Cohen K et al. Highly purified CD34-positive cells reconstitute hematopoiesis. J.Clin. Oncol. 1996; 14: 2224-33. [ Links ]
29. Vogel W, Scheding S, Kanz L, Brugger W. Clinical applications of CD34 (+) peripheral blood progenitor cells (PBPC). Stem Cells. 2000; 18: 87-92. [ Links ]
30. Verstegen MMA, Hennik PB, Terpstra W, van den Bos C, Wielenga JJ, van Rooijen N, et al. Transplantation of human umbilical cord blood cells in macrophage-depleted SCID mice: evidence for accessory cell involvement in expansion of immature CD34+CD38- cells. Blood. 1998; 91: 1966-76. [ Links ]
31. Bhatia M, Bonnet D, Murdoch B, Gan OI, Dick JE. A newly discovered class of human hematopoietic cells with SCID-repopulating activity. Nat. Med.1998; 4: 1038-1045. [ Links ]
32. Zanjani E, Almeida-Porada G, Livingston AG, Flake AW, Ogawa M. Human bone marrow CD34- cells engraft in vivo and undergo multilineage expression that includes giving rise to CD34+ cells. Exp Hematol. 1998; 26: 353-60. [ Links ]
33. Nakamura Y, Ando K, Chargui J, Kawada H, Sato T, Tsuji T, et al. Ex vivo generation of CD34+ cells from CD34- hematopoietic cells. Blood. 1999; 94: 4053-9. [ Links ]
34. Zanjani ED, Almeida-Porada G, Livingston AG, Zeng H, Ogawa M. Reversible expression of CD34 by adult human bone marrow long-term engrafting hematopoietic stem cells. Exp Hematol. 2003; 31: 406-12. [ Links ]
35. Gallacher L, Murdoch B, Wu DM, Karanu FN, Keeney M, Bhatia M. Isolation and characterization of human CD34-Lin- and CD34+Lin- hematopoietic stem cells using cell surface markers AC133 and CD7. Blood. 2000; 95: 2813-20. [ Links ]
36. Wang J, Kimura T, Asada R, Harada S, Yolota S, Kawamoto Y. et al. SCID-repopulating cell activity of human cord blood-derived CD34- cells assured by intrabone marrow injection. Blood. 2003; 101: 2924-31. [ Links ]
37. Yin AH, Miraglia S, Zanjani E, Almeida-Porada G, Ogawa M, Leary AG, et al. AC133, a novel marker for human hematopoietic stem and progenitor cells. Blood. 1997; 90: 5002-12. [ Links ]
38. Miraglia S, Godfrey W, Yin AH, Atkins K, Warnke R, Holden JT, et al. A novel five-transmembrane hematopoietic stem cell antigen: isolation, characterization, and molecular cloning. Blood. 1997; 90:5013-21. [ Links ]
39. Pasino M, Lanza T, Marotta F, Scarso L, De Biasio P, Amato,S, et al. Flow cytometric and functional characterization of AC133+ cells from human umbilical cord blood. Br. J. Haematol. 2000; 108: 793800. [ Links ]
40. Matsumoto K, Yasui K, Yamashita N, Horie Y, Yamada T, Tani Y, et al. In vitro proliferation potential of AC133 positive cells in peripheral blood. Stem Cells. 2000; 18: 196203. [ Links ]
41. Hess DA, Levac KD, Karanu FN, Rosu-Myles M, White MJ, Gallacher L et al. Functional analysis of human hematopoietic repopulating cells mobilized with granulocyte colony-stimulating factor alone versus granulocyte colony-stimulating factor in combination with stem cell factor. Blood. 2002; 100: 869-78. [ Links ]
42. Bhatia, M. AC133 expression in human stem cells. Leukemia. 2001; 15: 1685-88. [ Links ]
43. Hoffman R, Benz EJ, Shattil SJ, Furie B, Cohen HJ, Silberstein LE, McGlave P. Growth factors, Cytokines, and the Control of Hematopoiesis. En: Hematology: Basic principles and practice Philadelphia, EE.UU. Churchill Livingstone. 2000. p 139-54. [ Links ]
44. Conze T, Lammers R, Kuci S, Scherl-Mostageer M, Schwefer N, Kanz L et al. CDCP1 is a novel marker for hematopoietic stem cells. Ann N Y Acad Sci. 2003; 996: 222-26. [ Links ]
45. Bell DR, Van Zant G. Stem cells, aging, and cancer: invevitabilities and outcomes. Oncogen. 2004; 23:7290-96. [ Links ]
46. Attar EC, Scadden DT. Regulation of hematopoietic stem cell growth. Leukemia. 2004; 18: 176068. [ Links ]
47. Ezoe S. Matsumura I, Satoh Y, Tanaka H, Kanakura Y. Cell Cycle Regulation in Hematopoietic Stem/ Progenitor Cells. Cell Cycle. 2004; 3: 314-18. [ Links ]
48. Bhardwaj G, Murdoch B, Wu D, Baker DP, Williams KP, Chadwick K et al. Sonic hedgehog induces the proliferation of primitive human hematopoietic cells via BMP regulation. Nature Immunology. 2001; 2:172-180. [ Links ]
49. Hahn H, Christiansen J, Wicking C, Zaphiropoulos PG, Chidambaram A, Gerrard B, et al. A mammalian patched homolog is expressed in target tissues of sonic hedgehog and maps to a region associated with developmental abnormalities. J. Biol. Chem. 1996; 271: 12125-128. [ Links ]
50. Kalderon D. Transducing the Hedgehog signal. Cell. 2000; 103: 371-74. [ Links ]
51. Ingham PW. Trandsucing Hedgehog: the story so far. EMBO J. 1998; 17: 3505-11. [ Links ]
52. Taipale J, Beachy P. The Hedgehog and Wnt signalling pathways in cancer. Nature. 2001; 411: 349-54. [ Links ]
53. Peters C, Wolf A, Wagner M, Kuhlmann J, Waldmann H. The cholesterol membrane anchor of the Hedgehog protein confers stable membrane association to lipid-modified proteins. Proc. Natl. Acad. Sci. U.S.A. 2004; 101: 8531-6. [ Links ]
54. Artavanis-Tsakonas S, Rand MD, Lake R.J. Notch signaling: cell fate control and signal integration in development. Science. 1999; 284: 770-76. [ Links ]
55. Milner LA, Bigas A. Notch as a mediator of cell fate determination in hematopiesis: evidence and speculation. Blood. 1999; 93: 2431-48. [ Links ]
56. Aster JC, Pear WS. Notch signaling in leukemia. Curr Opin Hematol. 2001; 8: 237-244. [ Links ]
57. Bigas A, Martin DI, Milner LA. Notch1 and Notch2 inhibit myeloid differentiation in response to different cytokines. Molecular Cell Biology. 1998; 18: 2324-33. [ Links ]
58. Varnum-Finney B, Xu L, Brashem-Stein C, Nourigat C, Flowers D, Bakkour S, et al. Pluripotent, cytokine-dependent, hematopoietic stem cells are immortalized by constitutive Notch 1 signaling. Nat. Med. 2000; 6: 1278-81. [ Links ]
59. Staal FJT, Clevers HC. WNT signalling and haematopoiesis: a WNT situation. Nat. Rev. Immunol. 2005; 5: 21-30. [ Links ]
60. Willert K, Brown JD, Danenberg E, Duncan AW, Weissman IL, Reya T, et al. Wnt proteins are lipidmodified and can act as stem cell growth factors. Nature. 2003; 423: 448-52. [ Links ]
61. Nusse R. Wnts and Hedgehogs: lipid-modified proteins and similarities in signaling mechanisms at the cell surface. Development. 2003; 130: 5297-5305. [ Links ]
62. Wodarz A, Nusse R. Mechanisms of Wnt signaling in development. Annu. Rev. Cell Dev. Biol. 1998; 14:5988. [ Links ]
63. Mao J, Wang J, Liu B, Pan W, Farr GH 3rd, Flynn C, et al.. Low-density lipoprotein receptor-related protein-5 binds to Axin and regulates the canonical Wnt signaling pathway. Mol. Cell. 2001; 7: 801-9. [ Links ]
64. Behrens J, Jerchow BA, Wurtele M, Grimm J, Asbrand C, Wirtz R . Functional interaction of an axin homolog, conductin, with b-catenin, APC, and GSK3b. Science. 1998; 280: 59699. [ Links ]
65. Roose J, Molenaar M, Peterson J, Hurenkamp J, Brantjes H, Moerer P, et al. The Xenopus Wnt effector XTcf-3 interacts with Groucho-related transcriptional repressors. Nature. 1998; 395: 60812. [ Links ]
66. Barker N, Hurlstone A, Musisi H, Miles A., Bienz M, Clevers H. The chromatin remodeling factor Brg-1 interacts with b-catenin to promote target gene activation. EMBO J. 2001; 20: 493543. [ Links ]
67. Takemaru K, Yamaguchi S, Lee YS, Zhang Y, Carthew RW, Moon RT. Chibby, a nuclear ?-catenin associated antagonist of the Wnt/Wingless pathway. Nature. 2003; 422: 9059. [ Links ]
68. Daniels DL, Weis WI. ICAT inhibits ?-catenin binding to Tcf/Lef-family transcription factors and the general coactivator p300 using independent structural modules. Molecular Cell. 2002; 10: 573584. [ Links ]
69. Reya T, Duncan AW, Ailles L, Domen J, Scherer DC, Willert K, et al. A role for Wnt signaling in selfrenewal of haematopoietic stem cells. Nature. 2003; 423: 40914. [ Links ]
70. Maeno M, Mead PE, Kelley C, Xu RH, Kung HF, Suzuki A, et al. The role of BMP-4 and GATA-2 in the induction and differentiation of hematopoietic mesoderm in Xenopus laevis. Blood. 1996; 88: 196572. [ Links ]
71. Bhatia M, Bonnet D, Wu D, Murdoch B, Wrana J, Gallacher L. et al. Bone morphogenetic proteins regulate the developmental program of human hematopoietic stem cells. J. Exp. Med. 1999; 189: 113948. [ Links ]
72. Sauvageau G, Lansdorp PM, Eaves CJ, Hogge DE, Dragowska WH, Reid DS, et al. Differential expression of homeobox genes in functionally distinct CD34+ subpopulations of human bone marrow cells. Proc. Natl. Acad. Sci. U.S.A. 1994; 91: 122237. [ Links ]
73. Giampaolo A, Sterpetti P, Bulgarini D, Samoggia P, Pelosi E, Valtieri M let al.. Key functional role and lineage-specific expression of selected HOXB genes in purified hematopoietic progenitor differentiation. Blood. 1994; 84: 363747. [ Links ]
74. Amsellem S, Pflumio F, Bardinet D, Izac B, Charneau P, Romeo PH, et al. Ex vivo expansion of human hematopoietic stem cells by direct delivery of the HOXB4 homeoprotein. Nat Med. 2003; 9: 142327. [ Links ]
75. Krosl J, Austin P, Beslu N, Kroon E, Humphries RK, Sauvageau G. In vitro expansion of hematopoietic stem cells by recombinant TAT-HOXB4 protein. Nat. Med. 2003; 9: 142832. [ Links ]
76. Sauvageau G, Thorsteinsdotti U, Eaves CJ, Lawrence HJ, Largman C, Lansdorp PM, et al. Overexpression of HOXB4 in hematopoietic cells causes the selective expansion of more primitive populations in vitro and in vivo. Genes Dev. 1995; 9: 175365. [ Links ]
77. Thorsteinsdottir U, Sauvageau G, Humphries RK. Enhanced in vivo regenerative potential of HOXB4- transduced hematopoietic stem cells with regulation of their pool size. Blood. 1999; 94: 260512. [ Links ]
78. Park IK, Qian D, Kiel M, Becker MW, Pihalja M, Weissman IL, et al. Bmi-1 is required for maintenance of adult selfrenewing haematopoietic stem cells. Nature. 2003; 423: 3025. [ Links ]
79. Lessard J, Sauvageau G. Bmi-1 determines the proliferative capacity of normal and leukaemic stem cells. Nature. 2003; 423: 255260. [ Links ]
80. Kalderon D. Similarities between the Hedgehog and Wnt signalling pathways. Trends Cell Biol. 2002; 12:523-531. [ Links ]
81. Duncan AW, Rattis FM, DiMascio LN, Congdon KL, Pazianos G, Zhao C et al. Integration of Notch and Wnt signaling in hematopoietic stem cell maintenance. Nat. Immunol. 2005; 6: 314-322. [ Links ]
82. Jones P, May G, Healy L, Brown J, Hoyne G, Delassus S et al .Stromal expression of Jagged 1 promotes colony formation by fetal hematopoietic progenitor cells. Blood. 1998; 92: 1505-11. [ Links ] ]]>