INHIBICIÓN DE LESIONES POR FRÍO DE PITAYA AMARILLA (Acanthocereus pitajaya) A TRAVÉS DEL CHOQUE TÉRMICO: CATALASA, PEROXIDASA Y POLIFENOLOXIDASA
Inhibition of Chillyng Injury in Pitaya Amarilla (Acanthocereus pitajaya) Fruit by Heat Shock: Catalese, Peroxidase and Polyphenoloxidase
YENNY MARITZA DUEÑAS GÓMEZ1*, M.Sc.; CARLOS EDUARDO NARVÁEZ CUENCA1**, M.Sc.; LUZ PATRICIA RESTREPO SÁNCHEZ1***, M.Sc.
1Universidad Nacional de Colombia, Facultad de Ciencias, Departamento de Química. Carrera 30 No.45-03, Bogotá. *yemadugo@hotmail.com - **cenarvaezc@unal.edu.co ***lprestrepos@unal.edu.co
Presentado 4 de mayo de 2007, aceptado 11 de diciembre de 2007, correcciones 9 de febrero de 2008.
RESUMEN
En los ensayos de almacenamiento de pitaya a temperatura ambiente de Bogotá (18 ºC) se encontró que esta fruta tiene un comportamiento climatérico con un máximo en la respiración luego de tres días de iniciado el almacenamiento. En el máximo climatérico la actividad de catalasa fue máxima, en tanto que en la etapa de senescencia las actividades de peroxidasa y polifenoloxidasa exhibieron valores máximos. El choque térmico inhibió las lesiones por frío, vistas en los frutos refrigerados a 2 °C, este choque incrementó la actividad de catalasa y peroxidasa y disminuyó la actividad de polifenoloxidasa, respecto a los frutos refrigerados sin tratamiento de choque térmico. Los resultados muestran que la catalasa está en relación directa con la vida útil del fruto, mientras que polifenoloxidasa guarda estrecha relación con el deterioro. La peroxidasa manifiesta su acción antioxidante con la generación de pardeamiento, en frutos almacenados a temperatura ambiente, si bien en los tratados con choque térmico, su acción antioxidante no va de la mano con el incremento en el pardeamiento, por lo que en este caso, su expresión fue favorable. Los resultados encontrados se constituyen en un aporte en la búsqueda de técnicas que permitan mayores tiempos de vida en anaquel de los frutos.
Palabras clave: catalasa, peroxidasa, polifenoloxidasa, enzimas antioxidantes, pardeamiento.
ABSTRACT
]]> In the storage of yellow pitaya fruit at room temperature in Bogotá (18 ºC), it was found that this fruit has a climacteric behavior with a maximum in the respiration after 3 days of its storage. In the climacteric the activity of catalase was higher, while in the senescence stage the activities of peroxidase and polyphenoloxidase exhibited maximum values. The heat shock inhibited the chilling injury, shows in the fruits refrigerated at 2 °C, this heat shock increased the activity of catalase and peroxidase and it delayed the activity of polyphenoloxidase, regarding the fruits refrigerated without treatment of heat shock. The results show that catalase is in direct relationship with the useful life of the fruit, while polyphenoloxidase keeps it narrows relationship with the deterioration. In fruits stored at room temperature, peroxidase exhibited its antioxidant action with browning generation, although in the treaties with heat shock, their antioxidant action doesn’t go of the hand with increment in the browning, for that in this case, its expression was favorable. The opposing results are constituted in a contribution in the search of techniques that allow bigger times of life in shelf of the fruits.Key words: Catalase, peroxidase, polyphenoloxidase, antioxidant enzymes, browning.
INTRODUCCIÓN
La pitaya amarilla (Acanthocereus pitajaya) es una fruta exótica muy apetecida para su consumo en diversos países del mundo, gracias a su contenido nutricional, sabor, aroma y en general, al impacto sensorial que genera. En el marco de las exportaciones, para el mes de octubre de 2006 el país exportó 5,8 ton de pitaya amarilla, con un total de 117 ton entre los meses de enero a octubre, con importantes volúmenes a la Unión Europea y a Estados Unidos, entre otros (www.cci.org.co, 2008). Aunque existe un reporte que clasifica a la pitaya amarilla como fruto no climatérico (Nerd y Mizrahi, 1998); existen otros estudios que catalogan a la pitaya amarilla como fruto climatérico, porque se presenta un máximo en su actividad respiratoria y en sus características sensoriales luego de 14 días de almacenada a 18 ºC (Camargo y Moya, 1995) y de tres días luego de almacenada a 24 °C (Baquero et al., 2005). Después de este máximo se ha observado que el pardeamiento y la necrosis en la corteza son los principales factores de deterioro. Por esta razón, se han evaluado algunas técnicas que prolonguen su calidad por mayores períodos de tiempo, entre los que se encuentran la refrigeración tanto a 2 (Camargo y Moya, 1995) como a 8 ºC (Rodríguez y Patiño, 2003). Sin embargo, en ambos casos aparecen lesiones por frío. Estas lesiones se caracterizan por un comportamiento irregular en la respiración y la aparición de manchas de color marrón, zonas necróticas y ablandamiento excesivo (Camargo y Moya, 1995; Rodríguez y Patiño, 2003).
La aplicación de choque térmico, a 25 ºC durante 24 horas, antes de refrigeración de los frutos de pitaya a 2 ºC, se reporta como un método adecuado para aliviar las lesiones por frío, con lo que se logra conservar la calidad sensorial de la fruta durante 19 días (Camargo y Moya, 1995). Las zonas necróticas y el pardeamiento se han relacionado con la participación de enzimas como catalasa, peroxidasa y polifenoloxidasa. La catalasa (CAT, E.C. 1.11.1.6) degrada el H2O2 y tiene la particularidad de evitar la necrosis de los frutos que suele aparecer durante la senescencia y en las lesiones por frío (Omran, 1980; Sala y Lafuente, 2000). La polifenoloxidasa (PFO,E.C. 1.10.3.2 ó 1.14.18.1) y la peroxidasa (POD, E.C. 1.11.1.7) han sido relacionadas con el oscurecimiento de diversos vegetales durante la senescencia o durante la generación de lesiones por frío (Omran, 1980; Nete y Kadioglu, 2001; Zhou et al., 2003; Vicente et al., 2006). La PFO actúa sobre sustratos de carácter fenólico y como producto de su actividad se gene-ran quinonas que pueden polimerizarse para generar colores pardos. Por su parte, la POD degrada el H2O2, para lo cual usa un donador de protones que puede ser una sustancia de carácter fenólico; como producto de reacción aparecen quinonas que tras reacciones no enzimáticas generan polímeros pardos. La POD también puede usar el ascorbato como donador de protones en cuyo caso se habla de la ascorbato peroxidasa (AsPOD, EC 1.11.1.11). Esta enzima degrada el H2O2 con el beneficio de no generar colores pardos, por lo que es clasificada como enzima antioxidante (Sala y Lafuente, 2000; Zhou et al., 2003). Por tanto, dependiendo del sustrato sobre el cual actúe la POD, se va a degradar el H2O2 con la generación o no de pardeamiento. En estudios de almacenamiento, con miras a la prolongación del tiempo de vida útil, de diversos materiales vegetales, se muestra el papel importante que ejerce la CAT en la prevención de la aparición de lesiones por frío (Fernandez-Trujillo et al., 1998; Kang y Saltveit, 2002). En relación a la actividad antioxidante que eventualmente pudiera ejercer la AsPOD, se pone de manifiesto que ésta también contribuye en la prevención de los síntomas asociados a necrosis, tal como lo reportan en fresas (Vicente et al., 2006). También se reporta que un tratamiento de choque térmico realizado en uva, genera un incremento en la actividad tanto de CAT como de POD con respecto al control (Zhang et al., 2005). Con respecto a la PFO y POD vinculadas con el pardeamiento, los estudios demuestran que, aunque en algunos casos no se inhibe completamente la actividad de éstas, se logra una disminución de sus actividades luego de la maduración complementaria (Rubio, 1999; Nete y Kadioglu, 2001; Zhou et al., 2003) y por tanto se logra prolongar el tiempo de vida útil. En torno al deterioro de la pitaya se ha realizado un estudio parcial de las enzimas CAT, POD y PFO extraídas de la corteza de los frutos sensorialmente maduros (Castro et al., 2006).
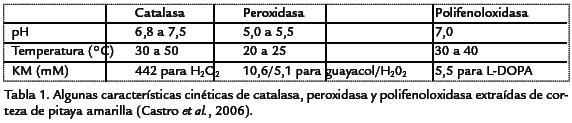
En este trabajo se reportan algunas características cinéticas como aparece en la Tabla 1. De acuerdo a los autores antes citados, estos resultados indican que efectivamente existe una alta afinidad de la PFO por L-DOPA, por lo que esta enzima puede ser responsable en buena medida del pardeamiento de la corteza de pitaya. De otro lado, los valores de afinidad para CAT y POD sugieren un papel complementario entre estas dos enzimas al momento de degradar el H2O2. En este sentido, se espera que cuando la concentración de H2O2 sea alta en la célula, la POD estará inhibida, en tanto que la CAT estará degradando efectivamente este compuesto. Si la concentración del H2O2 es baja, será la POD quien esté encargada de su degradación. Los resultados obtenidos en un ensayo de almacenamiento de este fruto a 24 °C (Baquero et al., 2005) proporcionan más herramientas para vincular la PFO y la POD con el pardeamiento observado en la corteza, en tanto que una alta actividad de CAT se relaciona con una alta calidad sensorial. Aunque se ha encontrado que la actividad de CATes alta durante el climaterio y que existe una relación directa entre el pardeamientode la corteza de pitaya amarilla con la actividad de POD y PFO (Baquero et al., 2005),no se ha evaluado el comportamiento de estas enzimas en frutos refrigerados ni en lostratados con choque térmico. El objetivo de este trabajo fue evaluar el papel de lasenzimas CAT, POD y PFO durante la maduración y senescencia de pitaya amarillaalmacenada a 18 °C. También se investigó la relación de estas enzimas tanto con losdaños como con la tolerancia al frío, inducida con un tratamiento de choque térmico.

MATERIALES Y METODOS
MATERIAL VEGETAL
]]> Se recolectaron las pitayas en estado verde-pintón (90% verde-10% amarilla en lacorteza), se seleccionaron por sanidad, se desinfectaron con hipoclorito de sodio al1% y se dividieron en tres grupos para su almacenamiento, cada uno con aproxi-madamente 40 frutos.ALMACENAMIENTO
Un primer lote de frutos se almacenó a temperatura ambiente de 18 ºC, durante 21días. En el segundo grupo, los frutos se refrigeraron a 2 ºC durante 15 días, con poste-rior almacenamiento a temperatura ambiente. Por último, en el tercer grupo, los fru-tos se almacenaron en una cámara a 25 ºC durante 24 horas (tratamiento de choquetérmico), tiempo después del cual se llevó a refrigeración (2 ºC) durante 15 días, conposterior maduración a temperatura ambiente, 18 °C. De cada ensayo de almace-namiento, se tomaron al azar tres pitayas, cada tres días, y se hicieron las medidas deintensidad respiratoria y de actividad de CAT, POD y PFO.
INTENSIDAD RESPITATORIA.
Se evaluó utilizando un sensor de CO2(Vernier Software & Technology, CO2Gas SensorCO2-BTA). La pitaya se pesó y se confinó durante una hora (tiempo en el que el frutoha respirado y modificado la atmósfera) en una cámara, donde una vez cumplido eltiempo, se hizo lectura del CO2producido por el fruto. La intensidad respiratoria sereportó como mg de CO2/kg de fruta*h.
ACTIVIDAD ENZIMÁTICA
Las enzimas se extrajeron a partir de la corteza de los frutos, teniendo en cuenta los resultados obtenidos por Castro et al.(2006). La técnica consistió en la obtención de polvos de acetona. Se homogenizó la corteza con acetona a -8 °C; se filtró y el retenido se lavó con acetona a -8 °C hasta obtener un sólido incoloro, el cual se resuspendió en buffer fosfatos 200 mM, pH 7,0, con agitación continua durante 24 horas a 2 °C. La relación entre la cantidad de corteza y el volumen de buffer fue de 1 g a 5 mL. Finalmente, el sobrenadante se centrifugó a 6.000 rpm durante 1 h a 4 ºC; el sedimento se desechó y el sobrenadante se utilizó para las medidas de proteína y de actividad enzimática.
CUANTIFICACIÓN DE PROTEÍNA
La proteína se cuantificó en los extractos enzimáticos por el método de Bradford modificado, con lectura de absorbancia a 450 nm y 590 nm. Como patrón de cuantificación se empleó BSA (Zor y Zellinger, 1996).
Actividad de catalasa. Para la medida de actividad se empleó el método permanganométrico. La medida se realizó teniendo en cuenta las recomendaciones efectuadas en un trabajo previo (Castro et al., 2006). El volumen final de la mezcla de reacción fue de 1 mL, que consistió en 100 µL de extracto enzimático más H2O2 500 mM en buffer fosfatos 200 mM pH 7,0 a 40 ºC. Luego de 5 min de incubación se adicionaron 250 µL de H2SO4 (1:3). Al final, se tituló el H2O2 no descompuesto con KMnO4 estandarizado (10 mM). Para el blanco, el H2SO4 se incorporó antes de adicionar el extracto enzimático. La actividad específica se expresó en unidades de actividad por mg de proteína (UCAT/mg proteína). Una unidad de actividad (UCAT) se definió como los µmol H2O2 descompuesto/min.
]]> Actividad de peroxidasa. La actividad de esta enzima se estimó por la medida espectrofotométrica del incremento de la absorbancia a 470 nm en espectrofotómetro cada 5 s durante 120 s. La mezcla con un volumen final de 2 mL, contenía 200 µL de extracto enzimático y una mezcla de guayacol/H2O2 40 mM/20 mM en buffer citratos pH 5,5. La mezcla se incubó a 25 ºC. Para el blanco de reacción la enzima se inactivó empleando un baño maría a 92 °C durante 10 min (Castro et al., 2006). Una unidad de actividad (UPOD) se definió como el cambio en una unidad de absorbancia por min. La actividad específica se expresó en unidades de actividad por mg de proteína (UPOD/mg proteína).Actividad de polifenoloxidasa. Para medir la actividad de esta enzima se efectuó lectura de absorbancia a 475 nm en un espectrofotómetro cada 5 s durante 120 s. La mezcla de reacción de 2 mL consistió en 1.000 µL de extracto enzimático más L-DOPA 14 mM en buffer fosfatos 200 mM pH 7,0 a 37 ºC. El blanco se preparó igual que en POD (Castro et al., 2006). Tanto la unidad de actividad (UPFO) como la actividad específica (UPFO/mg proteína) se definieron de igual manera que en POD.
ANÁLISIS DE DATOS
Las determinaciones de intensidad respiratoria se llevaron a cabo por triplicado. Las medidas de actividad enzimática se realizaron con un número total de nueve réplicas. Se calcularon los promedios y las desviaciones estándar. Además, se efectuó el análisis de varianza para todas las variables estudiadas.
RESULTADOS
RESPIRACIÓN
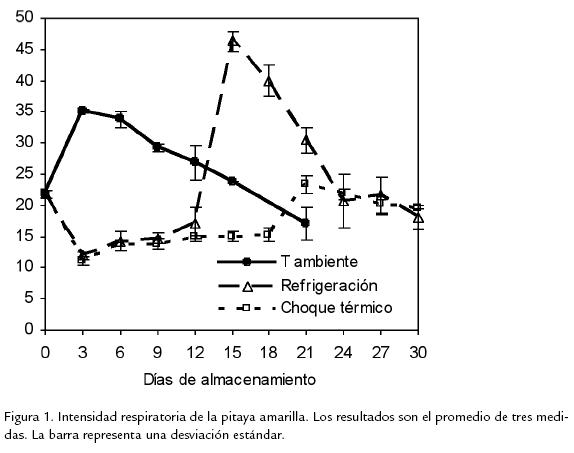
Cuando los frutos fueron almacenados a 18 °C hubo dos fases (Figura 1). En la primer fase, que va del día 0 al 3, hubo un incremento brusco en la respiración hasta un máximo, que coincidió con las mejores características sensoriales y en la segunda, de los días 6 a 21, fueron evidentes la disminución en la producción de CO2, que coincide con cambios negativos en el color y en la textura de la corteza. La refrigeración, con y sin choque térmico previo, disminuyó de manera significativa la respiración de los frutos. En los frutos refrigerados sin choque térmico previo, se presentó un máximo en la intensidad respiratoria hacia el día 15. Además, en este día empezaron a generarse zonas necróticas y de pardeamiento. Finalmente, tras la aplicación del choque térmico con posterior refrigeración, no se observó aumento significativo en la intensidad respiratoria al momento de sacar los frutos a maduración complementaria. Sin embargo, 6 días después, es decir en el día 21, el fruto había logrado las mejores características organolépticas y se observó un máximo en la respiración.
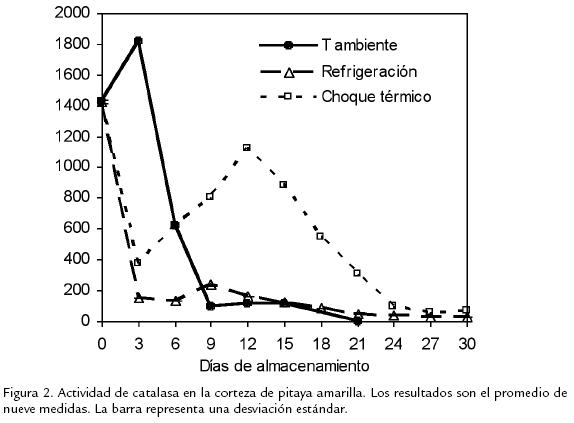
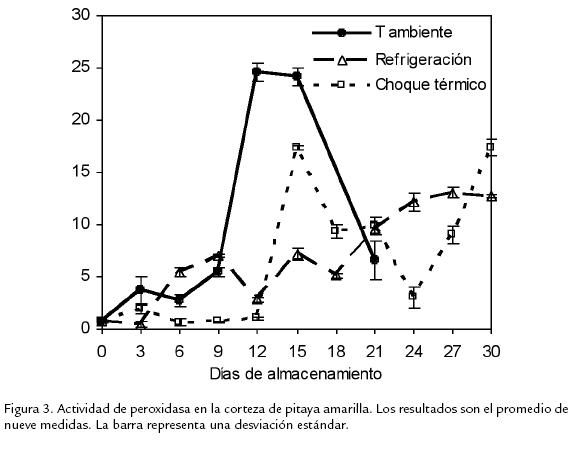
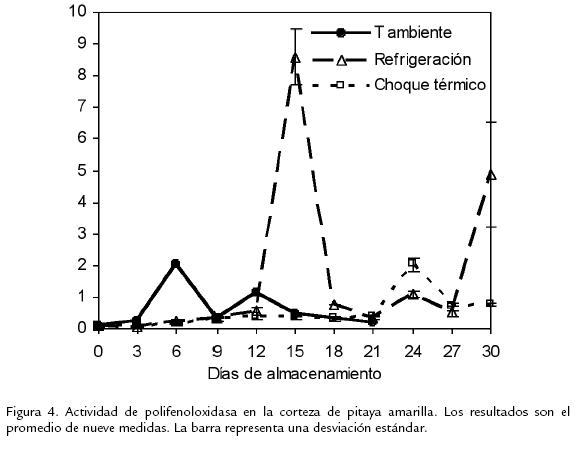
En la Figura 2, se observa que en los frutos almacenados a temperatura ambiente, la CAT manifestó su máximo de actividad en el día 3, con una consecuente disminución a partir del día 6 hasta el final del almacenamiento. En la misma figura, se aprecia también que el frío disminuyó la actividad de esta enzima. La actividad de CAT en los frutos refrigerados sin choque térmico previo permaneció significativamente inferior respecto de los frutos tratados con choque. En estos últimos hubo un máximo en la actividad de CAT luego de 12 días de almacenamiento en refrigeración. La actividad de POD en los frutos almacenados a temperatura ambiente (Figura 3), se incrementó a partir del día 9, justo cuando empezó la senescencia de la pitaya amarilla. En los frutos refrigerados se presentó una tendencia al incremento en la actividad de POD a lo largo de todo el almacenamiento. La actividad de la POD en los frutos tratados con choque térmico mostró un máximo una vez los frutos fueron llevados a maduración complementaria (día 15), con un descenso posterior en su actividad hasta el día 24, a partir del cual la actividad se hizo cada vez mayor. Los resultados mostrados en la Figura 4 indican que la actividad de PFO se incrementa de manera importante después del pico climatérico con una disminución posterior en su actividad. Durante el almacenamiento refrigerado la actividad de PFO se mantiene baja tanto en los frutos pretratados con choque térmico como en los que no recibieron este tipo de tratamiento. Una vez los frutos fueron retirados de la cámara de refrigeración y puestos a temperatura ambiente se presentó un pico en la actividad en los frutos refrigerados sin choque térmico previo, en tanto que en los frutos sometidos al choque térmico la actividad permaneció baja, excepto en el día 24 en el que hubo un máximo.
DISCUSIÓN
La pitaya presenta un comportamiento característico de un fruto climatérico, dado que en los tres tratamientos aplicados se aprecian dos fases características en el patrón respiratorio de este grupo de alimentos. La primera fase se caracteriza por un aumento en la intensidad respiratoria de los frutos, ya que los carbohidratos, proteínas y ácidos orgánicos son metabolizados, produciendo CO2, pO y energía en gran cantidad; de igual manera este incremento coincide con los cambios de color, aroma y textura. La segunda fase es aquella donde una vez alcanzadas las características sensoriales óptimas, la producción de CO2 decrece, razón por la cual, los frutos entran en la etapa de senescencia, caracterizada por un excesivo pardeamiento y ablandamiento. Los valores en la producción de CO2 en los frutos de pitaya amarilla almacenados a temperatura ambiente son similares a los reportados por Gallo (1996), los cuales oscilan entre 20 a 80 mg CO2/kg fruta*h. Las diferencias encontradas con relación al máximo climatérico reportadas en otros trabajos se pueden atribuir al estado de madurez de la fruta y a las variaciones de temperatura presentadas en dichos experimentos. Así, este máximo se presentó luego de seis días de almacenamiento a 24 °C (Baquero et al., 2005). En otros reportes se indica que los frutos alcanzan el máximo climatérico hacia los 14 (Camargo y Moya, 1995; Rodríguez y Patiño, 2003) y 16 días (Garnica y Quintero, 1994) de iniciado el almacenamiento a temperatura ambiente de Bogotá. La disminución en la respiración de los frutos refrigerados con y sin choque térmico previo, durante el almacenamiento en frío hace pensar que el metabolismo de las macromoléculas fue limitado. De otro lado, el incremento en la respiración observado en los frutos refrigerados sin choque térmico previo hacia el día 15 de almacenamiento se puede atribuir a un alto metabolismo de los principales constituyentes del fruto como respuesta al estrés generado por el cambio de temperatura. Este incremento en la respiración estuvo acompañado con la aparición de zonas necróticas, pardeamiento y ablandamiento excesivo en la corteza de los frutos, que se incrementaron durante el tiempo de almacenamiento por fuera de la cámara de refrigeración. Estas alteraciones son atribuidas a las lesiones por frío. A diferencia de los frutos refrigerados sin pretratamiento, en los tratados con choque térmico la respiración se mantuvo siempre baja, por lo que el metabolismo se controló de manera acertada, de tal manera que no hubo aparición de lesiones por frío. El máximo respiratorio observado en este tratamiento corresponde al máximo climatérico, puesto que allí el fruto había desarrollado su madurez sensorial. Con la aplicación del choque térmico, hubo inhibición de los daños por frío en la corteza de los frutos, factor favorable que permitió conservar y extender el tiempo de vida útil.
]]> CATALASAEn los frutos almacenados a temperatura ambiente la actividad de CAT fue máxima justo en el pico climatérico. En este período es de vital importancia el balance entre el alto metabolismo oxidativo y el control de especies reactivas de oxígeno, entre las que se encuentra el H2O2 (Omran, 1980), que debe conllevar a la maduración del fruto. Una vez alcanzada la madurez sensorial, el fruto continúa con los procesos oxidativos, dando lugar a la senescencia, con la aparición de zonas necróticas, lo que puede ser consecuencia del desequilibrio causado entre la alta concentración de oxígeno y la baja actividad de CAT (Saltveit, 2001). En los frutos refrigerados sin choque térmico el máximo en la intensidad respiratoria no va de la mano con una alta actividad de CAT, por lo que el H2O2 generado durante el metabolismo oxidativo no pudo ser degradado por enzimas como la CAT, como resultado de una posible alteración en la transcripción de esta enzima. Esta falla en la degradación del H2O2 pudo generar una acumulación de esta especie, con la generación de zonas necróticas, causadas por el frío. Con respecto al comportamiento de la CAT observado en los frutos tratados con choque térmico se puede inferir que la actividad de la enzima a lo largo del almacenamiento ejerció un papel importante, dado que en los frutos no se evidenciaron las zonas necróticas. La alta actividad de CAT durante el almacenamiento en frío, comparada con los frutos refrigerados sin choque, puede estar relacionada con una degradación efectiva del H2O2, con lo cual, se evitaría la aparición de los daños por frío. Puesto que el H2O2 es una fuente importante de radicales hidroxilo, sustancias que atacan las macromoléculas de la célula, una alta actividad de CAT controla la producción de radicales hidroxilo, al degradar el compuesto a partir del cual se generan (Sala, 1998).
PEROXIDASA
La coincidencia entre la alta actividad de POD y el pardeamiento presentado en los frutos post-climatéricos almacenados a temperatura ambiente pone a esta enzima como responsable del pardeamiento de la corteza de los frutos de pitaya. Como los procesos oxidativos prosiguen durante la senescencia, los niveles de H2O2 aumentan y hay rompimiento de las vacuolas que contienen los fenoles, permitiendo a la POD oxidarlos a quinonas, las cuales por polimerización generan pigmentos pardos, que son los que contribuyen al oscurecimiento de la corteza (Baquero et al., 2005). La disminución en la actividad de la POD hacia el final del almacenamiento a temperatura ambiente puede atribuirse al estado avanzado de senescencia de los frutos en el que los productos de reacción enzimática inhiben la enzima. De otro lado, el comportamiento en la actividad de la enzima en los frutos refrigerados, responde al pardeamiento reflejado en la corteza, dado que una vez los frutos fueron retirados de la cámara de refrigeración, el pardeamiento empezó a ser notorio. Aunque el pardeamiento a 2 ºC fue más intenso en comparación con el de los frutos almacenados a temperatura ambiente, se observaron mayores valores de actividad en los frutos almacenados a temperatura ambiente. Posiblemente el estrés generado en el fruto, como resultado de la refrigeración a 2 °C, generó una mayor descompartimentalización de las enzimas y de los sustratos, lo que generó un pardeamiento con mayor intensidad. En los frutos con choque térmico el máximo observado hacia el día 15 exhibe el papel antioxidante que puede llegar a ejercer esta enzima. En este sentido, es interesante que aunque se observa un máximo en la actividad en POD, no hubo deterioro apreciable en el color de la corteza de estos frutos. Cuando los frutos fueron tratados con choque térmico, las lesiones por frío fueron inhibidas y los frutos maduraron satisfactoriamente hacia el día 21. Podría pensarse que aunque la actividad de esta enzima sea alta, esté separada físicamente de los fenoles, por lo que no habría catálisis sobre este tipo de sustancias. También podría darse que el donador de protones no sea una sustancia de carácter fenólico sino el ascorbato, por ejemplo. Es conocido que la POD puede tener como donor de protones, además de sustancias de carácter fenólico, el ascorbato, por lo que en este caso la POD degrada el H2O2 sin la generación de colores pardos (Zhou et al., 2003). La tendencia al incremento en la actividad POD al finalizar el almacenamiento, se relaciona con el pardeamiento, aunque no muy avanzado, en la corteza de estos frutos.
POLIFENOLOXIDASA
La alta actividad de la PFO después del máximo climatérico explica el pardeamiento observado en los frutos de pitaya amarilla durante el almacenamiento a temperatura ambiente. Por otro lado, en los frutos refrigerados sin choque térmico, la máxima actividad de esta enzima se dio hacia el día 15, lo que coincide con el inicio de la formación de colores pardos en la corteza. En los frutos tratados con choque térmico la actividad de esta enzima se incrementó notoriamente hacia el día 24, día en el que, igual que en los tratamientos anteriores, se empezó a evidenciar el pardeamiento. La actividad de la PFO se redujo sustancialmente con la aplicación de choque térmico respecto a los frutos refrigerados sin choque, dado que con este tipo de tratamientos la actividad de las enzimas involucradas en el pardeamiento se inhibe, por tanto previene la formación de pigmentos oscuros. La formación de los pigmentos oscuros es debido a que según el estrés ejercido en el fruto, se altera la estructura del tejido, ocasionando una desorganización de los compartimentos que separan a la PFO de la célula incluyendo los sustratos fenólicos, creando un medio favorable para que la enzima y los polifenoles reaccionen y rápidamente formen quinonas poliméricas por oxidación enzimática (Concellón et al., 2004; Jiang et al., 2004). Los resultados obtenidos en la presente investigación muestran que la CAT ejerce un papel importante en la protección al frío inducida con un tratamiento de choque térmico. La PFO se relaciona de manera directa con el pardeamiento, y su actividad es marcadamente reducida como resultado de la aplicación del choque térmico. La POD responde también al pardeamiento observado en los frutos almacenados a 18 y a 2 °C sin choque térmico previo. Sin embargo, al aplicar el tratamiento de choque, se observó un pico de actividad después de la salida a maduración complementaria, en donde no hubo pardeamiento, por lo que su actividad podría relacionarse más con una actividad antioxidante, como AsPOD, que con su capacidad de generar pardeamiento, actividad POD. Las tendencias observadas en la actividad de las enzimas en los frutos almacenados a 18 °C es similar a la observada en un trabajo previo, en el que los frutos se almacenaron a 24 °C (Baquero et al., 2005).
AGRADECIMIENTOS
Los autores agradecen a la Universidad Nacional de Colombia por su apoyo económico a través de la DIB, código del proyecto: 8003003.
BIBLIOGRAFÍA
BAQUERO E, CASTRO J, NARVÁEZ C. Catalasa, peroxidasa y polifenoloxidasa en pitaya amarilla (Acanthocereus pitajaya): maduración y senescencia. Act biol. Colomb. 2005;10(2):49-60. [ Links ]
CAMARGO A, MOYA O. Estudio preliminar de la influencia del choque térmico en la inhibición de los daños por frío en la pitaya amarilla (Acanthocereus pitajaya) [trabajo de grado]. Bogotá: Departamento de Farmacia, Facultad de Ciencias, Universidad Nacional de Colombia; 1995. [ Links ]
CASTRO J, BAQUERO E, NARVÁEZ E. Catalasa, peroxidasa y polifenoloxidasa de pitaya amarilla (Acanthocereus pitajaya). Rev Col Quím. 2006;35:91-101. [ Links ]
CONCELLÓN A, AÑÓNM, CHAVES A. Characterization and Changes in Polyhenol Oxidase From Eggplant Fruit (Solanum melongena L.) During Storage at Low Temperature. Food Chem. 2004;88:17-24. [ Links ]
GALLO F. Índice de madurez para piña cayena lisa, guanábana, pitaya amarilla y maracuyá. En: Agrodesarrollo, 1996;4(1/2):171-200. [ Links ]
GARNICA G, QUINTERO E. Estudio preliminar de la influencia de las bajas temperaturas sobre algunas características de la maduración de la pitaya amarilla (Acanthocereus pitajaya ) [trabajo de grado]. Bogotá: Departamento de Farmacia, Facultad de Ciencias, Universidad Nacional de Colombia; 1994. [ Links ]
FERNANDEZ-TRUJILLO J, CANO A, ARTÉS F. Physiological Changes in Peaches Related to Chilling Injury and Ripening. Postharvest Biol Technol. 1998;13(2):109-119. [ Links ]
JIANG Y, DUAN X, JOYCE D, ZHANG Z, LI J. Advances in Understanding of Enzymatic Browning in Harvested Litchi Fruit. Food Chem. 2004;88:443-446. [ Links ]
KANG H, SALTVEIT M. Antioxidant Enzymes and DPPH-Radical Scavening Activity in Chilled and Heat-Shocked Rice (Oryza sativa L.) Seedlings Radicles. J Agric Food Chem. 2002;50:513-518. [ Links ]
NERD A, MIZRAHI Y. Fruit Development and Ripening in Yellow Piatya. J Am Hortic Sci. 1998;123:560-562. [ Links ]
NETE A, KADIOGLU A. Changes in the Chemical Composition, Polyphenol Oxidase and Peroxidase Activities During Development and Ripening of Medlar Fruits (Mespilus germanica L.). J Plant Physiol. 2001;27(3-4):85-92. [ Links ]
OMRAN R. Peroxide Levels and Activities of Catalase, Peroxidasa, and Indolacetic Acid Oxidase During and After Chilling Cucumber Seedlings. Plant Physiol.1980;65:407-408. [ Links ]
RODRÍGUEZ D, PATIÑO M. Efecto de dos índices de madurez y dos temperaturas de almacenamiento sobre el comportamiento poscosecha de la pitaya amarilla (Acanthocereus pitajaya) [trabajo de grado]. Bogotá, Facultad de Agronomía, Universidad Nacional de Colombia; 2003. [ Links ]
RUBIO E. Estudio del cambio de actividad de polifenoloxidasa, PFO, durante el proceso de maduración del lulo (Solanum quitoense L.) [tesis de maestría]. Bogotá: Maestría en Qímica, Departamento de Química, Facultad de Ciencias, Universidad Nacional de Colombia; 1999. [ Links ]
SALA J. Involvement of Oxidative Stress in Chilling Injury in Cold-Stored Mandarin Fruits. Postharvest Biol Technol. 1998;13:255-261. [ Links ]
SALA J, LAFUENTE M. Catalase Enzyme Activity is Related to Tolerance of Mandarin Fruits to Chilling. Postharvest Biol Technol. 2000;20(1):81-89. [ Links ]
SALTVEIT M. Chilling Injury is Reduced in Cucumber, Rice Seedlings and Tomato Pericarp Discs by Heat-Shocks Applied After Chilling. Postharvest Biol Technol. 2001;21(2):169-177. [ Links ]
VICENTE A, MARTINEZ G, CHAVES A, CIVELLO P. Effect of Heat Treatment on Strawberry Fruit Damage and Oxidative Metabolism During Storage. Postharvest Biol Technol. 2006;40(2):116-122. [ Links ]
ZHANG J, HUANG W, PAN Q, LIU Y. Improvement of Chilling Tolerance and Accumulation of Heat Shock Proteins in Grape Berries (Vitis vinifera cv. Jingxiu) by Heat Pretreatment. Postharvest Biol Technol. 2005;38(1):80-90. [ Links ]
ZHOU Y, DAHLER JM, UNDERHILL SJR, WILLS RBH. Enzymes Associated with Blackheart Development in Pineapple Fruit. Food Chem. 2003;565-572. [ Links ]
ZOR T, SELLINGER Z. Linearization of the Bradford Protein Assay Increases Its Sensivity: Theorical and Experimental Studies. Anal Biochem. 1996;236:302-308. [ Links ] ]]>