Ribonuclease Activity in Latex from Calotropis procera (Aiton) W.T. Aiton and Pedilanthus tithymaloides (L.) Poit
Emma Rueda de Arvelo1; Catalina Ramis2 y Francisco Triana Alonso3
1 Ingeniero Agrónomo. Dra. Jefe del Laboratorio de Enzimología y Toxicología. Cátedra de Bioquímica. Facultad de Ciencias Veterinarias. Universidad Central de Venezuela. Final Av. 19 de abril-vía El Limón. Maracay. <emma.rueda@ucv.ve>
2 Ingeniero Agrónomo. Coordinadora de Investigación. Centro de Investigaciones en Biotecnología Agrícola. Instituto de Genética. Facultad de Agronomía. Universidad Central de Venezuela. Final Av. 19 de abril-vía El Limón Maracay. <ramis.catalina@gmail.com>
3 Licenciado en Química. Ex Director del Instituto de Investigaciones Francisco Javier Triana-Alonso (BIOMED). Escuela de Medicina. Facultad de Ciencias de la Salud. Universidad de Carabobo. Calle Cecilio Acosta-Las Delicias. Maracay. <ftrianaalonso@yahoo.com>
Recibido: Noviembre 23 de 2012; aceptado: Agosto 2 de 2013.
]]>Resumen. Las enzimas ribonucleasas (RNasas) han sido utilizadas con efectividad en el tratamiento de ciertos tipos de cáncer y pueden tener otras propiedades aplicables en biotecnología. Con el objetivo de identificar la presencia de actividad RNasa en el látex de las plantas tropicales Calotropis procera y Pedilanthus tithymaloides se colectaron muestras a partir de plantas adultas ubicadas al norte del estado Aragua, Venezuela. Las proteínas solubles fueron extraídas con acetato de sodio 50 mM pH 5 (16 mL/mg de látex) y eliminada la porción poliisoprenoide por centrifugación a 16.000 x g durante 15 min. La actividad RNasa se estimó utilizando una técnica que incluye la aplicación de alícuotas de la mezcla de reacción sobre geles de poliacrilamida-urea y separadas por electroforesis. La degradación del sustrato fue cuantificada por densitometría. Se probaron diversos sustratos (ARNttotal, ARNtphe y ARNm transcrito in vitro a partir de ADN plasmídico). El látex de ambas especies presentó actividad RNasa, con actividades específicas iniciales de 1,42 ± 0,74 mg de ARN hidrolizado/min/mg de proteína; 0,45 ± 0,18 ng de ARN hidrolizado/min/ng de proteína y 0,28 ± 0,07 ng de ARN hidrolizado/min/ng de proteína para el ARNttotal, ARNm transcrito y ARNtphe, respectivamente, en C. procera, y de 0,02 ± 0,001 ng de ARN hidrolizado/min/ng de proteína para el ARNm transcrito y ARNtphe en P. tithymaloides. Este constituye el primer reporte acerca de la presencia de enzimas RNasas en el látex de estas especies.
Palabras clave: Enzima laticífera, extracto crudo, ARN, plantas tropicales.
Abstract. Ribonuclease enzymes (RNase) have been used effectively in the treatment of certain cancers and other properties that may be applicable in biotechnology. In order to identify the RNase activity in the latex of Calotropis procera and Pedilanthus tithymaloides, tropical plants samples were collected from adult plants located in the North State of Aragua, Venezuela. Soluble proteins were extracted with 50 mM sodium acetate pH 5 (16 mL/mg latex) and poliisoprenoide portion was removed by centrifugation at 16,000 x g for 15 min. RNase activity was estimated using a technique that involves the application of reaction mixture aliquots on polyacrylamide-urea gels and separated by electrophoresis. Substrate degradation was quantified by densitometry. Various substrates were tested (tRNAtotal, tRNAphe and mRNA transcribed in vitro from plasmid DNA). The latex from both species showed RNase activity, with initial specific activities of 1.42 ± 0.74 mg of RNA hydrolyzed/min/mg protein, 0.45 ± 0.18 ng RNA hydrolyzed/min/ng protein and 0.28 ± 0.07 ng RNA hydrolyzed/min/ng protein for the tRNAtotal, mRNA transcribed and tRNAphe, respectively, for C. procera; and 0.02 ± 0.001 ng RNA hydrolyzed/min/ng protein for the mRNA transcribed and tRNAphe in P. tithymaloides. This is the first report of RNases enzymes in the latex from these species.
Key words: Laticifer enzyme, crude extract, RNA, tropical plants.
Las enzimas Ribonucleasas (RNasas) hidrolizan enlaces fosfodiéster en numerosas formas de ARN y están presentes en todas las formas de vida celular (Aravind y Koonin, 2001). Las RNasas son intermediarias en el flujo de la información bioquímica desde los genes hacia las proteínas; es decir, desde la transcripción hasta la traducción (Porta, Paglino y Mutti, 2008). Adicionalmente, se les ha atribuido propiedades como en el caso de la ribonucleasa seminal bovina (RSB) que presenta actividad inmunosupresora, antitumoral, embriotóxica y espermatogénica (D'Alessio et al., 1997, 2001) y las RNasas de la superfamilia T2 que participan no solo en la degradación del ARN sino también modulando la respuesta inmune y actuando como citotoxinas extra e intracelulares (Luhtala y Parker 2010).
Las RNasas son potencialmente citotóxicas debido a su capacidad para degradar el ARN y en consecuencia inhibir la biosíntesis de proteínas, por lo cual recientemente ha aumentado el interés en el estudio de estas enzimas, presentes en protozoarios, hongos, bacterias, virus, animales y plantas, con el fin de conocer sus estructuras, funciones, mecanismos de acción y potencial biotecnológico. El interés por estas enzimas surge, en parte, de los trabajos en los cuales se ha demostrado actividad citotóxica, a bajas concentraciones, de algunas RNasas como la RSB (D'Alessio et al., 2001), y otras variantes y homólogas de la RSB como la enzima Ranpirnasa (Onconasa®) obtenida a partir de oocitos de Rana pipiens, una enzima 10 a 30 veces más citotóxica que la RSB (Matousek et al., 2003) y utilizada en la actualidad como medicamento efectivo en el tratamiento de mesotelioma maligno, un cáncer de pulmón asociado a la exposición al asbesto y otros materiales semejantes (Singh et al., 2007).
Por otra parte, es conocido el potencial farmacológico que exhiben numerosas especies de plantas, incluyendo las especies laticíferas, muchas de las cuales son utilizadas en la actualidad como fuente de principios activos para el tratamiento de enfermedades (Heijden et al., 2004). Calotropis procera y Pedilanthus tithymaloides son dos especies laticíferas de amplia distribución y adaptabilidad en las zonas tropicales.
C. procera (algodón de la India) (Familia Asclepiadaceae) es un arbusto naturalizado que suele invadir áreas alteradas y pastizales. En la India, de donde es nativa, es una planta medicinal. Sus propiedades han sido evaluadas en extractos de hojas y flores, así como en el látex. Del extracto etanólico de las flores se han reportado propiedades antimicrobiana, antiinflamatoria, antipirética, analgésica (Mascolo et al., 1988), anticancerosa (Smith et al., 1995) y antimalárica (Sharma y Sharma, 1999, 2001). Otros extractos de la planta en solventes orgánicos como etanol y acetona, han presentado actividades insecticida (Moursy, 1997), larvicida (Markouk et al., 2000), antibacteriana y antiparasitaria (Larhsini et al., 1999). Los extractos foliares, con importantes contenidos de triterpenos, antocianinas y alcaloides, presentaron efecto positivo en el control del helminto gastrointestinal Haemonchus contortus en pequeños rumiantes (Al-Qarawi et al., 2001). Asimismo, extractos florales de C. procera mostraron un efecto anticoccidial en pollos de engorde inoculados oralmente, observándose una reducción significativa, dependiente de la dosis y de los efectos patogénicos asociados con Eimeria tenella (Zaman et al., 2012).
]]> El látex integral de C. procera ha sido utilizado exitosamente para purificar la enzima cruda amilasa, a partir de fermentos cultivados de Aspergillus oryzae, por un mecanismo de acción semejante al del ácido poliacrílico, un polielectrolito sintético, que inclusive podría sustituir el uso de métodos convencionales para purificar enzimas, tales como la precipitación con sulfato de amonio. El látex con una dilución 10-2 permitió concentrar la amilasa en 4 veces con un 97% de recuperación con respecto a la actividad inicial en el cultivo (Kareem, Ahpan y Osho, 2003). Proteínas del látex de C. procera fueron efectivas en su actividad antifúngica contra diversos fitopatógenos, con una actividad inhibitoria preferencial hacia R. solani (IC50 = 20,7 mg mL-1) (Souza et al., 2011) y han sido probadas ser efectivas como un agente químico para destruir larvas de Aedes aegypti (Ramos et al., 2009).En la agroindustria, un extracto de enzimas del látex de C. procera fue probado como ablandador de carnes de cerdo, pollo y res. Los cortes marinados presentaron disminución del contenido de humedad y aumento significativo en la terneza, sin afectar el pH y el sabor de las carnes (Rawdkuen, Jaimakreu y Benjakul, 2013).
El látex integral de C. procera ha provocado efectos antioxidante y anti-hiperglicémico contra diabetes inducida por aloxano en ratas (Roy et al., 2005), actividad antiinflamatoria (Kumar y Basu, 1994, Alencar et al., 2004), anticoccidial (Mahmoud et al., 2001), antidiarreica (Kumar et al., 2001) y analgésica (Dewan, Sangraula y Kumar, 2000). El látex de esta planta ha sido utilizado para provocar inflamación de la piel y las membranas mucosas al inyectar un extracto acuoso de látex seco en la superficie podal de ratas y producir una respuesta hiperalgésica que permitió evaluar el efecto antiinflamatorio de algunas drogas como el diclofenaco, el rofecoxib y la ciproheptadina (Sehgal y Kumar, 2005), y mostró actividad anticonvulsionante y sedante en modelos de ratones debido a una acción depresiva sobre el sistema nervioso central (Lima et al., 2012). Inyecciones intraperitoneales de proteínas laticíferas redujeron marcadamente la procoagulación y la trombocitopenia en ratones infectados con Salmonella, lo cual fue atribuido a las actividades semejantes a la trombina y la plasmina que ejercen las proteasas laticíferas, sugiriendo un alto potencial terapéutico en condiciones asociadas con anormalidades de la coagulación (Ramos et al., 2012). Asimismo, fracciones conteniendo proteínas laticíferas han demostrado propiedades como agente citotóxico y anticanceroso (Soares et al., 2007, Samy et al., 2012, Rueda de Arvelo et al., 2013).
En la mayoría de los casos, las propiedades han sido atribuidas a las enzimas laticíferas. En el látex de esta planta se ha reportado la presencia de enzimas con actividad proteasa (Kumar y Jagannadham, 2003; Freitas et al., 2007; Rueda de Arvelo, 2012), quitinasa, superoxido dismutasa y ascorbato peroxidasa (Freitas et al., 2007).
P. tithymaloides (Familia Euphorbiaceae) es una planta oriunda de la América tropical, cultivada como ornamental en muchas regiones. En Venezuela se encuentra en estado natural en las regiones xerofíticas del norte del país. Un tamizaje fitoquímico del látex de P. tithymaloides detectó la presencia de triterpenos, esteroides, carotenos, azúcares reductores, aminas, fenoles, taninos y flavonoides (Sánchez et al., 2005). También se han aislado terpenoides y alcoholes de cadena larga con actividad biológica (Mohamed et al., 1996). El extracto etanólico de las hojas presentó actividad antimicrobiana, semejante a la tetraciclina, sobre Pseudomonas aeruginosa (Vidotti et al., 2006), actividad antiinflamatoria sobre un modelo de edema podal en ratas y capacidad antioxidante contra especies de oxígeno y nitrógeno reactivas.
Un extracto etanólico de las hojas de esta planta, demostró actividad biológica contra huevos, larvas y pupas de Culex quinquefasciatus, provocando alta mortalidad en cada estado de vida del insecto, un vector de un nemátodo altamente infeccioso, en Asia tropical (Kamalakannan et al., 2010).
En relación con los componentes proteicos del látex de P. tithymaloides, se ha reportado una lectina específica para galactosa con actividad mitogénica en linfocitos de bazo murino (Seshagirirao, 1995). Esta lectina se ha utilizado en estudios del patrón de hemaglutinación en pacientes con diabetes mellitus (Nagda y Deshmukh, 1998) y tuberculosis (Ankush et al., 2003).
A partir de Pedilanthus sp. se ha reportado una proteína, llamada pedilstatina, con acción inhibidora de crecimiento de la línea celular de leucemia linfocítica P388 (Pettit et al., 2002). Asimismo, se ha reportado una proteasa del látex, designada como "pedilantaína", con actividad antiinflamatoria oral (Dutta y Dhar, 1984; Dhar et al., 1988) y se ha logrado la purificación y caracterización de una proteasa, denominada pedilanthina, con una masa molecular aproximada de 63,1 kDa (Bhowmick et al., 2008).
La identificación, purificación y caracterización bioquímica de enzimas RNasas en el látex de estas plantas tropicales constituye la primera etapa de una serie de investigaciones conducentes a evaluar el potencial uso biotecnológico de las RNasas laticíferas como posibles agentes citotóxicos y antineoplásicos. El presente trabajo de investigación tuvo como objetivo determinar la actividad ribonucleasa en el extracto crudo de látex de C. procera y P. tithymaloides, dos especies con elevado potencial biotecnológico.
]]> MATERIALES Y MÉTODOS
Todos los experimentos se llevaron a cabo en el Laboratorio de Bioquímica de Proteínas y Ácidos Nucleicos del Instituto de Investigaciones Biomédicas "Dr. Francisco J. Triana-Alonso" (BIOMED) de la Universidad de Carabobo (UC), Maracay, estado Aragua, Venezuela.
Material vegetal. Las muestras de látex fueron colectadas de plantas adultas creciendo en el Campo Experimental de la Facultad de Agronomía-Universidad Central de Venezuela (FAGRO-UCV), Maracay, estado Aragua. Las especies fueron identificadas por la Dra. Thirza Ruiz, del Instituto de Botánica-FAGRO-UCV. El látex fue colectado en viales de microcentrifuga, realizando escisiones en el tallo, y transportado de inmediato a 4 ºC para obtener el extracto crudo de látex.
Preparación del extracto crudo de látex. El látex fue diluido con acetato de sodio 50 mM pH 5 (16 mL/mg de látex), agitado en vortex durante 1 min y centrifugado a 16.000 x g por 15 min en una microcentrífuga Eppendorf® 5415C (Hamburgo, Alemania) para descartar materiales insolubles. El sobrenadante se denominó "extracto crudo de látex" (ECL) y fue almacenado en alícuotas a -20 °C hasta su uso.
Contenido de proteína. Se determinó por el método de Lowry et al. (1951), con albúmina sérica bovina (BSA) como patrón, utilizando un espectrofotómetro Beckman DU 650® (Miami, Estados Unidos).
Síntesis in vitro de ARNm a partir de ADN plasmídico de Escherichia coli . El ARNm, uno de los sustratos utilizados en la determinación de la actividad RNasa, fue sintetizado por procedimientos de transcripción in vitro a partir de moléculas moldes de ADN plasmídico obtenido de cultivos de E. coli, a través del procedimiento descrito a continuación.
Purificación por electroforesis preparativa del ARNm transcrito. El ARNm transcrito fue purificado por electroforesis preparativa (EP) (Cunningham, Kittikamron y Lu, 1996), utilizando un equipo Bethesda Research Laboratories, Inc. (NY, Estados Unidos), con una columna cilíndrica de 10 mm de diámetro y 10 cm de alto, en la cual se preparó un gel de poliacrilamida-urea de 2 cm de altura. Muestras de 120 mL de ARNm transcrito, a una concentración de 15,2 mg mL-1, fueron precipitadas agregando 12 mL de acetato de sodio 3 M pH 5,5 y 300 mL de etanol a -20 °C, centrifugadas a 16.000 x g por 30 min en la microcentrífuga Eppendorf 5415C y resuspendidas en 100 mL de tampón desnaturalizante para ARN antes de ser aplicadas a la columna. Los procedimientos de EP se realizaron con un flujo de 1,6 mL min-1 con un tampón conteniendo Tris 50 mM, ácido acético 50 mM y EDTA 1 mM (TAE). Se colectaron fracciones de 3,2 mL en tubos que contenían 320 mL de acetato de sodio 3 M pH 5,5 y se leyó la DO a 260 y 280 nm. Alícuotas de 300 mL de cada fracción fueron precipitadas con 800 mL de etanol a -20 °C, dejadas en reposo toda la noche a -20 °C, centrifugadas a 16.000 x g por 30 min y lavadas nuevamente con etanol, para ser resuspendidas en 15 mL de tampón desnaturalizante para ARN y aplicadas en un gel plano de poliacrilamida-urea.
Determinación de la actividad Ribonucleasa. El método está basado en la técnica descrita por Arends y Schön (1997), con las siguientes modificaciones: la mezcla de reacción contenía Hepes 30 mM pH 7,5, acetato de potasio 100 mM y acetato de magnesio 3 mM, con 10,6 mg del ARN utilizado como sustrato en un volumen final de 10 mL. La reacción se inició al agregar un volumen de ECL, variable de acuerdo al contenido de proteína, y la mezcla fue incubada a 37 °C durante diversos intervalos de tiempo, hasta 60 min. La reacción fue detenida sumergiendo los tubos en nitrógeno líquido después de agregarles 20 mL de tampón desnaturalizante conteniendo Tris-HCl 10 mM pH 7,5, EDTA 1 mM, urea 8 M, xileno cianol 0,05% y azul de bromofenol 0,05%. La degradación del sustrato fue cuantificada por electroforesis en geles de poliacrilamida al 10%, urea 8 M, 0,1% de SDS, 0,25 mg mL-1 de persulfato de amonio y 0,125% de Temed con un tampón preparado con Tris 90 mM, ácido bórico 90 mM y EDTA 2 mM. Las muestras fueron sometidas a 70 °C durante 3 min antes de aplicarlas al gel. El gel fue pre-calentado durante 20 min a 300 V constantes. La electroforesis se realizó a 300 V constantes. Los geles fueron teñidos con azul de toluidina 0,1% y ácido acético glacial 10% (v/v) y desteñidos con 10% de etanol y 7% de ácido acético. Cuando la cantidad de ARN aplicado a los geles fue menor a 0,3 mg, se realizó tinción con nitrato de plata (An et al., 2009). La cuantificación del sustrato degradado se realizó utilizando técnicas densitométricas con el programa Multianalyst en un equipo Gel Doc 1000 (BIO-RAD) (Hercules, EUA). Se probó la actividad sobre tres sustratos diferentes. El ARNttotal y el ARNtphe fueron obtenidos en trabajos previos (Rosales, 2006) y almacenados liofilizados a -20° C. La actividad se expresó como porcentaje de degradación del sustrato. Al graficar la superficie de la banda o la cantidad de ARN en función del tiempo se obtuvieron, para cada concentración de proteína de látex evaluada, las ecuaciones de las líneas rectas a partir de las cuales se determinaron las pendientes que representan las velocidades iniciales de reacción expresadas en unidades de superficie de banda por unidad de tiempo (UA/min), o cantidad de ARN por unidad de tiempo (mg ARN min-1). Al relacionar estos valores con la concentración de proteína de látex en la mezcla de reacción se obtuvo la actividad específica. La velocidad inicial específica, determinada en los primeros 5 min de la reacción, se expresó como mg ARN/min/mg de proteína de látex. Se realizaron pruebas utilizando diversas concentraciones de proteína de ECL sin variar la concentración del sustrato.
Análisis estadístico. Los datos son presentados como promedios y desviaciones estándar. Se aplicó estadística descriptiva utilizando el programa Statistix 8.0.
RESULTADOS Y DISCUSIÓN
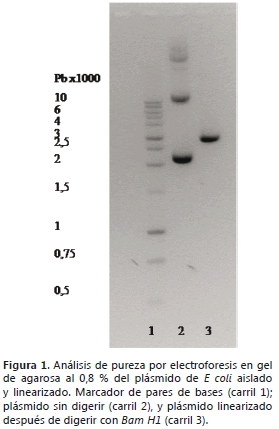
Calidad del ADN plasmídico. La relación 260/280 DO promedio fue de 1,83 ± 0,16 de un total de 8 procesos de purificación. La Figura 1 presenta una imagen representativa de la calidad del ADN purificado antes y después de linearizar a través del ensayo de restricción con la enzima Bam H1. Las tres bandas observadas en el carril del plásmido sin digerir se corresponden con parte del ADN genómico, la de mayor tamaño, seguida por el ADN circular distendido o relajado y finalmente el ADN circular superenrollado en la banda de menor tamaño. El plásmido digerido presenta una única banda ubicada entre 2500 y 3000 pb. Las bandas observadas en el gel y la relación 260/280 corroboran la calidad del ADN antes y después de linearizar, de acuerdo a lo establecido en la literatura (Sambrook y Russell, 2001).
Determinación de la actividad Ribonucleasa.
Calotropis procera. El ARNttotal utilizado como sustrato se separó durante la electroforesis en 3 bandas correspondientes a 120, 93 y 76 nucleótidos (nts). Esta última es la más abundante por lo que la estimación de la actividad RNasa sobre este sustrato se realizó cuantificando la degradación de la banda de 76 nts. Los fragmentos de menor tamaño migran a mayor velocidad sobre estos geles. Se puede observar en la Figura 2 que a medida que disminuye la intensidad de la banda correspondiente a 76 nts del ARNttotal se van haciendo más pronunciadas nuevas bandas que presentan menor tamaño y migran más rápidamente en el gel, correspondientes a los productos de degradación del ARN. Los resultados de la densitometría de los geles se presentan en la Tabla 1. Las características de la mezcla de reacción se presentan en la Tabla 2. La actividad específica inicial RNasa fue de 1,48 ± 0,66 mg ARNttotal/min/ mg de proteína de látex. La actividad, probada con tres concentraciones crecientes de proteína laticífera, aumentó proporcionalmente durante los primeros diez minutos de reacción y fue mayor a medida que se incrementó la concentración de enzima (Figura 3). Con 0,4 mg de proteína mL-1, el sustrato se hidrolizó en un 100% a los 30 min de reacción (Tabla 1). Después de 60 min de incubación a 37 °C con el ECL en presencia del sustrato, se degradó completamente el ARNt total cuando se utilizó una relación menor o igual a 5 mg de ARN/ mg proteína, en las mezclas de reacción en las cuales la concentración de proteína laticífera fue de 0,2 y 0,4 mg mL-1 (carriles 6 y 7 de la Figura 2). El ARNttotal (ARNtbulk) es un sustrato hidrolizable por estas RNasas, no obstante, dificulta la medición precisa de actividad de la enzima debido a que ésta puede actuar sobre las distintas moléculas de diferentes masas moleculares.
]]>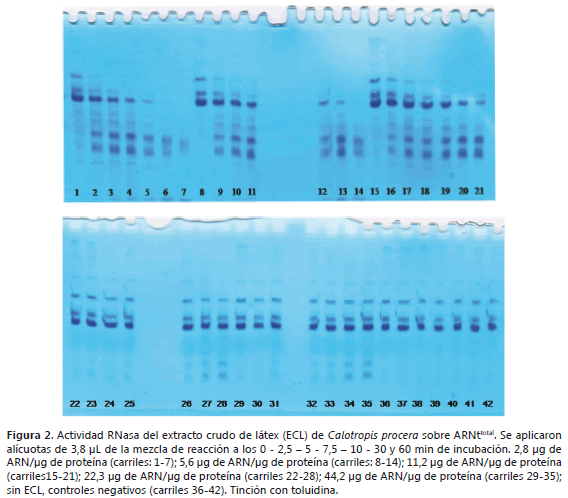
La cinética de actividad RNasa sobre ARNm transcrito y sobre ARNtphe determinada sobre el extracto crudo de látex de C. procera se presenta en la Figura 4. El ARNtphe contiene 76 nts de longitud (Byrne et al., 2010) y el ARNm transcrito contiene 140 nts (Triana-Alonso et al., 1995). Los resultados de la densitometría de los geles se presentan en la Tabla 3. Las características de la mezcla de reacción se presentan en la Tabla 4. La actividad específica promedio fue de 0,45 ± 0,18 ng ARNm/min/ng de proteína de látex y de 0,28 ± 0,07 ng ARNtphe/min/ ng de proteína de látex. La actividad RNasa sobre el ARNm y el ARNtphe alcanzó 84 y 40% de degradación, respectivamente, después de 60 min de incubación, cuando se utilizó una proporción de 1 mg de ARN/mg proteína (con 9,5 ng de proteína/mL) (carriles 15 y 25 de la Figura 4). En estos casos, la actividad sobre el ARN aumentó entre 20 y 48% sobre el ARNm y entre 67 y 72% sobre el ARNtphe en comparación con la actividad determinada en la mezcla de reacción conteniendo diez veces menos proteína laticífera, como se observa en la Figura 5.
]]> Pedilanthus tithymaloides. La actividad RNasa se determinó en el ECL de P. tithymaloides utilizando como sustratos ARNm transcrito y ARNtphe. Un gel representativo de la actividad sobre ARNm transcrito y ARNtphe se presenta en la Figura 6. Los resultados de la densitometría de los geles se presentan en la Tabla 5. La velocidad inicial en los primeros 5 min de reacción, fue de 0,02 ± 0,001 ng ARN /min/ng de proteína de látex para los dos sustratos evaluados. Durante el inicio de la reacción, la actividad de la RNasa presente en el ECL de P. tithymaloides fue semejante para ambos sustratos; no obstante, a los 60 min de incubación la degradación de los sustratos ARNm y ARNtphe fue de 84 y 32%, respectivamente (Figura 7).La actividad RNasa presente en el látex de P. tithymaloides es relativamente baja, si se compara con la reportada para otras especies, como en el caso de Chelidonium majus (Nawrot, Wolun-Cholewa y Gozdzicka-Józefiak, 2008) y C. procera, los únicos reportes de la actividad RNasa en látex de plantas. La degradación fue semejante durante los primeros minutos de reacción para ambos sustratos; no obstante, fue casi completa para el ARNm después de 60 min de incubación, esto puede ser debido a las diferencias estructurales de cada sustrato. Las estructuras secundarias influyen en la accesibilidad de las enzimas a los sitios específicos de identificación y acción. Posiblemente, la estructura secundaria del ARNm transcrito sea de mayor accesibiliad o posea mayor número de lugares con secuencias nucleotídicas de reconocimiento específico de la enzima. Es conocido que algunas RNasas pertenecientes a ciertas familias presentan variable especificidad de sustrato, como es el caso de las familias A y T1, las cuales tienden a ser específicas para pirimidinas o guanosina, respectivamente, a diferencia de las RNasas de la familia T2 que hidrolizan en cualquier sitio indistintamente de la base nitrogenada (Deshpande y Shankar, 2002; Irie, 1999). Estudios más detallados de las estructuras, tanto de las enzimas como de los sustratos y productos de la reacción, permitirían acercarse a una mejor caracterización de la especificidad de estas RNasas.
CONCLUSIÓN
El látex de plantas adultas de Calotropis procera y Pedilanthus tithymaloides contiene enzimas con actividad ribonucleasa capaz de hidrolizar diferentes tipos de ARN. La actividad específica del ECL de P. tithymaloides fue entre 12 y 23 veces menor en comparación con la de C. procera. Este constituye el primer reporte acerca de la actividad Rnasa en el látex de estas especies.
AGRADECIMIENTO
]]> Los autores agradecen al Consejo de Desarrollo Científico y Humanístico de la Universidad Central de Venezuela (CDCH-UCV) por el financiamiento de la presente investigación, a través del Proyecto de Investigación Nº PI-11-6939-2007/2 y la Ayuda Institucional Nº AIA-11-7117-2008.
BIBLIOGRAFÍA
Alencar, N.M. I. Figueiredo, M. Vale, F. Bitencourt, J. Oliveira, R. Ribeiro and M. Ramos. 2004. Anti-inflammatory effect of the latex from Calotropis procera in three different experimental models: peritonitis, paw edema and hemorrhagic cystitis. Planta Medica 70(12): 1144-1149. [ Links ]
Al-Qarawi, A. O. Mahmoud, M. Sobaih, E. Haroun, and S. Adam. 2001. A preliminary study on the antihelmintic activity of Calotropis procera latex against Haemonchus contortus infection in Najdi sheep. Veterinary Research Communications 25(1): 61-70. [ Links ]
An, Z.W. L.L. Xie, H. Cheng, Y. Zhou, Q. Zhang, XG. He, and H.S. Huang. 2009. A silver staining procedure for nucleic acids in polyacrylamide gels without fixation and pretreatment. Analitical Biochemistry 391(1): 77-79. [ Links ]
Ankush, R.D., K.K. Nagda, A.N. Suryakar and N.R. Ankush. 2003. Tuberculosis altering erythrocyte membrane topology - a lectin haemagglutination study. Indian Journal of Tuberculosis 50(2): 95-98. [ Links ]
Aravind, L. and E. Koonin. 2001. A natural classification of ribonucleases. Methods in Enzymology 341: 3-28. [ Links ]
Arends, S. and A. Schön. 1997. Partial purification and characterization of nuclear ribonuclease P from wheat. European Journal of Biochemistry 244(2): 635-645. [ Links ]
Bhowmick, R., N. Prasanna, M. Jagannadham and A. Kayastha. 2008. Purification and characterization of a novel protease from the latex of Pedilanthus tithymaloids. Protein and Peptide Letters 15(9): 1009-1016. [ Links ]
Byrne, R.T., A.L. Konevega, M. Rodnina and A. Antson. 2010. The crystal structure of unmodified tRNAphe from Escherichia coli. Nucleic Acids Research 38(12): 4154-4162. [ Links ]
Cunningham, L., K. Kittikamron and Y. Lu. 1996. Preparative-scale purification of RNA using an efficient method which combines gel electrophoresis and column chromatography. Nucleic Acids Research 24(18): 3647-3648. [ Links ]
D'Alessio, G., A. Di Donato, L. Mazzarella and R. Piccoli. 1997. Ribonucleases: structures and function. pp. 383-423. Edited by D'Alessio, G. & J. F. Riordan. Academic Press, New York. 570 p. [ Links ]
D'Alessio, G., A. Di Donato, R. Piccoli and N. Russo. 2001. Seminal ribonuclease: preparation of natural and recombinant enzyme, quaternary isoforms, isoenzymes, monomeric forms; assay for selective cytotoxicity of the enzyme. Methods in Enzymology 341: 248- 263. [ Links ]
Dhar, S.N., S.M. Ray, A. Roy, and S.K. Dutta. 1988. Oral anti-inflammatory activity of pedilanthain-a new proteolytic enzyme from Pedilanthus tithymaloides poit. Indian Journal of Pharmaceutical Sciences 50(5): 281-283. [ Links ]
Deshpande, R. and V. Shankar. 2002. Ribonucleases from T2 family. Critical Reviews in Microbiology 28(2): 79-122. [ Links ]
Dewan, S., H. Sangraula and V. Kumar. 2000. Preliminary studies on the analgesic activity of látex of Calotropis procera. Journal of Ethnopharmacology 73(1-2): 307-311. [ Links ]
Dutta, S.K. and S.N.A. Dhar. 1984. A new proteolytic enzyme from Pedilanthus tithymaloides. Indian Journal of Pharmaceutical Sciences 46: 223-224. [ Links ]
Freitas, C., J. Soares, M. Miranda, N. Macedo, M. Pereira, L. Villas-Boas and M. Viana. 2007. Enzymatic activities and protein profile of látex from Calotropis procera. Plant Physiology and Biochemistry 45(10-11): 781-789. [ Links ]
Heijden, R. v.d, D. Jacobs, W. Snoeijer, D. Hallard, and R. Verpoorte. 2004. The Catharanthus alkaloids: pharmacognosy and biotechnology. Current Medical Chemistry 11(5): 607-628. [ Links ]
Irie, M. 1999. Structure-function relationships of acid ribonucleases: lysosomal, vacuolar and periplasmic enzymes. Pharmacology and Therapeutics 81(2): 77-89. [ Links ]
Kamalakannan, S., P. Madhiyazhagan, A. Dhandapani, K. Murugan, and D. Barnard. 2010. Pedilanthus tithymaloides (Euphorbiaceae) leaf extract phytochemicals: toxicity to the filariasis vector Culex quinquefasciatus (Diptera: Culicidae). Vector Borne Zoonotic Disease 10(8): 817-820. [ Links ]
Kareem, S.O., I. Akpan and M. Osho. 2003. Calotropis procera (Sodom apple) a potential material for enzyme purification. Short communication. Bioresource Technology 87(1): 133-135. [ Links ]
Kumar, V. and N. Basu. 1994. Anti-inflammatory activity of the latex of Calotropis procera. Journal of Ethnopharmacology 44(2): 123-125. [ Links ]
Kumar, S., S. Dewan, H. Sangraula and V. Kumar. 2001. Anti-diarrhoeal activity of the latex of Calotropis procera. Journal of Ethnopharmacology 76(1): 115-118. [ Links ]
Kumar, V. and M. Jagannadham. 2003. Procerain, a stable cysteine protease from the latex of Calotropis procera. Phytochemistry 62(7): 1057-1071. [ Links ]
Larhsini, M. L. Oumoulid, H. Lazrek, S. Wataleb, M. Bousaid, M. Bekkouche, M. Markouk and M. Jana. 1999. Screening of antibacterial and anti parasitic activity of six Moroccan medicinal plants. Thérapie 54(6): 763-765. [ Links ]
Lima, R., M. Silva, C. Aguiar, E. Chaves, K. Dias, D. Macêdo, F. de Sousa, K. Carvalho, M. Ramos and S. Vasconcelos. 2012. Anticonvulsant action of Calotropis procera latex proteins. Epilepsy & Behavior 23(2): 123-126. [ Links ]
Lowry, O., N. Rosebrough, L. Farr and R.J. Randall. 1951. Protein measurement with the folin phenol reagent. The Journal of Biological Chemistry 193(1): 265-275. [ Links ]
Luhtala, N. and R. Parker. 2010. T2 Family Ribonucleases: ancient enzymes with diverse roles. Trends in Biochemistry Science. 35(5): 253-259. [ Links ]
Mahmoud, O.M., E. Haroun, M. Sobaih, O. Omer and S. Adam. 2001. Comparative efficacy of Calotropis procera látex and sulfadimidine against experimentally-induced Eimeria ovinoidales infection in Najdi lambs. Small Ruminants Research 42(2): 135-140. [ Links ]
Markouk, M., K. Bekkouche, M. Larhsini, M. Bousaid, H. Lazrek and M. Jana. 2000. Evaluation of some Moroccan medicinal plants extracts for larvicidal activity. Journal of Ethnopharmacology 73(1-2): 293-297. [ Links ]
Mascolo, N., R. Sharma, S.C. Jain and F. Calpasso. 1988. Ethnopharmacology of Calotropis procera flowers. Journal of Ethnopharmacology 22(2): 211-221. [ Links ]
Matousek, J., J. Soucek, T. Slavík, M. Tománek, J.E. Lee, and R.T. Raines. 2003. Comprehensive comparison of the cytotoxic activities of onconase and bovine seminal ribonuclease. Comparative Biochemistry and Physiology. C, Toxicology & Pharmacology 136(4): 343-356. [ Links ]
Mohamed, S., S. Saka, S.H. El-Sharkawy, A.M. Ali, and S. Muid. 1996. Antimycotic screening of 58 Malaysian plants against plant pathogens. Pesticide Science 47(3): 259-264. [ Links ]
Moursy, L.E. 1997. Insecticidal activity of Calotropis procera extract on the flesfly, Sarcophaga haemorrhoidalis fallen. Journal of Egyptian Society of Parasitology 27(2): 505-514. [ Links ]
Nagda, K.K. and B. Deshmukh, 1998. Hemagglutination pattern of galactose specific lectin from Pedilanthus tithymaloides in diabetes mellitus. Indian Journal of Experimental Biology 36(4): 426-428. [ Links ]
Nawrot, R., M. Wolun-Cholewa, and A. Gozdzicka-Józefiak. 2008. Nucleases isolated from Chelidonium majus L. milky sap can induce apoptosis in human cervical carcinoma HeLa cells but not in Chinese Hamster ovary CHO cells. Folia Histochemica et Cytobiologica 46(1): 79-83. [ Links ]
Ogden, R. and D. Adams. 1987. Electrophoresis in agarose and acrylamide gels. Methods in Enzymology. 152: 61-87. [ Links ]
Pettit, G.R., S. Ducki, R. Tan, R.S. Gardella, J.B. McMahon, M.R. Boyd, G.R. Pettit, P.M. III, Blumberg, N.E. Lewin, D.L. Doubek and M.D. Williams. 2002. Isolation and structure of pedilstatin from a Republic of Maldives Pedilanthus sp. Journal of Natural Products 65(9): 1262-1265. [ Links ]
Porta, C., C. Paglino, and L. Mutti. 2008. Ranpirnase and its potential for the treatment of unresectable malignant mesothelioma. Review. Biologics: Targets and Therapy 2(4): 601-609. [ Links ]
Ramos, M., D. Pereira, D. Souza, E. Araújo, C. Freitas, M. Cavalheiro, M. Matos and A. Carvalho. 2009. Potential of laticifer fluids for inhibiting Aedes aegypti larval development: evidence for the involvement of proteolytic activity. Memórias do Instituto Oswaldo Cruz, Rio de Janeiro 104(6): 805-812. [ Links ]
Ramos, M., C. Viana, A. Silva, C. I. Figueiredo, R. Oliveira, N . Alencar, J. Lima-Filho and V. Kumar. 2012. Proteins derived from latex of C. procera maintain coagulation homeostasis in septic mice and exhibit thrombin- and plasmin-like activities. Naunyn-Schmiedeberg's Archives of Pharmacology 385(5): 455-463. [ Links ]
Rawdkuen, S., M. Jaimakreu, and S. Benjakul. 2013. Physicochemical properties and tenderness of meat samples using proteolytic extract from Calotropis procera latex. Food Chemistry 136(2): 909-916. [ Links ]
Rosales, R. 2006. Actividad traduccional de un sistema mitocondrial in vitro derivado de placenta humana. Maracay. 190 h. Tesis Maestría en Ciencias Biomédicas Mención Bioquímica y Biología Molecular. Universidad de Carabobo. Facultad de Ciencias de la Salud. [ Links ]
Roy, S. R. Sehgal, B. Padhy and V. Kumar, 2005. Antioxidant and protective effect of latex of Calotropis procera against alloxan-induced diabetes in rats. Journal of Ethnopharmacology 102(3): 470-473. [ Links ]
Rueda de Arvelo, E. 2012. Aislamiento y purificación de proteasas y una fracción enriquecida en terpenos de látex de Calotropis procera y Pedilanthus tithymaloides y evaluación in vitro de su efecto citotóxico. Maracay. 140 h. Tesis Doctorado en Ciencias Agrícolas. Universidad Central de Venezuela. Facultad de Agronomía. [ Links ]
Rueda de Arvelo, E., C. Ramis, G. Frail, y F. Triana-Alonso. 2013. Citotoxicidad in vitro de extractos laticiferos de Calotropis procera (Aiton) W.T. Aiton y Pedilanthus tithymaloides (L.) Poit. En: Boletín Latinoamericano y del Caribe de Plantas Medicinales y Aromáticas. En imprenta. [ Links ]
Samy, R.P., P. Rajendran, F. Li, N.M. Anandi, B.G. Stiles, S. Ignacimuthu, G. Sethi and V.T. Chow, 2012. Identification of a novel Calotropis procera protein that can suppress tumor growth in breast cancer through the suppression of NF-kB Pathway. PLoS ONE. Vol. 7, No 12, http://www.e48514.doi:10.1371/journal.pone.0048514; consultada: Septiembre 2013. [ Links ]
Sánchez, E. A. Pérez, D. Chávez e I. Hechevarría. 2005. Caracterización farmacognóstica de Pedilanthus tithymaloides L. Poit. En: Revista Cubana de Plantas Medicinales. Vol. 10, No 1; http://scielo.sld.cu/scielo.php?script=sci_arttext&pid=S102847962005000100004&lng=es&nrm=iso>. ISSN 1028-4796; consultada: Septiembre 2013. [ Links ]
Sehgal, R. and V. Kumar. 2005. Calotropis procera latex-induced inflammatory hyperalgesia-effect of antiinflammatory drugs. Mediators of Inflammation. 2005(4): 216-220. [ Links ]
Seshagirirao, K. 1995. Purification and partial characterization of a lectin from Pedilanthus tithymaloides latex. Biochemical Archives 11: 197-201. [ Links ]
Sharma, P. and J.D. Sharma. 1999. Evaluation of in vitro schizontocidal activity of plant parts of Calotropis procera-an ethanobotanical approach. Journal of Ethnopharmacology 68(1-3): 83-95. [ Links ]
Sharma, P. and J.D. Sharma. 2001. In vitro hydrolysis of erythrocytes by plant extracts with anti plasmodial activity. Journal of Ethnopharmacology 74(3): 239-243. [ Links ]
Sambrook, J. and D. Russell. 2001. Molecular cloning. A laboratory manual. Vol 1. 3rd edition. Cold Spring Harbor Laboratory Press, New York, USA. 999 p. [ Links ]
Singh, U., W. Ardelt, S.K Saxena, D.E. Holloway, E. Vidunas, H.S. Lee, A. Saxena, K. Shogen and K.R. Acharya. 2007. Enzymatic and structural characterisation of amphinase, a novel cytotoxic ribonuclease from Rana pipiens oocytes. Journal of Molecular Biology 371(1): 93-111. [ Links ]
Smith, H., H. Woerdenbag, R. Singh, G. Meulenbeld, R. Labadie and J. Zwaving. 1995. Ayurvedic herbal drug with possible cytostatic activity. Journal of Ethnopharmacology 47(2): 75-84. [ Links ]
Soares de Oliveira J., D. Pereira Bezerra, C.D. Teixeira de Freitas, M.F.J. Delano Barreto, M. Odorico de Moraes, C. Pessoa, L.V Costa-Lotufo and MV. Ramos. 2007. In vitro cytotoxicity against different human cancer cell lines of laticifer proteins of Calotropis procera (Ait.) R. Br. Toxicology in vitro 21(8): 1563-1573. [ Links ]
Souza, D.P. C.D. Freitas, D.A. Pereira, F.C. Nogueira, F.D. Silva, C.E. Salas, and M.V. Ramos. 2011. Laticifer proteins play a defensive role against hemibiotrophic and necrotrophic phytopathogens. Planta. 234(1): 183-193. [ Links ]
Triana-Alonso, F.J., M. Dabrowski, J. Wadzack, and K. Nierhaus. 1995. Self-coded 3'-extension of run-off transcripts produces aberrant products during in vitro transcription with T7 RNA polymerase. The Journal of Biological Chemistry 270(11): 6298-6307. [ Links ]
Vidotti, G., A. Zimmermann, M. Sarragiotto, C. Nakamura and B. Días. 2006. Antimicrobial and phytochemical studies on Pedilanthus tithymaloides. Short report. Fitoterapia 77(1): 43-46. [ Links ]
Zaman, M.A., Z. Iqbal, R.Z. Abbas and M.N. Khan. 2012. Anticoccidial activity of herbal complex in broiler chickens challenged with Eimeria tenella. Parasitology 139(2): 237-243. [ Links ]
]]>