 ]]>
Figura 1. Representación esquemática de la sílice
]]>
Figura 1. Representación esquemática de la sílice Figure 1. Schematic representation of silica
SYNTHESIS OF SILICON OXIDE WITH HIGH SUPERFICIAL AREA AND POROSITY THROUGH SOL-GEL TECHNIQUE USING GLYCEROL AND GLYCERYL MONOSTEARATE AS TEMPLATES
JUAN PEÑA
Grupo Procesos Fisicoquímicos Aplicados, Departamento de Ingeniería Química, Universidad de Antioquia
ELIANA CARDONA
Grupo Procesos Fisicoquímicos Aplicados, Departamento de Ingeniería Química, Universidad de Antioquia
LUIS RIOS
Grupo Procesos Fisicoquímicos Aplicados, Departamento de Ingeniería Química, Universidad de Antioquia, larios@udea.edu.co
]]> Recibido para revisar Septiembre 25 de 2007, aceptado Junio 18 de 2008, versión final Julio 04 de 2008
RESUMEN: Este trabajo reporta una forma novedosa para la producción de óxidos de silicio (sílice) porosos mediante la técnica sol-gel usando tetraetilortosilicato (TEOS) como precursor de silicio y como orientadores de la estructura porosa glicerol (Gly) y monoestearato de glicerilo (ME), los cuales son de bajo costo y de alta disponibilidad comercial. Las sílices obtenidas presentan características porosas interesantes para una potencial aplicación en catálisis heterogénea, como por ejemplo áreas superficiales (método BET) de alrededor de 736.3 m2/g, volumen total de poros de 0.41 cm3/g y estrecha distribución de tamaños de poro (método BJH) de aproximadamente 36 Å.
PALABRAS CLAVE: estructurante, glicerol, método sol-gel, monoestearato de glicerilo, óxidos de silicio, sílice porosa, Tetraetilortosilicato (TEOS).
ABSTRACT: This paper reports a novel synthetic route for the production of porous silicon oxides (silica) by means of the sol-gel technique using tetraethylorthosilicate (TEOS) as silicon source and glycerol (Gly) and glycerol monostearate (ME) as templates, which have low cost and wide commercial availability. The so-obtained silicas have many interesting porous characteristics for potential applications in heterogenous catalysis: specific surface area (BET method) of 736.3 m2/g, total porous volume of 0,41 cm3/g and pore size narrows distribution (BJH method) around 36 Å
KEYWORDS: Template, glycerol, glyceryl monostearate, silicon oxides, porous silica, sol-gel technique, tetraethylorthosilicate (TEOS).
1. INTRODUCCIÓN
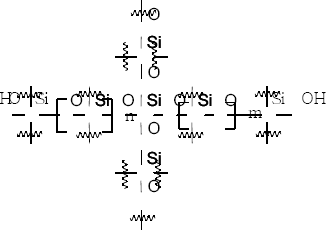
Los óxidos de silicio (sílice, SiO2), véase figura 1, son materiales inorgánicos extensamente usados en procesos de separación y adsorción de moléculas, biomedicina, cromatografía líquida (HPLC), aditivos en pinturas, cargas reforzantes en caucho sintético, tecnología de membranas e ingeniería molecular, electrónica y óptica, tratamiento superficial químico-mecánico, y una aplicación industrial muy importante es su uso como soporte de catalizadores para formar catalizadores heterogéneos. Para todas estas aplicaciones se requiere que la sílice presente altas área superficial y porosidad, está última propiedad debe ser preferiblemente del tipo mesoporosa; además, para algunas de estas aplicaciones la sílice debe tener una morfología de partícula específica [1-4].
 ]]>
Figura 1. Representación esquemática de la sílice
]]>
Figura 1. Representación esquemática de la sílice
Figure 1. Schematic representation of silica
La formación de mesoporosidad en la sílice se logra con la adición de surfactantes o agentes porógenos (AP) en el medio de síntesis, en el cual se da una interacción entre silicatos libres y el surfactante, lo que conduce a la formación de miscelas hibridas. La presencia de tales miscelas en el medio hace que los silicatos en exceso condensen a su alrededor dando como resultado un material silíceo formado con un esqueleto orgánico. La remoción del material orgánico mediante extracción con solventes no corrosivos o calcinación, da origen a una estructura sólida porosa basada en un arreglo regular o irregular de canales definidos por paredes de sílice [1-5].
La interacción entre el surfactante y los silicatos para la formación de la porosidad en el material depende de la naturaleza de dicho surfactante, la cual puede ser electrostática, típica de surfactantes aniónicos y catiónicos, o inducida por puentes de hidrógeno en forma directa o coordinada cuando están presente iones de mediación, tales como F- en medios ácidos, véase figura 2, o iones metálicos como Na+ en medios básicos. Los surfactantes de uso convencional son de naturaleza diversa: iónicos, aniónicos, aminas, entre otros, y su selección depende de las características morfológicas logradas por las micelas formadas durante la reacción para una estructura porosa deseada. Estudios recientes muestran las ventajas de usar surfactantes no iónicos (neutros), con relación a surfactantes que involucran interacciones electrostáticas, tales como su fácil remoción y la tendencia de los surfactantes neutros a producir estructuras con paredes más gruesas y sólidos de menor tamaño de partícula, lo cual mejora la estabilidad y la textura porosa [5-6].
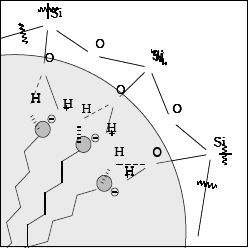
Figura 2. Interacción entre especies de sílice con porógenos no iónicos
Figure 2. Nonionic interaction between silica and porogen
Para la síntesis de sílices porosas se han utilizado tradicionalmente surfactantes no iónicos tales como Triton X-100 (C8H17(C6H4)(EO)10H), Brij 56 (C16H33(EO)10H), Pluronic F108 (PEO-PPO-PEO) [7,8]. La mayor desventaja de estos surfactantes es su alto costo y la necesidad de importarlos debido a que ninguno es producido localmente. Con el fin de contrarrestar esta desventaja, en esta investigación se evaluó el uso de agentes porógenos baratos y de alta disponibilidad comercial, específicamente glicerol y monoestearato de glicerilo, los cuales son derivados de la industria oleoquimica.
Actualmente existe gran preocupación mundial por encontrarle aplicaciones al exceso de glicerol que se obtiene en los procesos oleoquímicos, los cuales han tenido un gran desarrollo en la última década como consecuencia del impulso que se la ha dado a los procesos que usan materias primas renovables y bio-combustibles. La naturaleza química del glicerol, al ser un polialcohol orgánico con tres grupos hidroxilo le confiere un carácter polar e hidrofílico; además es un líquido viscoso, no tóxico y de bajo precio. Todas estas características hacen que sea interesante su uso como porógeno no iónico para la producción de sílices porosas. Debido a que la glicerina tiene un tamaño molecular relativamente pequeño, se espera que genere poros pequeños en la sílice; para tratar de aumentar el tamaño de dichos poros se investigó también el uso de monoestearato de glicerilo como surfactante no iónico. En la figura 3, se muestra la representación esquemática de las estructuras moleculares del glicerol y el monoestearato de glicerilo.
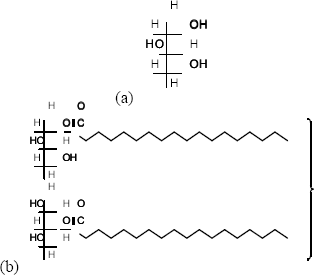 ]]>
Figura 3. Estructuras moleculares del (a) glicerol y (b) monoestearato de glicerilo
]]>
Figura 3. Estructuras moleculares del (a) glicerol y (b) monoestearato de glicerilo
Figure 3. (a) glycerol and (b) glyceryl monostearate molecular structure
Con este artículo se pretende mostrar una forma novedosa de sintetizar óxidos de silicio mesoporosos, en la cual se hace uso glicerol y monoestearato de glicerilo como orientadores de la estructura porosa y tetraetilortosilicato (TEOS) en medio ácido como precursor de silicatos. Adicional a esto, se evaluó la estabilidad hidrotérmica de la sílice que presentó algunas de las mejores características texturales.
2. EXPERIMENTAL
2.1 Reactivos2.2 Pretratamiento del Precursor de Silicatos: TEOS
El TEOS es un líquido altamente insoluble en agua, el cual fue necesario tratar con una solución fuertemente ácida para inducir la hidrólisis de los enlaces etoxi y liberar los grupos silicatos del precursor. La hidrólisis se llevo a cabo adicionando el TEOS a una solución de ácido clorhídrico (pH=2) bajo fuerte agitación magnética. La agitación se mantuvo hasta eliminar completamente la emulsión y obtener una solución homogénea y traslucida.
2.3 Condiciones de Síntesis
De acuerdo con las características fisicoquímicas del monoestearato de glicerilo (Surf), el cual es poco soluble en agua, las condiciones para la síntesis, determinadas experimentalmente, son:
La cantidad de catalizador NaF, es una variable del método de síntesis que fue determinada por tanteo, es decir, se adicionaron pequeñas dosis de la sal hasta encontrar la cantidad mínima necesaria para iniciar la reacción de condensación de la sílice.
2.4 Procedimiento de Síntesis ]]> El agente porógeno fue disuelto en etanol a una temperatura de 60ºC y bajo agitación magnética suave. Luego se adicionó lentamente la solución que contiene el precursor de silicio disuelto, calentada a 90ºC. El volumen se ajustó de tal forma que se mantuvo la relación volumétrica 1:1 etanol-agua y posteriormente se adicionó fluoruro de sodio (NaF). La mezcla fue sometida a tratamiento térmico a 85ºC por tres días. Al terminar el calentamiento, el material fue dispersado mediante ultrasonido, filtrado, lavado con etanol caliente y secado a 90ºC por 12h.El agente porógeno incorporado en la estructura del material obtenido fue removido por calcinación en aire calentando de 25ºC a 100ºC a una velocidad de 1.5ºC/min. Alcanzados los 100ºC se mantuvo esta temperatura por 1 hora y luego se incrementó hasta 550ºC a 1.5ºC/min, manteniéndose durante 5 horas a esta temperatura.
2.5 Prueba de Estabilidad Hidrotérmica2.6 Caracterización
2.6.1 Microscopía Electrónica de Barrido (SEM)
Las micrografías fueron tomadas en un microscopio JEOL JSM 5910LV, con el fin de determinar la morfología y tamaño de las partículas.
2.6.2 Análisis Térmico (TGA-DTA)
El análisis térmico se efectúo sobre las muestras sólidas sin calcinar en un rango de temperaturas entre 25 y 1000°C con un incremento de 5°C/min en un equipo LINSEIS TMA - PT1600 .
2.6.3 Adsorción de nitrógeno
Las características porosas se determinaron mediante un equipo MICROMERITICS GEMINI V que permite medir isotermas de adsorción-desorción de nitrógeno sobre materiales adsorbentes. Las muestras, después de ser calcinadas, fueron tratadas con un gas inerte (nitrógeno) a 100ºC por una hora y luego con vacío a 300ºC por dos horas. Las isotermas generadas por el equipo permitieron determinar el área superficial usando el modelo BET en un intervalo de presión relativa que va desde 0.05 hasta 0.35, la distribución de tamaños de poro entre 1.7 y 20nm por el método BJH y el tamaño de poro medio corresponde al máximo de la curva de distribución de tamaño de poro. El volumen de los mesoporos fue determinado por el método BJH disponible en el software del equipo.
3. RESULTADOS Y DISCUSIÓN
3.1 Análisis Superficial y MorfológicoTabla 1. Propiedades porosas de las sílices sintetizadas
Tabla 1. porous properties of synthesized silica
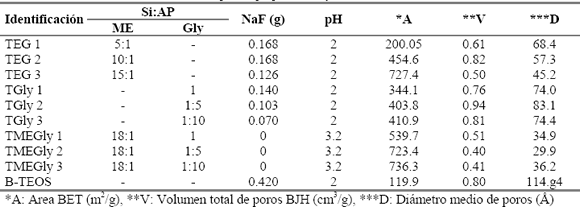
El tipo de agente porógeno (glicerol, monoestearato de glicerilo (ME) y mezclas de ambos) influye enormemente en el área superficial BET de las sílices producidas, como puede apreciarse en la tabla 1. Según la tendencia de los datos, no es posible establecer una correlación general entre la relación molar Si:AP y el área superficial BET, ya que en el caso de las sílices preparadas solo con ME, familia TEG, el área superficial tiende a incrementar cuando se incrementa la relación molar Si:AP, mientras que en los casos donde las sílices fueron preparadas solo con glicerol, familia TGly, y mezclas entre glicerol y ME, el área superficial tiende a incrementar cuando se disminuye la relación Si:AP, es decir, cuando se incrementa el contenido de agente porógeno en la síntesis aumenta el área superficial BET de las sílices producidas.
En el caso de las sílices preparadas con glicerol, el incremento en el área superficial generado por aumento en el contenido de agente porógeno se debe la gran afinidad que existe entre el glicerol y el agua, esto hace que todo el glicerol adicionado este disperso completamente en el medio de síntesis y de esta manera, mayor cantidad quede incorporado en la sílice condensada.
Las sílices con mayor área superficial BET son aquellas que en cuya síntesis se involucró el uso de ME mezclado con glicerol, familia TMEGly. La sílice TEG3 en particular, es una de las sílices con mayor área superficial (727.4m2/g) y es la síntesis que involucró la relación molar Si:AP mas alta de todas, es decir, la menor cantidad de agente porógeno usado. Este efecto se atribuye al comportamiento de la microemulsión formada por el ME en el solvente de síntesis (etanol/agua) a 85ºC. Las miscelas de ME que forman la microemulsion se ven atraídas por los grupos hidroxilos polares de los silicatos con quienes pueden forman puentes de hidrógeno, de tal forma que al incrementar la presencia de silicatos en el medio de reacción, se incrementa la atracción de micelas al seno de la solución, lo que favorece la formación de porosidad en la sílice final.
En cuanto al volumen total de poros, los datos no muestran una tendencia claramente definida cuando se correlacionan con la relación molar Si:AP; esto se debe a que la técnica usada para medir dicha variable incluye tanto poros intra-particulares como poros extra-particulares presentes en el sólido. Las sílicas B-TEOS obtenida sin agente porógeno muestran un valor bastante alto de esta variable según puede apreciarse en la Tabla 1; pese a este valor alto de volumen total de poros, su área superficial BET es baja y su distribución de tamaños de poros, Figura 4, es bastante ancha y achatada, lo que confirma la presencia de mesoporos extraparticulares altamente irregulares e inestables. Este tipo de mesoporos extraparticulares se generan por el acomodamiento libre de las partículas sólidas, los cuales tienden a desaparecer cuando el material es sometido a cargas externas, como por ejemplo en procesos de empastillado para su uso en catálisis heterogénea.
]]>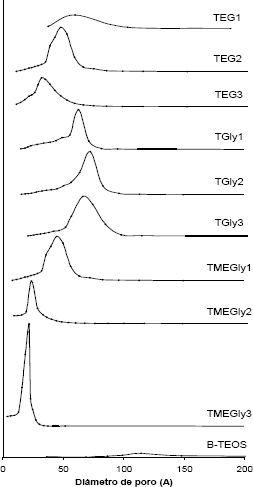
Para el caso de las sílices producidas con ME, familia TEG, se observa una tendencia a disminuir su tamaño de poro a medida que se incrementa la relación molar Si:AP; para los demás casos no fue posible correlacionar los datos de diámetro medio de poro con la relación molar Si:AP, sin embargo, se obtiene un resultado muy positivo en todos los casos y es que los poros de todas las sílicas producidas están dentro del rango meso (20 y 500 Å). Un resultado inquietante es que la sílice que fue preparada sin agente porógeno presenta el valor mas alto para el diámetro medio de poro. Este resultado junto con la curva de distribución de tamaño de poro, el área superficial y el volumen total de poros son fuertes evidencias de que la porosidad en este material es de tipo extra-particular.
En cuanto a las características morfológicas de las sílices, el uso de los agentes porógenos estudiados, glicerol, monoestearato de glicerilo y sus mezclas, conducen a la formación de sólidos completamente amorfos, compuestos de aglomerados de partículas sin forma definida.
En la Figura 5 se muestran las micrografías SEM de las sílices TEG2, producida con monoestearato de glicerilo, TGly2, producida con glicerol, y TMEGly2, producida con una mezcla de ambos porógenos.

Figura 5. Micrografías SEM de las sílices (a) TEG2, (b) TGly2, y (c) TMEGly2
Figure 5. SEM micrographs of silica (a) TEG2, (b) TGly2, y (c) TMEGly2
Las sílices con estas características no tendrían aplicación como fases estacionarias en cromatografía líquida de alta definición (HPLC) o como material abrasivo para el tratamiento superficial químico-mecánico acabado espejo, donde la forma de las partículas asume un rol muy importante. Sin embargo, en aplicaciones donde esta característica es de baja importancia y el área superficial y demás características porosas son dominantes, como es el caso de su uso como soporte de catalizadores químicos para formar catalizadores heterogéneos, estas sílices producidas con los porógenos en mención cobran valor y se hace interesante investigar su aplicación en catálisis heterogénea.
3.2 Análisis Térmico ]]> El análisis térmico de la sílice B-TEOS, muestra en el DTA (figura 6) cambios energéticos abruptos que son característicos de modificaciones estructurales en el sólido por efecto de la temperatura. Dicho fenómeno lo presentan aquellos materiales con grandes defectos estructurales que tienden a ser corregidos a altas temperaturas cuando las moléculas alcanzan un potencial energético que les permite adoptar fases más densas y estables termodinámicamente. El gel de sílice obtenido a pH ácidos incorpora grandes cantidades de agua en su estructura cuya posterior remoción induce la formación de múltiples defectos en su esqueleto inorgánico que se reflejan en la elevada área superficial BET, a pesar de ser una sílice producida sin agente porógeno.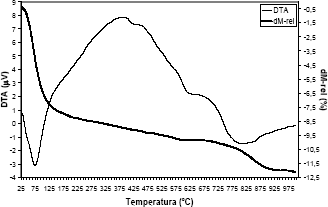
Figura 6. Análisis Térmico (TGA-DTA) de la sílice B-TEOS
Figure 6. Thermal analysis of silica B-TEOS
En la figura 6 puede verse claramente que en el intervalo de temperatura 30- 130°C ocurre un evento endotérmico producto de la evaporación del solvente (etanol/agua), y remoción de humedad ligada y no ligada presente en el material que equivale a una perdida de aproximadamente un 8% de su peso. A temperaturas más altas, el calentamiento induce la liberación de moléculas de agua provenientes de la asociación de grupos hidroxilos superficiales y formación de enlaces siloxanos (-Si-O-Si-) para dar paso a una sílice más densa y estable.
El análisis térmico de las sílices producidas con diferentes cantidades de glicerol como porógeno muestran los mismos eventos entre sí, solo se diferencian en la cantidad de porógeno que es liberado durante el calentamiento, siendo mayor en la sílice que fue preparada con mayor cantidad de glicerol y menor para la sílice preparada con menor cantidad de glicerol. En la figura 7 se muestra el análisis térmico de la sílice TGly2, en el cual puede identificarse tres eventos fácilmente diferenciables, el primero es endotérmico y corresponde a deshidratación y evaporación de solvente en un intervalo el temperatura 30- 130ºC aproximadamente, el segundo también endotérmico, en el intervalo de temperatura 165- 265ºC, y corresponde a la evaporación del glicerol, el tercero es exotérmico y se atribuye a la combustión del exceso de glicerol que no logro ser evaporado a temperaturas mas bajas. Las perdidas de peso mas significativas corresponden a deshidratación y evaporación de solvente con un 12% aproximadamente y remoción del glicerol con un 32% aproximadamente.
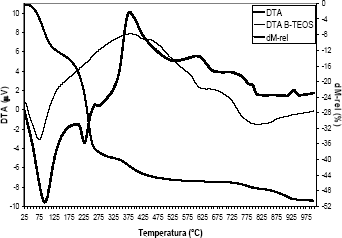
Figura 7. Análisis Térmico (TGA-DTA) de la sílice TGly2
Figure 7. Thermal analysis of silica TGly2
Para las sílices en cuya síntesis se uso monoestearato de glicerilo como porógeno, se presenta el mismo fenómeno que en los casos donde se usó glicerol, las tres sílices producidas presentan los mismos eventos en el análisis térmico. En la figura 8 se muestra el análisis termogravimétrico de la sílice TEG2. En este caso los eventos más significativos se atribuyen a deshidratación y evaporación de solvente entre 30- 115ºC con una perdida de masa de 13.5% aproximadamente, combustión del monoestarato de glicerilo entre 215- 400ºC con una pérdida de masa de 8% aproximadamente y transiciones de fase (deshidroxilación) entre 765- 815ºC.
]]> Como era de esperarse, el termograma de la sílice producida por la mezcla de porógenos es aproximadamente la superposición de los termogramas mostrados en las figuras 7 y 8, que corresponden a las sílices producidas con glicerol y monoestearato de glicerilo respectivamente. Las pérdidas de masa más significativas de la sílice TMEGly2, figura 9, corresponden en un 18% aproximadamente a deshidratación y evaporación de solvente entre 30- 115ºC, un 42% aproximadamente a la evaporación de glicerol entre 115- 300ºC y un 16% aproximadamente a la combustión del exceso de glicerol y del monoestearato de glicerilo.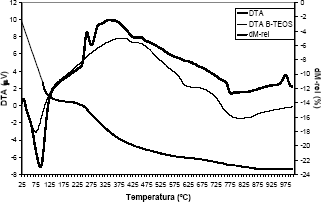
Figura 8. Análisis Térmico (TGA-DTA) de la sílice TEG2
Figure 8. Thermal analysis of silica TEG2
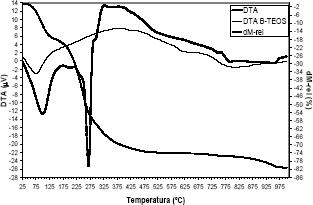
Figura 9. Análisis Térmico (TGA-DTA) para la sílice TMEGly2
Figure 9. Thermal analysis of silica
3.3 Estabilidad Hidrotérmica
En la figura 10 se muestran las isotermas de adsorbión-desorción de nitrógeno para la sílice TEG3 que fue sometida a la prueba hidrotérmica. Allí puede apreciarse que la formación de la histéresis es desplazada de 0.45 a 0.60 (p/p0), lo que se interpreta como una fuerte evidencia de reducción en el área superficial después del tratamiento hidrotérmico. Debido a la forma de las isotermas de adsorción-desorción de nitrógeno se puede apreciar que gran parte de la porosidad del material se conserva y que ésta es del tipo mesoporo.
]]>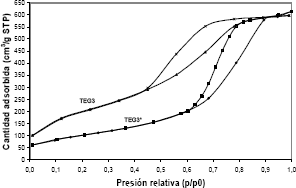
La prueba hidrotérmica realizada sobre la sílice TEG3 fue reproducida del procedimiento descrito por Cassiers et al. con el fin de comparar la estabilidad hidrotérmica de la sílice sintetiza en esta investigación con las evaluadas por ellos, como es el caso de las sílices MCM-48, MCM-41 y FSM-16 que presentan reducción en su área superficial de 86%, 87% y 94% respectivamente. La sílice con mejor estabilidad hidrotérmica estudiada por Cassiers et al., es la SBA-15 que presentó una reducción en su área superficial de 56%. Si comparamos este resultado con el obtenido para la sílice TEG3, figura 11, puede observarse que esta resulta ser más estable hidrotérmicamente que la SBA-15 reportada por Cassiers et al., con una reducción en el área superficial de 50%, que comparada con la MCM-48, la MCM-41 y la FSM-16, es mucho menor.
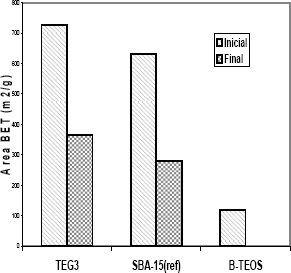
Figura 11. Efecto de la prueba hidrotérmica en el área superficial de las sílices TEG3 y SBA-15
Figure 11. Effect of hydrothermal treatment of silica TEG3 and SBA-15 on surface area
4. CONCLUSIONES
El mecanismo de síntesis en dos etapas en medio fuertemente ácido (pH de 2 y 3.2), basado en la formación de micelas híbridas estables producto de la asociación de los silicatos y los agentes porógenos no iónicos estudiados (monoestearato de glicerilo, glicerol y mezclas de ambos) en la primera etapa y la policondensación inducida por la adición de NaF en la segunda, conduce a la formación de mesoporosidad en la sílice obtenida con características superficiales adecuadas para su aplicación en catálisis heterogénea, como es su alta área superficial y porosidad; además, tales porógenos conducen a la formación de aglomerados de partículas completamente amorfas e irregulares, de tamaños variados y con características porosas diversas según la cantidad y el tipo de porógeno usado.
]]> La naturaleza de los agentes porógenos afecta fuertemente las características porosas del material. El glicerol conduce a la formación de sílices con área superficial BET que no supera los 500 m2/g, donde el efecto de la concentración sobre el área superficial es bastante bajo, según se aprecia en la tabla 1. Debido a la baja solubilidad en agua del monoestarato de glicerilo, su concentración no es una variable que pueda variarse con el fin de incrementar la porosidad de la sílice, sin embargo, al usarse mezclado con glicerol se favorece notablemente su desempeño en la formación de mesoporos en la sílice, dando como resultado un material con alta área superficial y con poros de tamaño muy homogéneo, que son ideales en procesos de separación selectiva de moléculas por tamaño.La sílice con las mejores características mesoporosas es la TMEGly3, con área superficial BET de 736.3 m2/g, volumen total de poros de 0.41 cm3/g y estrecha distribución de tamaños de poro alrededor de 36 Ǻ. La formación de los mesoporos fue generada por la mezcla entre glicerol y monoestearato de glicerilo y sus características superficiales son ideales para su aplicación en catálisis heterogénea.
La sílice TEG3 producida en esta investigación es hidrotérmicamente más estable que las sílices MCM-48, MCM-41, FSM-16 y SBA-15, estudiadas por Cassiers et al.
5. AGRADECIMIENTOS
Los autores agradecen el apoyo de la Universidad de Antioquia y COLCIENCIAS para la realización de esta investigación.
REFERENCIAS
[1] VALENCIA, A. RENDÓN, M. J. Utilización de sílice mesoporosa como carga reforzante o semireforzante en la industria del caucho. Tesis de pregrado Universidad de Antioquia, 2000. [ Links ]
[2] HERNÁNDEZ, B. M. RÍOS, J. E. Funcionalización de sílice mesoporosa (MCM-41) por el mecanismo de silanización, mejoramiento para el uso como carga reforzante en la industria del caucho. Tesis de pregrado Universidad de Antioquia, 2001. [ Links ]
[3] SIERRA, L. LÓPEZ, B. GUTH, J. L. Preparation of mesoporous silica particles with controlled morphology from sodium silicate solutions and a non-ionic surfactant at pH values between 2 and 6. Micropor. Mesopor. Mater. vol. 39, pp. 519-527, 2000. [ Links ]
[4] VACASSY,R. FLATT, R. J. HOFMANN, H. CHOI, K. S. SINGH, R. K.. Synthesis of microporous silica spheres. J. Colloid Interface Sci. vol. 227, pp. 302-315, 2000. [ Links ]
[5] ARAMENDIA, M. A. BORAU, V. JIMENEZ, C. MARINAS, J. M. ROMERO, F. J. Poly(ethylene oxide)-based surfactants as templates for the synthesis of mesoporous silica materials. J. Colloid Interface Sci. vol. 269, pp. 394-402, 2004. [ Links ]
[6] PROUZET, E. BOISSIÈRE, C. A review on the synthesis, structure and applications in separation processes of mesoporous MSU-X silica obtained with the two-step process. C. R. Chimie 8, 2005. [ Links ]
[7] DALE, P. J. KIJLSTRA, J. VINCENT, B. Adsorption of Non-Ionic Surfactants on Hydrophobic Silica Particles and the Stability of the Corresponding Aqueous Dispersions. Langmuir vol. 21:26, pp. 12250-12256, 2005. [ Links ]
[8] ZHANG, W. GLOMSKI, B. PAULY, T. R. PINNAVAIA, T. J. A new nonionic surfactant pathway to mesoporous molecular sieve silicas with long range framework order. Chem. Commun. pp. 18031804, 1999. [ Links ]
[9] CASSIERS, K. LINSSEN, T. MATHIEU, M. BENJELLOUN, M. SCHRIJNEMAKERS, K. VAN DER VOORT, P. COOL, P. AND VANSANT, E. F.. A Detailed Study of Thermal, Hydrothermal, and Mechanical Stabilities of a Wide Range of Surfactant Assembled Mesoporous Silicas. Chem. Mater. 14, 2317-2324, 2002. [ Links ] ]]>