1. Introducción
Las curtiembres son consideradas una de las industria más contaminantes [1]. Durante los procesos de pelambre y curtido se utilizan grandes volúmenes de agua y las pieles son puestas en contacto con azufre y cromo, por lo cual se generan efluentes industriales ricos en estos elementos, que pueden terminar siendo vertidos sin ningún tratamiento directamente sobre los cuerpos de agua naturales, especialmente en países en vía de desarrollo como Colombia. De igual forma, estas aguas residuales presentan altos valores de DBO y DQO además de nitrógeno y fósforo, lo que puede generar procesos de eutrofización en sistemas naturales con la subsecuente pérdida de biodiversidad y problemas de salud pública [2].
Debido a esta problemática, múltiples tratamientos han sido propuestos con el fin de reducir el potencial contaminante de estas aguas. Estos incluyen tratamientos fisicoquímicos como la filtración [3],[4], coagulación, floculación y oxidación electroquímica [5],[6],[7], entre otros. Sin embargo, estos tratamientos suelen ser complejos y costosos, especialmente cuando deben ser utilizados en países como Colombia, donde la industria del curtido es principalmente artesanal y llevada a cabo por familias de bajos recursos. Es por esto que los tratamiento biológicos han ido ganando importancia bajo estas circunstancia, ya que pueden ser más económicos, fáciles de instalar y operar, además de generar una biomasa que podría ser utilizada en procesos biotecnológicos [8],[9]. En estos tratamientos, microorganismos como bacterias y hongos, son utilizados con el fin de oxidar, aeróbicamente o anaeróbicamente, la materia orgánica presente en el agua, además de transformaciones químicas de otros compuestos contaminantes como metales y nutrientes inorgánicos.
Dentro de los tratamientos biológicos, el uso de microalgas ha ganado amplia atención en las últimas décadas. Estos microorganismos fotosintéticos tienen la capacidad de usar el nitrógeno y el fósforo de los efluentes residuales para su crecimiento [10],[11], además de presentar la capacidad de remover importantes cantidades de metales pesados por medio de procesos de absorción y adsorción [12],[13]. De igual forma, generan asociaciones con bacterias que pueden contribuir a la eliminación de materia orgánica y reducción de sólidos suspendidos, además de consumir directamente compuestos orgánicos disueltos en aquellas especies que exhiben comportamientos de mixotrofía [14],[15],[16].
Con el fin de optimizar el tratamiento con microalgas, se ha propuesto la inmovilización celular como una estrategia para aumentar la eficiencia de remoción de los contaminantes. De esta forma, se han probado diferentes matrices de inmovilización como son el alginato de sodio, el poli-estireno y las espumas de poliuretano [17],[18]. Sin embargo, el uso de fibras naturales podría hacer el proceso más económico y ambientalmente sostenible, por lo cual se ha utilizado la matriz del fruto de la Luffa cylindrica, planta ampliamente producida en países de las zonas tropicales y subtropicales, donde su fruto es utilizado como esponjas de baño, debido a su estructura fibrosa de lignina y celulosa y que presenta múltiples microcanales que producen un sistema de poros, lo cual ha mostrado buenos resultados tanto en el atrapamiento de las microalgas, como en la remoción de contaminantes por parte de estas [19],[20],[21].
En el presente trabajo se evaluó la capacidad del crecimiento de la microalga verde Scenedesmus sp. en un agua residual de curtiembre, determinando la remoción de los principales contaminantes del efluente y comparando la eficiencia entre un tratamiento con células libres y otro con células inmovilizadas en una matriz de Luffa. Finalmente se evaluó el contenido de lípidos de la biomasa obtenida, con el fin de estimar su potencial uso en la generación de biodiesel.
2. Materiales y Métodos
Toma de muestra y caracterización del agua residual
Una muestra puntual de agua residual fue recolectada en una curtiembre ubicada en el barrio San Benito de la ciudad de Bogotá D.C, en la salida de una caja de filtración donde se retiran los pelos y pedazos de carne provenientes de los procesos de pelambre y curtido de la piel [Figura 1].

Figura 1: Punto de recolección de la muestra de agua residual de curtiembre. Se observa una caja rejilla con sustrato filtrante (rocas) con el fin de retirar pelos y carne procedente del proceso de pelambre. El flujo del agua es de izquierda a derecha y la muestra fue recolectada en la salida de la caja.
En este punto el agua no presentaba ningún tipo de tratamiento. La muestra fue tomada en un recipiente de 20 L oscurecido con bolsas plásticas negras y fue transportada en refrigeración hasta el laboratorio. Paralelamente se realizaron mediciones in situ de oxígeno disuelto (Numak ODZ-608), pH (Hanna HI 98128), conductividad (Hach SensION5) y turbidez (HACH 2100Q).
Posteriormente en el laboratorio, la muestra se dejó en decantación con el fin de permitir la precipitación de cualquier material particulado que pudiera estar presente y fue caracterizada utilizando los kits de análisis por espectrofotometría de HACH para los parámetros de nitritos (método 8507), nitratos (método 8171), amonio (método 8155), sulfatos (método 8051), fosfatos (método 8048), cromo hexavalente (método 8023) y demanda química de oxigeno DQO (método 8000). De igual forma, se determinó la demanda bioquímica de oxígeno por incubación durante 5 días (DBO 5) y la concentración de cromo total por absorción atómica de llama (ContrAA700).
2.2 Inmovilización de la microalga
La inmovilización celular se hizo con 15 días de anticipación a los experimentos, para esto primero se cortó el estropajo en forma de discos, con diámetro aproximado de 1 cm y altura de 0.5 cm. Después para eliminar las impurezas, fueron lavados con agua del grifo durante 5 min, posteriormente se sumergieron en agua destilada por 24 horas durante las cuales se realizaron recambios del agua cada 8 horas. Finalmente los discos fueron dejados en un horno a 70°C durante 24 horas con el fin de eliminar la humedad y se esterilizaron en autoclave a 120°C durante 20 min.
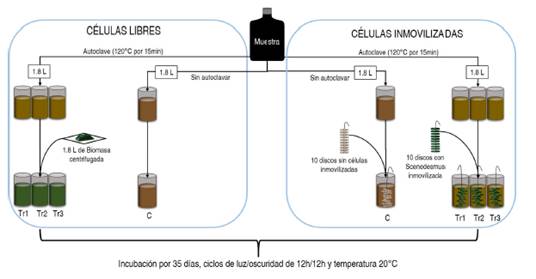
Finalizada la esterilización, cada disco fue identificado y pesado, con el fin de hacer seguimiento a la biomasa inmovilizada. Inmediatamente NPK al 1 %) durante 10 min y posteriormente fueron introducidos al cultivo después, se sumergieron en un litro de medio de cultivo estéril (fertilizante NPK al 1%) durante 10 min y posteriormente fueron introducidos al cultivo de la microalga, donde se dejaron por un periodo de 4 días, con un ciclo de luz y oscuridad de 12 horas, con el fin de permitir la inmovilización de Scenedesmus. Finalmente, los discos con el microorganismos inmovilizado fueron puestos en medio fresco y dejados por 7 días más para su crecimiento, momento en el cual fueron pesados con el fin de establecer la cantidad inicial de biomasa en la matriz de Luffa [Figura 2].
2.3 Montaje de los experimentos
2.3.1 Experimento con células libres
La evaluación de la capacidad de crecimiento y remoción de contaminantes por parte de Scenedesmus en suspensión, se realizó en reactores tipo batch con un volumen efectivo 2 L. Para el montaje, el agua residual fue esterilizada a 120°C por 20 minutos para eliminar los posibles microorganismos que estuviesen presentes y se diluyó 1:1 con agua destilada con el fin de disminuir la turbidez del agua, lo cual podría afectar la captación de la luz por parte de la microalga. Al reactor se agregó 1.8 L de la dilución y se adicionó un volumen igual (1.8 L) de un cultivo en crecimiento exponencial de Scenedesmus sp. Sin embargo este volumen de cultivo fue previamente centrifugado a 6000 RPM (3830G) durante 2 min y agregado solo el pellet obtenido. Cada tratamiento fue realizado por triplicado y se tuvo un control que consistió en un reactor que contenía 1.8 L del agua residual diluida esterilizada sin la adición del microorganismo. Los cuatro reactores fueron mantenidos en condiciones controladas, a una temperatura de 20°C y ciclos de luz/oscuridad de 12 horas [Figura 3].
2.3.2 Experimento con células inmovilizadas
Los experimentos realizados con las células inmovilizadas, consistieron en reactores de un volumen de 2 L donde se adicionaron 1.8 L del agua residual diluida estéril como se explica en el apartado 2.3.1. Al reactor fue adicionado diez discos de Luffa donde se habían inmovilizado previamente las células de Scenedesmus y que fueron marcados y pesados inicialmente, con el fin de determinar los cambios en la biomasa de la microalga. Los tratamientos se realizaron por triplicado y adicionalmente se realizó un control que consistió en un reactor que contenía 1.8 L del agua residual diluida sin esterilizar y 10 discos de Luffa sin células inmovilizadas. Los cuatro reactores fueron mantenidos en condiciones controladas, a una temperatura de 20°C y ciclos de luz/oscuridad de 12 horas [Figura 3].
2.3.3 Seguimiento de los experimentos
A cada uno de los experimentos se les realizó un seguimiento diario del crecimiento de la microalga, por un periodo total de 33 días. Para las células libres se realizaron mediciones de densidad óptica a una muestra de 10 mL, en una longitud de onda de 660 nm utilizando un espectrofotómetro UV/visible (HACH DR6000).Posteriormente los datos fueron transformados a biomasa de peso seco utilizando la relación Y = 0.19299X + 0.09812 , reportada por Pérez Silva et al. [22] para esta misma especie, donde X corresponde al valor de absorbancia a 660 nm y Y a la biomasa en mgmL −1 . Por su parte, para el tratamiento con células inmovilizadas, dos discos, los mismos en cada medición, fueron pesados a diario en una balanza analítica para determinar el incremento o disminución de la biomasa atrapada en la matriz de Luffa. Esta biomasa posteriormente fue expresada mgmL −1 teniendo en cuenta el volumen aproximado de los diez discos.
Finalizados los 33 días, la biomasa fue cosechada con el fin de analizar las características del agua resultante. En el caso de los tratamientos con células libres, el agua de los diferentes reactores fue centrifugada a 6000 RPM por 3 min, con el fin de sedimentar la biomasa y el sobrenadante fue recolectado para su posterior análisis. En los tratamientos con células inmovilizadas la cosecha consistió en retirar los discos con la biomasa inmovilizada. El agua residual proveniente de los diferentes tratamientos, fue caracterizada fisicoquímicamente de la misma forma como se explicó en el apartado 2.1, con el fin de comparar las condiciones previas y posteriores a tratamiento con la microalga.
La biomasa obtenida en los dos tratamientos, fue analizada para determinar su contenido de lípidos, con el fin de evaluar su potencial uso en la generación de biocombustibles. Para esto, tanto la biomasa libre como la atrapada en la matriz de Luffa, fueron secadas en un horno a 70°C durante 24 horas y posteriormente fue aplicado el protocolo de extracción de lípidos por solventes propuesto por Folch et al. [23] y finalmente cuantificados por el método de gravimetría.
2.4 Análisis de datos
Para determinar las posibles diferencias en el crecimiento de Scenedesmus en los dos tratamientos evaluados (libre e inmóvil) se realizó una prueba no paramétrica U de Mann-Whitney, ya que los datos no presentaron una distribución normal. De igual forma, se compararon los valores iniciales y finales de los diferentes parámetros fisicoquímicos y se calculó el porcentaje de remoción por medio de la Ecuación [1]
3 Resultados y Discusión
3.1 Características del agua residual
En la Tabla 1 se pueden observar las características fisicoquímicas del agua residual de curtiembre utilizada en el presente trabajo. El nitrógeno presente se encontró principalmente en la forma de nitratos y amonio con valores de 350 y 118 mgL −1 respectivamente.
Tabla 1 Características fisicoquímicas del agua residual de curtiembres utilizada en el presente trabajo
| Parámetro | (Valor Inicial) | Unidades |
| NO3- | 70 | mgL−1 |
| NO2- | 0.1 | mgL−1 |
| NH4+ | 23.6 | mgL−1 |
| PO43- | 30.6 | mgL−1 |
| RatioNP | 3.06 | |
| SO42- | 10200 | mgL−1 |
| DBO | 3280 | mgL−1 |
| DQO | 7960 | mgL−1 |
| Cr total | 156.7 | mgL−1 |
| Cr+6 | 0.08 | mgL−1 |
| pH | 8.55 | |
| Conductividad | > 2999 | µScm−1 |
| SST | 0.01 | mgL−1 |
| SS | 1.5 | mlL−1 |
| Oxigeno Disuelto | 0.23 | mlL−1 |
De igual forma, se observó una concentración de fosfatos de 153 mgL −1 , lo que representa un ratio N:P aproximado de 3, lo cual indica un efluente limitado por nitrógeno, lo cual puede tener efectos directos sobre el crecimiento de las microorganismos y su estequiometría [24],[25]. Por su parte la DBO y DQO presentaron valores de 3280 y 7960 mgL −1 respectivamente, los cuales son similares a los reportados en otros trabajos para aguas residuales de curtiembres [26], así mismo la proporción de DQO:DBO es de 2.43, indicando una alta biodegradabilidad de este efluente. Finalmente, el agua residual presentó concentraciones de cromo total de 156,7 mgL −1 y 0,08 mgL −1 en su forma hexavalente (Cr +6), elemento utilizado en forma de sales de cromo durante el proceso de curtido de la piel. Es importante destacar, que los valores obtenidos tanto para DBO, DQO como Cromo son más altos que los permitidos por la legislación vigente en Colombia para efluentes provenientes del proceso de curtido y trasformación de la piel [27], lo cual hace necesario un tratamiento de estas aguas previo a su vertimiento sobre un cuerpo de agua superficial.
3.2 Crecimiento de la microalga en el agua residual
En la Figura 4 se observa el crecimiento presentado por Scenedesmus durante el periodo de experimentación, tanto en la forma de células libres (4a) como inmovilizadas (4b). La tasa de crecimiento en los tratamientos con células libres correspondió a 0.006d −1 con una producción diaria de biomasa de 0.013 mgmL −1 d −1 , mientras que las células inmovilizadas presentaron una tasa de decrecimiento de 0.022 d −1 con una disminución diaria de biomasa inmovilizada de 17.88 mgmL −1 d −1 . Las diferencias en el crecimiento entre ambos tratamientos fueron estadísticamente significativas (p < 0.05; n = 102). Si bien la inmovilización celular ha sido planteada como una estrategia para facilitar la recolección de la biomasa y disminuir los costos asociados a esta operación, así como aumentar la eficiencia de remoción de contaminantes [28], presenta una serie de limitaciones, especialmente relacionadas en la difusión de nutrientes y factores de crecimiento requeridos por lo microorganismos inmovilizados [29],[21],[30]. En el presente trabajo se observó una disminución de la biomasa adherida a los discos de Luffa, lo cual podría ser debido a una baja difusión a través de la matriz, de los nutrientes necesarios para su crecimiento, sin embargo durante el desarrollo de los experimentos se evidenció una acumulación de biomasa en el fondo de los reactores, lo cual podría indicar un desprendimiento de la microalga, bien a causa de la manipulación de los discos en el momento de hacer las mediciones de peso, o bien por una saturación del área efectiva de adhesión de los discos.
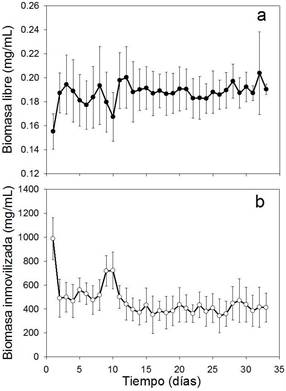
Figura 4 Gráficas de crecimiento de la biomasa priomedio de Scenedesmus sp. durante el periodo del experimento. A) tratamiento con células libres, b) tratamiento con células inmovilizadas.
En el presente trabajo se utilizó la matriz del fruto de la planta Luffa, debido a que es un material económico y de fácil acceso en un país como Colombia, de igual forma ha sido utilizado previamente en otros trabajos para la inmovilización de microalgas con el objetivo de remover metales pesados [31],[19]. Sin embargo, otros materiales de inmovilización como el alginato [30], polivinilos [32], poliuretano [33] y poliestirenos [34] también han sido utilizados para el crecimiento microalgas y la remoción de nutrientes y otros contaminantes en el agua, obteniendo resultados similares a los encontrados en el presente estudio.
El tratamiento con células libres exhibió un mayor crecimiento con respecto a las células inmovilizadas, sin embargo la biomasa obtenida durante el periodo de experimentación es menor a los reportados en otros trabajos. Ajayan et al. [14] evaluaron el crecimiento de Scenedesmus en aguas residuales de curtiembres en la India, alcanzado una tasa específica de crecimiento de 1.24 d −1 . De igual forma Ballén-Segura et al. [15] utilizando también Scenedesmus en aguas residuales de curtiembres, obtuvieron una tasa de crecimiento durante 15 días de 0.085 d −1 una producción de biomasa de 0.01 mgmL −1 d −1 . Estas diferencias, especialmente con la primera referencia, pueden ser debidos a las características propias del agua, ya que el agua residual de curtiembres utilizada en el presente estudio, presentó valores ampliamente superiores de cromo (156.7 vs 12.8 mgL −1 ), el cual ha sido reportado por afectar el crecimiento y la fotosíntesis de las microalgas [35],[36], así como una fuerte limitación por nitrógeno (Ratio N/P 3.06 vs 12.56), que también puede influir sobre el crecimiento de los microorganismos autótrofos.
La capacidad de uso de los nutrientes presentes en aguas residuales industriales por parte de microalgas ha sido ampliamente reportada [14],[37], [38]. En el presente trabajo, se observó una importante reducción de la concentración de nitrógeno tanto en forma de amonio como nitratos, y de fósforo inorgánico [Tabla 2 y 3) todos estos asimilables por las microalgas, lo cual permite pensar que el efluente fue utilizado como sustrato de crecimiento por Scenedesmus, especialmente en los tratamientos con células libres.
3.3 Remoción de contaminantes del agua residual
Las microalgas tienen la capacidad de utilizar el nitrógeno y el fósforo inorgánico presente en las aguas residuales, los cuales son utilizados para la síntesis de proteínas, generación de ATP, formación de membranas, entre otras. En el agua de curtiembre utilizada, el nitrógeno se presentó principalmente en forma de nitratos y amonio, éste primero fue removido en un 99 % tanto en el tratamiento con células libres [Tabla 2] como inmovilizadas [Tabla 3], mientras que el amonio fue removido en 95 % en ambos un porcentaje superior al 83 % en ambos tratamientos. Estos valores son casos. Por su parte el fósforo, en la forma de ortofosfatos fue eliminado en similares a los reportados por otros estudios en aguas residuales de curtiembres [15] y otros efluentes municipales [39]. Sin embargo, cabe destacar que en los controles realizados tanto para las células libres como inmovilizadas se alcanzaron porcentajes de remoción similar. Esto parece indicar que además de la absorción directa que pueden realizar las microalgas sobre estos nutrientes, otros factores adicionales participaron en dicha eliminación. Dentro de estos podemos ver el papel de las bacterias (control 2), las cuales no solo utilizan parte de estos nutrientes, sino que pueden participar en la transformación de los nitratos en nitritos, los cuales presentaron menores valores de remoción [Tabla 2 y 3), por medio del proceso de desnitrificación [40], el cual pudo verse favorecido ante las bajas concentraciones de oxígeno disuelto presentes en el agua residual (0.23 mgL −1 ).
Tabla 2 Concentración de contaminantes inicial y final, y porcentajes de remoción obtenidos con el tratamiento de Scenedesmus sp. en forma de células libres.
| Parametro | Concentración Inicial (mgL−1) | Concentración final (mgL−1) | % Remoción | |||
| Tratamiento | Control | Tratamiento | Control | |||
| NO3 - | 70 | 0.60 ± 0.20 | 0.40 | 99.14 | 99.43 | |
| NO2 - | 0.1 | 0.03 ± 0.01 | 0.06 | 73.33 | 38.00 | |
| NH4 + | 23.6 | > 1.00 | > 1.00 | > 95.76 | > 95.76 | |
| PO4 3- | 30.6 | > 5.00 | > 5.00 | > 83.66 | > 83.66 | |
| SO4 2- | 2040 | 210.66 ± 21.94 | 212.00 | 89.67 | 89.61 | |
| DBO | 3280 | 63.33 ± 54.12 | 104.00 | 98.07 | 96.83 | |
| DQO | 7960 | 442 ± 22.54 | 434.00 | 94.45 | 94.55 | |
| Cr total | 156.7 | 2.27 ± 0.86 | 2.28 | 98.55 | 98.54 | |
| Cr+6 | 0.08 | 0.04 ± 0.02 | 0.14 | 40.83 | -75.00 | |
Tabla 3 Concentración de contaminantes inicial y final, y porcentajes de remoción obtenidos con el tratamiento de Scenedesmus sp. en forma de células inmovilizadas.
| Parámetro | Concentración Inicial (mgL−1) | Concentración final (mgL−1) | % Remoción | |||
| Tratamiento | Control | Tratamiento | Control | |||
| NO3 - | 70 | 0.60 ± 0.35 | 0.60 | 99.14 | 99.14 | |
| NO2 - | 0.1 | 0.050 ± 0.04 | 0.08 | 49.33 | 16.00 | |
| NH4 + | 23.6 | > 1.00 | > 1.00 | > 95.76 | > 95.76 | |
| PO4 3- | 30.6 | > 5.00 | > 5.00 | > 83.66 | > 83.66 | |
| SO4 2- | 2040 | 224 ± 2 | 212.00 | 89.02 | 89.61 | |
| DBO | 3280 | 84.66 ± 34.64 | 202.00 | 89.02 | 89.61 | |
| DQO | 7960 | 142.66 ± 42.02 | 296.00 | 98.21 | 96.28 | |
| Cr total | 156.7 | 3.06 ± 1.43 | 9.30 | 98.05 | 94.07 | |
| Cr+6 | 0.08 | 0.03 ± 0.02 | 0.12 | 53.33 | -50.00 | |
Por su parte, los sulfatos fueron removidos en porcentajes superiores al 89%. Esta remoción puede ser llevada a cabo directamente por la microalga, la cual puede incorporar el azufre a su metabolismo central, ser reducido y utilizado en la síntesis de proteínas, ácidos nucleicos y vitaminas [41]. De igual forma, las bacterias pudieron contribuir a esta eliminación del azufre, por medio de su participación en el ciclo del azufre, donde llevan a cabo procesos de sulfato reducción en condiciones anaeróbicas, con la subsecuente formación de sulfuro de hidrógeno, lo cual pudo ser evidenciado en el olor que se desprendían de los reactores.
Por otro lado, la materia orgánica, medida como DBO y DQO, presentó remociones del 98 y 94 % para el tratamiento con células libres [Tabla 2] y del 97 y 98 % para el tratamiento con células inmovilizadas [Tabla 3] respectivamente. Estos valores son superiores a los reportados por Ajayan et al. [14] para aguas de curtido, donde observaron eliminaciones del 35 % para DBO y 40 % para DQO por parte de Scenedesmus. De igual forma, et al. [15] con un 88 %. Estas diferencias pueden ser debidas al tiempo de son levemente superiores a los encontrados para DBO por Ballén-Segura duración del experimento, ya que ellos realizaron incubaciones de 12 y 15 días respectivamente, mientras en el presente las incubaciones fueron de 33 días, dando mayor tiempo para la asimilación de esta materia orgánica tanto por parte de las microalgas, como de las bacterias presentes (control 2).
A pesar de que las microalgas, especialmente las algas verdes grupo al cual pertenece Scenedesmus, son conocidos como organismos autótrofos, una creciente evidencia ha demostrado que estos organismos pueden presentar la capacidad de utilizar compuestos orgánicos como fuente de carbono, fenómeno conocido como mixotrofía [42],[43],[44]. De esta forma, es posible pensar que en el presente trabajo Scenedesmus pudo utilizar parte de la materia orgánica disuelta como una fuente complementaria de carbono, llevando a la reducción y remoción de la DBO. Así mismo, es bien reconocido desde la postulación por Azam et al. [45] del bucle microbiano (microbial loop), que las microalgas y las bacterias generan interacciones de sinergísmo, en las cuales el carbono orgánico disuelto (COD) es utilizado por parte de las bacterias quien a su vez remineralizan esta materia orgánica, colocando de nuevo a disposición de las microalgas lo nutrientes inorgánicos requeridos para su crecimiento. En el presente trabajo, Scenedesmus se encontraba en un monocultivo, sin embargo no era axénico, por lo cual las bacterias acompañantes pudieron contribuir en la oxidación de la materia orgánica presente en el efluente. En cualquier caso, cabe destacar que los valores permitidos por la legislación en Colombia tanto para DQO como DBO son de 1200 y 600 mgL −1 respectivamente, por lo cual el tratamiento utilizado con Scenedesmus permitió reducir los valores iniciales hasta valores dentro de este rango.
Las microalgas son utilizadas para el tratamiento de aguas contaminadas con metales pesados, debido a su capacidad de tolerancia [46]. El cromo es el principal metal pesado presente en las aguas residuales de curtiembres y en el presente trabajo se encontró en concentraciones de 156.7 mgL-1 para el total y 0.08 mgL-1 para la forma hexavalente. Después del tratamiento con Scenedesmus se alcanzaron remociones de cromo total de 98 % tanto en la forma de células libres como inmovilizadas y del 40 y 53 % para el cromo hexavalente [Tabla 2 y 3). Previos trabajos como los de Ajayan et al. [14], Das et al. [47], Subashini and Rajiv [48] y Das et al. [49] han reportado porcentajes similares de remoción con diversas especies de microalgas, y se han descrito diferentes mecanismos por los cuales estas pueden remover metales pesados del agua, entre los cuales cabe destacar procesos de sorción (adsorción y absorción) que involucran la superficie celular o ligandos intracelulares [50]. De igual manera, las microalgas pueden facilitar la precipitación química de los metales debido al cambio de pH generado durante su crecimiento fotosintético [51]. Finalmente, de los resultados obtenidos en el presente trabajo, se observa que no hubo diferencias significativas entre los tratamientos con células libres e inmovilizadas, sin embargo, la inmovilización celular, sigue siendo una alternativa viable desde el punto de vista económico, ya que reduce los costos asociados a la recolección y separación de la biomasa microalgal generada durante el tratamiento, biomasa que puede ser posteriormente utilizada como materia prima para diversos procesos biotecnológicos, dando un valor adicional al tratamiento convencional de aguas residuales.
3.4 Concentración de lípidos de la biomasa
En la Figura 5 se observa los valores promedio obtenidos para la cuantificación de lípidos de cada experimento. En el caso de las células libres el porcentaje de lípidos con respecto a la biomasa seca fue 28.82 %, mientras en las células inmovilizadas fue 32.26 %. Estos valores son altos comparados con los reportados por Ruiz-Marín et al. [52] quienes evaluaron la producción de lípidos en Scenedesmus obliquus en aguas residuales con valores de 12-14 %. De igual forma, son altos comparados por los encontrados por Aravantinou et al. [53] en un agua residual sintética, en la cual Scenedesmus rubescens acumuló un promedio de lípidos entre 4.97 a 14.91 %. Esta diferencia puede ser debida a que el agua residual utilizada en este trabajo, presento una fuerte limitación de nitrógeno (ratio N:P de 3), lo cual ha sido demostrado como un factor generador de estrés en microalgas, lo cual dispara el metabolismo de los ácidos grasos, aumentando la producción de lípidos [54],[25], especialmente en microalgas oleaginosas como lo son los individuos del genero Scenedesmus [55].
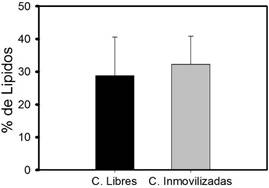
Figura 5 Valores promedio del porcentaje de lípidos en relación a la biomasa seca de Scenedesmus en los dos tratamientos evaluados en el presente trabajo
La producción de biomasa rica en lípidos, como en el caso de presente estudio, aporta un valor agregado a los tratamientos de aguas residuales, ya que dichos lípidos, formados por ácidos grasos y triglicéridos, pueden ser extraídos y transesterificados con el fin de obtener ácidos grados metil-esteres (FAMES por sus siglas en inglés) compuestos principales del biodiesel [56]. Sin embargo es de tener en cuenta que la producción o uso de microalgas que han estado en contacto con sustancias peligrosas como los metales, podrían ser un obstáculo para su comercialización, ya que los productos derivados de estas tendrían altas concentraciones de estas sustancias y su combustión generaría emisiones contaminantes a la atmósfera. De esta forma, sería necesario acoplar otros tratamientos adicionales sobre los efluentes, con el fin de reducir la concentración de los metales previo al contacto con las microalgas.
Conclusiones
En base a los resultados obtenidos en el presente trabajo se puede concluir que el la microalga Scenedesmus creció utilizando el agua residual de curtiembre como sustrato, especialmente en forma de células libres. Sin embargo, a pesar de estas diferencias en el crecimiento, ambos tratamientos (libres e inmovilizadas) presentaron remociones importantes de N, P, Cr y materia orgánica (medida como DBO y DQO). Esto indica que es viable utilizar esta microalga como agente de remoción de compuestos contaminantes, al menos a escalas de laboratorio. Son necesarios estudios posteriores que permita evaluar a escalas mayores, donde otros factores como el uso de reactores, la incidencia de la luz y la agitación pueden afectar el crecimiento y por lo tanto las tasas de remoción.
De igual forma, esta reducción de contaminantes no puede ser atribuida solamente a la microalga, ya que los controles utilizados (agua sin esterilizar) presentaron valores similares, lo cual demuestra el papel jugado por las bacterias dentro de estos tratamientos. Finalmente, el porcentaje de lípidos fue superior a lo reportado en otros estudios similares, posiblemente debido a la fuerte limitación de nitrógeno que presentaba el agua evaluada, lo cual convierte esta biomasa en una potencial materia prima para la generación de biocombustibles u otros procesos biotecnológicos siempre teniendo en cuenta la posible interferencia que puede ejercer la presencia de altas concentraciones de metales en la biomasa microalgal o bioproductos derivados de ella, lo cual hace actualmente inviable el doble uso (tratamiento de aguas y producción de biocombustibles).