Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Revista Colombiana de Entomología
Print version ISSN 0120-0488On-line version ISSN 2665-4385
Rev. Colomb. Entomol. vol.33 no.2 Bogotá June/Dec. 2007
Sección Medica
Experiencia de un análisis entomológico de criaderos de Aedes aegypti y Culex quinquefasciatus en Cali, Colombia
Experience of an entomological analysis of the breeding sites of Aedes aegypti and Culex quinquefasciatus in Cali, Colombia
RANULFO GONZÁLEZ OBANDO1, FEDERICO GAMBOA2, ORLANDO PERAFÁN2, MARCO FIDEL SUÁREZ3, JAMES MONTOYA LERMA1
1 Biólogos, Profesores. Grupo de Investigaciones Entomológicas. Depar-tamento de Biología. Universidad del Valle. A.A 25360 Cali. ranulfog@univalle.edu.co, jamesmon@univalle.edu.co
2 Exfuncionarios Servicio Erradicación de la Malaria, SEM. Cali.
3 Biólogo, Funcionario OPS, masuarez@hotmail.com
Resumen: Mediante muestreos larvales se evaluó la positividad y asociación poblacional del vector de dengue, Aedes aegypti, con Culex quinquefasciatus, vector del virus del Nilo, en 537 sumideros ubicados en 19 comunas de seis SILOS (Sistemas Locales de Salud) de la Ciudad de Cali, Colombia. Los índices promedio de positividad de sumideros (IS) fueron 57,2 y 73,6% para cada especie, respectivamente. Aunque sólo fue una tendencia, estos valores variaron acorde al estrato social de la ciudad y en todas las áreas evaluadas se estableció que ambas especies presentan una asociación poblacional positiva de alta significancia. Al evaluar la importancia relativa de los sumideros en la producción de A. aegypti, se observó que estos criaderos son tan o más importantes que los encontrados en áreas intra y peridomiciliares de los barrios y unidades residenciales. El análisis de las casas de 10 manzanas, incluyendo 62 sumideros ubicados en la vecindad próxima de las viviendas, mostró que en el intradomicilio no se producen pupas. Si se asume una tasa constante de sobrevivencia diaria de 0,80, el número de hembras/manzana estimado para los sumideros fue mayor que la de otros criaderos del peridomicilio. Para los sumideros la densidad absoluta varió entre 45 y 555 (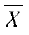 = 200 hembras/manzana), mientras que en los segundos, éste varió únicamente entre 0 y 69 (
= 200 hembras/manzana), mientras que en los segundos, éste varió únicamente entre 0 y 69 ( 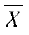 = 22 hembras/manzana).
= 22 hembras/manzana).
Palabras clave: Población. Vector dengue. Índices criaderos. Sumideros urbanos.
Abstract:Larval sampling was carried out to evaluate the presence and population relationship between the vector of dengue, Aedes aegypti and Culex quinquefasciatus, vector of West Nile virus, in 537 sinks, located in 19 “comunas” (quarter associations) of the six SILOS (i.e. local health systems) of the city of Cali, Colombia. The mean positivity index (IS) for the sinks was 57.2% and 73.6% for each species, respectively. Although it was only a tendency, these values varied according to city social strata, and in all of the areas evaluated it was established that each species had a highly significant positive population correlation. In evaluating the relative importance of the city sinks in the production of A. aegypti, it was established that those breeding sites are equally or more important than intra or peridomiciliar breeding sites. The analysis of houses in 10 city blocks, including 62 street sinks in the nearby vicinity, revealed that intradomiciliar settings do not produce pupae. Assuming a constant adult survival rate of 0.80 per day, the number of females per block estimated for the sinks was greater than peridomiciliar breeding sites. For the street sinks, absolute density varied between 45 and 555 ( 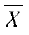 200 female/block), while in the peridomiciliar settings it was only 0 and 69 (
200 female/block), while in the peridomiciliar settings it was only 0 and 69 (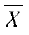 22 female/block).
22 female/block).
Key words: Vector. Dengue population. Breeding site indices. Urban sinks.
Introducción
El dengue clásico y sus manifestaciones clínicas más graves, hemorrágico (DH) y síndrome del choque (SCD) son patologías que originan amplia morbilidad y mortalidad en salud pública (OPS 1995). Estas enfermedades son endémicas y, en ocasiones han alcanzado características epidémicas en más de 100 países de zonas tropicales de América, África y Asia, donde la prevalencia está asociada a su principal vector, Aedes aegypti L., 1762 aunque, eventualmente, A. albopictus (Skuse, 1894) puede estar involucrado (OPS 1987; Rai 1991). En el mundo se estima en 50 millones de infecciones al año (San Martín y Prado 2004) y en las Américas, la situación se ha agravado durante los últimos 20 años como consecuencia del incremento del número de casos y de países afectados así como por el incremento de las manifestaciones graves de DH y del SCD. En el año 2002, de 1’019.196 casos, 17.363 fueron de DH (San Martín y Prado 2004). En Colombia, especialmente a partir de 1980, se han presentado epidemias en varias regiones del país. En el año 2003 fueron registrados 58.335 casos, de los cuales 5.026 fueron atribuidos a DH (Sivigila 2004) y se estima que aproximadamente 18 millones de personas se encuentran en áreas de riesgo de contraer la enfermedad (Camacho 1991).
La detección temprana de casos unida al monitoreo entomológico representan, indiscutiblemente, es la forma más eficaz de evitar brotes epidémicos. Sin embargo, la vigilancia serológica y viral están fuera del alcance de los recursos de la gran mayoría de países afectados. Además, por lo general, la transmisión de los diferentes serotipos está altamente correlacionada con el crecimiento desordenado de las ciudades, indebido manejo doméstico del agua, limitada cobertura de los servicios de acueducto y/o deposición de materiales “inservibles” o “desechos” (Nelson 1986). Por lo tanto, no es sorprendente que las inferencias de infección y consecuentes medidas de control estén determinadas por la variación de las poblaciones (adultas y larvales) del vector.
Tradicionalmente, las medidas de control están encaminadas a reducir al mínimo las poblaciones de A. aegypti, mediante la eliminación o tratamiento, generalmente químico, de los hábitats de las formas inmaduras (huevos, larvas y pupas). En las Américas, la colonización de A. aegypti se ha asociado a una gran diversidad de criaderos naturales y artificiales (Trapido y Galindo 1956; Tinker 1974; Chadee 1984, 1992; Nelson 1986; Chadee et al. 1998) siendo las llantas probablemente las principales fuentes de cría del mosquito (Nelson 1986). En Trinidad, Focks y Chadee (1997) al analizar, en términos de producción de pupas, el aporte por tipo de criadero, registraron que solamente cuatro de 11 de los criaderos encontrados (tanques, tinas, baldes y pequeños contenedores), presentaban más del 90% de las pupas de A. aegypti. La utilización de criaderos permanentes y temporales sugiere, que, esta especie, sufre cambios de comportamiento debido a la presión de insecticidas y eliminación de criaderos domiciliares y peridomiciliares (Chadee et al. 1998). Sin embargo, hasta ahora, no existen datos del aporte relativo de cada tipo de criadero en una comunidad determinada.
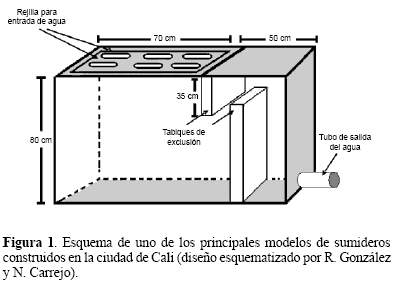
Los sumideros (Fig.1), son construcciones muy comunes en las áreas urbanas para el desagüe de las vías publicas, son considerados muy prolíficos en la producción de especies de Culex, en especial C. quinquefasciatus Say 1823 debido a que retienen agua y materia orgánica por largos periodos (Geery y Holub 1989). Observaciones preliminares realizadas en la ciudad de Cali, indicaron que estos sitios han sido, paulatinamente, colonizados también por A. aegypti. Por ejemplo, en el Campus de la Universidad del Valle se encontró que de 47 sumideros más del 50% eran positivos para A. aegypti, independiente del nivel de fermentación o contenido de materia orgánica (R. González, datos no publicados). Para comienzos de 1991 se desconocía si esta situación prevalecía en toda la ciudad de Cali y, por lo tanto, a mediados de ese año, con personal del antiguo Servicio de Erradicación de la Malaria (SEM), se realizó una encuesta entomológica para determinar el índice de sumideros positivos (IS), la densidad relativa de las especies de C. quinquefasciatus y A. aegypti y la estratificación de su importancia según las comunas de los denominados en ese entonces Sistemas Locales de Salud (SILOS). Aunque los resultados sirvieron de base para adelantar un programa de control, aún vigente, por la secretaria de salud municipal, el estudio nunca fue publicado. En el presente documento, se retoma y analiza la información, no solo en el sentido de presentar los índices aédicos de ese momento, sino también que a partir de los índices de asociación o repulsión entre A. aegypti y C. quinquefasciatus, establecer los parámetros de importancia de las dos especies de Culicidae dominantes en este hábitat urbano. Complementariamente, con el fin de contribuir al entendimiento de la relación entre la densidad larval y la producción de pupas de A. aegypti por manzana, se incluyen los resultados de una evaluación en un área de la ciudad con alto índice de sumideros positivos para esta especie, realizada posteriormente, entre diciembre de 1994 y enero de 1995.
Materiales y Métodos
Área de estudio. La investigación se desarrolló en 19 comunas, cubriendo los seis Sistemas Locales de Salud (SILOS) que integran el Municipio de Santiago de Cali (3°24’56”N, 76°30’10”W), Departamento del Valle del Cauca. Cada zona presenta características propias en cuanto a su panorama urbanístico y arquitectónico, generando condiciones ambientales muy variables (Arévalo 1998). Las zonas verdes de las comunas han sido arborizadas con especies ornamentales, pero algunas áreas aún conservan parte de la vegetación natural del bosque seco tropical (Arévalo 1998). En todas se presentan sumideros que por lo general proporcionan un ambiente adecuado para la cría, establecimiento y diseminación de poblaciones de A. aegypti. Asimismo, en el área de estudio se presentan casas, conjuntos residenciales y comerciales, que poseen, tanto en su interior como externamente, sitios depósitos artificiales (floreros, sanitarios, botellas, platos de materas, llantas, huecos, etc.) favorables para la cría y establecimiento de mosquitos.
Muestreo de sumideros. En cada SILOS se realizó conteo y mapeo de los sumideros. Seguidamente, de forma aleatoria, se hizo búsqueda de larvas de Culicidae en el 5% (537) de aquellos sumideros con agua. Las muestras, tomadas con un cucharón de 300 cc en las cuatro esquinas de cada sumidero, fueron depositadas en un concentrador larval, luego vertidas a un recipiente con alcohol al 80% y, finalmente, trasladadas al laboratorio de Entomología de la Universidad del Valle, donde se separaron y determinaron hasta especie. Cada muestra se acompañó de un formulario, con datos de localidad, fecha y características físicas del sumidero. En todos los casos, se cuantificó la densidad promedio de larvas por cucharón de cada especie.
Comparación de la producción de A. aegypti entre criaderos. Con el objeto de evaluar y comparar la producción de pupas de A. aegypti en diferentes tipos de criaderos, se seleccionaron diez manzanas, correspondientes a cuatro barrios del SILOS VI, área en donde se detectó la mayor frecuencia de sumideros positivos. En cada manzana se inspeccionaron todos los sumideros de las calles que la delimitaban y casi la totalidad de las viviendas. De cada casa se obtuvo el número de criaderos (positivos y negativos) en el intra y peridomicilio.De todos los criaderos positivos, incluyendo los sumideros, se extrajo la totalidad de larvas y pupas, utilizando una red de organza y cucharones. Cada muestra fue concentrada, fijada en alcohol al 70% y trasladada al laboratorio en donde se realizó la separación, determinación, y cuantificación de las larvas y pupas de A. aegypti.
Análisis numérico y estadístico. Los sumideros fueron analizados por grupos (comunas), en los cuales se determinó el índice de positividad, densidad relativa por cazo y/o sumidero. Se realizaron análisis de correlación lineal (correlación de Pearson) de asociación y de similitud para las especies de Culicidae dominantes, mediante los programas Statistical Ecology de Ludwig y Reynolds (1988) y Statistix para Windows 98, versión 2.0. Las medidas de asociación interespecíficas se estimaron a partir de datos de presencia o ausencia de las dos especies más abundantes. Este análisis mide la independencia de la distribución de las dos especies y asume que la probabilidad de ocurrencia de ellas es constante en todas las muestras.
La evaluación de la producción de pupas de A. aegypti, fueron analizados para normalidad y se calcularon los estadísticos descriptivos y las tasas de densidades encontradas entre sumideros y los criaderos para cada manzana, de acuerdo con Focks et al. (1981):

Para el promedio de todas las manzanas el divisor de la fórmula anterior fue multiplicado por el número de manzanas:

La comparación de medias entre la producción de larvas y pupas en ambas situaciones (domicilio, sumideros) se realizó mediante una prueba no paramétrica de pares ajustados de Wilcoxon. Se estimó la población absoluta de hembras de A. aegypti por manzana, a partir de sumideros y otros criaderos, mediante la fórmula de Focks et al. (1981),
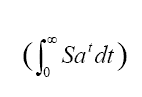
que asume una tasa de supervivencia diaria de adultos hembra constante (Sa = 0,8) e independiente de la edad (t). Ante la imposibilidad de registrar el 100% de las personas (unas pocas viviendas no pudieron ser encuestadas) no se realizó la determinación del número de pupas por persona.
Resultados y Discusión
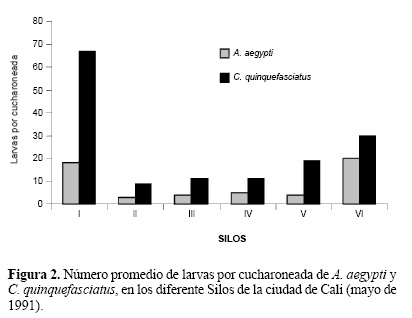
Índices de sumideros (IS) por especie. Se inspeccionaron 537 sumideros en las 19 comunas de la ciudad. En promedio, los IS fueron 57,2% para A. aegypti y 73,6% para C. quinquefasciatus, las dos especies de mosquitos dominantes. En ambas, el IS por especie varió por SILOS, Comuna y Barrio. Los mayores IS positivos, tanto para A. aegypti como C. quinquefasciatus, se presentaron en los SILOS IV y VI. No obstante, aquellos de menor porcentaje de positividad no fueron coincidentes, mientras que para la primera especie correspondió al SILO V, con 36,4%, el silo II lo fue para C. quinquefasciatus (Tabla 1). Las densidades relativas, analizadas en número promedio por cucharoneada por sumidero por comuna, variaron entre 0,2 y 44,6 pero sus valores no tuvieron correlación con los índices de positividad de cada comuna (r = 0,115, P = 0,639). Esto significa que una mayor positividad de criaderos no necesariamente implica una mayor densidad de población por área. Sin embargo, en las comunas tres, 18 y 19, que presentaron índices mayores al 40%, estuvieron asociados a densidades elevadas (Fig. 2; Tabla 2), lo cual representaba un factor de riesgo entomológico importante para la transmisión de dengue. El 84% de las comunas en estudio, presentaron una densidad promedio por debajo de siete larvas por cucharoneada por sumidero (0,2 a 6,9). Aunque en apariencia estos valores son bajos no representan la densidad absoluta por sumidero. Al realizar un análisis de agrupamiento (figura no presentada) con las densidades promedio de A. aegypti por comuna, se revela la existencia de tres grupos principales: uno de mayor densidad conformado por las comunas tres y 18 (33,06 y 44,57 larvas/cucharoneada/sumidero); la comuna 19 (15,50 L/C/S) se ubica, por separado, entre las anteriores y el resto de comunas, las cuales conformaron dos subgrupos, uno por las comunas 6, 11, 15 y 17 (densidades entre 5,12 y 7,27 L/C/S) y otro representado por el resto de comunas con densidades entre 0,20 y 3,32 L/C/S.
Los resultados sugieren que no existe un patrón fijo de distribución para la densidad larvaria, ya que está sujeta a la dinámica de los factores físicos y fisicoquímicos de cada sumidero; sin embargo, en nuestro caso su estado estuvo aparentemente relacionado con el estrato social del área residencial o tipo de actividad desarrollada en la zona. Tal como se ha establecido en otros trabajos (Tun-Lin et al. 1995a, 1995b), es plausible que factores tales como la arborización, limpieza de las vías, topografía del terreno y hábitos de las personas próximas al sumidero, influyan en la positividad y densidad larvaria de mosquitos.
Índices de asociación entre A. aegypti y C. quinquefasciatus. En casi la totalidad de las comunas de la ciudad, la densidad relativa promedio de C. quinquefasciatus fue significativamente mayor que aquellas registradas para A. aegypti (Tabla 2).
Al considerar únicamente la presencia o ausencia de cada especie en todos los sumideros evaluados, se observaron algunos criaderos que contenían sólo una de las dos especies, pero considerando la densidad relativa, los coeficientes de correlación entre las dos especies fueron positivos y estadísticamente significativos. Lo anterior sugiere una tendencia, en siete de las comunas, donde independiente del análisis comparativo de sus medias existen sumideros que presentan características ambientales igualmente buenas para ambas especies (Tabla 3).
Resultados similares se obtuvieron cuando el análisis se particularizó para cada SILOS, pero no fue aplicable al SILOS IV, ya que en este en mas del 80% de las muestras se encontraron juntos y no se encontró ningún sumidero con únicamente A. aegypti. Lo anterior corrobora la afirmación de Frager (1957, citado por Southwood 1978), quien establece que, en estos casos a pesar de que desde el punto de vista biológico la asociación es obvia, es estadísticamente indeterminada. Una situación similar se observó en el análisis por comunas (Tabla 4), en tres de ellas la asociación fue indeterminada pero muy evidente biológicamente. Aunque en el 99% de las comunas se observó un índice de asociación positivo entre las dos especies, en 12 de ellas no fue recomendable la prueba de Chi-cuadrado, ya que la frecuencia esperada en alguna de las celdas fue menor que uno y en más de dos menor que cinco (Southwood 1978).
En casi todas las comunas se presento diferencia significativa entre las medias de las dos especies por comuna, sin embargo, el análisis de los coeficientes de correlación de Pearson entre las densidades relativas mostró que solo en siete de las comunas se presentaba una correlación estadísticamente significativa, independientemente de si se observaba diferencias significativas entre sus medias; esto podría indicar una tendencia a que ciertos sumideros presenten características ambientales igualmente buenas para ambas especies. En once de las comunas restantes posiblemente las características de los sumideros no solamente fueron más favorables para C.quinquefasciatus, si no que también su densidad no estuvo correlacionada con la de A. aegypti.
Varios autores han demostrado la adaptación de C. quinquefasciatus a aguas servidas o polutas (Hammerschmidt y Fitzgerald 2005; Farah et al. 2004). Laird (1988) plantea que la presencia de ciertas bacterias, e.g. Pseudomonas, aisladas del hábitat larval de mosquitos, produce tanto atracción como estímulo para la oviposición de esta especie. Es posible que esta situación, en sumideros con mayor carga orgánica, mayor proceso de oxidación y de consumo de oxígeno moderadamente alto, condiciones favorables para C. quinquefasciatus pero desfavorables para una alta densidad larval o el establecimiento exitoso de A. aegypti se presentara en once de las comunas restantes.
Comparación en la producción de criaderos A. aegypti. El IS para A. aegypti, en las 156 casas y 62 sumideros de las 10 manzanas inspeccionadas fue alto, con valores entre 57,1 y 100%. En tres de las manzanas el 100% de los sumideros muestreados fue positivo. En contraste, los índices de viviendas (IV) y criaderos (IC) del intra y peridomicilio fueron más bajos (Tabla 5). En promedio se presentaron 2,27 criaderos domiciliares positivos por cada sumidero positivo, una relación relativamente baja con respecto a lo esperado. Cabe destacar que en el intradomicilio no se observó producción de pupas (Tabla 6) lo cual concuerda con lo expresado por Focks y Chadee (1997) y Focks et al. (1981) quienes aseveran que, algunos criaderos intradomiciliares, positivos para larvas no llegan a producir adultos, como consecuencia de la manipulación de los recipientes por parte de los habitantes del domicilio. Por el contrario, los criaderos del peridomicilio, de mayor tamaño, contribuyen de manera notable con pupas. En consecuencia las medidas de control deben estar dirigidas hacia estas fuentes principales de producción de adultos. En nuestro análisis, a pesar de que no se sumaron las densidades observadas en los criaderos del peridomicilio a la de la producción observada en los sumideros, fue evidente la mayor productividad de pupas de A. aegypti en estos últimos (Tabla 6; Fig. 3). Es posible que las frecuentes campañas educativas dirigidas a reducir los criaderos caseros hayan surtido efecto. No obstante, los sumideros permanecieron relativamente sin observación, aspecto aprovechado por la especie para colonizar exitosamente este tipo de ambientes. Según Nelson (1986) esta especie es característicamente oportunista en lo que se refiere a la búsqueda de criaderos.
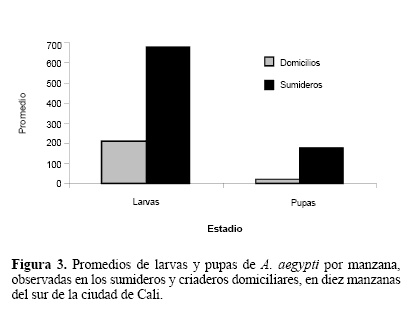
Se observó una gran variabilidad entre manzanas (Tabla 6), pero en general los promedios de larvas y pupas de los sumideros fueron significativamente mayores (P < 0,05000) que los de los criaderos domiciliares (P = 0,0125, larvas; P = 0,00506, pupas). Considerando los promedios de las tasas (sumideros/criaderos del domicilio) por manzana, para el total de las diez manzanas se produjo 30,3 pupas en los sumideros por cada pupa obtenida en los criaderos domiciliares; sin embargo, cuando se comparó la tasa con relación a la densidad total de las diez manzanas, sin considerar separadamente cada manzana, este valor fue menor (8,9), es decir que la variabilidad de los datos entre manzanas es grande. En una de las manzanas esta relación llegó a 165,0, mientras que en otra fue apenas de 2,6; en el primer caso este valor estuvo influenciado por una alta presencia de pupas (495) en los sumideros de la manzana, mientras que en el segundo caso la densidad de pupas en el domicilio (111) estuvo influenciada por la presencia de llantas en el peridomicilio. Es decir que cuando en el peridomicilio se encuentran criaderos apropiados, como llantas y tanques abandonados, la producción de A. aegypti alcanza a ser comparable a la registrada en sumideros. Según Focks y Chadee (1997) a pesar de que los índices Stegómicos (IC, IV, IB) tradicionales siguen siendo una herramienta importante en la vigilancia de muchos programas de control de dengue, son inadecuados para medir el riesgo de transmisión o la efectividad de las operaciones de control. De acuerdo con estos autores los tres índices tienen la desventaja de no considerar la cantidad variable de adultos producidos por cada criadero, algunos intradomiciliares que son encontrados con larvas no llegan a producir ningún imago, mientras que otros peridomiciliares independiente del tamaño contribuyen de manera notable con un mayor número de pupas. En el caso de A. aegypti, la producción de pupas puede ser tomada como indicador de los adultos producidos, ya que en este estado no se alimenta y en ausencia de factores externos como depredadores o parásitos su mortalidad es baja, es decir que aquellos que lleguen al estado pupal tienen una alta probabilidad de ser adultos.
Uno de los aspectos más relevantes del presente estudio es que demuestra que aunque A. aegypti se reproduce en sus ampliamente reconocidos criaderos, intra y peridomiciliares (matas en agua, floreros, sanitarios, botellas, platos de materas, llantas, huecos en árboles, etc.) también ha colonizado, en forma exitosa, los sumideros como sitio de cría y que, en ocasiones, desplaza a C. quinquefasciatus, la especie tradicionalmente dominante en estos ambientes. Este hallazgo tiene implicaciones prácticas en cuanto a la producción diaria de mosquitos de los sumideros y la toma de decisiones por parte de los organismos sanitarios del estado y la comunidad.
Basados en los presentes resultados, en las condiciones urbanas, es previsible que los sumideros aporten de manera significativa y constante al incremento de la tasa de contacto del humano con el vector. Es válido estimar que, sumideros sin tratamiento, pueden aportar entre 40 y 495 pupas/manzana (Tabla 6). Asumiendo una tasa de supervivencia diaria de hembras (Sa) de 0,8, la población absoluta por manzana aportada por los sumideros es considerablemente mayor a aquella del domicilio (Tabla 7) y, en consecuencia, la población absoluta variará entre 45 y 555 adultos por manzana, la cual produce una relación por habitante (datos no calculados) importante para que ocurra y se mantenga la transmisión de dengue en la población humana susceptible que, según Focks et al. (2000), a partir de simulaciones matemáticas (CIMSiM DENSiM), el umbral requerido de A. aegypti está entre 0,5 y 1,5 pupas por persona a 28ºC con una seroprevalencia inicial de 0 a 67%.
En conclusión, desde el punto de vista de control, a partir de los datos obtenidos sumados a otros no considerados en este estudio es posible realizar una simulación matemática para determinar el umbral de densidad de Aedes especialmente en sumideros y llantas de la ciudad de Cali y calcular, así, el grado de reducción de criaderos requerido para eliminar el umbral de transmisión de la enfermedad por cada comuna. Esto permitiría realizar un manejo selectivo del vector. Por otro lado este estudio confirma la importancia de evaluar el riesgo entomológico para dengue a partir de un índice de pupas, ya que permite valorar la importancia del criadero en términos de su capacidad de producir adultos, lo cual combinado con la información demográfica provee un estimado del número de pupas por persona de una comunidad.
Agradecimientos
A la Universidad del Valle y al Servicio de Erradicación de la Malaria (SEM), Seccional Cali en especial a su ex Directora, Dra. F. Vargas, y operarios por su gran apoyo logístico. A los señores, O. Méndez y H. Cruz, por su cooperación en la obtención de las muestras.
Literatura Citada
ARÉVALO, D. P. (ed.). 1998. Agenda Ambiental: Comunas 17, 18 y 19. Departamento Administrativo de Gestión del medio ambiente. DAGMA. Alcaldía Santiago de Cali. [ Links ]
CAMACHO, R. 1991. Situación actual del dengue en Colombia, pp. 81-95. En: Ministerio de Salud Colombia O. P. S. III reunión de investigadores de malaria y otras enfermedades tropicales. Río Negro: 150 p. [ Links ]
CHADEE, D. D 1984. An evaluation of Temephos in water drums in Trinidad, W. I. Mosquito News 44: 51-53. [ Links ]
CHADEE, D. D. 1992. Seasonal incidence and vertical distribution patterns oviposition by Aedes aegypti in an urban environment in Trinidad, W.I. Journal of the American Mosquito Control Association 8: 281-284. [ Links ]
CHADEE, D. D; WARD, R A; NOVAK, R. 1998. Natural habitats of Aedes aegypti in the Caribbean - review. Journal of the American Mosquito Control Association 14 (1): 5-11. [ Links ]
FARAH, M. A., ATEEQ, B., ALI, M. N., SABIR, R., AHMAD, W. 2004. Studies on lethal concentrations and toxicity stress of some xenobiotics on aquatic organisms. Chemosphere 55 (2): 257-265. [ Links ]
FOCKS, D. A; CHADEE, D. D. 1997. Pupal survey: An epidemiologically significant surveillance method for Aedes aegypti: An example using data from Trinidad. Journal of the American Mosquito Control Association 56: 159-167. [ Links ]
FOCKS, D. A.; SACKETT, S. R.; BAILEY, D. L.; DAME, D. A. 1981. Observations on container-breeding mosquitoes in New Orleans, Louisiana with an estimate of the population's density of Aedes aegypti (L.). American Journal of Tropical Medicine and Hygiene 30: 1329-1335. [ Links ]
FOCKS, D. A.; BRENNER, R. A.; DANIELS, E.; HAYES, J. 2000. Transmission thresholds for dengue in terms of Aedes aegypti pupae per person with discussion of their utility in source reduction efforts. American Journal of Tropical Medicine and Hygiene 62: 11-18. [ Links ]
GEERY, P. R.; HOLUB, R. E. 1989. Seasonal abundance and control of Culex spp. in catch basins in Illinois. Journal of the American Mosquito Control Association 5 (4): 537-540. [ Links ]
HAMMERSCHMIDT, C. R.; FITZGERALD, W. F. 2005. Methylmercury in mosquitoes related to atmospheric mercury deposition and contamination. Environmental Science and Technology 39 (9): 3034-3039. [ Links ]
LAIRD, M. 1988. The Natural history of larval mosquito habitats. Academic Press. Harcourt Brace Jaconovih, Publisher. N.Y. 555 p. [ Links ]
LUDWIG, J. A.; REYNOLDS, J. F. 1988. Statistical Ecology, a primer on methods and computing. John Wiley & Sons. New York. 329 p. [ Links ]
NELSON, M. J. 1986. Aedes aegypti: biology and ecology. Pan- American. Health Organization Washington, D.C. PNSP/86-63. 50 p. [ Links ]
OPS. 1987. Aedes albopictus en las Américas. Boletín Sanitaria Panamericana 102 (6): 624-33. [ Links ]
OPS. 1995. Dengue y dengue hemorrágico en las Américas: Guías para su prevención y control. Publicación Científica 548. 109 p. RAI, K. S. 1991. Aedes albopictus in the Americas. Annual Review of Entomology 36: 459-484. [ Links ] [ Links ]
SAN MARTÍN, J. L.; PRADO, M. 2004. Percepción del riesgo y estrategias de comunicación social sobre el dengue en las Américas. Revista Panamericana de la Salud Pública 15 (2): 135- 139. [ Links ]
SIVIGILA (Sistema de Vigilancia en Salud Pública). 2004. Situación epidemiológica de las enfermedades. Boletín Epidemiológico Semanal. Semana Epidemiológica No. 08 (http://www.col.opsoms.org/sivigila/IndiceBoletines2004.asp [ Links ]
SOUTHWOOD, T. R. E. 1978. Ecological Methods. Chapman & Hall, Londres. 524 p. [ Links ]
TINKER, M. E. 1974. Aedes aegypti larval habitats in Surinam. Bulletin of the Pan-American. Health Organization 8: 293-301. TRAPIDO, H.; GALINDO, P. 1956. The epidemiology of yellow fever in Middle America. Experimental Parasitology 5: 285-323. [ Links ] [ Links ]
TUN-LIN, W.; KAY, B. H.; BARNES, A. 1995a. The Premise Condition Index: a tool for streamlining surveys of Aedes aegypti. American Journal of Tropical Medicine and Hygiene 53: 591- 594. [ Links ]
TUN-LIN, W.; KAY, B. H.; BARNES, A. 1995b. Understanding productivity, a key to Aedes aegypti surveillance. American Journal of Tropical Medicine and Hygiene 53: 595-601. [ Links ]
Recibido: 31-ago-2006 - Aceptado: 22-ago-2007














