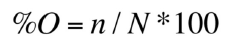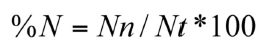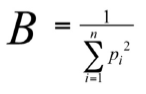Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Acta Biológica Colombiana
Print version ISSN 0120-548X
Acta biol.Colomb. vol.17 no.2 Bogotá May/Aug. 2012
ECOLOGÍA ALIMENTARIA DE LA RANA DE LLUVIA ENDÉMICA Pristimantis jubatus (CRAUGASTORIDAE) EN EL PARQUE NACIONAL NATURAL MUNCHIQUE, COLOMBIA
Feeding Ecology of the Endemic Rain Frog Pristimantis jubatus (Craugastoridae) in Munchique National Park, Colombia
JUAN CARLOS GARCÍA R.1, M.Sc.; LEONARDO LUCAS-VELÁSQUEZ2, B.Sc.; HEIBER CÁRDENAS HENAO3, M.Sc.; CARMEN ELISA POSSO GÓMEZ4, M.Sc.
1Institute of Natural Resources, Massey University, Private Bag 11-222, Palmerston North, New Zealand.
2Universidad del Valle. Calle 13 # 100-00, Cali, Colombia.
3Grupo de Estudios Ecogenéticos y de Biología Molecular, Departamento de Biología, Universidad del Valle, 25360. Cali, Colombia.
4Sección de Entomología, Departamento de Biología, Universidad del Valle, Cali. 25360, Cali, Colombia. Correspondencia: Juan Carlos García R. j.c.garciaramirez@massey.ac.nz
Presentado el 29 de junio de 2011, aceptado el 26 de noviembre de 2011, correcciones el 7 de junio de 2012.
RESUMEN
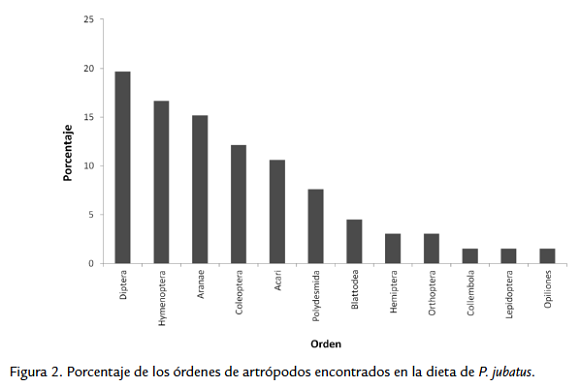
Se estudió la dieta de la rana de lluvia Pristimantis jubatus con base en los contenidos estomacales e intestinales de 29 individuos colectados en tres diferentes localidades del Parque Nacional Natural Munchique, Colombia. La dieta estuvo compuesta exclusivamente de artrópodos, identificándose un total de 66 presas correspondientes a 32 taxa. Diptera e Hymenoptera fueron los artrópodos más frecuentemente encontrados, 19,7 % y 16,7 % respectivamente, seguidos de Araneae (15,1 %) y de Coleoptera (12,1 %). Esta especie no mostró preferencia por ninguno de los tipos de presa y presentó un alto valor de amplitud de nicho (0,68), lo cual indica una dieta generalista. Adultos y juveniles forrajean en diferentes alturas de percha, encontrándose los primeros a alturas mayores que los segundos. El número de categorías encontradas y el uso del hábitat muestran a P. jubatus como una especie que puede consumir oportunamente cualquier artrópodo disponible en los estratos del bosque donde forrajea.
Palabras clave: amplitud del nicho, Colombia, dieta, Parque Nacional Natural Munchique, Pristimantis jubatus.
ABSTRACT
We studied the diet of the rain frog Pristimantis jubatus based on stomach and intestinal contents of 29 individuals from three different localities at Munchique National Park, Colombia. The diet was composed exclusively of arthropods, comprising a total of 66 prey which were in 32 taxa. The most frequent dietary items were Diptera and Hymenoptera, 19.7 % and 16.7 % respectively, followed by Araneae (15.1 %) and Coleoptera (12.1 %). Plant consumption was considered incidental because of its low frequency. This species showed no preference for any type of prey, with a high value of niche breadth (0.68) indicating a generalist diet. Adults and juveniles occupy different perch height. Habitat use and the variety of items found show P. jubatus as a species that can consume any kind of arthropod available in the strata of the forest where it is foraging.
Key words: Colombia, diet, Munchique National Park, niche breadth, Pristimantis jubatus.
INTRODUCCIÓN
La dieta es definida como el alimento consumido habitualmente por los individuos de una especie, desde un simple periodo de alimentación, hasta los periodos en los cuales la abundancia relativa disponible del alimento decrece por debajo del promedio (Westoby, 1978). La información de los hábitos alimenticios de una especie es importante para entender su historia de vida, reconocer causas posibles de fluctuaciones poblacionales, y examinar las relaciones evolutivas, ecológicas y filogenéticas entre poblaciones y clados (Anderson, 1991; Vitt y Pianka, 2005; Colston et al., 2010).
Habitualmente, el estudio de la dieta en grupos de vertebrados como los anuros es dividida en dos categorías: tamaño (longitud y/o volumen de presas) y taxa (identidad y frecuencia de las presas). Estas variables son importantes para establecer la caracterización y el patrón de presas en la alimentación (Lima y Magnusson, 1998). Generalmente, las ranas son depredadoras generalistas con comportamiento de alimentación oportunista. La mayoría de anuros adultos consumen invertebrados como anélidos, milpiés, ciempiés, crustáceos, arácnidos y principalmente insectos, aunque especies de mayor tamaño pueden depredar otros anuros, aves y pequeños mamíferos (Duellman y Trueb, 1986; Daza-Vaca y Castro-Herrera, 1999). Sin embargo, algunas especies presentan cierto grado de especialización (Simon y Toft, 1991; Toft, 1995) o incluyen porciones significativas de vegetales en su dieta (Silva et al., 1989).
Este estudio examina los contenidos estomacales e intestinales de Pristimantis jubatus (García y Lynch, 2006) para elucidar los hábitos de alimentación y la amplitud de la dieta de la especie. Los resultados obtenidos permiten conocer el papel trófico desempeñado por esta especie de anuro endémica de los bosques montanos del Parque Nacional Natural Munchique en Colombia.
MATERIALES Y MÉTODOS
ÁREA DE ESTUDIO
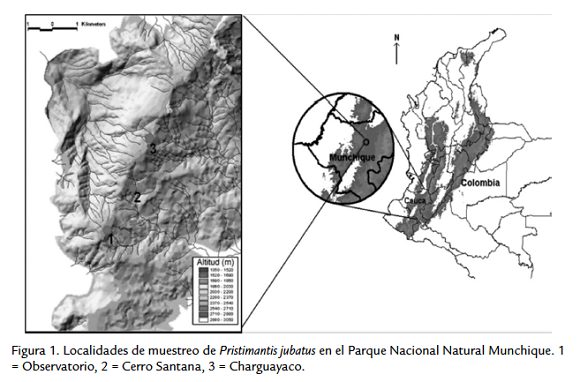
El estudio se llevó a cabo en tres localidades del sector de La Romelia, Parque Nacional Natural Munchique (2°40' Norte y 76°55' Oeste), municipio de El Tambo, departamento del Cauca, Colombia: Observatorio, Cerro Santana y Charguayaco (Fig. 1).
MUESTREO Y RECOPILACIÓN DE DATOS
Los especímenes de P. jubatus fueron colectados manualmente por medio de la inspección por encuentros visuales (Crump y Scout, 1994), entre las 19:00 y las 24:00 horas, en un periodo de 5 días consecutivos en mayo de 2008. Fueron registrados datos del uso del hábitat como la altura de percha y el sustrato en que fue encontrado cada individuo. Adicionalmente, fueron obtenidos artrópodos de la hojarasca utilizando trampas de caída para ser comparados con los encontrados en los contenidos estomacales. Las ranas fueron sacrificadas en campo en una solución de cloretone (2 mL de clorobutanol en 250 mL de agua destilada) seis a ocho horas después de su captura. Los especímenes se encuentran depositados en la colección de Herpetología de la Universidad del Valle (UVC15812-13, 15815-16, 15818, 15838, 15842, 15847, 15854, 15860, 15864-66, 15877, 15880, 15884, 15890, 15892-94, 15899, 15901-03, 15911, 15915, 15917, 15919, 15920).
Se extrajeron los tractos gastrointestinales desde la faringe hasta la porción distal del intestino grueso cerca a la apertura cloacal. Los tractos gastrointestinales fueron conservados en etanol 70 % y trasladados al laboratorio de Entomología de la Universidad del Valle para su disección. El número de presas encontradas en cada estómago fueron contadas y además, para obtener una mayor caracterización de la dieta, se examinaron las presas halladas en la región intestinal. Las presas se determinaron hasta el nivel taxonómico de orden o familia de acuerdo con las claves dicotómicas de Triplehorn y Johnson (2005) y por comparación con los especímenes colectados en campo y la colección de insectos de referencia de la Universidad del Valle (MUSENUV) - Sede Meléndez, Cali.
ANÁLISIS DE DATOS
Los artrópodos fueron separados por tamaño y tipo de categorías de acuerdo con el grupo taxonómico y estado de desarrollo. La importancia cuantitativa de cada grupo en la dieta de P. jubatus fue estimada usando la (1) frecuencia de ocurrencia (%O) y el (2) porcentaje por número (%N), así:
(1)
(2)
Donde n = número de estómagos que poseen la presa i, N = número total de estómagos analizados; Nn = número de ítems de presa del taxón n, Nt = número total de ítems de presas de todos los taxa de presa. La contribución en peso de cada presa no fue estimada por el grado de digestión, de desarticulación o del tamaño en que se encontraban. Además, fue estimado el grado de especialismo/generalismo en la dieta de P. jubatus usando el índice de amplitud de nicho trófico de Levins (1968), de acuerdo a la frecuencia (pi) de cada taxón de presa:
Este índice oscila entre uno y n (número total de taxa de presas analizado). Sin embargo, para facilitar la comparación con las dietas de otras especies, se calculó el índice estandarizado de amplitud del nicho trófico de Levins (Ba). Este índice toma valores desde 0 cuando la dieta es totalmente especialista hasta 1 cuando es totalmente generalista (Krebs, 1989):
Igualmente, fue realizada una prueba no-paramétrica de Kruskal-Wallis para evaluar las preferencias en la altura de percha entre los estados de madurez (juveniles-adultos) de los especímenes evaluados de P. jubatus.RESULTADOS
En general, de los 29 individuos analizados (seis adultos y 20 juveniles), el 90 % (26 individuos) presentó al menos una categoría de presa. Se encontraron 66 presas las cuales fueron designadas en 32 categorías de artrópodos: seis órdenes, un suborden, 24 familias, y "Otros artrópodos" (Tabla 1). Siete presas (10,6 %) fueron encontradas en los seis individuos adultos y las 59 presas restantes (89,4 %) en los 20 individuos juveniles. El 63,6 % de las presas se ubicaron en alguna de las categorías de familia, mientras el restante 36,4 % en orden, suborden u "Otros artrópodos" debido a que presentaban un grado de digestión más avanzado. Los dípteros fueron los artrópodos más abundantes (19,7 %), seguidos de los himenópteros (16,7 %), arañas (15,2 %) y coleópteros (12,1 %) (Fig. 2). Los ácaros y polydesmidos fueron los ítem de presa más frecuentemente encontrados, 20,7 % y 17,2 % respectivamente, seguidos de Acari, Cybaeidae, Carabidae, Tipulidae, Blattellidae e Hymenoptera con el 10,3 % (Tabla 1). Los componentes vegetales (ramas y semillas pequeñas) se presentaron en dos individuos pero no se incluyeron como parte de la dieta, considerando su presencia como accidental. No obstante, algunos autores sostienen que los vegetales pueden ser consumidos activamente para ayudar a eliminar parásitos intestinales y exoesqueletos de invertebrados o como complemento de nutrientes y agua (Núñez et al., 1982; Anderson et al., 1999).
Todos los órdenes de artrópodos consumidos por P. jubatus fueron encontrados en los estómagos, mientras que las presas de menor tamaño como ácaros y arañas y fragmentos digeridos de otras presas de cuerpo blando que fueron identificadas hasta orden o en las familias Salticidae y Mymaridae solo se encontraron en los intestinos. Los artrópodos de mayor tamaño y dureza como los opiliones, polidésmidos y coleópteros se hallaron solo en los estómagos y muy conservados, probablemente porque necesitan un mayor tiempo de digestión para pasar a través del intestino delgado.
El resultado del índice estandarizado de amplitud de nicho trófico considerando todas las categorías de presas (Ba = 0,68) indica un comportamiento de alimentación generalista de P. jubatus. Todos los individuos de P. jubatus fueron observados a alturas entre 0,10-1,80 m del suelo. Las alturas más frecuentemente observadas fueron entre 0,10-0,50 m, mayoritariamente ocupadas por juveniles (8 de 9 individuos registrados). Las hojas fueron el sitio preferido de percha de P. jubatus (100 %). El resultado de la prueba de Kruskal-Wallis mostró diferencia estadísticamente significativa en el uso de percha entre juveniles y adultos de P. jubatus (H1,29 = 4,47; P = 0,03).
DISCUSIÓN
Pristimantis jubatus consume una amplia variedad de presas de artrópodos, aunque con mayor frecuencia artrópodos asociados a vegetación arbustiva y arbórea, especialmente dípteros, un recurso alimenticio de gran abundancia en los bosques húmedos tropicales (Didham, 1997). Esto podría indicar que P. jubatus posee hábitos arbóreos y forrajea en este microhábitat como lo hacen la mayoría de las especies pertenecientes al género Pristimantis (Taigen et al., 1982; Lynch y Duellman, 1997; Parmelee, 1999).
En las ranas de hábitos arbóreos, el sistema de forrajeo de sentarse y esperar y la actividad nocturna son comunes (Menéndez-Guerrero, 2001; Guayasamin et al., 2004; Santos et al., 2004) permitiendo capturar presas de forma que se reduzca el peligro de depredación (Toft, 1985). Este sistema de caza pasivo es ideal para capturar presas móviles, lo que explica la alta frecuencia de ácaros (Acari), de miriápodos (Polydesmida) y de arañas (Cybaedae) en la dieta de P. jubatus. Sin embargo, en la dieta de esta especie fueron encontrados artrópodos de hábitos terrestres y menos móviles como colémbolos y opiliones (García-Gómez et al., 2011; Johnson y Catley, 2005), entre otros.
El índice estandarizado de amplitud de nicho trófico y el número de categorías de presas encontradas en la dieta de P. jubatus demuestran que esta especie puede consumir oportunamente cualquier artrópodo disponible en los estratos del bosque donde forrajea. El uso diferencial de estratos en individuos adultos y juveniles de P. jubatus es consistente con los resultados de uso de microhábitat reportados por García et al. (2005) y García y Lynch (2006), quienes encontraron que la mayoría de adultos prefieren las alturas de 1,2 a 2 m, mientras que los juveniles prefieren alturas menores de 80 cm, posiblemente para evitar competencia por recursos al alimentarse en estratos diferentes.
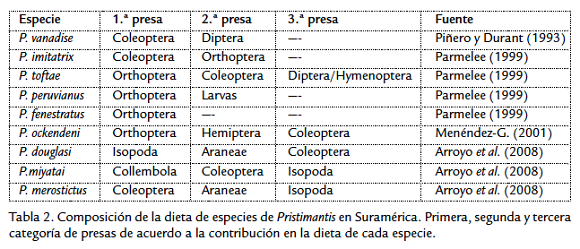
Otras ranas del género Pristimantis estudiadas en Suramérica, (Tabla 2), han registrado igualmente un amplio número de taxa consumidas (entre 16 y 22). No obstante, el número de presas reportadas por individuo es pequeño (2 a 3) y predomina la presencia de coleópteros e himenópteros en sus dietas. De acuerdo con Alonso et al., (2001) ingerir menos presas por unidad de tiempo es una estrategia para ahorrar energía en la búsqueda de alimento, aunque debe tenerse en cuenta que la presencia y abundancia de las presas pueden variar según la altitud y el tipo de vegetación predominante en cada sitio. Por ejemplo, Ovaska (1991) y Ortega et al. (2005) encontraron predominancia de Formicidae en la dieta de Eleutherodactylus johnstonei en localidades de menor altitud (1.000-1.100 m), mientras que otras especies de desarrollo directo estudiadas en bosques de niebla a alturas superiores presentaron un mayor consumo de colémbolos, coleópteros e isópodos (Gutiérrez, 2003; Arroyo et al., 2008).
De acuerdo a Parmelee (1999), las hormigas son un componente importante en la dieta de varias especies de Pristimantis de tierras bajas en la amazonía, pero su contribución en la dieta de P. jubatus fue muy baja. Posiblemente, este resultado se debe a que la densidad de hormigas puede descender en los bosques montanos en comparación con los bosques de tierras bajas, porque la disminución de la temperatura afecta a las hormigas en la obtención eficiente de su alimento y desarrollo de sus larvas. Otra posible explicación al pequeño aporte de las hormigas en la dieta de las especies montanas de desarrollo directo podría encontrarse en que la base de sus recursos alimenticios es demasiado baja para que puedan coexistir grandes poblaciones de los homópteros asociados (Basset, 2001).
En conclusión, P. jubatus presenta una dieta generalista, con un rango amplio de categorías de presas que incluyen insectos en su mayoría, pero también arácnidos y miriápodos. La existencia de presas de hábitos terrestres en la dieta de esta especie indica que el uso de microhábitat arbustivo o arbóreo no es exclusivo en su comportamiento de alimentación, sino que puede utilizar y alternar diferentes estratos del bosque. Finalmente, consideramos que la dificultad en la identificación de los artrópodos hasta el nivel de familia (o niveles inferiores) se debe al tiempo de digestión transcurrido entre la captura y el sacrificio de las ranas (6-8 horas). Esto podría ocasionar pérdida de información y subestimación de la variedad de presas consumidas, porque varios autores han demostrado que la precisión y amplitud en la descripción de la dieta es inversamente proporcional al tiempo transcurrido desde la captura de las ranas hasta el momento de su sacrificio (Caldwell, 1996; Menéndez-Guerrero, 2001).
AGRADECIMIENTOS
Agradecemos a Isaac Bedoya, a Huber Pino y al Sistema de Parques Nacionales Naturales del Ministerio de Ambiente, Vivienda y Desarrollo Territorial de Colombia por su colaboración y permisos para realizar el estudio en el PNN Munchique. A la Universidad del Valle por la financiación del proyecto (Convocatoria Interna Proyecto n.° 746), a la Sección de Entomología por el acceso a la colección y el apoyo en la identificación de invertebrados. A Sylvia Weil y a dos evaluadores anónimos por sus interesantes y útiles comentarios para el mejoramiento del manuscrito.
BIBLIOGRAFÍA
ALONSO R, RODRÍGUEZ-GÓMEZ A, ESTRADA AR. Patrones de actividad acústica y trófica de machos cantores de Eleutherodactylus eileenae (Anura: Leptodactylidae). Rev Esp Herpetol. 2001;15:45-52. [ Links ]
ANDERSON SH. Managing our Wildlife Resources. Merrill Publishing Co., Columbus, OH; 1991. [ Links ]
ANDERSON A, HAUKOS D, ANDERSON J. Diet composition of three anurans from the Playa wetlands of northwest Texas. Copeia. 1999;515-520. [ Links ]
ARROYO SB, SERRANO-CARDOZO VH, RAMÍREZ-PINILLA MP. Diet, microhabitat and time of activity in a Pristimantis (Anura, Strabomantidae) assemblage. Phyllomedusa. 2008;7:109-119. [ Links ]
BASSET Y. Invertebrates in the canopy of tropical rain forests: how much do we really know? Plant Ecol. 2001;153:87-107. [ Links ]
CALDWELL JP. The evolution of myrmecophagy and its correlates in poison frogs (Family Dendrobatidae). J Zool (Lond). 1996;240:75-101. [ Links ]
COLSTON TJ, COSTA GC, VITT LJ. Snake diets and the deep history hypothesis. Biol J Linn Soc. 2010;101:476-486. [ Links ]
CRUMP ML, SCOTT NJ JR. Visual Encounter Surveys. En: Heyer WR, Donnelly MA, McDiarmid RW, Hayek LC, Foster MS, editors. Measuring and monitoring biological diversity: standard methods for amphibians. Washington: Smithsonian Institution Press; 1994. p. 84-92. [ Links ]
DAZA-VACA JD, CASTRO-HERRERA F. Hábitos alimenticios de la rana toro (Rana catesbeiana) Anura: Ranidae, en el Valle del Cauca, Colombia. Rev Acad Colomb Cienc Exactas Fís Nat. 1999;23:265-274. [ Links ]
DIDHAM RK. Dipteran tree-crown assemblages in a diverse southern temperate rain forest. En: Stork NE, Adis J, Didham RK, editors. Canopy arthropods. London: Chapman y Hall; 1997. p. 320-343. [ Links ]
DUELLMAN WE, TRUEB L. The biology of amphibians. New York: McGraw-Hill; 1986. [ Links ]
GARCIA-GOMEZ A, CASTANO-MENESES G, PALACIOS-VARGAS J. Distribu- ción y diversidad de colémbolos (Hexapoda: Collembola) en el gradiente altitudinal de un bosque templado en México, Rev Biol Trop. 2011;59(1):315-327. [ Links ]
GARCÍA-R JC, CASTRO F, CÁRDENAS H. Relación entre la distribución de anuros y variables del hábitat en el sector La Romelia del Parque Nacional Natural Munchique (Cauca, Colombia), Caldasia. 2005;27:299-310. [ Links ]
GARCÍA JC, LYNCH JD. A new species of frog (genus Eleutherodactylus) from a cloud forest in Western Colombia. Zootaxa. 2006;1171:39-45. [ Links ]
GUAYASAMIN JM, BONACCORSO E, MENÉNDEZ PA, BUSTAMANTE MR. Morphological variation, diet, and vocalization of Eleutherodactylus eugeniae (Anura: Leptodactylidae) with notes on its reproduction and ecology. Herpetol Rev. 2004;35(1):17-23. [ Links ]
GUTIÉRREZ DL. Composición, dieta, microhábitat y horas de actividad de los anuros presentes en dos tipos de bosque dentro del santuario de Fauna y Flora Guanentá, Alto Río Fonce [tesis de pregrado]. Santander: Escuela de Biología, Universidad Industrial de Santander; 2003. [ Links ]
JOHNSON E, CATLEY K. La vida en la hojarasca. New York: American Museum of Natural History; 2005. [ Links ]
KREBS CJ. Ecological methodology. New York: Harper y Rows Publishers; 1989. [ Links ]
LEVINS R. Evolution in changing environments. Princeton: Princeton University Press; 1968. [ Links ]
LIMA AP, MAGNUSSON WE. Partitioning seasonal time: interactions among size, foraging activity and diet in leaf-litter frogs. Oecologia. 1998;116:259-266. [ Links ]
LYNCH JD, DUELLMAN WE. Frogs of the genus Eleutherodactylus (Leptodactylidae) in Western Ecuador: Systematic, ecology and biogeography. Lawrence: The University of Kansas Natural History Museum; 1997. [ Links ]
MENÉNDEZ-GUERRERO PA. Ecología trófica de la diversidad de anuros del Parque Nacional Yasuní en la Amazonía Ecuatoriana [tesis de pregrado]. Quito: Facultad de Ciencias Exactas y Naturales, Pontificia Universidad Católica del Ecuador; 2001. [ Links ]
NÚÑEZ H, LABRA MA, NÚÑEZ J. Hábitos alimentarios de dos poblaciones andinas de Bufo spinulosus Wiegmann, 1985 (Anura: Bufonidae). Bol Mus Nac Hist Nat (Santiago). 1982;39:81-91. [ Links ]
ORTEGA JE, SERRANO VH, RAMÍREZ-PINILLA MP. Diet composition and microhabitat of Eleutherodactylus johnstonei in an introduced population at Bucaramanga City, Colombia. Herpetol Rev. 2005;36(3):238-241. [ Links ]
OVASKA K. Diet of the frog Eleutherodactylus johnstonei (Leptodactylidae) in Barbados, West Indies. J Herpetol. 1991;25(4):486-488. [ Links ]
PARMELEE JR. Trophic ecology of a tropical anuran assemblage. Sci Pap Nat Hist Mus Univ Kansas. 1999;11:1-59. [ Links ]
PIÑERO J, DURANT P. Dieta y hábitat de una comunidad de anuros de selva nublada en los Andes merideños. Ecotropicos. 1993;6(2):1-9. [ Links ]
SANTOS EM, ALMEIDA AV, VASCONCELOS SD. Feeding habits of six anuran (Amphibia: Anura) species in a rainforest fragment in Northeastern Brazil. Iheringia Ser Zool. 2004;94(4):433-438. [ Links ]
SILVA HR, BRITTO-PEREIRA MC, CARAMASCHI U. Frugivory and seed dispersal by Hyla truncata, a Neotropical tree-frog. Copeia. 1989;1989:785-794. [ Links ]
SIMON MP, TOFT CA. Diet specialization in small vertebrates: mite-eating in frogs. Oikos. 1991;61:263-278. [ Links ]
TAIGEN TL, EMERSON SB, POUGH FH. Ecological correlates of anuran exercise physiology. Oecologia. 1982;52:49-56. [ Links ]
TOFT CA. Resource partitioning in amphibians and reptiles. Copeia. 1985;1985:1-21. [ Links ]
TOFT CA. Evolution of diet specialization in poison-dart frogs (Dendrobatidae). Herpetologica. 1995;51:202-216. [ Links ]
TRIPLEHORN CA, JOHNSON NF. Borror and DeLong's introduction to the study of insects. 7 ed. USA: Thomson Brooks/Cole; 2005. [ Links ]
VITT LJ, PIANKA ER. Deep history impacts present-day ecology and biodiversity. Proc Natl Acad Sci USA. 2005;102:7877-7881. [ Links ]
WESTOBY M. What are the biological bases of varied diets? Am Nat. 1978;112:627-631. [ Links ]