Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Revista Colombiana de Química
Print version ISSN 0120-2804On-line version ISSN 2357-3791
Rev.Colomb.Quim. vol.40 no.1 Bogotá Jan./Apr. 2011
FLAVONOIDES CON ACTIVIDAD ANTIFÚNGICA AISLADOS DE Piper septuplinervium (Miq.) C. DC. (Piperaceae)
ANTIFUNGAL FLAVONOIDS ISOLATED FROM Piper septuplinervium (Miq.) C. DC (Piperaceae)
FLAVONÓIDES COM ATIVIDADE ANTIFÚNGICA ISOLADOS DE Piper septuplinervium (Miq.) C. DC (Piperaceae)
Mónica C. Ávila1,2, Óscar J. Patino1, Juliet A. Prieto1, Wilman A. Delgado1, Luis E. Cuca1
1 Departamento de Química, Facultad de Ciencias, Universidad Nacional de Colombia, Sede Bogotá. Bogotá, Colombia.
Recibido: 29/03/11 - Aceptado: 29/04/11
RESUMEN
El fraccionamiento bioguiado del extracto etanólico de la parte aérea de Piper septuplinervium (Piperaceae) permitió la obtención de dos substancias de tipo flavonoide, activas contra dos cepas de hongos fitopatógenos (Fusarium oxysporum f. sp. dianthiyBotrytis cinerea). Las estructuras de los compuestos aislados fueron determinadas de acuerdo con el análisis espectroscópico (RMN uni y bidimensional, EMAR). La actividad anti-fúngica fue determinada por ensayo en disco, seguido por bioautografía directa sobre las dos cepas de hongos en prueba.
Palabras clave: Piper septuplinervium, Piperaceae, flavonoides, actividad antifúngica.
ABSTRACT
Guided fractionation of ethanolic extract of aerial part of Piper septuplinervium (Piperaceae) yielded two flavonoid-type active substances against two strains of phytopathogenic fungi (Fusarium oxysporum f. sp. dianthi and Botrytis cinerea). The structures of isolated compounds were determined by spectroscopic analysis (single-and two-dimensional NMR, HRMS). The antifungal activity was determined by disk test, followed by direct bioautography against the two strains of fungi tested.
KeyWords: Piper septuplinervium,Piperaceae, flavonoids, antifungal activity.
RESUMO
O fracionamento bio-guiado do extrato etanólico da parte aérea de Piper septuplinervium (Piperaceae) permitiuobter duas substâncias flavonóidesativas contra duas linhagens de fungos patogênicos (Fusarium oxysporum f. sp. Dianthi e Botrytis cinerea). Mediante a análise espectroscópica (RMN mono e bidimensional, RMS) determinaram-se as estruturas desses compostos. A atividade antifúngica foi determinada pelo teste de disco, seguido por bio-autografia direta sobre duas inhagens fúngicas testadas.
Palavras-chave: Piper septuplinervium, Piperaceae, flavonóides, atividade antifúngica.
INTRODUCCIÓN
La agricultura en Colombia representa un renglón importante en la economía del país, teniendo en cuenta que esta contribuye con un 20% al producto interno bruto (1). Según el Ministerio de Comercio, Industria y Turismo del país, de los 20 productos más exportados por Colombia, 13 son productos agrícolas, entre los que se destacan el café, diversos tipos de frutas y las flores (2).
Varios problemas fitosanitarios afectan los cultivos, como el ataque de patógenos que disminuyen notablemente tanto la calidad como la cantidad de la producción. Las pérdidas en las cosechas debidas a enfermedades fúngicas pueden estar cercanas al 12% en el mejor de los casos; los países en desarrollo pueden superar este valor (3).
Para el control de los hongos fitopatógenos se emplean fungicidas sintéticos, muchos de los cuales son altamente tóxicos tanto para los agricultores como para los consumidores y el ambiente. Por tal motivo, se están buscando alternativas para disminuir al máximo el uso de estas sustancias tóxicas, mediante el desarrollo de nuevos productos fitosanitarios de bajo impacto ambiental y de acción específica (4). Las plantas pueden ser una fuente para encontrar sustancias útiles en el sector agrícola, pues producen diversos metabolitos secundarios como defensa química y han sido usadas empíricamente por el hombre como agentes de protección de cultivos desde hace muchos años (5). Ejemplo de esto son las especies vegetales pertenecientes a la familia Piperaceae, ampliamente utilizadas de manera tradicional en la protección de cultivos y como fuente de fitomedicamentos (6). El género Piper, perteneciente a la familia Piperaceae, es el más abundante con un total de 1000 especies; a pesar de su origen asiático, en el país existe cerca del 20% del total de especies del género Piper reportadas en el mundo (7), muchas de las cuales son especies endémicas colombianas, como la especie Piper septuplinervium, objeto del presente estudio.
Además de la importancia que revisten las especies del género Piper por sus usos tradicionales, son relevantes los estudios fitoquímicos los cuales han mostrado la presencia de metabolitos secundarios como amidas, flavonoides, derivados de ácido benzoico y fenil propanoides principalmente (8), los que en su mayoría poseen actividades insecticidas y antifúngicas comprobadas (9-12). En este trabajo se presenta el aislamiento bioguiado de dos metabolitos tipo flavonoide con actividad antifúngica contra dos cepas de hongos fitopatógenos: Fusarium oxysporum f sp. dianthi, responsable del marchitamiento vascular del clavel, y Botrytis cinerea responsable de la enfermedad conocida como moho gris característica de hortalizas y frutas que comúnmente se manifiesta como tizones en las inflorescencias, pudrición de los frutos, así como cancrosis o pudriciones de los tallos (13). Las cepas escogidas para este estudio poseen una importancia económica teniendo en cuenta que los productos agrícolas que se ven afectados por estos hongos son de importancia económica para nuestro país ya que tanto el clavel como las frutas y hortalizas son actualmente productos de exportación y generan importantes dividendos económicos.
MATERIALES Y MÉTODOS General
En la cromatografía de columna flash se usó sílica gel 60 de 0,040 mm a 0,063 mm Merck®, para la cromatografía en capa delgada se emplearon cromatoplacas Merck® de sílica gel HF254 de 0,3 mm de espesor usando como reveladores luz UV de 254 nm, 365 nm, vapores de I2 y vainillina-acido fosfórico 50%. Los espectros RMN 'H, RMN 13C, COSY, DEPT, HMQC, HMBC, fueron registrados en un equipo Brucker Avance 400 utilizando TMS como estándar interno. Los puntos de fusión fueron tomados en un equipo Mel-temp II Laboratory Devices. Los espectros de masas EMAR fueron tomados en el equipo LCMS-IT-TOF Shimadzu DGU-20AS.
Material vegetai
La muestra utilizada para este estudio corresponde a la parte aérea de la especie Piper septuplinervium (Piperaceae), recolectada en la vereda San José Bajo del municipio de Granada (Cundinamarca) y determinada por el biólogo Adolfo Jara Muñoz. Un espécimen reposa en el Herbario Nacional Colombiano del Instituto de Ciencias Naturales con el número COL-517695.
Material biològico
Las cepas fúngicas empleadas en el ensayo corresponden a F. oxysporum f. sp. dianthi y B. cinerea. Todas las cepas fueron mantenidas en incubadora a 27 ± 1 °C en medio de papa-dextrosa-agar (PDA).
Ensayo de actividad antifúngica
La determinación de la actividad antifúngica del extracto se realizó por el método de difusión en disco (14). El medio de cultivo (PDA) fue inoculado con 100 µL de una suspensión de esporas de 105 UFC en una caja de Petri de 9 mm de diámetro. Se prepararon soluciones en metanol de cada extracto en diferentes concentraciones (50,40,25 y 10µg/µL) y se aplicaron 10 µL de cada solución sobre discos de papel filtro, colocados sobre el medio inoculado, correspondiendo a 500, 400, 250 y 100 µg de cada extracto aplicado. Las cajas de Petri fueron selladas con parafilm e incubadas por tres días a 28 °C. Posteriormente, se midió el halo de inhibición alrededor de los discos de papel en mm y se determinó la CMI de cada extracto, definida como la mínima cantidad de extracto que causa inhibición en el crecimiento del hongo. Cada ensayo se realizó por triplicado y se usaron Benomil e Iprodiona como controles positivos para las cepas de F. oxysporum ydeB. cinerea, respectivamente, en cantidad mínima de 10 µg en ambos casos.
La determinación de la actividad antifúngica de las fracciones y los compuestos puros se realizó por el método de bioautografía directa (15). Diez microlitros de las soluciones de las fracciones y los compuestos puros se prepararon, en diferentes concentraciones correspondientes a 100, 50, 25, 10, 5, 2 y 1 ugde compuestospuros, y300ugdefracciones aplicados. Las muestras se aplicaron a las placas de TLC y se eluyeron en los sistemas cloroformo-metanol (95:5) y n-hexano-AcOEt (8:2). Después de dejar secar los cromatogramas para eliminar totalmente el solvente, se procedió a asperjarlos con una suspensión de esporas de hongos en solución de caldo nutritivo de KH2PO4 0,7%, Na2HPO4. 2H2O 0,3%, KNO3 0,4%, MgSO4.7H2O 0,1%, NaCl 0,1% y glucosa 30%; posteriormente, las placas se incubaron durante 72 horas en la oscuridad en una cámara húmeda a 25 °C. Finalmente, las placas de TLC se expusieron a la luz UV (254 nm) y a los vapores de yodo para detectar las zonas de inhibición, lo que indica la actividad inhibitoria contra el crecimiento del hongo. Se utilizó Benomil e Iprodiona como control positivo a una cantidad de 1 µg enambos casos; los disolventes utilizados para las muestras se emplearon como controles negativos.
Extracción y aislamiento
La parte aérea de Piper septuplinervium seca y molida (980 g) fue sometida a extracción por percolación con etanol al 96%, obteniéndose 70 gramos de extracto, fraccionado por cromatografía en columna flash con la mezcla tolueno-acetato de isopropilo en gradiente desde 9:1 hasta 1:9 y posterior lavado con metanol, obteniendo 18 fracciones totales marcadas como F1 a F18. Las fracciones activas, de acuerdo con la bioautografía en cromatografía en capa delgada sobre sílica gel, fueron purificadas por medio de cromatografía en columna flash sucesiva con las mezclas hexano-acetona y diclorometa-no-acetona en diferentes proporciones, obteniendo los compuestos 1 (512 mg), 2 (150 mg).
RESULTADOS Y DISCUSIÓN
El compuesto 1 es un sólido blanco que cristaliza en forma de agujas, pf: 189-190 °C, no posee absorción en el UV λ365 nm, presenta coloración amarilla con vainillina-ácido fosfórico, y coloración negra con vapores de I2, da prueba positiva al reactivo de FeCl3 indicando la presencia de OH fenólico. El espectro RMN 1H (400 MHz, Me2CO-d6) muestra la presencia de las señales en δ7,27 (d, J=7,3 Hz, 4H) y δ7,17 (m, 1H), características de los hidrógenos de un anillo aromático monosustituido. Las señales de los protonesen δ6,03 (d, J = 2,1Hz, 1H) y δ5,97 (d, J=2,1, 1H) son características de un anillo aromático tetrasustituido cuyos hidrógenos se encuentran en posición meta. La presencia de los dos anillos aromáticos se confirma por las señales del espectro de RMN 13C (100 MHz, Me2COd) en δ92,9, δ97,9, δ106,8, δ127,6, δ130,1, δ130,2, δ143,7, δ165,5, δ166,6, δ169,5, las cuales corresponden a desplazamientos típicos de carbonos sp2, en especial carbonos aromáticos que, según el experimento DEPT 135 y en comparación con el espectro RMN 13C, corresponden a 7 metinos y 5 carbonos cuaternarios, los tres últimos carbonos cuyo desplazamiento químico se debe a la presencia de sustituyentes oxigenados. Es importante anotar que dos de las señales demetinos en δ130,1 y δ130,2poseen el doble de la intensidad de las demás, con lo cual se concluye que cada una corresponde a dos carbonos que deben ser equivalentes (16). Las señales en δ32,4 y δ47,4, las cuales según el espectro HMQC se correlacionan con las señales en δ2,95 (t, J = 7,7, 2H) y δ3,3 (t, J = 7,7, 2H), respectivamente, junto con la señal en δ206 correspondiente a un carbono carbonílico cetónico, son características de un sistema de carbonilo; los protones α y β de una estructura tipo dihidrochalcona (17a).
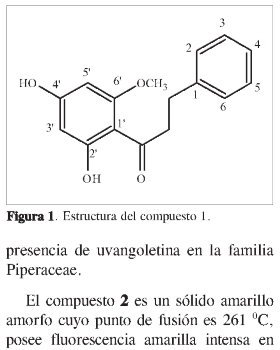
La señal en δ14,9 (s, 1H) es característica de un hidrógeno quelatado con un grupo carbonilo, lo cual es común en sistemas flavonoides y confirma la presencia de OH fenólico. Finalmente, los acoplamientos a larga distancia presentados en el experimento HMBC entre la señal en δ3,3 y δ2,95 a dos y tres enlaces con la señal en δ143, así como entre la señal de δ3,3 y δ2,95 a dos y tres enlaces con la señal en δ206 permiten hacer la conexión entre los fragmentos e identificar el compuesto 1 como 2', 4'- dihidroxi-6'-metoxi-dihidrochalcona, comúnmente conocida como uvangoletina, aislada de especies de las familias Anonacea (18), Ptaeroxylaceae (19), y Zingiberaceae (20) En la Figura 1 se presenta la estructura de la uvangoletina.
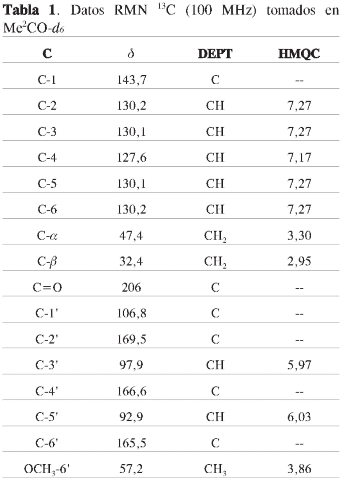
A pesar de que este compuesto ha sido reportado anteriormente, los datos espectroscópicos reportados corresponden a experimentos RMN 13C de 15 MHz (21); por tanto, en la Tabla 1 se reportan los datos espectroscópicos correspondientes a 13C 100 MHz. Este es el primer reporte de la UV λ365 nm, coloración naranja intensa al revelarse con vainillina-ácido fosfórico, y coloración amarilla con vapores de I2. Presenta prueba positiva con el reactivo de FeCl3 indicando la presencia de OH fenólico. La asignación por resonancia magnética nuclear (1H, 13C, DEPT, COSY, HMQC,HMBC),EMAR, y la comparación con los datos reportados en la literatura (17b) permitieron identificar el compuesto 2 como 5,7-dihidroxi-flavona, comúnmente conocida como chrysina, aislada anteriormente de especies de las familias Lamiaceae (22), Fabaceae (23), Chenopodiaceae (24), Orchidaceae (25).
Uvangoletina y chrysina son objeto de investigación continua por su importante y comprobada actividad citotóxica sobre varias líneas celulares. Además, se ha comprobado la actividad antifúngica in vitro de la chrysina sobre cinco cepas de hongos, entre las cuales se encuentra la forma especial cepae del hongo Fusarium oxysporum, la cual ataca específicamente cultivos de ajo y cebolla (25). En esta investigación, mediante el aislamiento bioguiado del extracto etanólico de la parte aérea de Piper septuplinervium, se evidenció la importante actividad antifúngica contra Fusarium oxysporum f. sp. dianthi y Botrytis cinerea de los anteriores compuestos de tipo flavonoide, representada en los valores determinados en la cantidad mínima inhibitoria, los cuales se presentan en las Tablas 2 y 3.
La Tabla 2 evidencia la cantidad mínima inhibitoria del extracto de Piper septuplinervium, comparada con los controles utilizados para el ensayo, que corresponden a los principios activos de fungicidas comerciales comúnmente utilizados en el tratamiento en campo de las enfermedades causadas por las cepas de hongos objeto de esta investigación. Si bien las cantidades mínimas inhibitorias de los controles no son comparables con la obtenida para el extracto. Es importante tener en cuenta que los controles usados en el ensayo son compuestos puros y los extractos vegetales son mezclas muy complejas de cientos de compuestos en diversas cantidades; por eso se ensayan concentraciones relativamente altas de forma que es bastante posible que los metabolitos causantes de la actividad ejerzan su efecto en cantidades muy pequeñas. Lo anterior se confirma con los resultados de la Tabla 3, pues a diferencia de lo que sucede con el extracto, las cantidades mínimas inhibitorias presentadas por uvangoletina (1) y chrysina (2) son comparables con los controles positivos usados en el ensayo. Es de destacar que los compuestos aislados tienen mayor efecto sobre la Fusarium oxysporum f. sp. dianthi, lo cual es un resultado bastante importante, considerando que las mayores pérdidas de los productores de clavel se deben al marchitamiento vascular de los esquejes, causado por Fusarium oxysporum f. sp. dianthi. Esta situación repercute enormemente en las divisas por exportaciones si se tiene en cuenta que Colombia es el segundo exportador mundial después de Holanda. (26)
AGRADECIMIENTOS
Los autores agradecemos:
Al Laboratorio de investigación hospedero-patógeno del Departamento de Química de la Universidad Nacional de Colombia y al Laboratorio de Bromatología y Fitoquímica del Jardín Botánico José Celestino Mutis de la ciudad de Bogotá por proporcionar el material biológico usado en esta investigación.
Al Herbario Nacional Colombiano de la Universidad Nacional de Colombiapor la determinación de las especies vegetales utilizadas en la presente investigación.
A los laboratorios de Resonancia Magnética Nuclear y Cromatografía liquida-espectrometría de masas del Departamento de Química de la Universidad Nacional de Colombia por la toma de los espectros utilizados en la elucidación estructural.
REFERENCIAS BIBLIOGRÁFICAS
1. Ministerio de Agricultura y Desarrollo Rural. Colombia. Análisis Macroeconomico del Sector Agropecuario en Colombia, 2007. [Consultado en abril de 2011].Disponible en: http://www.minagricultura.gov.co/documentos/macroeconomica_25sep07.ppt. [Consulta, abril de 2011]. [ Links ]
2. Ministerio de Comercio, Industria y Turismo. Colombia. Comercio exterior de Colombia 2010. [Consultado en abril de 2011]. Disponible en: http://www.mincomercio.gov.co/econtent/documentos/estudioseconomicos/2010-expopresentacionjulio.pdf. [ Links ]
3. Bajpai, V.; Shukla, S.; Kang, S. Chemical composition and antifungal activity of essential oil and various extract of Silene armeria L. Bioresource Technology. 2008. 99: 8903-8908. [ Links ]
4. Lizarazo, K.; Mendoza, C.; Carrero, R. Efecto de extractos vegetales de Polygonum hydropiperoides, Solanum nigrum y Caliandra pittieri sobre el gusano cogollero (Spodoptera frugiperda). Agronomía Colombiana. 2008. 26(3): 427-434. [ Links ]
5. Abad, M. J.; Ansuategui, M.; Bermejo P. Active antifungal substances from natural sources. Arkivoc. 2007. 8: 116-145. [ Links ]
6. Regnault-Roger, C.; Philogene, B.; Vincent, C. Biopesticides d'origine vegetale. Tec&Doc-Lavoisier. Paris. 2003. p. 46. [ Links ]
7. Garcia Barriga, H. Flora medicinal de Colombia. Tercer Mundo Editores. Bogotá. 1992. p. 222. [ Links ]
8. Parmar, V.; Jain, S.; Bisht, K.; Jain R.; Taneja, P.; Jha, A.; Tyagi, O.; Prasad, A.; Wengel J.; Olsen C.; Boll P. Phytochemistry of genus Piper. Phytochemistry. 1997.46: 567-673. [ Links ]
9. Steenkamp, V.; Fernandes, A. C.; Van Rensburg, C. E. J.; Screening of Venda medicinal plants for antifungal activity against Candida albicans. South African Journal of Botany. 2005. 73: 248-256. [ Links ]
10. Nyane, A.; Biyiti, L.; Bouchet, P.; Nkengfack, A.; Zollo, A. Antifungal activity of Piper guineense of Cameroon. Fitoterapia. 2003. 74: 464-468. [ Links ]
11. Lago, H.; Ramos, C.; Casanova, D.; Morandi, A.; Bergamo, D.; Cavalheiro, A.; Bolzani, V.; Furlan, M.; Guimaraez, E.; Young, M.; Kato, M. Benzoic acids derivates from Piper species and their fungitoxic activity against Cladosporium cladosporoides and Cladosporium sphaerospermun. Journal ofNatural Products. 2004. 67: 1783-1788. [ Links ]
12. Danelutte, A.; Lago, J.; Young, M.; Kato, M. Antifungal flavones and prenylated hydroquinones from Piper crassinervium Kunth. Phytochemistry. 2003. 64: 555-559. [ Links ]
13. Agrios, G. Plant pathology. Elsevier Academic Press. USA. 2005. Pp. 126-127. [ Links ]
14. Pabón, L.; Cuca, L. Aporphine alkaloids from Ocotea macrophylla (Lauraceae). Química Nova. 2010. 33(4): 875-879. [ Links ]
15. Patino, O.; Cuca, L. Chemicalconstituents of the wood from Zanthoxylum quinduense Tul (Rutaceae). Química Nova. 2010. 33 (5): 1019-1021. [ Links ]
16. Crews, P.; Rodríguez, J.; Jaspars, M. Organic structures analysis. Oxford University Press. New York. 2010. p. 74. [ Links ]
17a.Harborne; J. B. The flavonoids. Advances in research since 1986. Chapman and Hall. London. 1994. p. 401. [ Links ]
17b.Harborne; J. B. The flavonoids. Advances in research since 1986. Chapman and Hall. London. 1994. p. 261. [ Links ]
18. Ichimaru, M.; Nakatani, N.; Takahashi, T.; Nishiyama, Y.; Moriyasu, M.; Kato, A.; Mathenge, S.; Juma, F.; Nganga, J. Citotoxyc C-benzilated Dihydrochalcones from Uvaria acuminata. Chemical and Pharmaceutical Bulletin. 2004. 52(1): 138-141. [ Links ]
19. Koorbanally, N.; Randrianarivelojosia, M.; Mulholland, D.; Ufford, L.; Van den Berg, A. Chalcones from the seed of Cedrepolis grevei (Ptaeroxylaceae). Phytochemistry. 2003. 62(8): 1225-1229. [ Links ]
20. Subhadhirasakul, S.; Karalai, C.; Ponglimanont, C.; Pracha, S. Anti-inflammatory effects of compounds from Kaempferia parviflora and Boesenbergia pandurata. Food Chemistry. 20098. 115(2): 534-536. [ Links ]
21. Hufford, H. Oguntimein, B. Dihydrochalcones from Uvaria angolensis. Phytochemistry. 1980. 19(9): 2036-2038. [ Links ]
22. Tomimori, T.; Miyaiachi, Y.; Imoto, Y.; Kizu, H.; Namba, T. Studies on the Nepalese crude drugs. XI: On the flavonoid constituents of the aerial parts of Scutellaria discolor. Chemical and Pharmaceutical Bulletin. 1988. 36 (9): 3654-3658. [ Links ]
23. Amer, M.E.; Abdel-Kader, M.S.; Mahmoud, Z.F.; Abdel, N.A.; Gang, S.; Mabry, T. Revista Latinoamericana de Química. 1989. 20:152-155. [ Links ]
24. Mata, R.; Navarrete, A.; Alvarez, L.; Miranda, R.; Delgado, G.; De Vivar, A. R. Flavonoids and terpenoids of Chenopodium graveolens. Phytochemistry. 1986. 26(1): 191-193. [ Links ]
25. Shimura, H.; Matsura, M.; Takada, N.; Koda, Y. An antifungal compound involved in symbiotic germination of Cypripedium macranthus var. rebunense (Orchidaceae). Phytochemistry. 2007 . 68 (10):1442-1447 [ Links ]
26. Ministerio de Agricultura y Desarrollo Rural. Colombia. 2011. [Consultado en abril de 2011]. Disponible en: http://www.minagricultura.gov.co/archivos/agenda_prospectiva_de_investigacion_y_desarrollo_tecnologico_para_la_cadena_productiva_de_flores_y_follajes_con_enfasis_en_clavel.pdf. [ Links ]