Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Ingeniería e Investigación
Print version ISSN 0120-5609
Ing. Investig. vol.30 no.2 Bogotá May/Aug. 2010
Carlos Alberto Guerrero Fajardo1, Iván David Osorio León2 y Fabio Emiro Sierra Vargas3
1 Ingeniero Mecánico. M.Sc., en Ingeniería Ambiental. Ph.D. Sc., en Ingeniería Química, Facultad de Ciencias, Universidad Nacional de Colombia. caguerrerofa@unal.edu.co 2 Estudiante Ingeniería Química, Facultad de ingeniería, Universidad Nacional de Colombia. idosoriole@unal.edu.co 3Ingeniero Mecánico. Ph.D. Sc., en Ingeniería - Energías renovables, Facultad de Ingeniería, Universidad Nacional de Colombia. fesierrav@unal.edu.co
RESUMEN
Los conflictos entre los biocombustibles y el uso de alimentos como materias primas han abierto la posibilidad de investigar el uso de materias primas no comestibles para su producción. Este trabajo busca estudiar el efecto que tiene la temperatura sobre la conversión en la producción de biodiesel usando aceite de higuerilla. La transesterificación del aceite con metanol se realiza vía catálisis básica (0,5 % de NaOH) en un tiempo de 1 hora, usando una relación molar 6:1 de alcohol/aceite, bajo presión atmosférica, y dejando como variable libre la temperatura, a la cual se le asignaron los valores de 20, 30, 40 y 50 °C, llevando a cabo una réplica para cada valor. Los productos de reacción se analizaron mediante cromatografía de gases (CG-FID) para cuantificar la presencia de FAME (metil ésteres de ácidos grasos). Los resultados presentaron dispersiones diferentes dependiendo de la temperatura, encontrando la menor dispersión con el biodiesel obtenido a 50 °C. El análisis por cromatografía de gases demuestra que el contenido de FAME de mayor proporción se alcanza en las muestras de 50 °C, temperatura a la cual fue mayor la conversión del ácido ricinoleico (el de mayor presencia en el aceite de Higuerilla). La cromatografía también revela que el tiempo de reacción es el adecuado, a las condiciones de proceso establecidas, para lograr una conversión del 94,26% basada en el ácido ricinoleico.
Palabras clave: aceite de higuerilla, biodiesel, transesterificación, catálisis básica.
ABSTRACT
Problems arising between biofuels and food as raw materials have led to investigating the use of inedible raw materials for their production. This work was aimed at studying the effect of temperature on converting castor oil in biodiesel production. Oil transesterification with methanol was carried out using an alkaline catalyst (0.5% NaOH - water solution) for 1 hour using a 6:1 alcohol/oil molar ratio, at atmospheric pressure and taking temperature as a free variable. The temperature was evaluated at 68°F, 86°F, 104°F and 122°F. The reaction products were analysed by gas chromatography (CG-FID) for quantifying the fatty acid methyl esters (FAME) present. The results showed different dispersion depending on temperature, finding that 122°F resulted in less dispersion than the others. CG-FID analysis showed that most FAME content was reached at 122°F, such temperature giving the highest ricinoleic acid conversion rate. Gas chromatography also revealed that reaction time was adequate, in process conditions, for obtaining ricinoleic acid-based 94.26% conversion.
Keywords: castor oil, biodiesel, transesterification, alkaline catalysis.
Recibido: mayo 27 de 2009Aceptado: junio 20 de 2010
Introducción
La sustitución parcial del petrodiesel, o diesel derivado del petróleo, por fuentes de energía renovables, es una tendencia que se viene afianzando a nivel mundial, ya que esta sustitución trae consigo efectos ambientales favorables, entre los que se cuentan la reducción de sustancias contaminantes en las ciudades y la disminución de gases de efecto invernadero (Corporación para el Desarrollo Industrial de la Biotecnología y Producción Limpia, Corpodib, 2003).
De las alternativas que mayor desarrollo y atención han recibido se encuentran los biocombustibles, entre los cuales figura el biodiesel como una solución bastante prometedora para obtener combustibles líquidos (Conceicao, 2005). El biodiesel ofrece beneficios como combustible, entre los cuales se destacan: funcionar en cualquier motor diesel convencional sin necesidad de modificaciones, poderse usar puro o en mezclas con el diesel, no contiene azufre, reduce las emisiones de CO, no presenta emisiones netas de CO2 y puede llegar a mejorar la vida útil de los motores (Corpodib, 2007; Guerrero Rodríguez, 2003).
Sin embargo, uno de los principales problemas sociales en los que se ha visto involucrado el biodiesel ha sido la amenaza de la seguridad alimentaria, pues algunas de las materias primas usadas en el proceso son también una parte importante del mercado alimenticio (Guerrero Rodríguez, 2003; Demirbas, 2008).
Como respuesta a esta problemática ha venido cobrando una mayor importancia el uso de materias primas no comestibles para la producción de biocombustibles, y en nuestro caso específico, de biodiesel (Guerrero Rodríguez, 2003). Es así como, la semilla de la higuerilla ha surgido como una solución bastante atractiva, conteniendo aproximadamente el 40% de su peso en aceite de ricino, caracterizado por tener cerca de un 90% en peso de ácido ricinoleico, lo que hace de este aceite el de mayor proporción de ácidos grasos de todos los aceites vegetales (Conceicao, 2005).
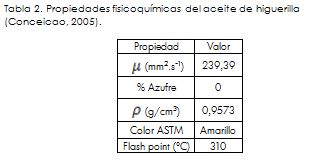
La transesterificación de los ácidos grasos contenidos en el aceite de higuerilla es un proceso químico mediante el cual se logra reducir la viscosidad del aceite por medio de la formación de metil ésteres de ácidos grasos (para el caso donde los ácidos grasos reaccionan con metanol), y se obtiene un fluido de mejores propiedades para su uso como combustible dentro de motores (Demirbas, 2002), especialmente por la reducción de la viscosidad, que pasa de 239,39 a 13,75 mm2.s-1, según Conceicao (2005). Dentro de las variables que deben controlarse en la reacción de transesterificación de ácidos grasos se ha encontrado que el contenido de agua del aceite, así como el de ácidos grasos libres, tiene repercusiones en la formación de jabones y en consumo del catalizador, reduciendo la efectividad de este último (Isayama, 2003; Demirbas, 2007). Algunas otras variables tratadas en la literatura y con influencia en el desarrollo de la transesterificación de ácidos grasos libres, son el tipo de catalizador (Demirbas, 2007; Demirbas, 2005), tipo de alcohol (Demirbas, 2008) y la relación molar alcohol/aceite (Guerrero Rodríguez, 2003).
Como sucede con todo proceso que tenga impacto sobre la economía y la sociedad, es bastante importante encontrar la manera de optimizarlo para que su implementación sea viable económicamente.
Este trabajo contiene la descripción del procedimiento experimental realizado para transformar el aceite de higuerilla en biodiesel a las diferentes temperaturas establecidas. Con esta intención, las variables de reacción diferentes a la temperatura se establecen con base en trabajos previos, y la temperatura se fija en cuatro valores diferentes. Dicho procedimiento permite identificar el efecto de esta variable en el desempeño de la reacción. Posteriormente, con base en los análisis cromatográficos de los productos de reacción, se identifica la temperatura que permite obtener una mayor producción de biodiesel. Finalmente, se presentan las conclusiones del trabajo y los agradecimientos respectivos.
Trabajo experimental
El trabajo experimental se efectuó en los laboratorios de Biomasa y Energía del departamento de Química de la Universidad Nacional de Colombia, en Bogotá.
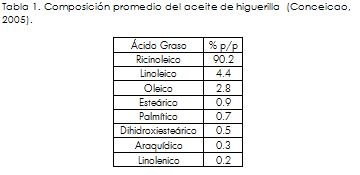
Como materias primas para el estudio se toma aceite de higuerilla (densidad: 0,957 g/ml), metanol (0,7918 g/ml) al 99,5%, y como catalizador se emplea un 0,5% en peso de NaOH grado comercial. De acuerdo con (Martinez Ávila, 2007), se ha encontrado que la relación molar alcohol/aceite de mejor rendimiento en la reacción, es 6:1. La composición, así como otras propiedades de interés acerca del aceite empleado, se presentan a continuación:
La reacción de transesterificación se realiza en un reactor batch de 500 ml fabricado en vidrio, equipado con un condensador vertical a reflujo refrigerado con agua, y con una chaqueta de vidrio por la cual se condujo agua proveniente de un termostato, el cual permite controlar la temperatura dentro del reactor (Figura 1).

Mediante un conducto al ambiente ubicado en la parte superior del condensador a reflujo se garantiza que la presión dentro del sistema sea la barométrica de Bogotá (560 mm Hg). Con el fin de proporcionar agitación y garantizar la mezcla requerida para iniciar la reacción, también se dispone de una plancha calefactora con agitador magnético, sobre la que reposa el reactor descrito.
Previendo inconvenientes indeseados en el transcurso de la reacción, y como medida de seguridad, se procura que la mezcla reaccionante no ocupe todo el volumen del reactor, por lo que se usan cantidades tales que ocupen aproximadamente un 40% (200 ml) del volumen disponible; tales cantidades fueron:
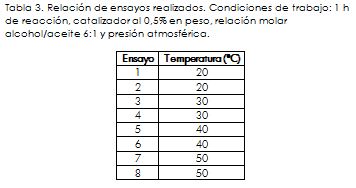
Para determinar el efecto de la temperatura la reacción se desarrolla por un tiempo de una hora a cuatro temperaturas: 20, 30, 40 y 50 °C, haciendo además una réplica de cada valor de temperatura. Al cabo de la hora la reacción se neutraliza con 1 ml de HCl (37% w/w), cantidad requerida para detener la reacción. Dicha canti-dad se determina teniendo en cuenta la cantidad de NaOH que actúa como catalizador y la que va a neutralizar los ácidos grasos libres, determinados por medio del valor ácido (medición determinada según la norma ASTM D1980-87) (American Society for Testing and Materials, 1998).
Los productos que se obtienen en la reacción se llevan a un embudo de decantación y se dejan allí por un tiempo aproximado de 12 horas, al cabo del cual se observa la separación de dos fases, don-de la fase de mayor proporción (la liviana), es la fase biodiesel, y la otra es glicerina (fase pesada).
La glicerina presente en el embudo se separa de la fase biodiesel, y esta última se somete a un proceso de lavado (consistente en una extracción líquido-líquido), en la que el agente de lavado es una solución acuosa de CH3COOH al 10% w/w y 20 °C, la cual se aplica en una proporción volumétrica 2:1 con relación al biodiesel. Éste se somete a 3 lavados con agitación suave por 5 minutos, según los trabajos de Martinez Ávila (2007).
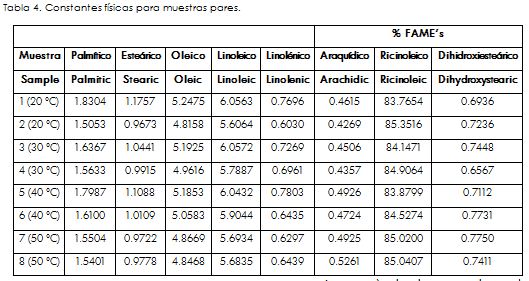
El biodiesel lavado se caracteriza por medio de la medición de constantes físicas tales como densidad e índice de refracción (Tabla 4).
Finalmente, se hace una caracterización por medio de cromatografía de gases (CG-FID) con el objeto de identificar el grado de conversión de la reacción como una función de la presencia de FAME en tales productos (Guerrero, 2009).
Resultados
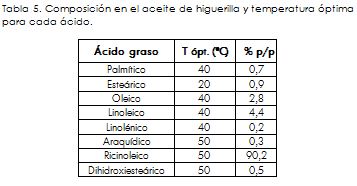
Los resultados obtenidos para cada ensayo se muestran en la Tabla 5, la cual presenta el contenido porcentual de FAME de cada ácido en las diferentes muestras de biodiesel.
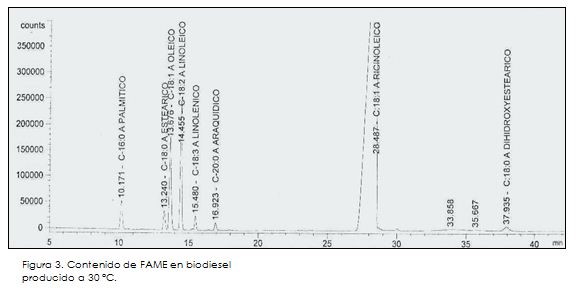
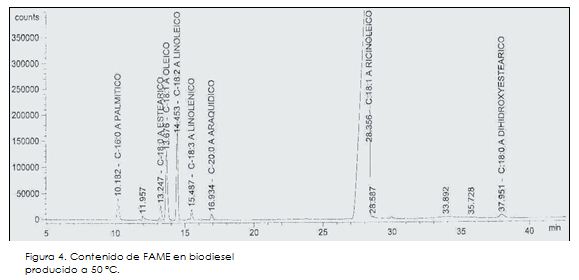
Adicionalmente, se ofrece el cromatograma del aceite de higuerilla en su estado inicial, apreciándose que al inicio de la reacción el contenido de metil ésteres es prácticamente nulo en el reactor (Figura 2). Además, se exponen los cromatogramas de dos muestras de biodiesel obtenidas a 30 y 50 °C (Figuras 3 y 4, respectivamente), donde se puede ver la conversión de los ácidos grasos en metil ésteres por medio de los picos de cromatografía.

Análisis y discusión
Como primera observación de los resultados obtenidos, debe destacarse el mayor porcentaje del éster metílico del ácido ricinoleico (84,58% en promedio) en todas las muestras analizadas; en segúndo lugar, el FAME del ácido linoleico (5,85% en promedio); y en tercer lugar, el FAME del ácido oleico (5,02% en promedio). De otra parte, no se observa una diferencia significativa en la producción de los FAME con la temperatura, por tal razón se evalúa la diferencia entre la dispersión de los resultados de una temperatura a otra, con el propósito de mejorar la correlación y establecer con precisión el efecto de la temperatura sobre la producción de los FAME. El resultado de este tratamiento de datos se muestra en las figuras 5 a 12, obteniendo a las temperaturas de 20 y 40 °C las mayores dispersiones, y a las restantes (30 y 50 °C) la menor dispersión entre resultados. Es importante hacer mención sobre este comportamiento de los datos, pues la dispersión es un sinónimo de la confiabilidad de los resultados, siendo más precisa la determinación en cuanto menor sea la dispersión de los valores. De acuerdo con lo anterior, se aprecia que los resultados correspondientes a los ensayos a 30 y 50 °C son los que proporcionan una mayor precisión y por tanto confiabilidad, siendo esta última temperatura la que presentó la menor dispersión entre ensayos. Sin embargo, con el ánimo de poder comparar los diferentes ensayos y observar las tendencias en su comportamiento, las parejas de valores obtenidos para cada temperatura se promediaron.
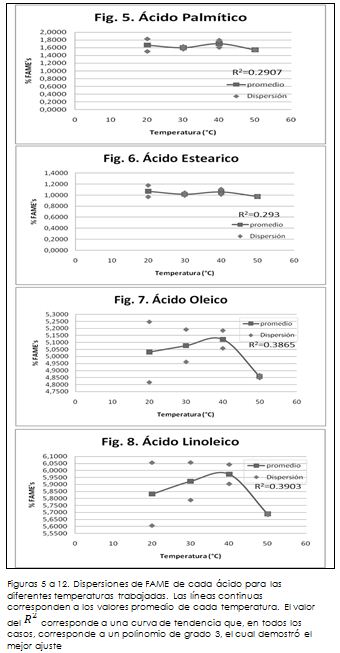
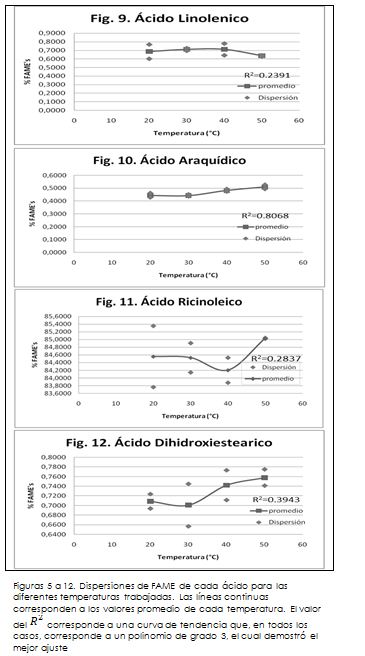
El análisis de estas gráficas deja en evidencia varios aspectos interesantes. En primer lugar, se aprecia que el mayor contenido de FAME de cada ácido fue diferente para cada una de las temperaturas trabajadas. Por ejemplo, para los ácidos palmítico, oleico, linoleico y linolénico (que se denominan grupo 1), la mayor presencia de FAME se presenta en las muestras trabajadas a 40 °C; no obstante, para ácidos como el araquídico, el ricinoleico y el dihidroxiesteárico (que se denominan grupo 2), el mayor contenido de FAME se alcanzó con las muestras a 50 °C. Esta observación sugiere dos posibles opciones térmicas[4] para llevar a cabo la reacción: trabajar a 40 °C, favoreciendo la transesterificación de los ácidos del grupo 1, o hacerlo a 50 °C, favoreciendo la formación de metil ésteres de los ácidos del grupo 2. Esta disyuntiva puede ser resuelta al sopesar la presencia de los ácidos de los grupos 1 y 2 en el aceite de higuerilla, pues el grupo 2 al incluir al ácido de mayor importancia[5] toma más peso dentro de la reacción y debe ser éste el que se favorezca; una ganancia en la conversión de los ácidos de este grupo (fundamentalmente del ricinoleico) significa una ganancia a nivel global para la reacción de mayor importancia que si fuera para el grupo 1.
La información de la Tabla 1 permite entonces realizar una ponderación que indique cuál grupo de ácidos grasos tiene más peso dentro del aceite de higuerilla y de esta manera definir cuál temperatura es la más adecuada para la reacción.
Sumando las composiciones en peso de los ácidos pertenecientes al grupo 1 se encuentra como resultado que estos ácidos representan el 8,1% del aceite, mientras que en el grupo 2 equivalen al 91,0%, lo cual establece que la temperatura de reacción que afecta más positivamente la conversión es la de 50 °C.
Finalmente, cabe resaltar el buen grado de avance que presentó la reacción para todas las temperaturas, pero especialmente para 50 °C, temperatura a la que reaccionó la mayor cantidad de ácido ricinoleico (el de mayor presencia en el aceite de higuerilla) para su transformación en ricinoleato de metilo. Lo anterior se afirma al observar en la Tabla 4 el porcentaje de FAME que se forma de este ácido. Se constata que para las diferentes temperaturas el porcentaje de FAME de cada uno de los ácidos está cerca de la composición correspondiente en la Tabla 1, significando que prácticamente la totalidad de los ácidos están reaccionando con el metanol para producir biodiesel, y también, que el tiempo de reacción de 1 hora es suficiente para llevar a cabo la reacción bajo las condiciones manejadas. Por ejemplo, para el ácido ricinoleico, en el primer ensayo a 50 °C se deriva de la Tabla 4 que el porcentaje de FAME es del 85,02%, y de acuerdo con la Tabla 1, su porcentaje en el aceite es del 90,2%. Según lo anterior, a las condiciones de reacción establecidas y a 50 °C, reaccionó el 94,26% del ácido ricinoleico, siendo un porcentaje que demuestra un aceptable grado de avance de la reacción.
Conclusiones
Del trabajo realizado se puede deducir, en primer lugar, que los datos obtenidos para los diferentes ensayos presentaron diferentes grados de dispersión, siendo los ensayos más precisos los llevados a cabo a la temperatura de 50 °C (menor dispersión), seguidos por los de 30 °C.
En segundo lugar, se concluye que la temperatura más conveniente para efectuar la reacción de transesterificación en las condiciones establecidas de reacción es la de 50 °C, pues a estos grados se encontró la máxima conversión en FAME del ácido de mayor presencia en el aceite de higuerilla (ácido ricinoleico).
Finalmente, se concluye que a las condiciones de proceso empleadas, un tiempo de reacción de 1 hora es suficiente para obtener una conversión de prácticamente la totalidad de los ácidos grasos presentes inicialmente en el aceite.
Agradecimientos
Se expresa por parte de los autores un especial reconocimiento al laboratorio químico Antek S. A., por su colaboración en el análisis cromatográfico de las muestras de biodiesel.
Bibliografía
Alizadeh, A. M., Reza, M. P., Shanrokhi, M., Analysis of control structure for recycled reaction/separation processes with first order reaction., Petroleum and Coal, Vol. 48, 2006, pp. 48-60. [ Links ]
American Society for Testing and Materials., ASTM D1980-87. Standard Test Method for Acid Value of Fatty Acids and Polymerized Fatty Acids. [on-line], 1998. www.astm.org. [ Links ]
Conceicao, M., Candeiab, R., Silvac, F., Bezerrab, A., Fernandes, V., Souzab, A., Thermoanalytical characterization of castor oil biodiesel., Renewable & sustainable energy reviews, Vol. 11, No. 5, June, 2007, pp. 964-975. [ Links ]
CORPODIB y INDUPALMA S.A., Programa estratégico para la producción de biodiesel -combustible automotriz- a partir de aceites vegetales., Bogotá: Unidad de Planeación Minero energética, 2003. [ Links ]
CORPODIB., Estado del Arte de las Tecnologías de Producción de Biodiesel., Bogotá: s.n., 2007, pp. 323-326. [ Links ]
Demirbas, A., Biodiesel fuels from vegetable oils via catalytic and non-catalytic supercritical alcohol transesterifications and other methods: a survey., Energy Conversion & Managment, Trabzon, Turkey: s.n., 2002. [ Links ]
Demirbas, A., Biodiesel production from vegetable oils via catalytic and non.catalytic supercritical methanol transesterification methods., Progress in Energy and Combustion Science, Elsevier, 2005. [ Links ]
Demirbas, A., Comparison of transesterification methods for production of biodiesel from vegetable oils and fats., Energy Conversion & Managment, Trabzon, Turkey: s.n., 2007. [ Links ]
Demirbas, A., Biofuels sources, biofuel policy, biofuel economy and global biofuel projections., Energy Conversion & Managment. Trabzon, Turkey: s.n., 2008. [ Links ]
Demirbas, A., Production of biodiesel fuels from linseed oil using methanol and ethanol in non-catalytic SCF condition. Trabzan: Elsevier, 2008, Biomass & Bioenergy. [ Links ]
Guerrero, C. A., Sierra, F., Olmos, G., Aceite de Higuerilla alternativa como combustible., AIMUN (ed.), 1st Ed, Bogotá-Colombia, Universidad Nacional de Colombia, 2009, pp. 49-70. [ Links ]
Guerrero, A. M., Narváez, P.C., Prospectiva de la producción en Colombia de oleoquímicos derivados del aceite de Higuerilla., Bogotá: BSc thesis, Universidad Nacional de Colombia, 2003. [ Links ]
Isayama, Y., Saka, S., Effects of Water on biodiesel fuel production by supercritical methanol treatment., Bioresource Technology, Japon, Elsevier, 2003. [ Links ]
Martinez O., Sánchez F. J., Suárez, O. Y., Producción de ésteres etílicos a partir de aceite de palma RBD., Revista de Ingeniería e Investigación, 2007. [ Links ]
[4] Una tercera opción es la de trabajar a 20 °C, temperatura a la cual es máximo el contenido de estearato de metilo; sin embargo, se deja de lado, pues esta temperatura beneficia únicamente al ácido esteárico, que se encuentra en baja proporción en el aceite de higuerilla.
[5] Se ha considerado que el ácido ricinoleico es el más importante, ya que es el principal componente del aceite de higuerilla según la Tabla 1.











 text in
text in 


