Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Boletín de Investigaciones Marinas y Costeras - INVEMAR
Print version ISSN 0122-9761
Bol. Invest. Mar. Cost. vol.40 no.1 Santa Marta Jan./June 2011
REVISIÓN DE LOS TAXONES DEL GÉNERO NEOCERATIUM F. GÓMEZ, D. MOREIRA ET P. LÓPEZGARCÍA (DINOPHYCEAE) Y PRIMER REGISTRO DE N. DENS EN EL MAR CARIBE COLOMBIANO
REVISION OF THE TAXA OF THE GENUS NEOCERATIUM F. GÓMEZ, D. MOREIRA ET P. LÓPEZ-GARCÍA (DINOPHYCEAE) AND FIRST REPORT OF N. DENS IN THE COLOMBIAN CARIBBEAN
Luis Alfonso Vidal1 y Yesid Lozano-Duque2
1 Santa Marta, Colombia. lavidalve@yahoo.com
2 Universidad del Valle, Facultad de Ciencias, Departamento de Biología, Grupo de Investigación en Estuarios y Manglares. Calle 13 No. 100-00. Cali, Colombia. yesidlozanoduque@yahoo.com.mx; yesilodu@univalle.edu.co
RESUMEN
Se presenta una síntesis de los taxones del género Neoceratium hallados en un transecto a lo largo de la costa Caribe colombiana, en las bahías de Gaira y Santa Marta y en la Ciénaga Grande de Santa Marta. Con base a una extensiva revisión bibliográfica, se encontró que de los 65 taxones del género Neoceratium registrados en este estudio, 56 lo han sido ya para el mar Caribe colombiano y los nueve restantes son registros nuevos para la región. Neoceratium arietinum f. gracilentum, N. breve var. curvulum, N. humile, N. symmetricum var. coarctatum, N. longissimum y N. horridum, buceros > horridum se registran por primera vez para el Caribe colombiano. Neoceratium dens, sin registros en el Atlántico y mares adyacentes, se encuentra por primera vez para esta parte del Atlántico (mar Caribe), frente a las costas del Caribe colombiano. Neoceratium breve forma A y N. tenue forma A no pudieron ser ubicadas dentro de ninguna variedad o forma de la especie respectiva. Para los nueve taxones que son registrados por primera vez en el Caribe colombiano, se presenta revisión bibliográfica, tallas, distribución y datos ecológicos. Los porcentajes de abundancia del género Neoceratium más altos, correspondieron a las estaciones frente a los departamentos de La Guajira y el Magdalena; los más bajos, frente a los departamentos localizados hacia el sur de la costa Caribe colombiana. Esta distribución, aparentemente se encuentra ligada a la distribución de las masas de agua, siendo estas de naturaleza más oceánica hacia el norte y con influencia más costera hacia el sur.
PALABRAS CLAVE: Fitoplancton, Dinophyceae, Caribe colombiano, Neoceratium dens.
ABSTRACT
This work summarizes the taxa within the genus Neoceratium found in a transect along the Colombian Caribbean coast, in Gaira and Santa Marta bays, and Ciénaga Grande de Santa Marta. Based on an extensive literature review, 56 of the 65 taxa of Neoceratium reported in this study have been recorded for the Colombian Caribbean Sea, and the remaining nine are new reports for the region. Neoceratium arietinum f. gracilentum, N. breve var. curvulum, N. humile, N. symmetricum var. coarctatum, N. longissimum and N. horridum, buceros > horridum were first recorded for the Colombian Caribbean. Neoceratium dens, not registered in the Atlantic Ocean and adjacent seas, is reported for the first time in this part of the Atlantic Ocean (Caribbean Sea), along the Colombian Caribbean Coast. Neoceratium breve form A and N. tenue form A could not be placed within any variety or form of the respective species. A literature review, description of sizes and distributions, and ecological information are included for the nine taxa recorded for the first time in the Colombian Caribbean. The highest percentages of abundance of the genus Neoceratium werefound in the stations located off the coast of the La Guajira and the Magdalena provinces, and the lowest in the stations located in the departments situated off the southern part of the Colombian Caribbean coast. This distribution apparently is related to the distribution of water masses, which have more northward oceanic influence, and more southward coastal influence.
KEY WORDS: Phytoplankton, Dinophyceae, Colombian Caribbean, Neoceratium dens.
INTRODUCCIÓN
El género Neoceratium F. Gómez, D. Moreira et P. López-García, es un grupo recientemente propuesto para todas las especies marinas que pertenecían a Ceratium Schrank, el cual fue el primer género establecido en el grupo de los dinoflagelados. El género Ceratium fue creado en 1793 por F. Von Paula Schrank basado en la identificación de especies de agua dulce, aunque después también se ubicaron las especies marinas. Sournia (1986) apoyado en el número de placas cingulares señaló las diferencias entre las especies de agua dulce y marinas. Gómez et al. (2010) validan la separación de Ceratium en dos diferentes géneros, separando las especies de aguas continentales en Ceratium, y las especies marinas en el nuevo género Neoceratium. Esta separación se basa en el número de placas cingulares y en la diferencia evolutiva de sus secuencias SSU del ADN ribosomal.
Debido al gran tamaño de sus células, la dureza de sus tecas y su amplia distribución y abundancia se ha facilitado el estudio de este género. De los 120 taxones marinos (especies, infraespecies, variedades o formas) que han sido descritos para este género, sólo 63 especies son consideradas validas (Gómez, 2005). El género Neoceratium ha sido considerado como uno de los más útiles en estudios biogeográficos, definiendo corrientes oceanográficas, masas de agua y posiblemente será útil en estudios de cambio global (Dodge y Marshall, 1994; Tunin-Ley et al. 2007). Este género ha sido utilizado como indicador biológico de masas de agua en el océano Atlántico norte (Dodge y Marshall, 1994; Raine et al. 2002), océano Pacífico (Dodge, 1993), mar Mediterráneo (Tunin-Ley et al., 2007) y en el océano Ártico (Okolodkov, 1996).
Varios autores han publicado o registrado taxones del género Neoceratium en diferentes sitios del Caribe colombiano. Caycedo (1977), registró seis especies para la bahía de Nenguange, Parque Nacional Natural Tayrona, en muestreos de fitoplancton realizados entre septiembre y noviembre de 1974 y octubre y noviembre de 1975. Carbonell (1979) registró 23 taxones, entre especies, variedades y formas, para la bahía de Cartagena, de noviembre de 1975 a octubre de 1976. Carbonell (1982) registró 32 taxones, entre especies, variedades y formas, para las islas del Rosario, entre noviembre de 1977 y junio de 1978. Varias especies se han registrado para la Ciénaga Grande de Santa Marta (CGSM) en trabajos de tesis (Carmona, 1979; Vidal, 1995) e informes no publicados. Fernández y García (1998) registraron 27 taxones, entre especies, variedades y formas, para el golfo de Salamanca, como resultado de cruceros efectuados en los meses de marzo, abril, agosto y diciembre de 1996. Vidal y Ramos (datos sin publicar) registraron los taxones del fitoplancton, entre ellos los del género Neoceratium, para la bahía de Santa Marta, hallados en muestras colectadas en los meses de agosto, septiembre y noviembre 2004 y enero 2005. Vidal (datos sin publicar) durante los últimos 12 años ha registrado, entre otros, los taxones del género Neoceratium, con base en muestreos llevados a cabo en la bahía de Gaira en dos meses del año, normalmente febrero y agosto, correspondientes a la época seca y a la época de lluvias respectivamente.
Durante el primer período de 2008, de febrero a junio, se llevó a cabo un crucero oceanográfico-biológico en el buque B/I Ancón del Instituto de Investigaciones Marinas y Costeras (INVEMAR), sobre un transecto a lo largo de la costa Caribe colombiana, desde La Guajira hasta el golfo de Urabá, en el que se colectaron muestras de fitoplancton. El resultado del análisis de éstas, muestra que el género Neoceratium es uno de los más diversos. El interés de ampliar el conocimiento de la biodiversidad marina de esta parte del Caribe motivó la realización de este estudio. En este trabajo se dan a conocer los taxones de Neoceratium registrados en un transecto a lo largo de la costa Caribe colombiana, en las bahías de Santa Marta y Gaira y en la CGSM y se comparan con los resultados de los trabajos publicados, con el fin de verificar nuevos registros para el Caribe colombiano, así como hacer una actualización de los nombres de los taxones mencionados por los diferentes autores.
ÁREA DE ESTUDIO
El mar Caribe colombiano está localizado en el extremo noroeste de Suramérica con una longitud de línea costera de 1760 Km y un área de zona costera de 35207 Km2. Esta zona se encuentra bajo la influencia de los desplazamientos norte-sur de la Zona de Convergencia Intertropical y del movimiento meridional del sistema de monzones americanos. En general, en el mar Caribe colombiano se da un clima tropical semiárido con dos períodos climáticos principales, una época seca entre los meses de diciembre-abril y una época de máxima precipitación de agosto a noviembre; además, se considera una época de transición entre mayo y junio. Hacia la zona norte, en la península de La Guajira donde se encuentra una zona de surgencia, se presenta un clima desértico a semidesértico, con los valores más bajos de precipitación, el cual va cambiando a húmedo cuando se acerca a la Sierra Nevada de Santa Marta. Hacia el suroccidente, la costa Caribe colombiana presenta la mayor humedad por la presencia de los cinturones de San Jacinto y Sinú (Montes de María) y la serranía del Darién, zona donde se presentan altos valores de precipitación. El río Magdalena es la fuente principal de agua dulce en el mar Caribe, pues su flujo de agua tiene un fuerte efecto en las condiciones ambientales de la región. Además, existen aportes de agua dulce desde las cuencas hidrográficas de la alta Guajira, el río Ranchería, norte y oeste de la Sierra Nevada de Santa Marta, la CGSM, el río Sinú, el río Atrato y otros aportes menores (CORPES, 1992; Posada y Henao, 2008).
La circulación superficial del mar Caribe colombiano está dominada por dos sistemas de corrientes, la corriente superficial del Caribe la cual recorre la mayor parte del año en dirección oriente-occidente y la contracorriente del Darién o de Panamá-Colombia, que recorre desde Panamá hasta isla Fuerte y en otras ocasiones llega hasta la Guajira. A nivel superficial, la temperatura del agua de mar varía desde 26 °C en la época seca hasta 29 °C en la de lluvias; la salinidad presenta valores típicos marinos con variaciones anuales por el aporte de los ríos (Andrade-Amaya, 2000).
MATERIALES Y MÉTODOS
Muestreo y análisis de muestras
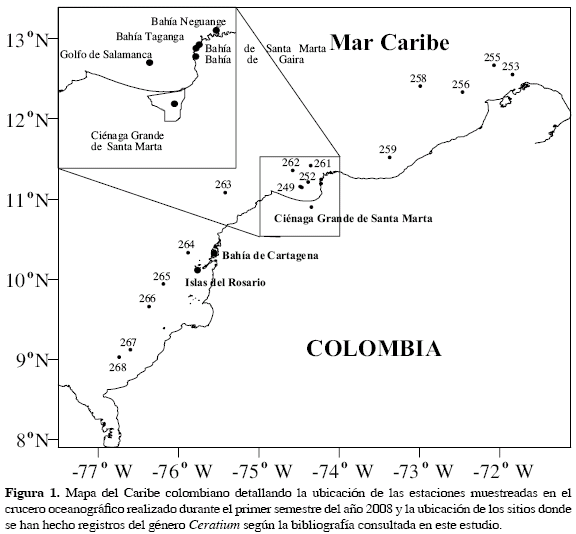
La mayoría de los muestreos del crucero oceanográfico fueron realizados durante los meses de mayo y junio, que corresponden, en la región, a la primera época lluviosa del año, excepto los dos primeros muestreos que fueron hechos frente al departamento del Magdalena durante el mes de febrero, que corresponde a la época seca. Las muestras de fitoplancton fueron colectadas en 15 estaciones distribuidas a lo largo de la costa Caribe colombiana (Figura 1). Los datos de posición geográfica, fecha, temperatura, salinidad y profundidad de arrastre de cada estación se presentan en la Tabla 1. Para la obtención de las muestras, en cada estación se realizó un arrastre vertical con red cónica de 2.2 m de longitud, 0.58 m de diámetro de boca, con malla de 20 µm de tamaño de ojo. El arrastre vertical se realizó desde el inicio de la termoclina hasta la superficie. La termoclina se determinó con base a los datos de temperatura y presión (profundidad) obtenidos mediante una sonda multiparámetros. La red se bajó cerrada a la profundidad determinada (termoclina), una vez en esta profundidad se abría la red y se hacía el arrastre vertical hasta la superficie. En las estaciones 249 y 252 el arrastre vertical se realizó desde los 200 m de profundidad hasta la superficie, no se tuvo en cuenta la termoclina. Las muestras biológicas colectadas se fijaron con lugol y formalina al 4 %, neutralizada con tetraborato de sodio.
Dos mililitros de cada muestra fueron vertidos en la placa Sedgewick-Rafter; se analizaron y se contaron las células en las columnas 13, 25 y 37, procurando llegar hasta las 300 células. Para observar la distribución de la abundancia del género, las diferentes poblaciones se expresaron como porcentajes dentro de la muestra. Aquí se dan los porcentajes sólo para los taxones hallados del género Neoceratium (Tabla 2). El método para hacer un recuento de abundancias relativas (porcentajes) no es del todo recomendable, aunque se justifica porque en este trabajo no se intenta calcular densidades absolutas y el método es homogéneo en el recuento de todas las muestras. Para la observación específica y toma de fotomicrografías con objetivos de 10x, 45x y 100x las células fueron separadas mediante un capilar y depositadas en placas portaobjetos con cubreobjetos.
Se elaboraron listas con los taxones de Neoceratium hallados a lo largo de la costa Caribe colombiana, en la bahía de Santa Marta, en la bahía de Gaira y en la CGSM (Tabla 3). Los taxones registrados en las cuatro listas son tratados de manera particular, exceptuando aquellos ya registrados en trabajos publicados (Caycedo, 1977; Carbonell, 1979, 1982; Fernández y García, 1998). Neoceratium karstenii y N. horridum var. molle, son tenidos en cuenta con miras a la actualización de los nombres de los taxones mencionados por los autores. De todos estos taxones se aporta revisión bibliográfica, tamaños, distribución geográfica a nivel del mar Caribe colombiano, mar Caribe, golfo de México y mundial y notas ecológicas según los autores consultados. La mayoría de los taxones van acompañados con observaciones. Las medidas de los taxones se dan en micras (µm) y se utilizaron las siguientes siglas: A= ancho; E= altura de la epiteca; H= altura de la hipoteca; LT= longitud total; Trd= trasdiámetro (ancho cuerpo).
RESULTADOS
Se registraron 38 taxones del género Neoceratium sobre un transecto a lo largo de la costa Caribe colombiana, 15 taxones en la bahía de Santa Marta, 38 taxones en la bahía de Gaira y 13 taxones en la CGSM (Tabla 3). Entre estas cuatro listas, se halló un taxón sin registros para el mar Caribe y el golfo de México: N. dens (Ostenfeld y Schmidt, 1901) Gómez, Moreira et López-García. Junto con el anterior, se identificaron seis taxones más, sin registros para el Caribe colombiano: Neoceratium arietinum f. gracilentum (Jörgensen, 1920) Gómez, Moreira et López-García; N. breve var. curvulum (Jörgensen, 1911) Gómez, Moreira et López-García; N. humile (Jörgensen, 1911) Gómez, Moreira et López-García; N. symmetricum var. coarctatum (Pavillard) Gómez, Moreira et López-García; N. longissimum (Schröder) Gómez, Moreira et López-García y N. horridum, buceros > horridum (Sournia, 1968) Gómez, Moreira et López-García. Se consideran dos taxones más que no pudieron ser ubicados dentro de alguna variedad o forma de la especie respectiva, designados como: N. breve forma A y N. tenue forma A.
Casi todos los taxones se registraron en el transecto a lo largo de la costa Caribe colombiana (Tabla 3), excepto, N. longissimum y N. horridum, buceros > horridum que aparecen registrados sólo para la bahía de Gaira. Neoceratium gravidum estaría registrado sólo para la bahía de Gaira, pero también aparece en Murray y Whitting (1899), durante un crucero oceanográfico realizado a finales del siglo XIX. Neoceratium geniculatum aparece registrado en las bahías de Gaira y de Santa Marta. Neoceratium arietinum f. gracilentum, N. breve var. curvulum, N. dens y N. symmetricum coarctatum también se registraron para la bahía de Gaira. Neoceratium azoricum aparece registrado en el transecto a lo largo de la costa Caribe colombiana, en las bahías de Gaira y de Santa Marta, N. tripos tripodioides aparece en el transecto a lo largo de la costa Caribe colombiana, en la CGSM y, posiblemente, en el golfo de Salamanca (ver discusión), N. symmetricum aparece registrado en los cuatro listados.
De los 38 taxones (Tabla 2) registrados a lo largo del transecto, frente a la costa Caribe colombiana, según la literatura consultada, 21 son de ambiente oceánico, algunos de ellos con características umbrófilas, cinco están adaptados a vivir indistintamente en ambientes oceánico y nerítico, siete se consideran neríticos o litorales y tres no se encuentran claramente definidos: Neoceratium breve curvulum, N. tripos tripodioides y N. carriense (Schiller, 1937; Graham y Bronikovsky, 1944; Gaarder, 1954; Halim, 1967; Balech, 1988; Hernández-Becerril, 1989; Licea et al., 1995).
El número de taxones (Tabla 2) del género Neoceratium en las estaciones del crucero oceanográfico, varió desde 2 hasta 22. El número de taxones más bajo se encontró en E253, frente a La Guajira, y el número más alto, en E258 también en La Guajira.
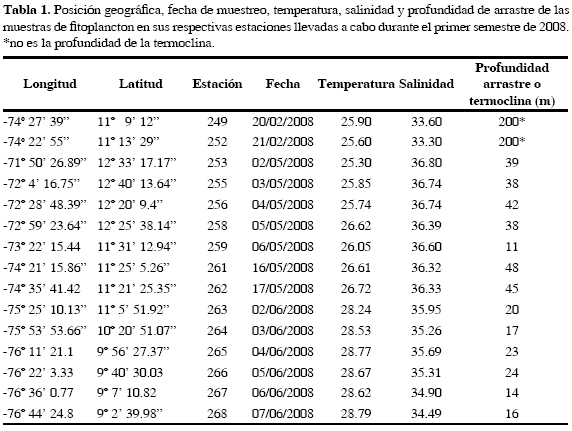
Neoceratium gravidum (Gourret, 1883) Gómez, Moreira et López-García, 2010
(Fig 2A)
Gómez, Moreira et López-García: 2010, pág. 12, tabla 2.
Ceratium gravidum Gourret, 1883, pág. 58, pl.1, fig. 15; Murray y Whitting, 1899, tablas 3, 5-6, 8-9; Jörgensen, 1911, pág. 10, Tafel 1, fig. 7-8, 11, Tafel 2, fig. 12; Jörgensen, 1920, pág. 8, fig. 4; Schiller, 1937, pág. 357, fig. 389; Steemann Nielsen, 1939, pág. 6, fig. 4; Graham y Bronikovsky, 1944, pág. 15, fig. 3-4, chart 3, appendix table 3; Gaarder, 1954, pág. 12; Wood, 1954, pág. 272, fig. 186 a-c; Trégouboff y Rosé, 1957, pág. , pl. 25, fig. 2; Halim, 1967, pág. 719, pl. 1, fig. 9-10; Sournia, 1968, pág. 388, pl. 1, fig. 3; Wood, 1968, pág. 31, fig. 62; Margalef, 1969, pág. 281; Steidinger y Williams, 1970, pl. 42, fig. 157; Taylor, 1976, pág. 57, pl. 11, fig. 99-100, 101 a-b; Rampi y Bernhard, 1980, pág.37, tab. 15; Dodge, 1982, pág. 227, fig. 28B; Pesantes, 1983, pág. 296, lám. 8 fig. 8; Dodge, 1985, pág. 98; Balech 1988, pág. 127, lám. 54, fig. 1; Hernández-Becerril, 1989, pág. 35, fig. 2; Licea et al., 1995, pág. 38, lám. 18, fig. 9; Licea et al., 2004, pág. 424; Okolodkov y Gárate-Lizárraga, 2006, pág. 28.
C. gravidum var. angustum Jörgensen: Okolodkov y Gárate-Lizárraga, 2006, pág. 28. C. gravidum var. elongatum Wood: 1963, pág. 40 (548), fig. 146; Carbonell, 1981, pág. 21.
Medidas. 354 LT, 206 A máximo; 400 LT, 200 A máximo.
Distribución Caribe colombiano. Al este de las islas de San Andrés y Providencia: 13° 06'N, 78° 41'W (Murray y Whitting, 1899). La Guajira, 11° 49' 59'' N, 72° 48' 30'' W, 18 noviembre 1995, 13:00, 27 °C superficial, salinidad 36.1 a 5 m (datos no publicados). Bahía Gaira, arrastre subsuperficial, 26 agosto 1997, 27 °C, salinidad 35. Bahía Gaira, arrastre subsuperficial, 28 enero 2005.
Distribución resto Caribe y golfo de México. Venezuela: Estrecho Cariaco, en aguas cálidas, de profundidad, entre 50 y 100 m, pero también en superficie en áreas de afloramiento (Halim, 1967). República Dominicana al sur (Carbonell, 1981). Al sur de Puerto Rico, al sur del canal de La Mona, al sur de la isla Española, al sur y al este de Jamaica, frente a Panamá, costa costarricense (Murray y Whitting, 1899). Canal Providencia al noroeste, estrechos de La Florida (Wood, 1968). Golfo de México (Steidinger y Williams, 1970). Golfo de México al suroeste (Licea et al., 2004).
Distribución mundial. Corriente de Brasil (Balech, 1988). Atlántico norte 23°-39° N (Murray y Whitting, 1899). Atlántico desde 27° S hasta 48° N, corriente de Bengala al norte, entre Escocia y Groenlandia, islas Azores (Jörgensen, 1911). Atlántico oriental a la altura de las islas Canarias (Margalef, 1969). Bahía Española frente al estrecho de Gibraltar (Gaarder, 1954). Interoceánica, en aguas cálidas, también en el Mediterráneo, en arrastres de 100 a 200 m, umbrófila (Schiller, 1937). A lo largo de casi todo el Atlántico tropical, en aguas oligotróficas, nunca por debajo de 20 °C; en el Pacífico también en aguas tropicales y al sureste; se halla entre los 40° norte y 40° sur en ambos océanos, también en aguas eutróficas, de penumbra entre 200 y 100 m (Graham y Bronikovsky, 1944). Al oeste de las islas Británicas en la Corriente del Golfo (Dodge, 1982). Atlántico tropical este (Dodge, 1985). Mediterráneo: golfo de Marsella (Gourret, 1883). Bahía de Cádiz, estrecho de Gibraltar, Mediterráneo en mar de Alborán, golfo de Lyon, mares Tirreno y Ligure, Nápoles, entre Barca y Sicilia, mar Jónico, mar Egeo, sobre la costa africana, hallado a profundidad y en superficie; también en el Atlántico tropical y subtropical, hasta los 57° N entre las islas Británicas y Groenlandia, océano Indico, al sur del Japón (Jörgensen, 1920). Mediterráneo (Trégouboff y Rosé, 1957; Rampi y Bernhard, 1980). Ecuador: golfo de Guayaquil, en agosto, rara (Pesantes, 1983). Golfo de California, oceánica (Hernández-Becerril, 1989; Licea et al., 1995). Costa pacífica mexicana (Okolodkov y Gárate-Lizárraga, 2006). Región australiana: Australia este, Port Jackson, Eden, Point Danger, Queensland, Port Hacking, Trial Bay, también en Nueva Zelanda, islas Salomón (Wood, 1954). Región australiana: Jibbon Cape y mar de Coral (Wood, 1963). Índico hasta los 36° S en el Cono surafricano y aguas asiáticas al este (Steemann-Nielsen, 1939). Índico: Tuléar en Madagascar, raro, Mar Rojo, golfo de Adén, mar de Arabia (Sournia, 1968). Índico, hasta 20° S (Taylor, 1976).
Observaciones. Inicialmente, se pensó que los registros para la bahía de Gaira eran los primeros para el Caribe colombiano (Tabla 3), pero la estación que corresponde a las coordenadas 13° 06'N, 78° 41'W (Murray y Whitting, 1899) se ubica dentro del mar territorial colombiano, al este de las islas de San Andrés y Providencia. Por lo tanto, el dato anterior es el primer registro de la especie para el Caribe colombiano. La forma en este estudio corresponde a var. latum Jörgensen (Jörgensen, 1911, Tafel 2, fig. 12), semejante a la fig. 10 en Halim (1967), a la fig. 3 en Sournia (1968) y a la fig. 100 en Taylor (1976); con todo, sus variedades son cuestionadas por Sournia (1968); según este autor, hasta la aplicación de un método estadístico apropiado.
Neoceratium geniculatum (Lemmermann) Gómez, Moreira et López-García, 2010
(Fig 2B)
Gómez, Moreira et López-García: 2010, pág. 12, tabla 2.
Ceratium geniculatum (Lemmermann) Cleve, 1900: Jörgensen, 1911, pág. 24, figs. 42-43; Jörgensen, 1920, pág. 34, fig. 24; Böhm, 1931, pág. 43, fig. 37 c-d; Schiller, 1937, pág. 375, fig. 414a; Steemann Nielsen, 1939, pág. 8; Graham y Bronikovsky, 1944, pág. 24, fig. 11J; Gaarder, 1954, pág. 12; Wood, 1954, pág. 279, fig. 197; Wood, 1963, pág. 40 (548), fig. 145; Wood, 1966, pág. 108; Sournia, 1968, pág. 407, figs. 30-31; Wood, 1968, pág. 30, fig. 60; Taylor, 1976, pág. 66, pl. 13, figs. 140 a-b; Carbonell, 1981, pág. 23, lám. 11, fig. 75; Rampi & Bernhard, 1980, pág. 39, tab. 16; Marshall y Solder, 1982, pág. 358; Balech, 1988, pág. 132, lam. 54, fig. 4; Hernández-Becerril, 1989, pág. 38, fig. 18; Licea et al., 1995, pág. 38; Licea et al., 2004, pág. 424; Okolodkov y Gárate-Lizárraga, 2006, pág. 27. C. tricarinatum Kofoid: 1907a, pág. 173, lám. 3, fig. 20.
Medidas. ca.300 LT; 350 LT, 176 E, 176 H; 319 LT, 38 Trd, 158 E, 158 H; 360 LT.
Distribución Caribe colombiano. Taganga, arrastre subsuperficial, 08 agosto 2000. Bahía Gaira, arrastre subsuperficial, 21 agosto 2001. Bahía Santa Marta, junio 2004. Bahía Gaira, arrastre subsuperficial, 20 agosto 2004.
Distribución resto Caribe y Golfo de México. Caribe al centro (Marshall y Solder, 1982). República Dominicana al sur (Carbonell, 1981). Al norte de Cuba (Jörgensen, 1911). Rara en los estrechos de La Florida (Wood, 1968). Golfo de México al suroeste (Licea et al., 2004).
Distribución mundial. Costa norte de Brasil: desembocadura rio Amazonas, entre 40 y 110 m de profundidad (Wood, 1966, 1968). Aguas sudbrasileñas en corriente de Brasil, Atlántico ecuatorial oeste, termófila (Balech, 1988). Islas Azores, estrecho de Gibraltar, entre Sri Lanka y Sumatra (Jörgensen, 1911). Costa oeste de Marruecos, al oeste de las islas Canarias, al sur de las Azores (Gaarder, 1954). Mediterráneo al oeste, migra desde el Atlántico a través del estrecho de Gibraltar, Sicilia, mar Tirreno, Nápoles (Jörgensen, 1920). Mediterráneo (Rampi y Bernhard, 1980). Baja California, golfo de California (Hernández-Becerril, 1989; Licea et al., 1995). Costa pacífica mexicana (Okolodkov y Gárate-Lizárraga, 2006, pág. 27). Pacífico este ca.11° S 95° W y ca.19° S 125° W (Kofoid, 1907a). Pacífico ecuatorial este (Graham y Bronikovsky, 1944). Región australiana (Wood, 1954). Región australiana: mar de Coral y Pacífico oeste (Wood, 1963). Al sur de la India (Böhm, 1931). Índico, interoceánica, tropical, superficial (Steemann-Nielsen, 1939). Índico: canal de Mozambique (Sournia, 1968). Índico: mar de Andamán, mar de Arabia, Reunión y Mombassa (Taylor, 1976). En aguas cálidas de todos los océanos, rara (Schiller, 1937).
Neoceratium azoricum (Cleve) Gómez, Moreira et López-García, 2010
(Fig 2C)
Gómez, Moreira et López-García, 2010: pág. 11, tabla 2.
Ceratium azoricum Cleve, 1900: Jörgensen, 1911, pág. 47, figs. 97-98; Jörgensen, 1920, pág. 69, fig. 66; Schiller, 1937, pág. 406, fig. 447; Steemann-Nielsen, 1939, pág. 12; Graham y Bronikovsky, 1944, pág. 30, fig. 16 M-P, chart 26, appendix table 30; Gaarder, 1954, pág. 9; Wood, 1954, pág. 295, fig. 222 a-b; Trégouboff y Rosé, 1957, pág. , pl. 26, fig. 6; Balech, 1962, pág. 183-184, lám. 26, fig. 398-399; Wood, 1966, pág. 108; López, 1966, pág. 330, fig. 26; Halim, 1967, pág. 712, pl. 1, fig. 4; Wood, 1968, 158 pág. 23, fig. 39; Sournia, 1968, pág. 435, fig. 58; Margalef, 1969, pág. 281; Steidinger & Williams, 1970, pág. 217; Hermosilla, 1973a, pág. 67, lám. 36, figs. 1-4; Hermosilla, 1973b, pág. 23, lám. 2, fig. 10; Léger, 1973b, pág. 10; Marshall, 1976, pág. 85; Taylor, 1976, pág. 79, pl. 15, fig. 160; Pesantes, 1983, pág. 287, lám. 2, figs. 4-5; Rampi y Bernhard, 1980, pág. 57, tab. 25; Marshall y Solder, 1982, pág. 358; Dodge, 1982, pág. 232, fig. 29F; Balech, 1988, pág. 137, lám. 57, fig. 6; Hernández-Becerril, 1989, pág. 43, fig. 25; Licea et al., 1995, pág. 30, lám. 1, fig. 4; Licea et al., 2004, pág. 423.
Medidas. 98 LT, 45 Trd; 96 LT, 41 Trd; 93 LT, 45 Trd; 100 LT, 45 Trd.
Distribución Caribe colombiano. Bahía Gaira, arrastre subsuperficial, 21 agosto 2001. Bahía Santa Marta, junio 2004. Bahía Gaira, arrastre subsuperficial, 18 agosto 2006. E258: 5 mayo 2008, frente a La Guajira; E261: 16 mayo 2008, frente departamento Magdalena.
Distribución resto Caribe y golfo de México. Venezuela: estrecho Cariaco, superficial, tolerante (Halim, 1967). Caribe al oeste (Marshall y Solder, 1982). Estrechos de La Florida (Wood, 1968). Golfo de México al noreste (Steidinger y Williams, 1970). Golfo de México al suroeste (Licea et al., 2004).
Distribución mundial. Región del Amazonas, superficial (Wood, 1966). Atlántico sudoccidental: en la corriente de Brasil (Balech, 1988). Costa este de Estados Unidos (Marshall, 1976). Atlántico Norte, común (Gaarder, 1954). Entre Islandia e islas Feroes, Atlántico y Pacífico ecuatorial (Halim, 1967). Sobre el Atlántico en la Corriente del Golfo hasta Inglaterra y más hacia el norte, difundida en el Mediterráneo, en aguas cálidas, interoceánica (Schiller, 1937). Común en la corriente del Golfo al oeste y al norte de las islas Británicas (Dodge, 1982). Islas Azores, golfo de Bizcaya, cono sur-africano (Jorgensen, 1911). Atlántico oriental a la altura de las islas Canarias (Margalef, 1969). Tanto en el Atlántico como en el Pacífico, tropical tolerante, distribución vertical no clara, se encuentra igualmente en superficie como a 50 y 100 m de profundidad (Graham y Bronikovsky, 1944). Mediterráneo: mar de Alborán, Túnez, mar Baleárico, golfo de Lyón, Nápoles, mar Jónico, Adriático, también en bahía de Cádiz, estrecho de Gibraltar, Lisboa, Atlántico norte, océano Índico, mar de Arabia (Jorgensen, 1920). Mediterráneo (Trégouboff y Rosé, 1957; Rampi y Bernhard, 1980). Mediterráneo occidental frente a las costas de Castellón y Valencia (López, 1966). Mediterráneo: Costa este de Córcega (Léger, 1973). Golfo de Guayaquil (Pesantes, 1983). Chile: bahía Concepción (Hermosilla, 1973a); archipiélago de Juán Fernández frente a Chile; también en Panamá, Angola, bahía de Algeria (Hermosilla, 1973b). Pacífico: expedición Downwind (Balech, 1962). Baja California, golfo de California (Hernández-Becerril, 1989; Licea et al., 1995). Australia: este de Australia, Eden, Moreton Bay, Queensland, costa sur de Albany, costa oeste de Australia, Islas Salomón, New Zealand (Wood, 1954). Índico, tropical-subtropical, superficial (Steemann-Nielsen, 1939); Índico: rara en el canal de Mozambique y costas de Natal, temperada, su distribución vertical es incierta (Sournia, 1968). Mar de Andamán, bahía de Bengala, islas Galápagos, en aguas eutróficas (Taylor, 1976).
Neoceratium arietinum (Cleve) f. gracilentum Jörgensen, 1920
(Fig 2D)
Ceratium arietinum f. gracilentum Jörgensen, 1920: pág. 64, fig. 62; Schiller, 1937, pág. 404, fig. 444c; Graham y Bronikovsky, 1944, pág. 31, fig. 16 F, K; Trégouboff y Rosé, 1957, pág. 115, pl. 26, fig. 4; Halim, 1967, pág. 712; Taylor, 1976, pág. 79, pl. 16, fig. 165; Rampi y Bernhard, 1980, pág. 53, tabl. 23; Balech 1988, pág. 143, lám. 61, fig. 6.
C. arietinum var. gracilentum (Jörgensen) Sournia, 1966: Sournia, 1968, pág. 431, fig. 54; Licea et al., 2004, pág. 423. C. arietinum gracilentum: Margalef, 1969, pág. 281. C. arietinum Cleve, 1900: Jörgensen, 1911, pág. 48, Tafel 5, fig. 105; López, 1966, pág. 330, fig. 27; Dodge, 1982, pag. 235, pl. 8, fig. B; Dodge, 1985, pág. 93. Medidas. 142 LT, 31 Trd; 234 LT, 39 Trd.
Medidas. 142 LT, 31 Trd; 234 LT, 39 Trd.
Distribución Caribe colombiano. Bahía Gaira, 01 marzo 2008. E263: 02 junio 2008, frente departamento Bolívar. Es primer registro para el Caribe colombiano.
Distribución resto Caribe y golfo de México. Venezuela: estrecho Cariaco en aguas de afloramiento en octubre de 1960 (Halim, 1967). Golfo de México al suroeste (Licea et al., 2004).
Distribución mundial. Corriente de Brasil, oceánica (Balech, 1988). En aguas cálidas del Atlántico, desde 43° S y el cono africano hasta 37° N en las costas americanas, islas Azores, mar Mediterráneo, rara en el Indico, mar Arábigo, mar Rojo, en el Pacífico conocida solamente del Japón (Jörgensen, 1911). En el Atlántico entre 12° N y 10° S (Halim, 1967). Islas Británicas al norte y al oeste con relación a la corriente del golfo (Dodge, 1982). Atlántico oriental a la altura de las islas Canarias (Margalef, 1969). Atlántico oriental (Dodge, 1985). En la corriente ecuatorial norte en el Atlántico y en el Pacífico tropical este, eutrófica, euriterma, de profundidad (Graham y Bronikovsky, 1944). Mediterráneo: bahía de Cádiz, estrecho de Gibraltar, mares Baleárico, Ligure, Tirreno, Jónico y Adriático (Jörgensen, 1920). Mediterráneo (Trégouboff y Rosé, 1957; Rampi y Bernhard, 1980). Mediterráneo occidental frente a las costas de Castellón y Valencia (López, 1966). Índico: Tuléar en Madagascar y en Mombasa, termófila, la más delicada de las variedades (Sournia, 1968). Índico hacia el sur, tropical (Taylor, 1976). Especie interoceánica, en aguas cálidas, de profundidad, por debajo de los 50 m (Schiller, 1937).
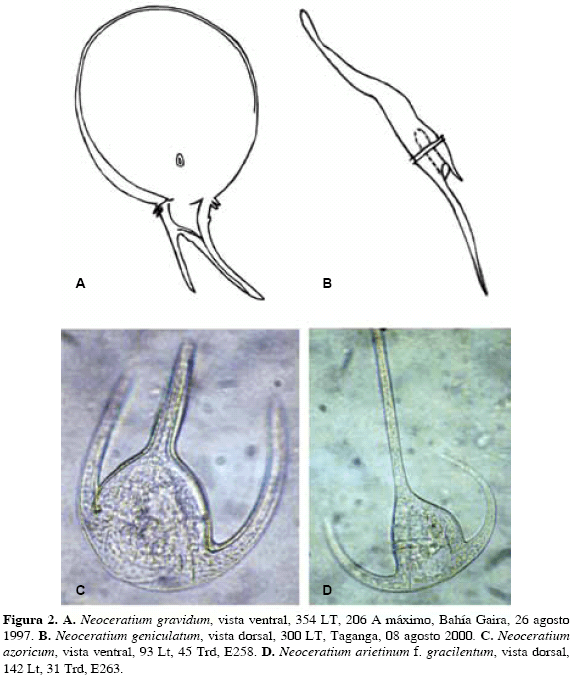
Observaciones. Sournia (1968) le da categoría de variedad. Las formas en Jörgensen (1911) y Dodge (1982, 1985) son semejantes a la de este estudio, pero mencionadas sólo como especies Neoceratium breve (Ostenfeld y Schmidt) forma A (Fig 3A).
Medidas. 217 LT, 56 Trd.
Distribución Caribe colombiano. E265: 04 junio 2008, frente departamento Sucre. Es primer registro para el Caribe colombiano.
Observaciones. De las formas que se muestran en Graham y Bronikovsky (1944), como Ceratium breve (Ostenfeld y Schmidt) Schröder, excepción hecha del ancho del cuerpo que en estas va de 70 a 88 pm, sus figuras 14 N-O, que corresponden a individuos hallados en aguas superficiales, cálidas del Atlántico, son semejantes a la forma en este estudio. Los autores mencionados no consideran variedades, aunque hablan de las formas de transición que presenta la especie y que conectan con otras especies. Esta forma se asimila a Ceratium breve var. schmidtii (Jörgensen) Sournia, 1966: Sournia, 1968, pág. 427, fig. 49, por el ancho del cuerpo (59 Trd en la forma de Sournia). Las demás variedades de la especie presentan cuerpos más anchos, por encima de 60 µm. Sournia considera C. schmidtii Jörgensen: 1911, pág. 50, fig. 110-111 como sinonimia de su variedad, pero aquí no se tiene en cuenta debido también al ancho del cuerpo de la especie de Jörgensen (76 Trd). La forma en este estudio se asemeja también a C. tripos schmidti (Jörgensen) Balech: 1988, pág. 197, lám.58, fig. 7, pero también, en este, el cuerpo es mucho más ancho (70-76 Trd). En la forma, en este estudio, llama la atención la separación amplia, con relación al cuerpo, de los cuernos antapicales. En este sentido, se acerca a las formas de las figuras 14 N-O de Graham y Bronikovsky (1944) y a la forma considerada aquí como C. breve var. curvulum Jörgensen, con las cuales podrían conformar un solo grupo, si no fuera por la diferencia tan marcada en el ancho del cuerpo.
Neoceratium breve (Ostenfeld y Schmidt) var. curvulum Jörgensen, 1911
(Fig 3B, 3C, 3D)
Ceratium breve var. curvulum Jörgensen, 1911: pág. 41, fig. 85; Halim, 1967, pág. 713, pl. 1, fig. 6; Taylor, 1976, pág. 80, pl. 14, fig. 143; Okolodkov y Gárate-Lizárraga, 2006, pág. 19.
C. breve (Ostenfeld y Schmidt) Schröder: Wood, 1954, pág. 288, fig. 209b. (?) C. breve var. parallelum (Schmidt) Jörgensen: Rampi y Bernhard, 1980, pág. 49, tab. 21. (?) C. tripos (O. F. Müller) Nitzsch: Margalef, 1961, pág. 81, fig. 26j.
Medidas. 137 LT, 75 Trd; 242 LT, 82 Trd; 279 LT, 85 Trd.
Distribución Caribe colombiano. Bahía Gaira, 21 agosto 2001. E 265: 04 junio 2008, frente departamento Sucre. E 267: 06 junio 2008, frente departamento Antioquia. Es primer registro para el Caribe colombiano.
Distribución resto Caribe y Golfo de México. Venezuela: Mochima Bay, esporádica (Halim, 1967). Entre Cuba y Haití (Jörgensen, 1911). Puerto Rico: al sur de La Parguera, rara, julio 1958 (Margalef, 1961).
Distribución mundial. Neoceratium breve (sensu lato) es una especie tropical rara; se halla en el Atlántico sobre la costa oeste de África, desde 10° S hasta 15° N; en el Índico, es muy frecuente, desde 25° S 56° E hasta el mar Rojo, mar Arábigo e islas Sonda; la forma más frecuente es var. curvulum (Jörgensen, 1911). Mediterráneo (Rampi y Bernhard, 1980). Costa Pacífica mexicana (Okolodkov y Gárate-Lizárraga, 2006). Costa este australiana, arrecife de la Gran Barrera, corriente Australiana del este, corriente ecuatorial del sur, islas Salomón, región de Panamá (Wood, 1954). Mar Arábigo al este, junto con var. schmidtii (Taylor, 1976).
Observaciones. Las formas halladas se ajustan a las características de Neoceratium breve var. curvulum Jörgensen por la curvatura del cuerno derecho, el ancho del cuerpo, el contorno antapical redondeado y la separación de los cuernos antapicales con relación al cuerpo. Según la revisión bibliográfica, los cuernos antapicales se separan cada vez más del cuerpo, en el siguiente orden, en Taylor (1976), Halim (1967) y Jörgensen (1911). La separación de los cuernos antapicales del cuerpo, de las formas halladas en este estudio, es más amplia que la de los autores aquí anotados. Las formas en este estudio son muy semejantes a C. breve var. paralellum (Schmidt) Jörgensen: Rampi y Bernhard (1980) y a C. tripos (O. F. Müller) Nitzsch: Margalef (1961), y es posible que ambas sean la misma var. curvulum. El ángulo de inclinación del cinturón con respecto al contorno del borde posterior del cuerpo (12°), de la figura 3C, es semejante al de las formas aquí comparadas. Este mismo ángulo, en la figura 3B, es mayor (15-20°). No se tuvo en cuenta la longitud del cuerno apical, pues en una colonia de Neoceratium, la longitud del cuerno apical de las células puede variar. Wood (1954), no considera variedades, les da el mismo valor específico.
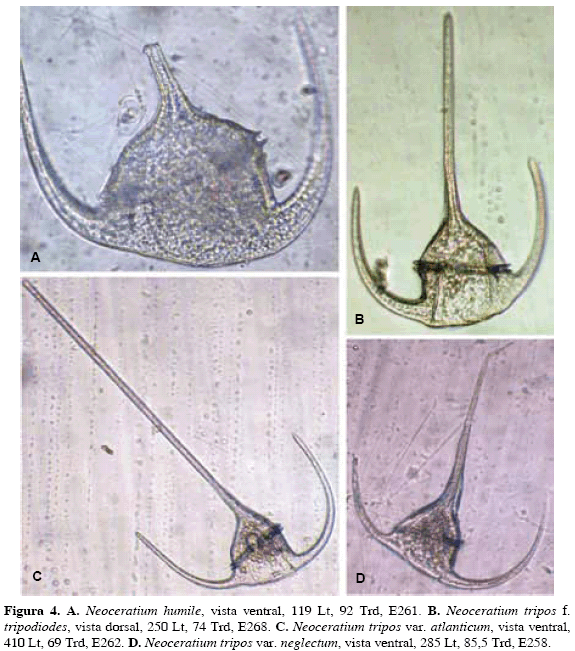
Neoceratium humile (Jörgensen) Gómez, Moreira et López-García, 2010
(Fig 4A)
Gómez, Moreira et López-García, 2010: pág. 12, tabla 2.
Ceratium humile Jörgensen, 1911: pág. 40, fig. 82-83; Böhm, 1931, pág. 45; Schiller, 1937, pág. 390, fig. 428; Steemann-Nielsen, 1939, pág. 11; Graham y Bronikovsky, 1944, pág. 27, fig. 14A; Wood, 1954, pág. 287, fig. 208; Halim, 1967, pág. 721, pl. 1, fig. 12; Wood, 1968, pág. 32, fig. 66; Steidinger y Williams, 1970, pág. 46; Taylor, 1976, pág. 84, pl. 14, fig. 148; Okolodkov y Gárate-Lizárraga, 2006, pág. 29.
Medidas. 119 LT, 92 Trd.
Distribución Caribe colombiano. E261: 16 mayo 2008, frente departamento Magdalena. Es primer registro para el Caribe colombiano.
Distribución resto Caribe y golfo de México. Venezuela: bahía de Mochima, golfo de Cariaco, estrecho Cariaco (Halim, 1967). Northwest Providence Channel, estrechos de La Florida, en el verano (Wood, 1968). Golfo de México al noreste (Steidinger y Williams, 1970).
Distribución mundial. En el Atlántico sobre la Corriente del Golfo, superficial, un solo ejemplar (Graham y Bronikovsky, 1944). Pacífico: en aguas cálidas, nerítica, rara (Schiller, 1937). Costa pacífica mexicana (Okolodkov y Gárate-Lizárraga, 2006). Región australiana: Bahía Storm en Tasmania en octubre de 1950, en la corriente ecuatorial a lo largo de la costa de New South Wales, Nueva Caledonia y Fiji, islas Salomón y al este de Australia (Wood, 1954). Índico: Estrecho Malaca y costa de Sumatra (Böhm, 1931). Aguas asiáticas del este, mar de Arafura, arrecife de la Gran Barrera (Steemann-Nielsen, 1939). Índico: bahía de Bengala, mar de Andamán, también al suroeste (Taylor, 1976). Japón: costa de Shirahama (Jörgensen, 1911).
Observaciones. La forma en este estudio se acerca mucho a la forma en Taylor (1976), encontrada en el Índico, por el contorno antapical casi plano, la inclinación marcada del cinturón y la separación y desarrollo de los cuernos antapicales. La forma en Taylor (1976), a su vez, se asemeja a la forma descrita por Jörgensen (1911), para el Japón, aunque difiere en que esta última presenta un mayor desarrollo del cuerno antapical derecho. La forma en este estudio se aleja mucho de las formas encontradas por Wood para el Pacífico (1954) y el Golfo de México y Caribe (1968). No se pudo comparar con la forma en Steidinger y Williams (1970), registrada para el golfo de México, pues el trabajo no trae figura de la especie.
Neoceratium tripos (O.F. Müller) tripodiodes Jörgensen
(Fig 4B)
Ceratium tripos tripodioides Jörgensen: Steemann Nielsen, 1939, pág. 10; Balech 1988, pág. 139, lám. 59, fig. 3-4; (?) Fernández y García, 1998, pág. 541, fig. 2.
C. tripos f. tripodiodes (Jörgensen) Paulsen, 1930: Wood, 1954, pág. 285, fig. 205c. C. tripos tripodiodes: Margalef, 1969, pág. 281; Non C. tripos var.
164 atlanticum Ostenfeld: Halim, 1967, pág. 725, pl. 2, fig. 26; Steidinger y Williams, 1970, pág. 47, pl. 14, fig. 37a; Vidal, 1995, lám. 29, fig. 261.
Medidas. 250 LT, 74 Trd.
Distribución Caribe colombiano. Ciénaga Grande de Santa Marta (Vidal, 1995). (?) Golfo de Salamanca (Fernández y García, 1998). E258: 05 mayo 2008, frente a La Guajira; E268: 07 junio 2008, frente departamento Antioquia.
Distribución resto Caribe y golfo de México. Venezuela: golfo de Paria (Halim, 1967). Golfo de México al noreste (Steidinger y Williams, 1970).
Distribución mundial. Atlántico sudoccidental provincias de Buenos Aires y Uruguay, región de Quequén, Puerto Deseado, en aguas cálidas y frías (Balech, 1988). Atlántico oriental a la altura de las Islas Canarias (Margalef, 1969). Pacífico Sur (Steemann-Nielsen, 1939). Australia este, islas Salomón (Wood, 1954).
Observaciones. La forma en este estudio presenta los cuernos antapicales orientados ligeramente hacia adentro, en la forma de Balech (1988), están distalmente orientados hacia fuera y el trasdiámetro del cuerpo es menor (62-68). Las formas en Halim (1967) y Steidinger y Williams (1970) concuerdan con la forma en este estudio: el ángulo de inclinación del cuerno apical con respecto al cinturón (92 y 94° respectivamente) en aquellos, es semejante al ángulo (92°), de la forma aquí considerada. Igualmente, los anchos de sus cuerpos (78 y 74 Trd respectivamente) también corresponden. La forma en Fernández y García (1998), parecería corresponder a la de este estudio, aunque el ángulo de inclinación del cuerno apical con relación al cinturón es menor (87°) y la curvatura posterior de la célula tampoco se presenta tan uniforme como en la forma tripodioides (ver: este estudio; Balech, 1988). Esta forma ya había sido colectada en la CGSM por Carmona (1979), en los meses de junio y agosto de 1978, en el sitio de la Barra que comunica con el mar; fue registrada por Vidal (1995). Ceratium tripos f. tripodioides (Jörgensen) Paulsen, en Schiller, 1937, pág. 384, fig. 421b es copia del mismo C. pulchellum f. tripodioides Jörgensen: 1920, pág. 54, fig. 42, que no se considera semejante a la forma en este estudio. Ceratium tripodioides (Jörgensen) Steemann Nielsen, que equivale a la forma aquí considerada, es sinonimia de C. tripos (O.F. Müller) Nitzsch, según Gómez, Moreira et López-García, 2010, pág. 14, tabla 2.
Neoceratium tripos (O.F. Müller) var. atlanticum (Ostenfeld) Paulsen, 1907
(Fig 4C)
Ceratium tripos var. atlanticum (Ostenfeld) Paulsen, 1907: Sournia, 1968, pág. 419, fig. 43; Taylor, 1976, pág. 88, pl. 14, fig. 149, 151; Rampi y Bernhard, 1980, pág. 57, tab. 25; Hernández-Becerril, 1989, pág. 42, fig. 17; Licea et al., 2004, pág. 424; Okolodkov y Gárate-Lizárraga, 2006, pág. 38.
C. tripos var. atlanticum Ostenfeld, 1903: Jörgensen, 1920, pág. 48, fig. 33-34; Nie, 1936, pág. 50; Wood, 1954, pág. 285, fig. 205a; López, 1966, pág. 362, fig. 33, foto 2.3; Marshall, 1976, pág. 85. C. tripos atlanticum: Margalef, 1969, pág. 281. C. tripos var. pulchellum (Schröder) López ex Sournia: Licea et al., 1995, pág. 49, lám. 5, fig. 7. C. tripos subsp. semipulchellum (Jörgensen): Graham y Bronikovsky, 1944, pág. 26, fig. 13 L-N, chart 19, appendix table 23. C. pulchellum f. semipulchellum Jörgensen: 1920, pág. 54, fig. 43; Schiller, 1937, pág. 387, fig. 423 a-b. C. pulchellum f. tripodioides Jörgensen: 1920, pág. 50-56, fig. 41, 42, 45. Non C. tripos f. tripodioides (Jörgensen) Paulsen, 1930: López, 1966, pág. 362, fig. 34, foto 2.2.
Medidas. 410 LT, 69 Trd.
Distribución Caribe colombiano. E262: 17 mayo 2008, frente departamento Magdalena. Es primer registro para el Caribe colombiano.
Distribución resto Caribe y golfo de México. Golfo de México al suroeste (Licea et al., 2004).
Distribución mundial. Costa este de los Estados Unidos (Marshall, 1976). Atlántico en aguas cálidas, oligotrófico, superficial pero también a 50 y 100 m de profundidad; también en el Pacífico sudeste y al noreste del Japón (Graham y Bronikovsky, 1944). Golfo de Bizcaya, bahía de Cádiz, estrecho de Gibraltar, Mediterráneo en Málaga, mar de Alborán, mar Baleárico, costa africana en Túnez, mar Tirreno, Nápoles, mar Jónico, mar Egeo (Jörgensen, 1920). Atlántico oriental a la altura de las islas Canarias (Margalef, 1969). Mediterráneo occidental: frente a las costas de Castellón y Valencia (López, 1966). Mediterráneo (Rampi y Bernhard, 1980). Baja California, golfo de California (Hernández-Becerril, 1989; Licea et al., 1995). Costa pacífica mexicana (Okolodkov y Gárate-Lizárraga, 2006). Australia al este, Nueva Zelanda, Georgia del Sur y sub-Antártico (Wood, 1954). Mar de China: isla Hainan (Nie, 1936). Índico: Tuléar y Nossi-Bé en Madagascar, isla Mauricio, en mares templados y tropicales (Sournia, 1968). Índico: mar de Andamán y bahía de Bengala, en ambas regiones bajo la influencia de ríos, golfo de Adén (Taylor, 1976). En aguas cálidas de todos los océanos y mares circumvecinos, estenohalina y euhalina (Schiller, 1937).
Observaciones. Esta forma es muy semejante a las de Schiller (1937), como C. pulchellum f. semipulchellum, tanto en la gracilidad de la forma como por la longitud de los cuernos antapicales. Por su forma, concuerda también, en todos sus aspectos, con C. tripos var. pulchellum (Licea et al., 1995), registrado para el golfo de California. Es semejante también a C. pulchellum f. tripodioides (Jörgensen, 1920, fig. 41, 42, 45), tanto por la forma del cuerpo, como por la longitud de los cuernos antapicales, siendo un poco más largos en las figuras 41 y 45 de este autor. Por la forma grácil se asemeja también a C. pulchellum f. semipulchellum (Jörgensen 1920, fig. 43); aún así, en éste, los cuernos antapicales son más cortos y orientados ligeramente hacia fuera. La forma C. tripos var. atlanticum Ostenfeld (Steidinger y Williams, 1970, pág. 47, fig. 37a), ha sido considerada en este estudio como var. tripodioides Jörgensen, pues el ángulo de inclinación del cuerno apical con respecto al cinturón (94°), es mucho más abierto que en la variedad aquí considerada (88°). Ceratium tripos f. tripodioides (Halim, 1967, pág. 726, pl. 2, fig. 27), registrada para las costas venezolanas, concuerda con las características de la variedad aquí tratada, inclusive en el ángulo de inclinación del cuerno apical con respecto al cinturón (87°), pero difiere en que el ancho del cuerpo es mucho menor (50 Trd). Ceratium tripos subsp. semipulchellun (Jörgensen) Graham y Bronikovsky (Pesantes, 1983, pág. 297, lám. 11, fig. 1-2), registrada para el golfo de Guayaquil, podría corresponder a esta variedad, su forma es la misma, pero el ancho del cuerpo también es menor (49-57 Trd). C. tripos f. tripodioides (Jörgensen) Paulsen, 1930 (López, 1966, pág. 362, fig. 34, foto 2.2), presenta el ángulo de inclinación del cuerno apical con respecto al cinturón de 89°, acercándose más a var. atlanticum que a f. tripodioides.
Ceratium tripos var. neglectum (Ostenfeld) Paulsen, 1908
(Fig 4D)
Balech 1988, pág. 139, lám. 59, fig. 5-6; Licea et al., 2004, pág. 424.
C. tripos var. atlanticum f. neglectum (Ostenfeld) Paulsen: Jörgensen, 1911, pág. 37, Tafel 4, fig. 74; Sournia, 1968, pág. 422, fig. 44. Non C. arcuatum Cleve var. robustum (Karsten): Böhm, 1931, pág. 26, fig. 23.
Medidas. 285 LT, 85,5 Trd.
Distribución Caribe colombiano. E258, 259: 05-06 mayo 2008, frente a La Guajira. Es primer registro para el Caribe colombiano.
Distribución resto Caribe y golfo de México. Golfo de México al suroeste (Licea et al., 2004).
Distribución mundial. Abundante en el Atlántico al norte, costas de Noruega al oeste (Jörgensen, 1911). Atlántico sudoccidental, en aguas frías (Balech, 1988). Pacífico oeste entre Hongkong y Shanghai (Böhm, 1931). Índico: Tuléar en Madagascar (Sournia, 1968).
Observaciones. La forma de este estudio encaja muy bien con la de Jörgensen (1911) por el ancho del cuerpo, las membranas adheridas a la base del cuerno apical y la amplitud de los cuernos antapicales. Se asemeja también a la forma de Balech (1988) aunque, curiosamente, en esta última es el cuerno antapical izquierdo el que presenta una orientación más pegada al cuerpo. Normalmente, en las especies del género, el cuerno antapical izquierdo es más estable en orientación y longitud que el derecho, el cual varía más en estas características. Sournia (1968), reproduce la forma de Jörgensen. La forma C. arcuatum Cleve var. robustum Karsten (Böhm, 1931, fig. 23), coincide, en todos sus aspectos, con Ceratium tripos var. neglectum (Ostenfeld) Paulsen (Balech, 1988, lám. 59, fig. 6). No se explica porqué el autor le aplicó este nombre pues, C. arcuatum (sinónimo de C. euarcuatum Jörgensen), es una forma distinta, con el borde posterior del lado derecho completamente inclinado (Balech, 1988, pág. 144, lám. 61, fig. 8). Var. neglectum no ha sido cambiada al género Neoceratium, pues es considerada sinonimia de N. tripos (O.F. Müller) Gómez, Moreira et López-García, 2010: pág. 14, tabla 2.
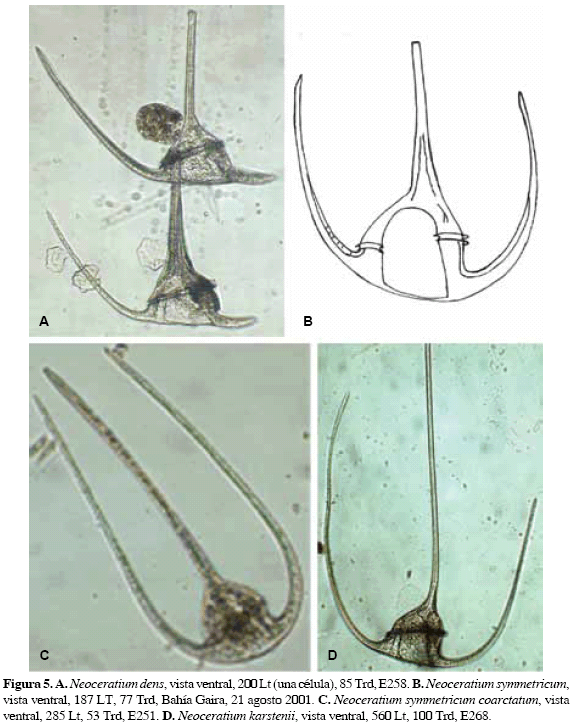
Neoceratium dens (Ostenfeld y Schmidt) Gómez, Moreira et López-García, 2010
(Fig 5A)
Gómez, Moreira et López-García, 2010: pág. 12, tabla 2.
Ceratium dens Ostenfeld y Schmidt, 1901: Jörgensen, 1911, pág. 31, pl. 3, fig. 58; Böhm, 1931, pág. 15, fig. 11 a-e; Nie, 1936, pág. 44, fig. 14; Schiller, 1937, pág. 381, fig.420 a-b; Steemann-Nielsen, 1939, pág. 9, fig. 5; Wood, 1954, pág. 284, fig. 204; Sournia, 1968, pág. 457, fig. 80; Taylor, 1976, pág. 68, pl. 17, fig. 172.
Medidas. 162 LT, 90 Trd; 182 LT, 85 Trd; 200 LT, 85 Trd.
Distribución Caribe colombiano. Bahía Gaira: 11° 12' 47' N, 74° 15'W, 24 agosto 2007; 11° 12'N, 74° 15'W, 01 marzo 2008, una célula; 11° 12'N, 74° 13'W, 19 noviembre 2008, tres células. E 252, 21 febrero 2008, golfo de Salamanca; E 253, 255, 256, 258, 02-05 mayo 2008, frente departamento La Guajira; E 267, 06 junio 2008, frente departamento Antioquia. Es primer registro para el Caribe colombiano.
Distribución resto Caribe y golfo de México. Sin registros para el Caribe y el golfo de México.
Distribución mundial. Índico: mar Rojo, mar Arábigo, costa este africana, Sumatra, también en golfo de Tailandia, Bangkok, costa este de Malacca, en aguas cálidas, rara, restringida a la zona tropical (Jörgensen, 1911). Índico, Pacífico y mares vecinos (Schiller, 1937). Índico, mar Asiático este, Australia en el arrecife de la Gran Barrera (Steemann-Nielsen, 1939). Índico: Canal de Mozambique en Nossi-Bé, golfo de Adén, islas Seychelles, también en islas Marquesas, nerítica (Sournia, 1968). Índico: mar Arábigo, golfo de Bengala, mar de Andamán (Taylor, 1976). Pacífico oeste entre Hongkong y Singapore, tropical (Böhm, 1931). Mar de China: isla Hainan (Nie, 1936). Al noreste de Australia, arrecife de la Gran Barrera, Estrecho Torres, isla Montague, Nueva Irlanda, islas Salomón, mar de Timor, especie indicadora de corrientes (Wood, 1954).
Observaciones. Esta especie está aparentemente restringida al Indopacífico (Sournia, 1970). Se encontró por primera vez en agosto del 2007 en la bahía Gaira, Caribe colombiano, solitaria o en pareja. Según la revisión bibliográfica, sus registros en el Pacífico se refieren sólo al Pacífico oeste y no se conocen registros de la especie para el Atlántico y mares adyacentes. Este sería el primer registro de la especie para esta parte del Atlántico. Es posible que su ingreso a la región se haya hecho en aguas de lastre. Por la distribución local (Tabla 2), se confirma que ya se encuentra distribuida a todo lo largo de la costa Caribe colombiana. Las formas de las figuras 3-5 de la lámina 69 en Balech (1988), identificadas como C. dens Ostenfeld y Schmidt, que presentan el cuerno apical ligeramente inclinado a la derecha y el cuerno antapical derecho apenas en desarrollo, no corresponden a esta especie. De la misma manera, las formas nominadas C. dens (Pesantes, 1983, pág. 298, lám. 13, fig. 3-4; Licea et al., 1995, pág. 34, lám. 18, fig. 2), registradas para el golfo de Guayaquil y el golfo de California respectivamente, son iguales o semejantes a la forma de la fig. 3 en Balech (1988) y, por lo tanto, no corresponden tampoco a esta especie.
Neoceratium symmetricum (Pavillard) Gómez, Moreira et López-García, 2010
(Fig 5B)
Gómez, Moreira et López-García, 2010: pág. 14, tabla 2.
Ceratium symmetricum Pavillard, 1905: Schiller, 1937, pág. 401, fig. 441d; Steemann-Nielsen, 1939, pág. 12; Graham y Bronikovsky, 1944, pág. 29, fig. 15 H-I, chart 24, appendix table 28; Gaarder, 1954, pág. 15; Wood, 1954, pág. 292, fig. 217a; López, 1966, pág. 330, fig. 29; Halim, 1967, pág. 725, pl. 1, fig. 13; Sournia, 1968, pág. 432, fig. 57; Margalef, 1969, pág. 281; Taylor, 1976, pág. 87, pl. 15, fig. 154; Rampi y Bernhard, 1980, pág. 57, tab. 25; Marshall y Solder, 1982, pág. 359; Balech 1988, pág. 143, lám. 61, fig. 7; Licea et al., 2004, pág. 424; Okolodkov y Gárate-Lizárraga, 2006, pág. 37.
C. gracile var. symmetricum (Pavillard) Jörgensen: 1911, pág. 44, Tafel 5, fig. 94; Jörgensen, 1920, pág. 60, fig. 57-59. Non C. breve: Vidal, 1995, lám. 62, fig. 543-544.
Medidas. 187 LT, 77 Trd.
Distribución Caribe colombiano. Ciénaga Grande de Santa Marta, La Barra, 15 junio 1978 (Vidal, 1995). Bahía Gaira, 21 agosto 2001, arrastre subsuperficial, 15:00. E258: 05 mayo 2008, frente a La Guajira.
Distribución resto Caribe y golfo de México. Venezuela: bahía de Mochima y estrecho Cariaco, rara (Halim, 1967). Caribe al este (Marshall y Solder, 1982). Golfo de México al suroeste (Licea et al., 2004).
Distribución mundial. Corriente de Brasil, termófila y umbrófila (Balech, 1988). Atlántico del Sur en el cono africano hasta 8° S 13° W, entre Cuba y Haití, frecuente y numeroso en el Atlántico a 30° N 57° W, islas Azores, común en el Mediterráneo, África del Norte al oeste a 25° N 27° W; en el Índico desde los 38° S 77° E hasta Cabo Guardafui, golfo de Bengala y Sumatra, en el Pacífico en Japón (Jörgensen, 1911). En el Atlántico y en el Pacífico, en aguas cálidas, en el Pacífico al sudeste, especie tropical ligeramente tolerante, principalmente de penumbra, en aguas oligotróficas (Graham y Bronikovsky, 1944). Región del Atlántico norte (Gaarder, 1954). Atlántico oriental a la altura de las islas Canarias (Margalef, 1969). Mediterráneo: mar de Alborán, también en costas de Portugal, corriente de las Antillas, corriente del Golfo hasta islas Azores, corriente de las Canarias (Jörgensen, 1920). Mediterráneo occidental frente a las costas de Valencia y Castellón (López, 1966). Mediterráneo (Rampi y Bernhard, 1980). Costa pacífica mexicana (Okolodkov y Gárate-Lizárraga, 2006). Aguas asiáticas del este, mar de China Este (Steemann-Nielsen, 1939). Región australiana, corriente ecuatorial del sur, islas Salomón, Nueva Zelanda al norte (Wood, 1954). Índico: Nossi-Bé y Tuléar en Madagascar, canal de Mozambique (Sournia, 1968). Índico al norte (Taylor, 1976).
Observaciones. Esta forma ya había sido colectada en la CGSM por Carmona (1979), en junio 15 de 1978, en el sitio de La Barra que comunica con el mar; fue registrada como C. breve por Vidal (1995).
Neoceratium symmetricum (Pavillard) coarctatum (Pavillard) Graham y Bronikovsky, 1944
(Fig 5C)
Ceratium symmetricum coarctatum (Pavillard) Graham y Bronikovsky, 1944: pág. 29, fig. 15 J-L; Sournia, 1968, pág. 433, fig. 56; Taylor, 1976, pág. 88, pl. 15, fig. 153; Rampi y Bernhard, 1980, pág. 57, tab. 25; Balech, 1988, pág. 144, lám. 61, fig. 9; Licea et al., 1995, pág. 47; Licea et al., 2004, pág. 424; Okolodkov y Gárate-Lizárraga, 2006, pág. 37.
C. symmetricum coarctatum Pavillard: López, 1966, pág. 330, fig. 30. C. symmetricum coarctatum: Margalef, 1969, pág. 281. C. symmetricum Pavillard, 1905: Schiller, 1937, pág. 401, fig. 441 a-b; Trégouboff y Rosé, 1957, pág. 115, pl. 26, fig. 3; Dodge, 1982, pág. 235, fig. 30G. C. coarctatum Pavillard: Halim, 1967, pág. 714, pl. 3, fig. 31. C. gracile α coarctatum (Pavillard) Jörgensen: Jörgensen, 1920, pág. 59, fig. 55. C. gracile (Gourret) Jörgensen: Jörgensen, 1911, pág. 44, fig. 92-93.
Medidas. 285 LT, 53 Trd; 260 LT, 50 Trd.
Distribución Caribe colombiano. E 252: 21 febrero 2008, golfo de Salamanca. Bahía Gaira, 13 febrero 2009. Es primer registro para el Caribe colombiano.
Distribución resto Caribe y golfo de México. Venezuela: estrecho Cariaco, rara, tropical y subtropical, de penumbra (Halim, 1967). Golfo de México al suroeste (Licea et al., 2004).
Distribución mundial. Atlántico sudoccidental: Corriente de Brasil, umbrófila y termófila (Balech, 1988). Atlántico oriental a la altura de las islas Canarias (Margalef, 1969). Atlántico oriental (Dodge, 1982). Mediterráneo: bahía de Cádiz, mar de Alborán, Mediterráneo este, también en Corriente de las Antillas, corriente del Golfo, islas Azores, islas Canarias (Jörgensen, 1920). Mediterráneo occidental, frente a Castellón y Valencia (López, 1966). Mediterráneo (Trégouboff y Rosé, 1957; Rampi y Bernhard, 1980). Pacífico al sudeste (Graham y Bronikovsky, 1944). Golfo de California (Licea et al., 1995). Costa pacífica mexicana (Okolodkov y Gárate-Lizárraga, 2006). Índico: Nossi-Bé y Tulear en Madagascar, canal de Mozambique (Sournia, 1968). Índico: al sur del canal de Mozambique y 30° S al centro (Taylor, 1976).
Observaciones. La forma, en este estudio, es semejante a C. gracile a coarctatum (Jörgensen, 1920, fig. 55), a C. symmetricum Pavillard (Trégouboff y Rosé, 1957) y a C. symmetricum coarctatum Pavillard (López, 1966), todas del Mediterráneo, en las que, inclusive, los brazos antapicales son más cerrados que los de la forma aquí presentada. Esta forma es semejante también a la presentada en Taylor (1976) para el Índico, pero el brazo derecho de su forma es más abierto. Esta forma, con relación a las formas en Rampi y Bernhard (1980) también del Mediterráneo, y en Balech (1988) para el Atlántico sudoccidental, se distancia más pues estas últimas presentan ambos brazos antapicales más abiertos.
Neoceratium longissimum (Schröder) Gómez, Moreira et López-García, 2010
Gómez, Moreira et López-García, 2010: pág. 13, tabla 2.
Ceratium longissimum (Schröder) Kofoid, 1907: Jörgensen, 1911, pág. 82, Tafel 10, fig. 173 a-b; Jörgensen, 1920, pág. 100, fig. 93; Schiller, 1937, pág. 413, fig. 454 a-b; Steemann Nielsen, 1939, pág. 15; Graham y Bronikovsky, 1944, pág. 43, fig. 26 A-B, chart 46, appendix table 51; Gaarder, 1954, pág. 14; Wood, 1954, pág. 299, fig. 228; Margalef, 1957, pag. 92, fig. 2e; Trégouboff y Rosé, 1957, pág. 115, pl. 26, fig. 11; Halim, 1967, pág. 707, 722; Taylor, 1976, pág. 85, pl. 17, fig. 175; Rampi y Bernhard, 1980, pág. 63, tav. 28; Balech, 1988, pág. 150, lám. 61, fig. 10; Licea et al., 1995, pág. 42, lám. 19, fig. 4; Licea et al., 2004, pág. 424; Okolodkov y Gárate-Lizárraga, 2006, pág. 31.
Medidas. 700 LT, 80 Trd (una célula).
Distribución Caribe colombiano. Bahía Gaira, arrastre subsuperficial, 28 enero 2005. Es primer registro para el Caribe colombiano.
Distribución resto Caribe y golfo de México. Venezuela: estrecho Cariaco, en aguas de afloramiento, octubre 1960, una célula (Halim, 1967). Golfo de México al suroeste (Licea et al., 2004).
Distribución mundial. En el Atlántico y en el Pacífico, tropical intolerante, en aguas oligotróficas, exclusivamente de penumbra (Graham y Bronikovsky, 1944). Atlántico: mar de los Sargassos al este, entre 200 y 100 m de profundidad, 24 junio 1910 (Gaarder, 1954). Atlántico sudoccidental termófila intolerante (Balech, 1988). Atlántico, en aguas cálidas (Schiller, 1937). Mediterráneo: Nápoles, Algeria, también en el Atlántico sobre el Ecuador 18° al oeste (Jorgensen, 1911). Mediterráneo: Nápoles, costa Dalmacia, golfo de Lyón, mar Jónico, Taormina, mar de Mármara, también en la corriente ecuatorial del sur, al oeste del golfo de Guinea (Jorgensen, 1920). Mediterráneo oeste: costas de Blanes (Margalef, 1957). Mediterráneo (Trégouboff y Rosé, 1957; Rampi y Bernhard, 1980). Golfo de California, en mares templados y tropicales (Licea et al., 1995). Pacífico mexicano (Okolodkov y Gárate-Lizárraga, 2006). Región australiana, corriente ecuatorial del Pacífico, corriente al este de Australia (Wood, 1954). Océano Índico, de penumbra (Steemann-Nielsen, 1939). Océano Índico al norte y central, mar de Andamán (Taylor, 1976).
Observaciones. Según la revisión bibliográfica, el trasdiámetro de la especie oscila entre 50 y 74 µm, con la mayoría de los datos entre 60 y 70 µm; desde este punto de vista, la célula aquí considerada presenta un trasdiámetro mayor (80 µm). La longitud de la célula sí se encuentra dentro del ámbito dado para la especie (500-1000 µm).
Neoceratium karstenii (Pavillard) Gómez, Moreira et López-García, 2010
(Fig 5D)
Gómez, Moreira et López-García, 2010: pág. 12, tabla 2.
Ceratium karstenii Pavillard, 1907: Jörgensen, 1911, pág. 53, Tafel 5, fig. 116; Schiller, 1937, pág. 393, fig. 431a, fig. 432a; Steemann-Nielsen, 1939, pág. 13; Gaarder, 1954, pág. 12; Wood, 1954, pág. 289, fig. 211 a-b; Trégouboff y Rosé, 1957, pág., pl. 25, fig. 16; Balech, 1962, pág. 185; Wood, 1966, pág. 108; López, 1966, pág. 332, fig. 37; Caycedo, 1977, pág. 28, lám.10, fig. 3a-c; Halim, 1967, pág. 722, tabla 6, pl. 3, fig. 39; Margalef, 1969, pág. 281; Marshall y Solder, 1982, pág. 359; Balech 1988, pág. 144, lám. 62, fig. 3, lám. 63, fig. 1 y 6.
C. contortum var. karstenii (Pavillard) Sournia: Sournia, 1966, pág. 1981; Sournia, 1968, pág. 442, fig. 71, pl. 3, fig. 10; Steidinger y Williams, 1970, pág. 45, pl. 6, fig. 17a; Taylor, 1976, pág. 81, pl. 18, fig. 184; Pesantes, 1983, pág. 288, lám. 5, fig. 3-4; Rampi y Bernhard, 1980, pág. 53, tabl. 23; Carbonell, 1981, pag. 20, 22, 23; Hernández-Becerril, 1989, pág. 44, fig. 19; Licea et al., 1995, pág. 33, lám. 2, fig. 2; Licea et al., 2004, pág. 423; Okolodkov y Gárate-Lizárraga, 2006, pág. 21. C. contortum (Gourret) Cleve "karstenii-robustum": Carbonell, 1979, pág. 33, lám. 2, fig. 10e. C. arcuatum f. karstenii (Pavillard) Jörgensen: Jörgensen, 1920, pág. 75, fig. 71. C. tripos var. arcuatum Gourret, 1883, pág. 25, pl. 2, fig. 42. C. longinum Karsten, 1906: Nie, 1936, pág. 57, fig. 24. C. schrankii Kofoid, 1907: Kofoid, 1907b, pág. 306, pl. 28, fig. 29a-31; Taylor, 1976, pág. 87, pl. 17, fig. 176-177; Carbonell, 1981, pags. 20, 22, 23, lám. 13, fig. 83; Carbonell, 1982, pág. 76, 88, lám. 2, fig. 15; Licea et al., 1995, pág. 46. Non C. contortum Cleve: Graham y Bronikovsky, 1944, pág. 175, fig. 18K.
Medidas. 473 LT, 91 Trd; 560 LT, 100 Trd.
Distribución Caribe colombiano. Bahía Nenguange, Parque Nacional Tayrona (Caycedo, 1977). Islas del Rosario (Carbonell, 1982). La Guajira, 18 noviembre 1995 (dato no publicado). Bahía Gaira, 21 agosto 2001, 15:00, arrastre subsuperficial. E 268: 07 junio 2008, frente departamento Antioquia.
Distribución resto Caribe y golfo de México. Venezuela: bahía de Mochima y estrecho de Cariaco, muy común (Halim, 1967). República Dominicana al sur (Carbonell, 1981). Al centro y al este del Caribe (Marshall y Solder, 1982). Golfo de México al noreste (Steidinger y Williams, 1970). Golfo de México al suroeste (Licea et al., 2004).
Distribución mundial. Atlántico, frecuente en todas sus aguas cálidas, desde el cono surafricano y La Plata hasta 37° N en la costa este americana, en la corriente del golfo hasta 48° N, costa suroeste de Irlanda hasta 56° N 36° W, Mediterráneo, Índico desde 36° S hasta el mar Rojo y Sumatra, mar de China en el Pacífico entre Taiwán y Futschou (Jörgensen, 1911). Brasil: región del Amazonas, rara (Wood, 1966). Corriente de Brasil, en aguas superficiales, cálidas (Balech, 1988). Bahía Española frente al estrecho de Gibraltar, común en la ruta del Atlántico al sur y un solo individuo en la ruta del Atlántico al norte, también en el Mediterráneo (Gaarder, 1954). Atlántico oriental a la altura de las islas Canarias (Margalef, 1969). Mediterráneo: golfo de Marsella (Gourret, 1883). Mediterráneo: Sicilia (Jörgensen, 1920). Mediterráneo (Trégouboff y Rosé, 1957; Rampi y Bernhard, 1980). Mediterráneo occidental frente a las costas de Castellón y Valencia (López, 1966). Ecuador: golfo de Guayaquil, en diciembre, escasa (Pesantes, 1983). Costa pacífica mexicana (Okolodkov y Gárate-Lizárraga, 2006). California: San Diego (Kofoid, 1907b). Frente a California (Graham y Bronikovsky, 1944). Pacífico: expedición Downwind (Balech, 1962). Baja California, Golfo de California (Hernández-Becerril, 1989; Licea, et al. 1995). Australia este, Nueva Zelanda al norte, Islas Salomón, Corriente Ecuatorial del Sur (Wood, 1954). Mar de China: isla Hainan (Nie, 1936). Índico, superficial, tropical-subtropical, interoceánica (Steemann-Nielsen, 1939). Índico: mar de Andamán al norte, Golfo de Bengala al oeste, en aguas cálidas, también en el canal de Mozambique (Taylor, 1976).
Observaciones. Las formas, en este estudio, presentan los cuernos antapicales orientados hacia adelante de la región ventral, característica que no es mencionada por los autores consultados.
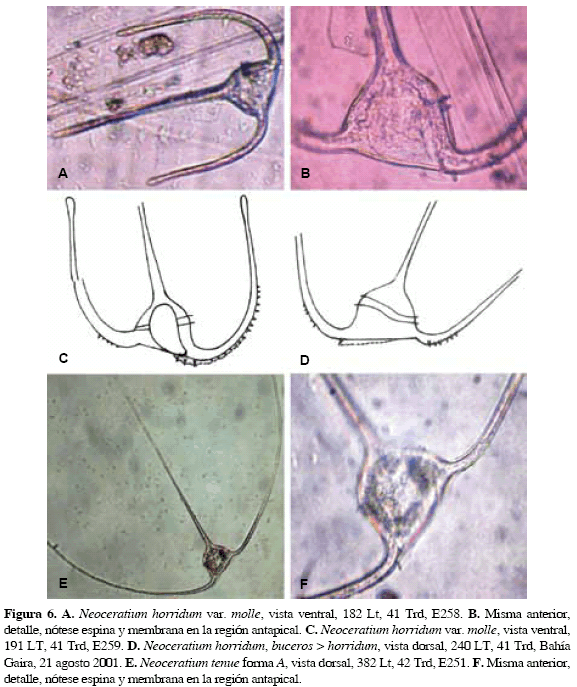
Neoceratium horridum (Gran) var. molle (Kofoid) Jorgensen, 1911
(Figs 6A, 6B y 6C)
Ceratium horridum var. molle (Kofoid) Jörgensen, 1911: Graham y Bronikovsky, 1944, pág. 42, fig. 23 I, K, fig. 25D; Halim, 1967, pág. 721, tabla 6, pl. 1, fig. 11, pl. 10, fig. 153; Balech 1988, pág. 149, lám. 65, fig. 8; Licea et al., 1995, pág. 40, lám. 3, fig. 4; Licea et al., 2004, pág. 424.
C. horridum var. molle Böhm, 1931: pág. 41, fig. 36 b-c; Okolodkov y Gárate-Lizárraga, 2006, pág. 29. C. horridum var. molle (Kofoid) Graham y Bronikovsky, 1944: Taylor, 1976, pág. 71, pl.21, fig. 208. C. horridum (Cleve) Gran, horridum > buceros Sournia: 1968, pág. 480, fig. 94; Steidinger y Williams, 1970, pág. 46; Carbonell, 1979, pág. 38, lám. 3, fig. 17a; Rampi y Bernhard, 1980, pág. 63, tab. 28. C. horridum (Cleve) Gran: Margalef, 1969, pág. 281, fig. 5D; Fernández y García, 1998, pág. 546, fig. 12. C. horridum var. claviger (Kofoid) Graham y Bronikovsky, 1944: pág. 42, fig. 23 J, L. C. buceros var. molle (Kofoid) Jörgensen: 1920, pág. 97, fig. 87. C. buceros f. molle (Kofoid) Schiller: 1937, pág. 417, fig. 457a; Wood, 1954, pág. 303, fig. 231g. C. mollis Kofoid: Kofoid, 1907b, pág. 304, lám. 27, fig. 26; Jörgensen, 1911, pág. 81, Tafel 9, fig. 170; Steemann-Nielsen, 1939, pág. 15. C. claviger Kofoid, 1907a: pág. 170, pl. 4, fig. 27. Non C. claviger Kofoid: Jörgensen, 1911, pág. 80, Tafel 9, fig. 169. Non C. longinum Karsten: Fernández y García, 1998, pág. 543, fig. 7.
Medidas. 182 LT, 41 Trd; 194 LT, 41 Trd; 200 LT, 38 Trd; 275 LT, 43 Trd.
Distribución Caribe colombiano. Bahía de Cartagena, entre Tierra Bomba y Castillo Grande, marzo 1976, un ejemplar (Carbonell, 1979). La Guajira, 18 noviembre 1995 (dato no publicado). Golfo de Salamanca (Fernández y García, 1998). Bahía Gaira, 21 agosto 2001. Bahía de Santa Marta, junio 2004. E 258, 259: 05-06 mayo 2008, frente a La Guajira. E 261, 262: 16-17 mayo 2008, frente departamento Magdalena.
Distribución resto Caribe y golfo de México. Venezuela: bahía de Mochima, estrecho Cariaco, golfo Cariaco, golfo de Paria, hallada en superficie, común hasta dominante (Halim, 1967). Golfo de México al noreste (Steidinger y Williams, 1970). Golfo de México al suroeste (Licea et al., 2004).
Distribución mundial. Corriente de Brasil, termófila (Balech, 1988). Atlántico en Indias occidentales danesas, 20° N 33° W, 14° S 6° W, Mediterráneo en Mónaco y Nápoles, Pacífico en San Diego California, Mar Rojo en el Índico (Jörgensen, 1911). En el Atlántico en la corriente ecuatorial del norte, en la corriente del golfo y en el Atlántico norte; en el Pacífico frente a California y entre isla Samoa e isla Phoenix (Graham y Bronikovsky, 1944). Atlántico oriental a la altura de las islas Canarias (Margalef, 1969). Mediterráneo: Nápoles (Jörgensen, 1920). Mediterráneo (Rampi y Bernhard, 1980). California: San Diego (Kofoid, 1907b). Golfo de California (Licea et al., 1995). Costa pacífica mexicana (Okolodkov y Gárate-Lizárraga, 2006). Pacífico tropical este (Kofoid, 1907a). Región australiana, corriente ecuatorial, Nueva Zelanda (Wood, 1954). Pacífico oeste: Shangai-Hongkong y Hongkong-Singapore (Böhm, 1931). Índico, umbrófila, tropical-subtropical, nétamente oceánica (Steemann-Nielsen, 1939). Índico: canal de Mozambique (Sournia, 1968). Índico: al sur de la India, costa este de la India, golfo de Bengala (Taylor, 1976).
Observaciones. La figura 169 de Jörgensen (1911), como C. claviger, es semejante a la forma en este estudio, concordando en todas sus características; con la de Sournia (1968), coincide en casi todas sus características, excepto en el ancho del cuerpo (60 Trd en este autor); con la fig. 87 de Jörgensen (1920), como C. buceros var. molle, difiere en que ésta presenta el cuerno antapical izquierdo dirigido hacia el cuerno apical en su región distal; no especifica medidas del ancho del cuerpo pero, como se refiere a ésta como una forma delicada, es posible que coincida en el ancho del cuerpo; la forma que se muestra en Rampi y Bernhard (1980), presenta los cuernos antapicales un poco más cerrados, en las demás características es semejante.
Neoceratium horridum (Gran) buceros > horridum Sournia
(Fig 6D)
Ceratium horridum, buceros > horridum Sournia, 1968: pág. 478, fig. 93. C. tenue (Ostenfeld y Schmidt) Jörgensen: 1911, pág. 77, pl. 9, fig. 163.
Medidas. 240 LT, 41 Trd.
Distribución Caribe colombiano. Bahía Gaira, 21 agosto 2001. Es primer registro para el Caribe colombiano.
Distribución mundial. Canal de Mozambique (Sournia, 1968).
Observaciones. Esta forma presenta el cuerno antapical derecho anguloso en su extremo proximal, coincidiendo en esto con la forma de Sournia (1968) y también con la forma de Jörgensen (1911) que, según el primer autor, corresponde a su forma.
Neoceratium tenue (Ostenfeld y Schmidt) forma A
(Figs. 6E, 6F)
Medidas. 382 LT, 42 Trd.
Distribución Caribe colombiano. E 252: 21 febrero 2008, golfo de Salamanca. Es primer registro para el Caribe colombiano.
Observaciones. Esta forma se caracteriza por su gracilidad, tener un cuerpo angosto (ca 40), una curva suave de los cuernos antapicales al salir del cuerpo que, luego se proyectan en una curva amplia con relación al cuerno apical y presencia de espina y membrana en la base, región posterior, del cuerno antapical izquierdo. Se asemeja a C. tenue tenuissimum (Kofoid) Balech: 1988, pág. 150, lám. 66, fig. 3, a C. buceros tenuissimum Jörgensen: 1920, pág. 97, fig. 89, a C. tenue var. buceros (Zacharias) Jörgensen: 1911, pág. 78, Tafel 9, fig. 165-166 y a C. tenuissimum Kofoid: 1907b, pág. 307, pl. 29, fig. 32-33. Con relación a los anteriores posee las mismas características anotadas arriba, excepto la proyección de los cuernos antapicales que, en éstos, es perpendicular al cuerno apical, semejando las alas extendidas de un ave en vuelo. La forma en este estudio se asemeja, a primera vista, a las variedades de C. carriense Gourret: var. carriense y var. volans (Cleve) Jörgensen (ver: Trégouboff y Rosé, 1957, pl. 26, fig. 16; López 1966, pág. 333, fig. 49; Steidinger y Williams, 1970, pág. 44, fig. 14 a-b; Rampi y Bernhard, 1980, pág. 65, tab. 29; Balech, 1988, pág. 148, lám. 65, fig. 1-2), por la proyección de los cuernos antapicales, pero, en esta especie, el cuerpo es más ancho (60-70), los cuernos antapicales, al salir del cuerpo, forman un ángulo más pronunciado y no existe espina en la base del cuerno antapical izquierdo; puede existir una membrana en la concavidad que forman los cuernos antapicales con el borde posterior del cuerpo. Así, la forma en este estudio no concuerda en todos sus aspectos con ninguna de las variedades anteriores. Neoceratium tenue (Ostenfeld y Schmidt) aparece habilitado en Gómez et al., (2010, pág. 14), pues previamente habia sido considerado como sinonimia de C. horridum (Cleve, 1897) Gran, 1902: Gómez (2005, pág. 175).
DISCUSIÓN
Con relación al número de taxones y la suma de los porcentajes de los taxones en las estaciones (Tabla 2), se halló alguna relación directa entre estas dos variables, aunque esta relación no se da en todos los casos: en algunos, a un bajo número de taxones se corresponde un porcentaje relativamente alto (E259) y, viceversa, a un porcentaje bajo se corresponde un número de taxones relativamente alto (E252). La suma de los porcentajes de la contribución del género Neoceratium dentro de la muestra (Tabla 2) va desde 0.4 % (E249), hasta 13 % (E259). Sólo hay tres porcentajes relativamente altos: 12.4 % (E258), 13 % (E259) y 9.9 % (E262); cuatro relativamente medios, desde 4.4 % hasta 5.6 %: 4.4 % (E267), 4.7 % (E261, E256) y 5.6 % (E253); los demás son relativamente bajos y se consideran desde 0.4 % hasta 3.3 %. Los porcentajes más altos corresponden a estaciones geográficamente cercanas entre sí, frente a los departamentos de La Guajira y el Magdalena. Los porcentajes considerados medios corresponden, también, a estaciones frente a estos mismos departamentos y uno frente al departamento de Antioquia, en el extremo suroeste de la costa Caribe colombiana. Los porcentajes más bajos corresponden a estaciones repartidas frente a todos los departamentos, pero muestran un patrón de valores seguidos, frente a Bolívar, Sucre y Córdoba. La distribución planteada, posiblemente, está ligada a la distribución de las masas de agua frente a la costa Caribe colombiana: las estaciones frente a La Guajira y el Magdalena, presentan menos influencia continental [26.13 °C promedio (0.54 SD), salinidad promedio 36.56 (0.21 SD)], a través de los ríos Ranchería y aquellos provenientes de la Sierra, que aquellas estaciones frente a Bolívar, Sucre, Córdoba y Antioquia [28.6 °C promedio (0.2 SD), salinidad promedio 35.27 (0.52 SD)], que tienen la influencia de los ríos Magdalena, Sinú y Atrato y pueden alcanzar un caudal alto durante la primera temporada de invierno.
De los 30 taxones registrados en las estaciones frente a La Guajira y el Magdalena (Tabla 2), 17 son de ambiente oceánico, cinco están adaptados a vivir indistintamente en ambientes oceánico y nerítico, siete son de ambiente nerítico y uno aparece como indeterminado. Neoceratium teres, aunque en la literatura consultada aparece como una especie de ambiente oceánico, aquí se consideró de ambiente nerítico, pues según su distribución se localizó más que todo hacia el sur en la costa Caribe, reflejando que está adaptada a un ambiente con clara influencia continental. Los taxones oceánicos están adaptados a salinidades de aguas abiertas y, posiblemente, se afectan ante masas de agua con salinidades más bajas (en aquellos sitios con marcada influencia continental), o algunos de ellos, tengan la capacidad de evitar dichas masas de agua. Los porcentajes bajos 0. 4 y 1. 6 %, correspondientes a las estaciones E249 y E252, localizadas frente al departamento del Magdalena y muestreadas durante el mes de febrero. A pesar de corresponder a una época seca, cuando soplan los vientos alisios y las aguas oceánicas predominan en la región, se consideran que están bajo la influencia de la desembocadura del río La Magdalena (salinidad 33.6 y 33.3 respectivamente). El porcentaje bajo, 1.6 %, se explicaría también por el número total de taxones (85) hallados dentro de la muestra, el más alto de todas las estaciones (Lozano-Duque et al., 2010), haciendo que los porcentajes se distribuyan entre más especies y sean relativamente más bajos.
Cuarenta y siete (47) especies del género Neoceratium, sin contar variedades y formas, aparecen registradas, como Ceratium, para el Caribe colombiano (Tabla 3). Sesenta y tres (63) especies marinas del género Neoceratium, como Ceratium, han sido descritas a nivel global (Gómez, 2005). Cuarenta y cuatro (44) especies son comunes a ambas listas, descontando C. buceros f. tenue (Ostenfeld y Schmidt) Schiller, 1937, que no es considerado en el trabajo de Gómez (2005) y C. tenue Ostenfeld y Schmidt, 1901 y C. inclinatum Kofoid, 1907, que aparecen, en el mismo trabajo, como sinonimia de C. horridum (Cleve, 1897) Gran, 1902. O sea que, en una sección del Caribe colombiano, aparecen registradas el 70 % de las especies marinas del género Neoceratium, como Ceratium, descritas a nivel global (Gómez, 2005).
Gómez et al. (2010) sólo consideraron cambios taxonómicos para las especies, pero no para las variedades y formas, lo que significa que han quedado en una situación incierta. Así, muchos taxones como: N. arietinum f. gracilentum, N. breve forma A, y var. curvulum, N. tripos tripodiodes, var. atlanticum, N. symmetricum coarctatum, N. horridum var molle y N. tenue forma A no han quedado bien ubicadas con sus nombres de autor actualizados, es un tema que aun queda por definir por lo expertos en el tema.
Cuarenta y siete (47) especies del género Neoceratium registradas para una sección del Caribe colombiano (35207 Km2), es un número bastante ajustado al número total de especies existentes en la región, si se compara con el número de especies registradas en extensiones más grandes: 49 para el suroeste del golfo de México (Licea et al., 2004); 53 para el golfo de California (Licea et al., 1995); 57 para el Caribe y áreas adyacentes (Wood, 1968); 58 para el Mediterráneo (Gómez, 2003); 53 para el Canal de Mozambique (Sournia, 1970); 51 para el Atlántico sudoccidental (Balech, 1988) y 58 para el océano Indico (Taylor, 1976). Desde este punto de vista, este listado de especies es una herramienta útil al conocimiento de la biodiversidad del fitoplancton en el mar Caribe colombiano.
AGRADECIMIENTOS
Se agradece a la Agencia de Nacional de Hidrocarburos (ANH) de Colombia y al Instituto de Investigaciones Marinas y Costeras-INVEMAR por la financiación y desarrollo del proyecto "Especies, ensamblajes y paisajes de los bloques marinos sujetos a exploración de hidrocarburos" dentro del cual se desarrolló parte del presente trabajo.
BIBLIOGRAFÍA
1 Andrade-Amaya, C. A. 2000. The circulation and variability of the Colombian Basin in the Caribbean Sea. Tesis Ph. D. University of Wales, Gales. 223 p. [ Links ]
2 Balech, E. 1962. Tintinnoinea y Dinoflagellata del Pacífico según material de las expediciones Norpac y Downwind del Instituto Scripps de Oceanografía. Rev. Mus. Argent. Cienc. Nat. Bernardino Rivadavia Inst. Nac. Invest. Cienc. Nat. (Argent) Zo, 7 (1): 207. [ Links ]
3 Balech, E. 1988. Los dinoflagelados del Atlántico sudoccidental. Publ. Espec. No 1, Instituto Español de Oceanografía, Madrid. 310 p. [ Links ]
4 Böhm, A. 1931. Distribution and variability of Ceratium in the Northern and western Pacific. Bull. Bernice P. Bishop Mus., 87: 1-46. [ Links ]
5 Carbonell, M. C. 1979. Ceratium Schrank (Peridiniales) en la bahía de Cartagena (10º 25'N y 75º 30'W). Bol. Cient. CIOH, 2: 21-53. [ Links ]
6 Carbonell, M. C. 1981. Fitoplancton de la República Dominicana. Bol. Cient. CIOH, 3: 11-52. [ Links ]
7 Carbonell, M. C. 1982. Ceratium Schrank (Dinoflagellatae, Peridiniales) de las islas del Rosario, Caribe Colombiano. An. Inst. Invest. Mar. Punta Betín, 12: 71-91. [ Links ]
8 Carmona, G. E. 1979. Contribuciones al conocimiento de la ecología del plancton de la Ciénaga Grande de Santa Marta. Tesis de grado, Univ. Antioquia, Medellín. 74 p. [ Links ]
9 Caycedo, I. E. 1977. Fitoplancton de la bahía de Nenguange (Parque Nacional Tayrona), mar Caribe, Colombia. An. Inst. Invest. Mar. Punta Betín, 9: 17-44. [ Links ]
10 CORPES. 1992. El Caribe colombiano. Realidad ambiental y desarrollo. Consejo Regional Planificación Costa Atlántica, Santa Marta. 275 p. [ Links ]
11 Dodge, J. D. 1982. Marine dinoflagellates of the British Isles. Her Majesty's Stationery Office, Londres. 303 p. [ Links ]
12 Dodge, J. D. 1985. Atlas of dinoflagellates. A scanning electron microscope survey. Farrand Press, Londres. 199 p. [ Links ]
13 Dodge, J. D. 1993. Biogeography of the planktonic dinoflagellate Ceratium in the western Pacific. Korean J. Phycol., 8: 109-119. [ Links ]
14 Dodge, J. D. y H. G. Marshall. 1994. Biogeographic analysis of the armored planktonic dinoflagellate Ceratium in the North Atlantic and adjacent seas. J. Phycol., 30: 905-922. [ Links ]
15 Fernández, C. E. y C. B. García. 1998. The dinoflagellates of the genera Ceratium and Ornithocercus collected in the Golfo the Salamanca, Colombian Caribbean Sea. Rev. Acad. Colomb. Cienc., 22 (85): 539-559. [ Links ]
16 Gaarder, K. R. 1954. Dinoflagellate from the "Michael Sars" North Atlantic deep-sea expedition 1910. Reports scientific results "Michael Sars" North Atlantic deep-sea expedition 1910, 2 (3): 1-62. [ Links ]
17 Gómez, F. 2005. A list of free-living dinoflagellate species in the word's oceans. Acta Bot. Croata, 64 (1): 129-212. [ Links ]
18 Gómez, F., D. Moreira y P. López-García. 2010. Neoceratium gen. nov., a new genus for all marine species currently assigned to Ceratium (Dinophyceae). Protist, 161: 35-54. [ Links ]
19 Gourret, M. P. 1883. Sur les péridiniens du Golfe de Marseille. Annales Mémoire Musée D' histoire naturelle de Marseille, Zoologie, 1 (8): 1-114. [ Links ]
20 Graham, H. W. y N. Bronikowsky. 1944. The genus Ceratium in the Pacific and North Atlantic oceans. Publication No. 565. Carnegie Institution of Washington, Washington. 209 p. [ Links ]
21 Halim, Y. 1967. Dinoflagellates of the South-east Caribbean Sea (East-Venezuela). Internationale Revue der gesamten Hydrobiologie und Hydrographie, 52 (5): 701-755. [ Links ]
22 Hermosilla, J. G. 1973a. Contribución al conocimiento sistemático de los dinoflagelados de la bahía de Concepción, Chile. Gayana Zool., 24: 1-149. [ Links ]
23 Hermosilla, J. G. 1973b. Contribución al conocimiento sistemático de los dinoflagelados y tintinidos del Archipiélago de Juan Fernández. Bol. Soc. Biol. Concepc., 46: 11-36. [ Links ]
24 Hernández-Becerril, D. U. 1989. Species of the flagellate genus Ceratium Schrank (Dinophyceae) in the Gulf of California and coasts off Baja California, Mexico. Nova Hedwigia, 48 (1-2): 33-54. [ Links ]
25 Jörgensen, E. 1911. Die Ceratien. Eine kurze monographie der Gattung Ceratium Schrank. Internationale Revue der gesamten Hydrobiologie und Hydrographie 4, Biol. Suppl., 1: 1-124. [ Links ]
26 Jörgensen, E. 1920. Mediterranean Ceratia. Report of the Danish oceanographic expedition to The Mediterranean and adjacent seas (Biology) J., 2 (1): 1-110. [ Links ]
27 Kofoid, C. A. 1907a. New species of dinoflagellates. Bull. Mus. Comp. Zool. Harv., 50: 163-209. [ Links ]
28 Kofoid, C. A. 1907b. Dinoflagellata of the San Diego region, III. Descriptions of new species. Univ. California Publ. Zool., 3 (13): 299-340. [ Links ]
29 Léger, G. 1973. Diatomées et dinoflagellés de la côte est de Corse. Systématique et distribution en Juillet 1964. Bulletin De L'institut Oceanographique Monaco, 71 (1426): 1-31. [ Links ]
30 Licea, S., J. L. Moreno, H. Santoyo y G. Figueroa. 1995. Dinoflagelados del golfo de California. Universidad Autónoma de Baja California Sur. México DF. 165 p. [ Links ]
31 Licea, S., M. E. Zamudio, L. Ruth y J. Soto. 2004. Free living dinoflagellates in the Southern Gulf of Mexico: Report of data (1979-2002). Phycol. Res., 52: 419-428. [ Links ]
32 López, J. 1966. Variación y regulación de la forma en el género Ceratium. Invest. Pesq., 30: 325-427. [ Links ]
33 Lozano-Duque, Y., L. A. Vidal y G. Navas. 2010. La comunidad fitoplanctonica en el mar Caribe Colombiano. 87-118. En: INVEMAR (Ed.). Biodiversidad del margen continental del Caribe colombiano. Serie de Publicaciones Especiales No. 20, INVEMAR, Santa Marta. 4588 p. [ Links ]
34 Margalef, R. 1957. Fitoplancton de las costas de Blanes (Gerona) de agosto de 1952 a junio 1956. Invest. Pesq., 8: 89-95. [ Links ]
35 Margalef, R. 1961. Hidrografía y fitoplancton de un área marina de la costa meridional de Puerto Rico. Invest. Pesq., 18: 33-96. [ Links ]
36 Margalef, R. 1969. Diverdidad de fitoplancton de red en dos áreas del Atlántico. Invest. Pesq., 33 (1): 275-286. [ Links ]
37 Marshall, H. G. 1976. Phytoplankton distribution along the eastern coast of the USA. I. Phytoplankton composition. Mar. Biol., 38: 81-89. [ Links ]
38 Marshall, H. G. y J. A. Solder. 1982. Pelagic phytoplankton in the Caribbean Sea. Bull. Mar. Sci., 32 (1): 354-365. [ Links ]
39 Murray, G. y F. Whitting. 1899. New Peridiniaceae from the Atlantic. Transac. Linnean Soc. London, 2nd Series Botany, 5 (9): 321-342. [ Links ]
40 Nie, D. 1936. Dinoflagellata of the Hainan region. I. Ceratium. Contributions from the Biological Laboratory of the Science Society of China, Nanking, Zool. Ser., 12 (3): 29-73. [ Links ]
41 Okolodkov, Y. B. 1996. Net phytoplankton from the Barents Sea and Svalbard waters collected on the cruise of the R/V "Geolog Fersman" in July-September 1992, with emphasis on the Ceratium species as biological indicators of the Atlantic waters. Bot. J. Russian Acad. Sci., 81: 1-9. [ Links ]
42 Okolodkov, Y. B. y I. Gárate-Lizárraga. 2006. An annotated checklist of dinoflagellates (Dinophyceae) from the Mexican Pacific. Acta Bot. Mex., 74: 1-154. [ Links ]
43 Pesantes, F. 1983. Dinoflagelados del fitoplancton del golfo de Guayaquil. Acta Oceanogr. Pacífico, 2 (2): 283-399. [ Links ]
44 Posada, B. O y W. Henao. 2008. Diagnóstico de la erosión en la zona costera del Caribe colombiano. Serie de Publicaciones Especiales No. 13, Instituto de Investigaciones Marinas y Costeras-INVEMAR, Santa Marta. 96 p. [ Links ]
45 Raine, R., M. White y J. D. Dodge. 2002. The summer distribution of net plankton dinoflagellates and their relation to water movements in the NE Atlantic Ocean, west of Ireland. J. Plankton Res., 24: 1131-1147. [ Links ]
46 Rampi, L. y M. Bernhard. 1980. Chiave per la determinazione delle peridinee pelagiche Mediterranee. Comitato Nazionale Energia Nucleare RT/BIO, (80) 8: 1-193. [ Links ]
47 Schiller, J. 1937. Dinoflagellatae (Peridineae) in monographischer Behandlung. En: Rabenhorst, L. (Ed.). Kryptogamen-Flora von Deutschland, Österreich und der Schweiz 2 Teil. Akademische, Leipzig. 589 p. [ Links ]
48 Sournia, A. 1966. Sur la variabilité infraspecifique de genre Ceratium (Peridinien planctonique) in milieu marin. Comptes-rendus Hebdomadaires des Seances de l'Académie des Sciences de Paris, 263 (25): 1980-1983. [ Links ]
49 Sournia, A. 1968. Le genre Ceratium (péridinien planctonique) dans le Canal de Mozambique. Contribution á une révision mondiale. Vie Milieu, Sér. A: Biologie marine, 18: 375-499. [ Links ]
50 Sournia, A. 1970. A checklist of planktonic diatoms and dinoflagellates from the Mozambique Channel. Bull. Mar. Sci., 20 (3): 678-696. [ Links ]
51 Sournia, A. 1986. Atlas du phytoplankton marin. Vol. 1: Introduccion, Cyanophycées, Dictyochophycées, Dinophycées et Raphidophycées. Éditiones du CNRS, París. 219 p. [ Links ]
52 Steemann-Nielsen, E. 1939. Die Ceratien des Indischen Ozeans und der ostasiatischen Gewässer mit einer allgemeinen zusammenfassung über die verbreitung der Ceratien in den Weltmeeren. Dana-Report 17. The Carlsberg Foundation's Oceanographical Expedition round the world 1928-30 and previous "Dana"-Expeditions, Londres. 33 p. [ Links ]
53 Steidinger, K. A. y J. Williams. 1970. Dinoflagellates. Memoirs of the Hourglass Cruises. Florida Department of Natural Resources. St. Petersburg, 2: 1-251. [ Links ]
54 Taylor, F. J. R. 1976. Dinoflagellates from the international Indian Ocean expedition. A report on material collected by the R.V. Anton Bruun 1963-1964. Bibliotheca Botanica. Sttutgart, Alemania, 132: 1-234. [ Links ]
55 Trégouboff, G. y M. Rosé. 1957. Manuel de planctologie Méditerranéenne. Centre National de la Recherche Scientifique, París. 587 p. [ Links ]
56 Tunin-Ley, A., J. P. Labat, S. Gasparini, L. Mousseau y R. Lemeé. 2007. Annual cycle and diversity of species and infraspecific taxa of Ceratium (Dinophycea) in the Ligurian Sea, Northwest Mediterranean. J. Phycol., 43: 1149-1163. [ Links ]
57 Vidal, L. A. 1995. Estudio del fitoplancton en el sistema lagunar estuarino tropical Ciénaga Grande de Santa Marta, Colombia, durante el año 1987. Tesis de Maestría, Univ. Nacional de Colombia, Bogotá. 207 p. [ Links ]
58 Wood, E. J. F. 1954. Dinoflagellates of the Australian region. Aust. J. Mar. Freshw. Res., 5 (2): 171-351. [ Links ]
59 Wood, E. J. F. 1963. Dinoflagellates in the Australian region II. Recent collections. International Indian Ocean Expedition, 2 (119): 511-563. [ Links ]
60 Wood, E. J. F. 1966. A phytoplankton study of the Amazon Region. Bull. Mar. Sci., 16 (1): 102-123. [ Links ]
61 Wood, E. J. F. 1968. Dinoflagellates of the Caribbean Sea and adjacent areas. University of Miami Press, Coral Gables, Florida. 143 p. [ Links ]
FECHA DE RECEPCIÓN: 12/11/2009 FECHA DE ACEPTACIÓN: 07/04/2011