Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Revista Lasallista de Investigación
Print version ISSN 1794-4449
Rev. Lasallista Investig. vol.8 no.2 Caldas July/Dec. 2011
Artículo original / Original article / Artigo original
* Derivado del proyecto de investigación: "FeCl3 and TiO2 interaction with H2O2 in the liquid waste treatment from the textile industry using artificial light trough factorial model", para optar al título de doctor of Science in Environmental Engineering. Financiado por el Fondo para el Desarrollo de la Investigación de la Corporación Universitaria Lasallista.
** Director de Investigación de la Corporación Universitaria Lasallista. Investigador Grupo GAMA
Correspondencia: Luis Fernando Garcés Giraldo, e-mail: lugarces@lasallista.edu.co
Artículo recibido: 03/04/2009; Artículo aprobado: 12/12/2011
Resumen
Introducción. La investigación consistió en la eliminación de sustancias recalcitrantes en el agua, es decir, contaminantes sintéticos presentes en aguas residuales, mediante el uso de FeCl3 y TiO2 y un agente oxidante como es el H2O2. Este sistema permite aprovechar la energía de la luz artificial para, sin ninguna etapa intermedia, provocar una serie de reacciones químicas que den lugar a la mineralización o eliminación de los contaminantes disueltos en las aguas objeto de estudio. Objetivo. Encontrar las condiciones óptimas para el tratamiento de aguas residuales con azul Novactive FHBRNS, por procesos de oxidación avanzada empleando luz artificial. Materiales y métodos. Se utilizó una lámpara de luz ultravioleta marca MIGTHY PURE de 60 Hz, con una cubeta de vidrio que almacena 15 L de muestra; la muestra se recirculó con bomba que manejó un flujo de 0.047 L/s. Resultados. Se obtuvieron un porcentaje de degradación del 97.3% y un porcentaje de mineralización de 65.8% con el FeCl3. En este mismo experimento fue donde se obtuvieron los mejores resultados para la degradación y mineralización del colorante con el TiO2. Conclusión. El colorante degrada y mineraliza más rápidamente con el FeCl3; esto sucedió en el ensayo E7 (60 mg/L FeCl3 y 1.0 mL/L de H2O2).
Palabras clave: fotodegradación, Azul Novactive FHBRNS, agente oxidante, fotólisis, fotócatalisis.
Abstract
Introduction. This research work consisted on the removal of recalcitrant substances in water. They are synthetic pollutants in waste water and can be removed by the use of FeCl3 and TiO2, plus an oxidation agent, like H2O2. This system allows the use of artificial light for, with no intermediate stages, provoke chemical reactions that bring the mineralization or the degradation of the pollutants dissolved in the water studied. Objective. To find the optimal conditions to treat waste waters with Novactive blue FHBRNS, by the use of oxidation processes that uses artificial light. Matetials and methods. A 60 Hz MIGTHY PURE ultraviolet lamp was used, with a glass cuvette that contained 15 L of the sample. The sample was recirculated with a pump, which had a 0.047L/s flow. Results. A 97.3% degradation rate and a 65.8% mineralization rates were obtained with FeCl3. In this same experiment the best degradation and mineralization rates of the dye were obtained with TiO2. Conclusion. The dye gets degraded and mineralized faster with FeCl3. This took place in the E7 trial (60 mg/L FeCl3 and 1.0 mL/L of H2O2).
Key words: photodegradation, Novactive blue FHBRNS, oxidation agent, photolysis, photocatalysis.
Resumo
Introdução. A investigação consistiu a eliminação de substâncias recalcitrantes na água, isto é, contaminantes sintéticos presentes em águas residuais, mediante o uso de FeCl3 e TiO2 e um agente oxidante como é o H2Ou2. Este sistema permite aproveitar a energia da luz artificial para, sem nenhuma etapa intermédia, provocar uma série de reações químicas que dêem lugar à mineração ou eliminação dos contaminantes dissolvidos nas águas objeto de estudo. Objetivo. Encontrar as condições ótimas para o tratamento de águas residuais com azul Novactive FHBRNS, por processos de oxidação avançada empregando luz artificial. Materiais e métodos. Utilizou-se um lustre de luz ultravioleta marca MIGTHY PURE de 60 Hz, com uma cuba de vidro que armazena 15 L de mostra; a mostra se re-circulou com bomba que manejou um fluxo de 0.047 L/s. Resultados. Obtiveram-se uma porcentagem de degradação de 97.3% e uma porcentagem de mineração de 65.8% com o FeCl3. Neste mesmo experimento foi onde se obtiveram os melhores resultados para a degradação e mineração do corante com o TiO2. Conclusão. O corante degrada e minera mais rapidamente com o FeCl3; isto sucedeu no ensaio E7 (60 mg/L FeCl3 e 1.0 ML/L de H2Ou2).
Palavras importantes: foto-degradação, azul No-vactive FHBRNS, agente oxidante, fotólises, foto-catalises.
Introducción
La fotocatálisis es definida como la aceleración de una fotorreacción mediante la presencia de un catalizador. El catalizador activado por la absorción de la luz acelera la reacción con el reactivo a través de un estado excitado o, bien, mediante la aparición de pares electrón-hueco, si el catalizador es un semiconductor (e- y h+). En este último caso, los electrones excitados son transferidos hacia la especie reducible, a la vez que el catalizador acepta electrones de la especie oxidable que ocuparán los huecos; de esa manera, el flujo neto de electrones será nulo, y el catalizador permanecerá inalterado1-10.
Una partícula semiconductora será el catalizador ideal para una reacción determinada: si los productos se forman con una elevada especificidad, si permanece inalterada durante el proceso, si se requiere la formación de pares electrón-hueco y si no se almacena energía fotónica en los productos finales, siendo una reacción exotérmica y, en principio, solo cinéticamente retardada9-16.
Materiales y métodos
El colorante Azul Novactive FHBRNS es uno de los más utilizados en la industria textil para el teñido de prendas. La concentración promedio en el agua fue de 300 mg/L, que es la concentración típica de los efluentes industriales textiles con este colorante. En la tabla 1 se presentan los ensayos que se realizaron; cada ensayo se hizo por triplicado para disminuir el error experimental. Para los experimentos se utilizó el peróxido de hidrógeno como agente oxidante (H2O2). La duración de los ensayos fue de dos horas.
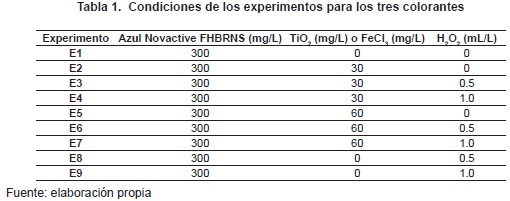
La degradación del colorante se evaluó midiendo la concentración del contaminante por seguimiento del color (fotometría), y la mineralización, utilizando la técnica del carbono orgánico total (COT).
Para el montaje de los experimentos se llevó a cabo el siguiente procedimiento:
-
Se midieron 15 L de agua, los cuales se colocaron en el tanque de vidrio.
-
Se adicionó el colorante en el tanque que quedó con una concentración de 300 mg/L.
-
Inicialmente se agitó manualmente la solución y luego se recirculó a través de la bomba y la lámpara.
-
Se tomó la muestra para medir el color y el COT inicial.
-
Se adicionaron las sustancias químicas de acuerdo con los experimentos de la tabla 1 (peróxido de hidrógeno, dióxido de titanio, cloruro férrico y sus respectivas mezclas).
-
Se midió continuamente el pH para ajustarlo en 4 cuando se trabajó con FeCl3; se adicionó H2SO4 o NaOH, según los valores. Con TiO2 los valores de pH fueron medidos sin requerir adicionar ácidos o bases, por ser más estables (pH aproximados a 7).
-
Se tomaron las muestras para ser analizadas en el laboratorio; estas fueron tomadas cada 20 minutos para medir el color, y cada 40 minutos se midió el COT.
-
Luego de terminar cada experimento se procedía a lavar la lámpara con solución de mezcla sulfocrómica diluida y bastante agua, para dejarlo limpio para el siguiente experimento.
-
Los análisis de color y COT fueron realizados inmediatamente en el laboratorio.
Para el procesamiento de la información se empleó el programa R 2.7.2, y los métodos utilizados fueron: análisis de varianza (ANOVA) de tres factores con un nivel de confianza del 95% y un nivel de potencia para detectar diferencias significativas del 100%, y análisis factorial 33 para optimizar las variables respuesta: porcentaje de degradación y porcentaje de mineralización.
Resultados y discusión
En la tabla 2 se presentan los resultados para la degradación y la mineralización de agua con el colorante Azul Novactive FHBRNS.
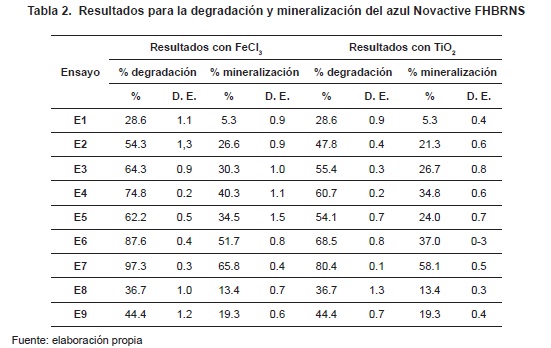
En la tabla 2 y en las figuras 1 y 2 se muestran los porcentajes de degradación y mineralización para diferentes ensayos con FeCl3 del colorante Azul Novactive FHBRNS; se infiere que en la fotólisis (E1) los porcentajes de degradación y mineralización fueron los resultados más bajos encontrados para este colorante: 28.6 y 5.3 %, respectivamente.
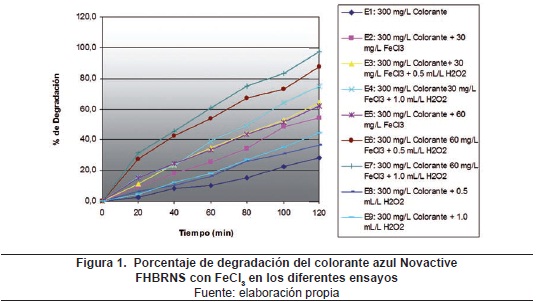
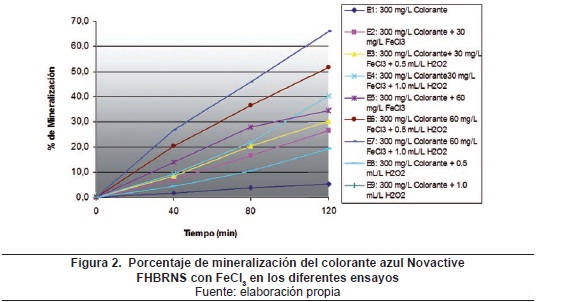
El empleo de 30 mg/L del FeCl3 (E2) incrementó el porcentaje de degradación y mineralización del colorante en un 54.3 y 26.6%, respectivamente; este ensayo se realizó con el objetivo de determinar si el FeCl3 fotoactivado es capaz de generar, a partir del agua, suficientes radicales hidroxilo libre como para degradar y mineralizar el azul Novactive FHBRNS. Por esta razón se hizo la fotocatálisis sin peróxido de hidrógeno.
En comparación con el uso de solo FeCl3, el empleo de 30 mg/L de FeCl3 y 0.5 mL/L de H2O2 (E3) incrementó los porcentajes de degradación y mineralización del colorante en un 64.3 y 30.3%, respectivamente. Esto es explicable ya que en este ensayo el agente oxidante es el radical hidroxilo. Con el aumento del peróxido de hidrógeno de 0.5 mL/L a 1.0 mL/L (E4) se pretendía incrementar la velocidad de degradación del azul Novactive FHBRNS, ya que esta es una fuente de radicales hidroxilo. Comparando los ensayos E3 y E4, se comprobó que a mayor peróxido de hidrógeno son mayores los porcentajes de degradación y mineralización del colorante (la cantidad de FeCl3 fue constante); para el ensayo E4 los porcentajes de degradación y mineralización fueron 74.8 y 40.3%, respectivamente.
El aumento del FeCl3 de 30 mg/L a 60 mg/L, usando solo el fotosensibilizador (ensayos E2 y E5, respectivamente), incrementó los porcentajes de degradación y mineralización del colorante en un 62.2% y 34.5%, respectivamente, aunque el aumento entre ambos ensayos no es significativo (7 y 8%, respectivamente). El ensayo con 60 mg/L de FeCl3 y 0.5 mL/L (E6) incrementó los porcentajes de degradación y mineralización en un 87.6% y 51.7%; este ensayo es uno de los mejores para este colorante. Al aumentar la cantidad de peróxido de hidrógeno en 1 mL/L (E7) se obtuvieron un 97.3% de degradación y un 65.8% de mineralización en dos horas. Este es el mejor ensayo obtenido para el colorante Azul Novactive FHBRNS.
Para comprobar la importancia de la oxidación química con peróxido de hidrógeno en esta investigación, se realizaron los ensayos E8 y E9 con 0.5 mL/L y 1.0 mL/L, respectivamente; se obtuvieron un 36.7 y un 44.4% de degradación, respectivamente, y un 13.4 y 19.3% de mineralización, respectivamente. Los porcentajes de degradación y mineralización del colorante aumentaron con el incremento en la cantidad del peróxido de hidrógeno; esto es muy probable debido a que el H2O2 tiene un alto potencial de oxidación.
La tabla 2 y las figuras 3 y 4 muestran los porcentajes de degradación y mineralización para diferentes ensayos con TiO2; para la fotólisis (E1) los porcentajes de degradación y mineralización fueron los resultados más bajos encontrados para este colorante: 28.6 y 5.3%, respectivamente. El empleo de 30 mg/L del TiO2 (E2) incrementó los porcentajes de degradación y mineralización del colorante en un 47.8 y 21.3%, respectivamente; este ensayo se realizó con el objetivo de determinar si el TiO2 fotoactivado es capaz de generar, a partir del agua, suficientes radicales hidroxilo libre como para degradar y mineralizar el Azul Novactive FHBRNS. Por esta razón se hizo la fotocatálisis sin peróxido de hidrógeno.
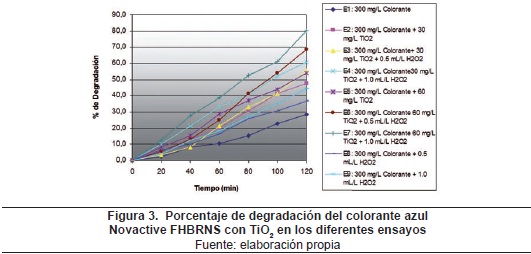

En comparación con el uso de solo TiO2, el empleo de 30 mg/L de TiO2 y 0.5 mL/L de H2O2 (E3) incrementó los porcentajes de degradación y mineralización del colorante en un 55.4 y 26.7%, respectivamente. Esto es explicable ya que en este ensayo el agente oxidante es el radical hidroxilo, de gran poder oxidante. El radical hidroxilo se forma fácilmente a partir del peróxido de hidrógeno por la presencia de dióxido de titanio, cuando este es fotoactivado por la luz ultravioleta.
Con el aumento del peróxido de hidrógeno de 0.5 mL/L a 1.0 mL/L (E4) se pretendía incrementar la velocidad de degradación del Azul Novactive FHBRNS. ya que esta es una fuente de radicales hidroxilo. Comparando los ensayos E3 y E4 se comprobó que a mayor peróxido de hidrógeno son mayores los porcentajes de degradación y mineralización del colorante (la cantidad de TiO2 fue constante).
Es interesante determinar si el TiO2 fotoactivado es capaz de generar, a partir del agua, suficientes radicales hidroxilo como para degradar y mineralizar el Azul Novactive FHBRNS. Por esta razón se hizo la fotocatálisis sin peróxido de hidrógeno. El aumento del TiO2 de 30 mg/L a 60 mg/L, usando solo el fotosensibilizador (ensayos E2 y E5, respectivamente), incrementó los porcentajes de degradación y mineralización del colorante en un 54.1% y 24.0%, respectivamente, aunque el aumento entre ambos ensayos no es significativo (7 y 3%, respectivamente).
El ensayo con 60 mg/L de TiO2 y 0.5 mL/L (E6) incrementó los porcentajes de degradación y mineralización en un 68.5% y 37.0%; este ensayo es uno de los mejores para este colorante con el TiO2. Al aumentar la cantidad de peróxido de hidrógeno en 1 mL/L (E7) se obtuvieron un 80.4% de degradación y un 58.1% de mineralización en dos horas. Este es el mejor ensayo obtenido para el colorante azul Novactive FHBRNS con TiO .
Conclusión
Si se comparan los fotocatalizadores utilizados para el colorante Azul Novactive FHBRNS (Fe-Cl3 y TiO2), se concluye que el colorante degrada y mineraliza más rápidamente con el FeCl3. Esto sucedió en el ensayo E7 (60 mg/L FeCl3 y 1.0 mL/L de H2O2), donde se obtuvieron un porcentaje de degradación del 97.3% y un porcentaje de mineralización de 65.8%. En este mismo experimento fue donde se obtuvieron los mejores resultados para la degradación y mineralización del colorante con el TiO2.
Referencias
1. GARCÉS GIRALDO, Luís Fernando. Fotocatálisis con TiO2 de los colorantes azul de metileno y naranja reactivo 84 utilizando colector solar. Medellín, 2003, 220 p. Tesis (Magíster en Ingeniería Ambiental). Universidad de Antioquia. Ingeniería Ambiental. [ Links ]
2. GARCÉS GIRALDO, Luis F. y et al. La fotocatálisis como alternativa para el tratamiento de aguas residuales. En: Revista Lasallista de Investigación. Corporación Universitaria Lasallista. Jun. 2004. Vol. 1, No. 1. p. 83-92. [ Links ]
3. MALATO RODRÍGUEZ, Sixto; et al. Descontaminación de aguas de lavado de envases de plaguicidas mediante Fotocatálisis solar. Madrid: Ciemat, 2001. 189 p. [ Links ]
4. LIU, G.; et al. Photooxidation pathway of sulforhodamine-B.dependence on the adsorption mode on TiO2 exposed to visible light radiation. En: Environmental science & technology. 2000. Vol. 34. p. 3982-3990. [ Links ]
5. GÓMEZ, L.; et al. Fotooxidación de vertidos químicos: Revisión y experiencias de procesos de oxidación avanzada. En: Ingeniería Química. Madrid. sep. 2000. No. 371. p. 211-216. [ Links ]
6. VIDAL, A.; et al. Oxidación solar fotocatalítica: Aplicación al tratamiento de afluentes cianurados. En: Ingeniería Química. Madrid. Ene. 2001, No 375. p. 161-165. [ Links ]
7. VIDAL, A.; et al. Procesos solares fotocatalíticos en el tratamiento de afluentes: aplicaciones al tratamiento de aguas de lavado conteniendo plaguicidas. En: Ingeniería Química. Madrid. Enero 2002. No 386. p. 106-111. [ Links ]
8. LI, X. Z. y LI, F. B. Study of Au/Au3+-Tio2 photocatalysis toward visible Photooxidation for water and wasterwater treatment. En: Environmental science & technology. 2001. No. 35. p. 2381-2387. [ Links ]
9. ZHAO, Wei; et al. Photodegradation of Sulforhodanine-B dye in platinized titania dispersions under visible light irradiation: Influence of Platinum as a functional co-catalyst. En: The Journal of physical chemistry. Mayo, 2002. Vol. 16, No. 16. p 5022-5028. [ Links ]
10. GULYAS, h.; et al. Experiences with solar application of photocatalytic oxidation for dye removal from a model textile industry wastewater. En: Water Plution VI. Modelling, Mearuring and Prediction. Editorial C.A. Brebbia. 2001. p 153-165. [ Links ]
11. PÉREZ, L.; et al. Degradación de desechos de laboratorio mediante fotocatálisis solar. México: Instituto Mexicano de Tecnología del Agua, 2001. [ Links ]
12. NI, Meng; et al. A review and recent developments in photocatalytic water-splitting using TiO2 for hydrogen production. In: Renewable and sustainable Energy Reviews. Mar. 2005. Vol. 20, No. 40. p. 1-26. [ Links ]
13. MANSILLA, H.; et al. Tratamiento de residuos líquidos de la industria de celulosa y textil. En: CYTED VII-G. Eliminación de contaminantes por fotocatálisis heterogénea. La Plata, Argentina : CYTED VII-G, 2001. p. 60-84. [ Links ]
14. TELLO RENDON, Erick Danilo. Optimización de tecnologías fotocataliticas de oxidación avanzada aplicadas al tratamiento de residuos líquidos de laboratorio. Las Palmas de Gran Canaria, 2000, 333 p. Tesis doctoral. Universidad de las Palmas de Gran Canaria. [ Links ]
15. GALINDO, Catherine; BARD, Allen J. And KISPERT, Lowell D. Photodegradation of the aminoazobenzene acid orange 52 by three advanced oxidation processes: UV/H2O2, UV/ TiO2, and VIS/TiO2. Comparative mechanistic anda kinetic investigations. In: Journal of Photochemistry and Photobiology. Jan. 2000. Vol. 130, No.1. p. 35-47. [ Links ]
16. POZZO, R. L.; et al. Radiation extinction of slurried TiO2 as a function of mechanical action and ionic composition of the suspending media: a key factor in the photocatalytic efficienciy. In: Applied Catalysis B: Environmental. Jul. 2002. Vol. 38, No. 1. p: 61-69. [ Links ]














